基于卷積神經網絡減小重建核函數對CT 影像組學特征穩定性的影響
李飛,張白霖,王學濤(通信作者)
廣州中醫藥大學第二附屬醫院 (廣東廣州 510006)
醫學影像學是醫學科學的重要分支,在腫瘤診斷、治療及預后評估中發揮著重要作用。腫瘤具有空間和時間異質性,且異質性是預測腫瘤患者預后的重要因素,但即使采用活檢也難以準確評估腫瘤異質性。近年來,隨著醫學及信息技術的發展,醫學成像分析成為了新的研究方向。影像組學通過采用先進的醫學圖像計算方法可定量描述腫瘤組織特征,從而進行數據化分析,輔助醫師對整個腫瘤進行評估,具有無創、可重復的優點。
Aerts 等[1]于2014 年開創性地發表了影像組學相關研究成果,在肺癌和頭頸癌患者的獨立數據集中,大量影像組學特征具有預測腫瘤患者在接受常規治療后各項身體機能恢復和預后復發情況的作用,從而可鑒定預后表型。Liu 等[2]基于35 例鼻咽癌患者腮腺的CT 影像組學特征建立模型,該模型預測鼻咽癌放療期間急性口干癥的靈敏度、特異度分別為1.000、0.922。Zhuo 等[3]建立了基于658 例非轉移性鼻咽癌患者的多參數MRI 影像組學特征模型,結果表明,該模型可將患者分為不同的生存亞組,且預后分層效果優于TNM 分期系統。但目前影像組學在推廣應用方面存在一些問題,如特征穩定性(可重復性)較差等。影像組學應用時需進行圖像采集、靶區勾畫、特征提取和臨床問題建模。由于各研究使用的數據及方法缺乏統一標準,影像組學應用過程中的每個步驟均可使結果產生差異。其中,非標準化的影像采集對樣本數據質量影響較大,導致特征穩定性較差,進而影響影像組學的臨床研究效果。因此,影像組學研究的標準化成為一個重要的研究領域。2016 年,Kim 等[4]通過卷積神經網絡學習低分辨率圖像和高分辨率圖像間的殘差,并利用殘差和低分辨率圖像之和將低分辨率圖像轉換為高分辨率圖像。Choe 等[5]在研究中將肺癌患者的CT 圖像進行轉換,分析重建核和圖像轉換對肺部腫瘤影像組學特征穩定性的影響。針對影像組學穩定性差的問題,本研究通過將深度學習卷積神經網絡應用于圖像轉換,從而減小CT 重建核函數對影像組學特征穩定性的影響。
1 材料與方法
1.1 實驗數據
選取29 例鼻咽癌患者的頭頸部CT 影像數據,每例均選擇4 種核函數(B10、B30、B50、B70)進行重建,并勾畫腫瘤靶區及腦干、眼球等14個感興趣區。
1.2 影像組學特征提取
采用分割算法分割感興趣區,然后利用Pyradiomics 庫以Python 語言提取影像組學特征,對每個樣本分別提取851 種特征,其中原始107 個,小波濾波744 個。
1.3 卷積神經網絡
本研究使用的卷積神經網絡具有6 個卷積層,核的大小為3×3,除最后一層外,每層均含64 個濾波器組,可提取64 個不同的特征圖。訓練的迭代次數為300 次,訓練1 次批量為5,以均方差為損失函數,優化方案為Adam(4),學習率為0.0001。以原始的512×512矩陣為輸入和輸出圖像的大小,并于訓練中應用殘差學習。圖像輸入網絡后,生成殘差圖像(輸入圖像和目標圖像之差),最終輸出轉換后的圖像(輸入圖像與殘差圖像之和),見圖1。B10、B30、B50、B70 圖像經轉換后分別變為fB70、fB50、fb30、fB10 圖像。以29 例頭頸部CT 圖像(共計4 417 張DICOM 圖像)為訓練集,以10 例頭頸部CT 圖像(共計1 333 張DICOM 圖像)為測試集。
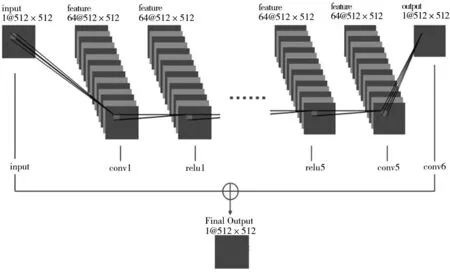
圖1 卷積神經網絡結構
1.4 圖像轉換
以核函數B10 重建的CT 圖像經卷積神經網絡轉換為fB70 的CT 圖像為例(圖2)。利用完成訓練的神經網絡模型結構及參數,將以核函數B10 重建的CT 圖像作為輸入圖像,即可得到以核函數B10 重建的CT 圖像與以核函數B70 重建的CT 圖像之間的殘差,將殘差值與輸入值相加即可得到輸出值,即生成fB70 的CT 圖像,見圖2B。同理,將4 種不同重建核函數的圖像進行轉換。
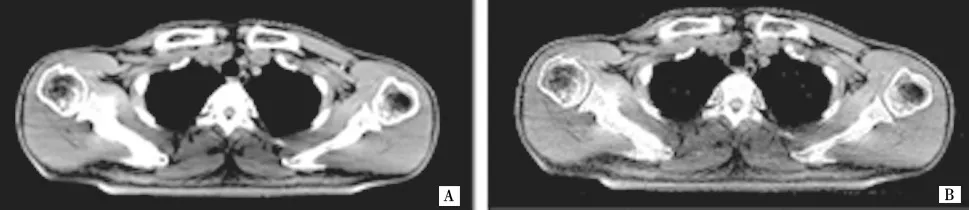
圖2 頭頸部CT 轉換圖
2 結果
2.1 轉換后圖像的一致性相關系數(concordance correlation coefficient,CCC)評估
以B10-B70 組圖像為例,對轉換后的fB10、fB70 圖像進行影像組學穩定性評估。將fB70 的CT圖像與重建核為B70 的CT 圖像進行配對,將fB10 的CT 圖像與重建核為B10 的CT 圖像進行配對,與重建核B10、B70 的CT 圖像CCC 進行比較。
以CCC 閾 值(0.60,0.65,0.70,0.75,0.80,0.85,0.90,0.95)為x軸,以達到各CCC 閾值的特征數量占比為y軸,繪制折線圖(圖3、圖4)。以CCC>0.85 為影像組學穩定的標準,符合標準的B70-fB70、B10-fB10 的CCC 的特征數量占比高于B10-B70。
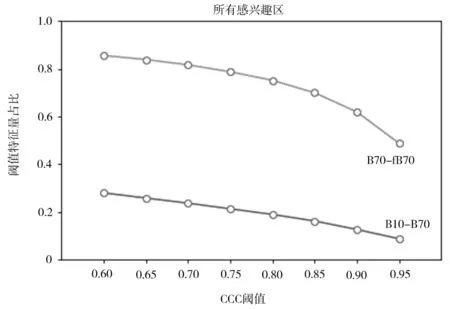
圖3 CCC 閾值折線圖(B70-fB70 與B10-B70)
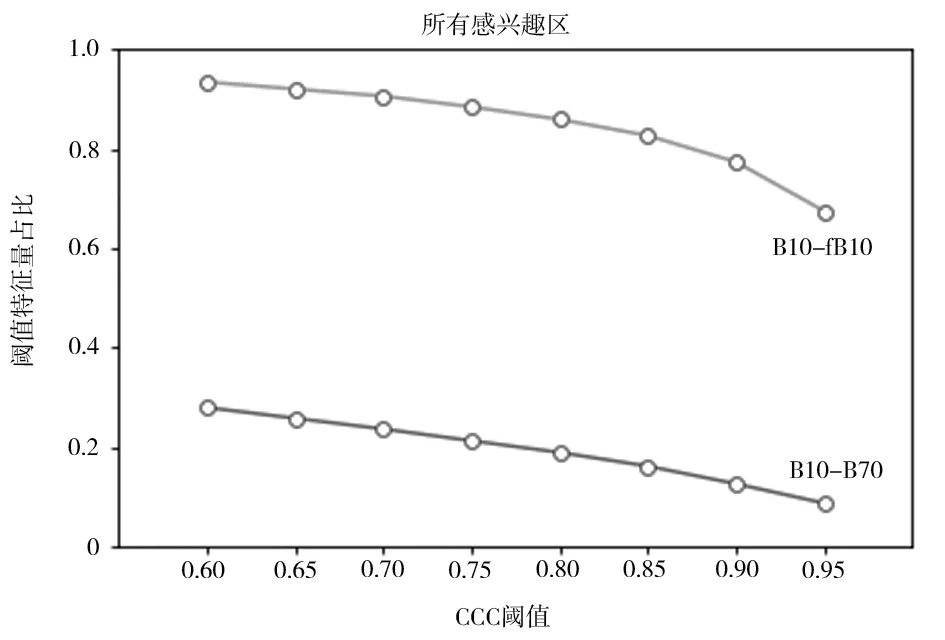
圖4 CCC 閾值折線圖(B10-fB10 與B10-B70)
2.2 轉換后圖像均方差、平均絕對值誤差、峰值信噪比、結構相似性指標評估
利用Python 提取并計算圖像fB10、fB70 的CT值,并分別計算fB10 與B10、fB70 與B70、B10 與B70 的均方差、平均絕對值誤差、峰值信噪比、結構相似性數值的平均值,見表1。由表1 可知,B10-fB10 與B70-fB70 的均方差、平均絕對值誤差均低于B10-B70,而B10-fB10 與B70-fB70 的峰值信噪比、結構相似性高于B10-B70。
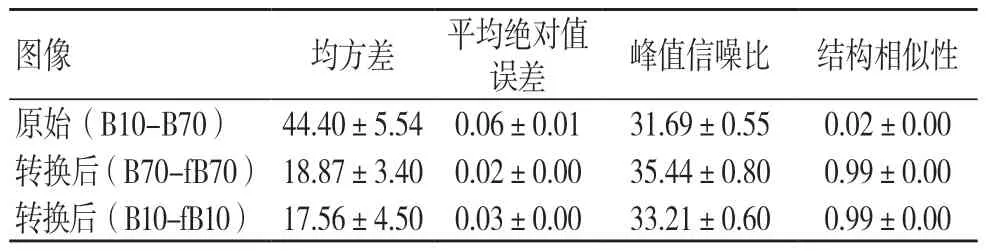
表1 轉換后圖像均方差、平均絕對值誤差、峰值信噪比、結構相似性指標
3 討論
影像組學的概念最早由荷蘭學者Lambin 等[6]提出,即從醫學影像中提取高通量成像特征并創建高維數據集。近年來,影像組學研究在疾病診斷、治療及預后評估方面取得了一系列進展。在疾病診斷和分類方面,Sun 等[7]對170 例患兒的腦部MRI圖像進行了研究,基于影像組學特征診斷注意力缺陷多動障礙并預測分型,取得了較好的預測結果。Kirienko 等[8]通過評估CT 和PET 影像組學特征將肺部病變分為原發性與轉移性,從而得知影像組學具有區分原發性肺癌組織學亞型的作用。在治療方案決策方面,Teruel 等[9]通過動態對比增強MRI 紋理分析可預測局部晚期乳腺癌患者對新輔助化療的臨床和病理反應的預處理,結果表明,紋理分析可輔助判斷治療方案的合理性,為臨床醫師提供參考信息。Shiradkar 等[10]基于影像組學的靶向放射治療計劃(Rad-TRaP)和MRI 前列腺癌治療計劃的計算框架可生成重點治療計劃,減少危及器官受照射劑量,并增加靶向癌性病變的劑量。
各項數據間差異較大是影像組學研究過程中需迫切解決的問題。CT 掃描為腫瘤診斷及治療的常用影像手段。研究表明,不同條件(掃描設備、掃描參數、重復掃描、感興趣區分割、特征提取)是影響CT 影像組學特征穩定性的不利因素[11-14]。Hunter 等[11]研究了不同掃描機器和不同圖像類型對特征穩定性造成的影響。有研究表明,過擬合和欠擬合均為影響統計學習或機器學習模型穩定性的重要因素,模型的泛化能力差,無法正確分類或預測,通過對CT 圖像進行重復掃描可提高模型穩定性[12-13]。另有研究表明,相較于手工勾畫,自動(或半自動)分割方法同時兼顧減少人工干預、提高分割精度及穩定性,因此能夠獲得更加穩定的感興趣區[14]。此外,使用不同核函數重建得到的圖像提供的診斷信息側重點不同。因此,臨床通常使用不同核函數進行圖像重建。卷積神經網絡是一類包含卷積計算且具有深度結構的前饋神經網絡,擅長處理圖像特別是大圖像的相關機器學習問題。卷積神經網絡通過一系列方法,可成功將數據量龐大的圖像識別問題不斷降維,最終使其能夠被訓練。本研究旨在分析基于卷積神經網絡重建核函數對頭頸部CT 影像組學特征穩定性的影響。與相關研究不同,本研究不僅評估腫瘤區的影像組學特征穩定性,同時也對如腦干、脊髓、中耳等共13 個正常器官予以評估,共勾畫14 個感興趣區,提取了851 種影像組學特征。結果顯示,符合標準(以CCC>0.85 為影像組學穩定的標準)的B70-fB70、B10-fB10 CCC 的特征數量占比高于B10-B70,B10-fB10 與B70-fB70 的均方差、平均絕對值誤差均低于B10-B70,而B10-fB10 與B70-fB70 的峰值信噪比、結構相似性高于B10-B70,表明通過卷積神經網絡實現圖像轉換可提高影像組學特征穩定性,減小不同重建核函數產生的差異。

