基于“質(zhì)-量”雙標的側柏葉質(zhì)量分析方法研究
于 浩,李天嬌, 2, 3,包永睿, 2, 3,王 帥, 2, 3,孟憲生, 2, 3*
基于“質(zhì)-量”雙標的側柏葉質(zhì)量分析方法研究
于 浩1,李天嬌1, 2, 3,包永睿1, 2, 3,王 帥1, 2, 3,孟憲生1, 2, 3*
1. 遼寧中醫(yī)藥大學藥學院,遼寧 大連 116600 2. 遼寧省中藥多維分析專業(yè)技術創(chuàng)新中心,遼寧 大連 116600 3. 遼寧省現(xiàn)代中藥研究工程實驗室,遼寧 大連 116600
建立以對照藥材為基準物質(zhì)的定性和不依賴多種對照品定量的側柏葉藥材“質(zhì)-量”雙標控制方法。采用HPLC技術,以對照藥材為基準物質(zhì)建立側柏葉特征圖譜,通過Q-TOF-MS技術,鑒定共有峰的化學成分,以對照藥材和供試藥材特征峰的相似度,明確藥材真?zhèn)危础百|(zhì)”;對內(nèi)標成分“柚皮苷”進行準確定量,以內(nèi)標成分計,計算不同批次供試品中各特征峰的相對含量,取“平均數(shù)-標準差”作為特征峰化學成分相對于內(nèi)標物質(zhì)化學成分的相對含量下限,依據(jù)特征峰相對含量下限明確側柏葉藥材優(yōu)劣,即“量”。建立的特征圖譜及含量測定方法符合方法學考察要求;確定了11個共有色譜峰,鑒定出了4個化學成分,分別為楊梅苷、槲皮苷、穗花杉雙黃酮、扁柏雙黃酮,各側柏葉供試藥材與側柏葉對照藥材的相似度均大于0.90;規(guī)定了側柏葉藥材特征峰化學成分相對含量下限。該方法不依賴多種對照品,能清晰、快速地判斷藥材的真?zhèn)蝺?yōu)劣,為側柏葉的質(zhì)量控制方法提供參考。
側柏葉;對照藥材;質(zhì)量控制;特征圖譜;楊梅苷;槲皮苷;穗花杉雙黃酮;扁柏雙黃酮
側柏葉始載于《神農(nóng)本草經(jīng)》,為柏科植物側柏(L.) Franco的干燥枝梢和葉,氣味清香,味道苦澀,歸肺、肝、脾經(jīng),具有涼血止血、止咳化痰和生發(fā)烏發(fā)等功效,常用于吐血、衄血、咯血、便血及崩漏下血、肺熱咳嗽、血熱脫發(fā)、須發(fā)早白等癥[1-2]。側柏葉作為一種重要的中藥資源,在我國除青海、新疆外大部分地區(qū)均有分布[3]。現(xiàn)代藥理研究表明,側柏葉含有楊梅苷、槲皮苷、異槲皮苷、穗花杉雙黃酮以及扁柏雙黃酮,它們是側柏葉中活性成分,具有抗炎、抗氧化、抗病菌以及止血的藥效作用[4-10]。
目前,側柏葉藥材質(zhì)量控制方法主要包括單指標含量測定法、多指標含量測定法和指紋圖譜與含量測定結合法[11-12],以上方法具有靈敏度高、重復性好的優(yōu)點,能夠為控制側柏葉藥材提供量化數(shù)據(jù),但存在著單一指標不能反映藥材整體特征、多指標含量測定依賴于多種對照品且某些指標成分不能反映藥效、指紋圖譜只能模糊地評價藥材相似性不能清晰地判斷供試品真?zhèn)蝺?yōu)劣的不足,且中藥復雜體系質(zhì)量評控技術難度和高額成本給中藥企業(yè)帶來了巨大的壓力,因而對中藥臨床合理用藥和臨床療效提升的指導和支持作用一直難以體現(xiàn)。針對上述問題,本實驗提出了基于“質(zhì)-量”雙標的側柏葉質(zhì)量分析方法研究,緊扣中藥多成分、多功效和整合作用的質(zhì)量內(nèi)涵和特點,以能夠反映其藥效的化學成分為指標;采用一種內(nèi)標物質(zhì)對特征峰化學成分進行相對定量,盡可能控制供試藥材有效化學成分含量同時,不需要大量購買對照品,在滿足中藥化學成分“整體性”與“清晰性”的同時減輕了中藥復雜體系質(zhì)量評控成本。本方法以對照藥材為基準物質(zhì)構建特征圖譜,并以可代表側柏葉藥效的有限個代表性成分作為特征峰,評價對照藥材和供試藥材特征峰的相似度,可以用于判斷側柏葉的真?zhèn)危贿x用保留時間穩(wěn)定且價格低廉易獲得的內(nèi)標物質(zhì)作為定量評價指標,開展基于內(nèi)標物質(zhì)的特征峰化學成分相對定量研究,通過內(nèi)標物質(zhì)化學成分準確定量,計算供試藥材特征峰化學成分的相對含量。基于“質(zhì)-量”雙標的側柏葉質(zhì)量分析方法可有效解決側柏葉有效成分同時快速測定和中藥復雜體系質(zhì)量評控成本高的問題。
1 儀器與材料
1.1 儀器
Agilent-1260 II高效液相色譜儀;Agilent 6550 Q-TOF-MS質(zhì)譜儀(美國安捷倫科技有限公司)。
1.2 材料
側柏葉供試藥材由遼寧中醫(yī)藥大學張慧教授鑒定為側柏(L.) Franco的干燥枝梢和葉,具體信息見表1。側柏葉對照藥材(批號120906-202003,中國食品藥品檢定研究院);對照品楊梅苷(批號111860-201703)、槲皮苷(批號111538-202007)、穗花杉雙黃酮(批號111902-201603),質(zhì)量分數(shù)均≥98%,均由中國食品藥品檢定研究院提供;扁柏雙黃酮(批號WKQ-0001065),質(zhì)量分數(shù)≥98%,由四川省維克奇生物科技有限公司提供;乙腈(質(zhì)譜級,德國Merck公司),水(純凈水,杭州娃哈哈集團有限公司)。
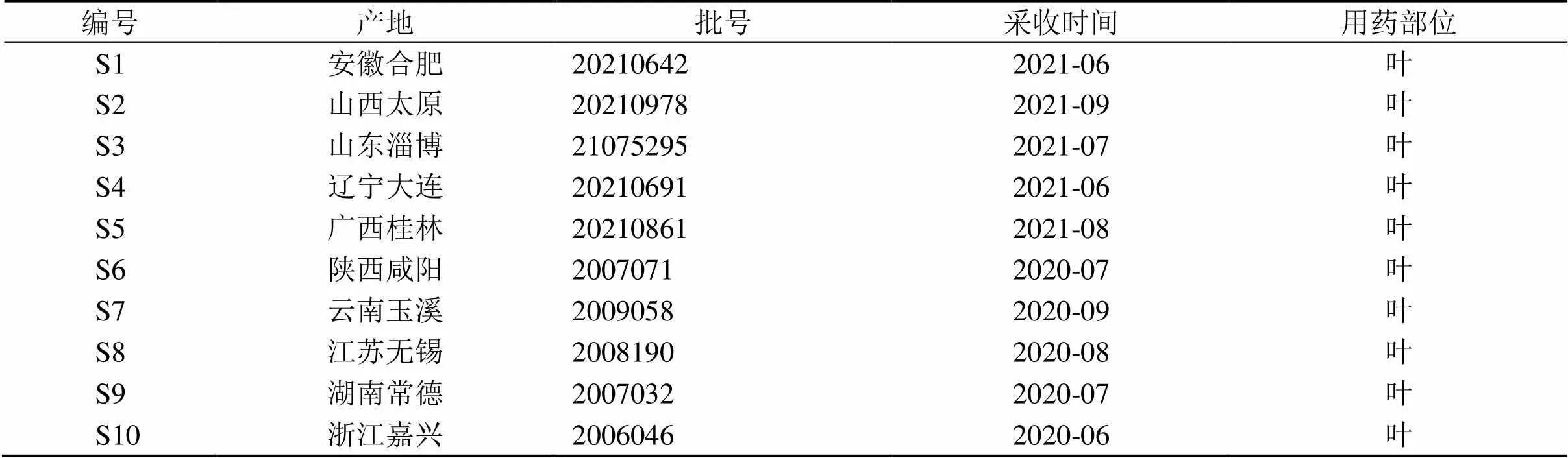
表1 側柏葉來源及批號信息
2 方法與結果
2.1 基于側柏葉對照藥材的特征圖譜建立
2.1.1 溶液的制備 取側柏葉對照藥材粉末0.50 g,精密稱定,置具塞錐形瓶中,精密加入80%甲醇25 mL,稱定質(zhì)量,超聲30 min,放冷,補足失重,搖勻,過0.22 μm微孔濾膜濾過,取續(xù)濾液,作為參照物溶液;取供試藥材粉末(過4號篩)0.50 g,按上述方法制成供試品溶液。取適量楊梅苷、槲皮苷、穗花杉雙黃酮、扁柏雙黃酮對照品精密稱定,置具塞錐形瓶中,精密加入80%甲醇,搖勻,作為混合對照品溶液。
2.1.2 色譜條件 色譜柱:Agilent Poroshell 120 SB-C18(100 mm×4.6 mm,2.7 μm);流動相為0.1%甲酸水(A)-乙腈(B),梯度洗脫:0~2 min,5~15% B;2~6 min,15~18% B;6~18 min,18~38% B;18~21 min,38~54% B;21~27 min,54~64% B;27~30 min,64~85% B;體積流量0.8 mL/min;柱溫30 ℃;DAD檢測器波長254 nm;進樣量5 μL。
2.1.3 特征圖譜的建立 將參照物溶液和供試品溶液,每份樣品平行2次,按色譜條件依次進樣檢測,將254 nm波長下的圖譜數(shù)據(jù)由分析檢測儀器中導入中國藥典委員會“中藥指紋圖譜相似度評價軟件”(2012.130727版本),獲得側柏葉藥材的HPLC特征圖譜,見圖1。以側柏葉對照藥材的圖譜為參照譜圖,使用中位數(shù)進行自動匹配,加以多點校正,共標定11個共有峰,共有峰面積占特征圖譜的75%以上,其中7號峰穩(wěn)定性、重復性、分離度好、位置居中,故以其為參照峰(S);將共有模式與對照藥材特征圖譜進行比對,見圖2。供試品色譜中應呈現(xiàn)11個特征峰,并應與對照藥材色譜圖中的11個特征峰保留時間相對應,見表2。
2.2 方法學考察
2.2.1 專屬性試驗 分別取混合對照品溶液、供試品溶液進行測定,各主峰與雜質(zhì)峰分離度良好,專屬性強,見圖3。
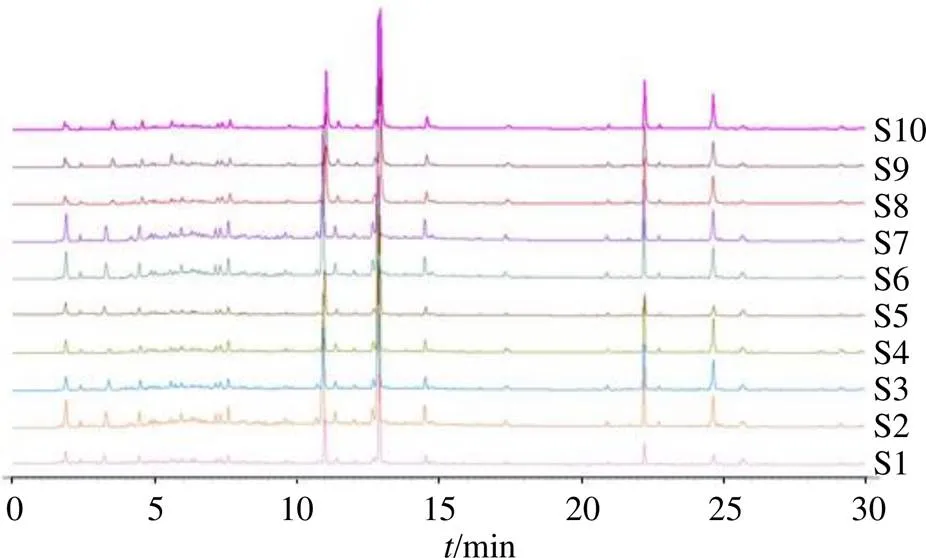
圖1 10批供試藥材的HPLC疊加圖譜
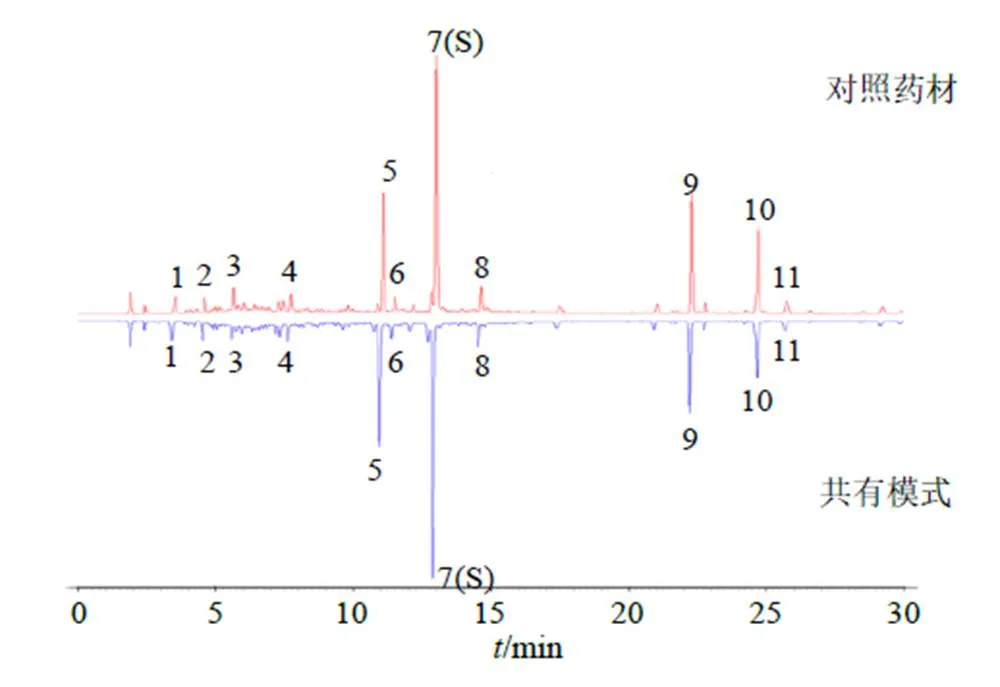
圖2 對照藥材特征圖譜及供試藥材共有模式圖
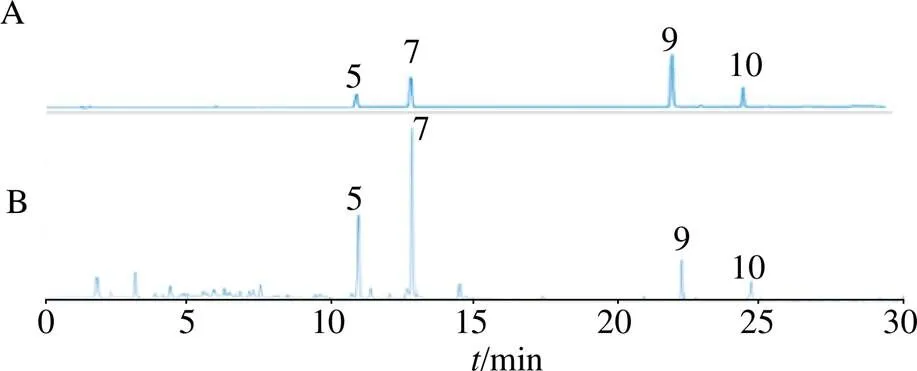
5-楊梅苷 7-槲皮苷 9-穗花杉雙黃酮 10-扁柏雙黃酮
2.2.2 精密度試驗 精密吸取同一供試品溶液5 μL,按“2.1.2”項下色譜條件測定,連續(xù)進樣6次,測定各色譜峰相對保留時間、相對峰面積,計算RSD值。各色譜峰相對保留時間、相對峰面積RSD值均小于1.0%,表明儀器精密度良好。
2.2.3 穩(wěn)定性試驗 精密吸取同一供試品溶液5 μL,按“2.1.2”項下色譜條件,分別在0、2、4、8、12、24 h進樣6次檢測,測定各色譜峰相對保留時間、相對峰面積,計算RSD值。各色譜峰相對保留時間、相對峰面積RSD值均小于2.6%,表明供試品溶液在24 h內(nèi)穩(wěn)定。
2.2.4 重復性試驗 按供試品溶液制備方法制備6份供試樣品,按“2.1.2”項下色譜條件,分別進樣檢測,測定各色譜峰相對保留時間、相對峰面積,計算RSD值。各色譜峰相對保留時間、相對峰面積RSD值均小于2.0%,表明方法重復性良好。
2.3 相似度評價
采用中國藥典委員會“中藥指紋圖譜相似度評價軟件”(2012.130727版本)進行數(shù)據(jù)處理,該軟件利用夾角余弦法計算每個色譜圖與對照藥材圖譜相比較的相似度。以側柏葉對照藥材和供試藥材特征峰的相似度明確側柏葉藥材真?zhèn)危粗兴幧V指紋圖譜相似度評價系統(tǒng)計算供試品與對照藥材特征圖譜的相似度應不得低于0.90。側柏葉供試藥材與對照藥材的相似度均大于0.90,說明所收集的側柏葉供試藥材的特征峰化學成分基本一致,質(zhì)量相對穩(wěn)定,相似度計算結果見表3。

表3 供試藥材相似度評價結果
2.4 特征峰化學成分解析
在初步采用Agilent-1260II高效液相色譜儀利用相對保留時間與對照品比對的基礎上,采用Agilent 6550 Q-TOF-MS質(zhì)譜儀,進行質(zhì)譜分析,運用Agilent MassHunter Qualitative Analysis軟件,通過對照品比對的方法對負離子模式進行化學成分解析,進一步明確特征峰的準確化學成分。
2.4.1 色譜分析條件 色譜柱:Agilent poroshell 120 SB-C18色譜柱(100 mm×2.1 mm,2.7 μm);流動相為0.1%甲酸水(A)-乙腈(B),梯度洗脫程序:0~3 min,5%~15% B;3~6 min,15%~20% B;6~15 min,20%~45% B;15~27 min,45%~85% B;27~32 min,85%~100% B;體積流量0.4 mL/min;柱溫30 ℃;進樣量1 μL。
2.4.2 質(zhì)譜分析條件 電噴霧離子源(Dual AJS ESI),負離子模式,毛細管電壓(Vcap)為3 500 V,干燥氣體體積流量(drying gas flow)為11 L/min,干燥氣體溫度(drying gas temp)為150 ℃,霧化器壓力(neulizer pressure)為172.4 kPa,鞘氣溫度(sheath gas temp)為350 ℃,鞘氣體積流量(sheath gas flow)為10 L/min,質(zhì)量掃描范圍(mass range)為/100~1000。
采用auto MS/MS模式,利用對照品比對及數(shù)據(jù)庫查詢等方法對特征峰化學成分進行解析。負離子模式鑒定出了11個特征峰中的4個化學成分。其中,5號峰為楊梅苷、7號峰為槲皮苷、9號峰為穗花杉雙黃酮、10號峰為扁柏雙黃酮,總離子流圖見圖4,鑒定結果見表4。
2.5 基于內(nèi)標物質(zhì)的特征峰化學成分相對定量研究
2.5.1 線性關系試驗 精密稱取槲皮苷對照品,用甲醇制成配制質(zhì)量濃度分別為0.013 4、0.026 8、0.053 6、0.107 2、0.214 4、0.428 8 mg/mL的溶液,按色譜條件,分別進樣檢測,以質(zhì)量為橫坐標(),峰面積為縱坐標(),繪制標準曲線并進行線性回歸,得到線性回歸方程(=2461+4.05)、=0.999 9。結果表明內(nèi)標物質(zhì)在線性范圍(0.067~2.144 μg)內(nèi)與峰面積呈良好的線性關系。
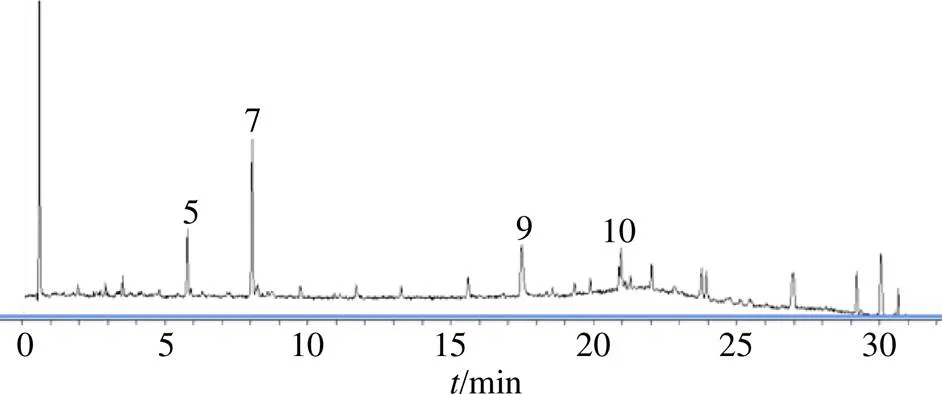
圖4 側柏葉負離子模式總離子流圖

表4 正、負離子模式特征峰化學成分解析結果
S該化合物是由對照品進行指認
SThis compound was identified using reference standards
2.5.2 精密度試驗 同“2.2.2”項下方法,計算槲皮苷相對峰面積RSD不高于1.50%,表明儀器精密度良好。
2.5.3 穩(wěn)定性試驗 同“2.2.3”項下方法,計算槲皮苷相對峰面積RSD不高于1.66%,表明供試品溶液在24 h內(nèi)穩(wěn)定。
2.5.4 重復性試驗 同“2.2.4”項下方法,計算槲皮苷相對峰面積RSD值不高于1.9%,表明方法重復性良好。
2.5.5 加樣回收率試驗 精密稱定側柏葉藥材粉末6份,分別精密加入槲皮苷對照品適量,按“2.1.1”項下方法制備供試品溶液,按“2.1.2”項下色譜條件,分別進樣檢測,計算得到柚皮苷的平均加樣回收率為99.67%,RSD為1.06%。
2.5.6 耐用性試驗 精密吸取同一供試品溶液,考察不同規(guī)格的色譜柱(Agilent poroshell 120 SB-C18、Agilent poroshell 120 EC-C18)、不同的高效液相色譜儀(Agilent-1260Ⅱ高效液相色譜儀、Agilent-1290型高效液相色譜儀)、不同柱溫(25、30、35 ℃)及不同流速(0.6、0.8、1.0 mL/min)對檢測結果的影響。結果顯示,指認出的4個化學成分的相對保留時間的RSD均小于1.92%,相對峰面積的RSD均小于1.07%,表明該方法的耐用性良好。
2.5.7 含量測定 根據(jù)《中國藥典》2020版?zhèn)劝厝~“含量測定”項下方法檢測,所有供試品均能符合藥典規(guī)定(槲皮苷不得少于0.10%)。7號峰“槲皮苷”為《中國藥典》2020版中側柏葉“含量測定”項下的指標之一,該峰分離效果好、保留時間穩(wěn)定居中、標準品價格低廉,故以其作為內(nèi)標物質(zhì),開展基于內(nèi)標物質(zhì)的特征峰化學成分相對定量研究。取供試品藥材,按“2.2.1”項下方法制備供試品溶液,按“2.1.2”項下色譜條件分析測定槲皮苷含量,每個供試品平行3份,結果見表5。每個供試品中特征峰化學成分的相對含量計算公式如下:
特征峰相對含量=特征峰峰面積×(槲皮苷含量/槲皮苷峰面積)
取“平均數(shù)-標準差”作為特征峰化學成分相對于內(nèi)標物質(zhì)化學成分的相對含量下限,供試藥材根據(jù)此方法測得的特征峰相對含量不低于該含量下限[13],結果見表6。
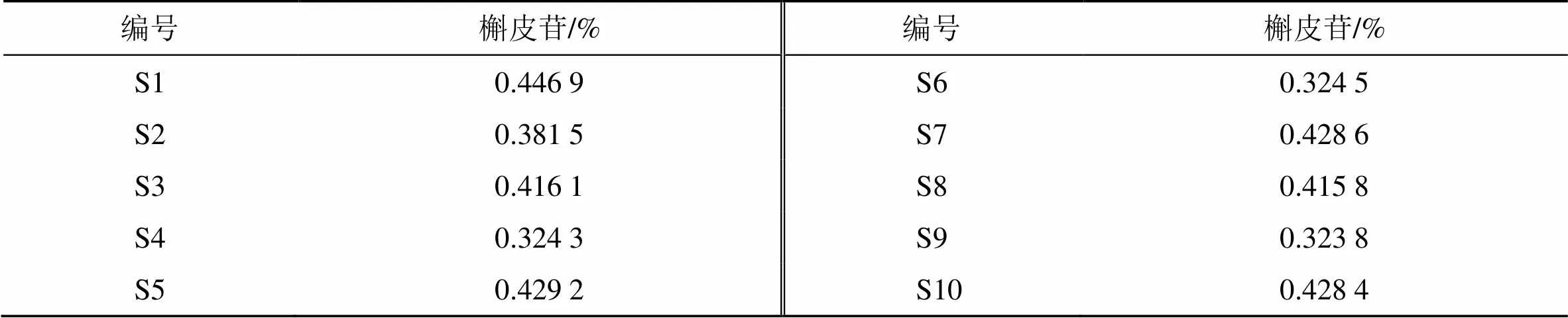
表5 內(nèi)標物質(zhì)槲皮苷的準確定量結果(n=2)
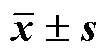
表6 基于內(nèi)標物質(zhì)的特征峰相對定量結果(, n = 3)
3 討論
中藥在我國已有數(shù)千年發(fā)展歷史,是我國傳統(tǒng)醫(yī)藥的重要組成部分。中藥質(zhì)量是保證中藥臨床應用安全、有效的前提,但在對中藥進行質(zhì)量控制的過程中存在基原復雜、不同批次樣品中成分差異大等問題,使中藥質(zhì)量難以保證均一穩(wěn)定。目前,《中國藥典》2020年版中質(zhì)量控制項對多成分指標進行測定的中藥品種已有上百種,且有些對照品價格昂貴,加大了企業(yè)生產(chǎn)和民眾的用藥成本。
為解決以上問題,本研究創(chuàng)新研究思路,不依賴多種對照品,以價格低廉易獲得的對照藥材為基準物質(zhì)的定性和不依賴多種對照品定量的側柏葉藥材“質(zhì)-量”雙標控制方法。通過構建側柏葉對照藥材及10個不同產(chǎn)地側柏葉供試藥材的特征圖譜,以對照藥材為基準物質(zhì),評價對照藥材和供試藥材特征峰的相似度,可以用于判斷側柏葉藥材的真?zhèn)危础百|(zhì)”;同時準確定量1種內(nèi)標物質(zhì)化學成分,計算側柏葉藥材其余各特征峰的相對含量,確定的各特征峰相對含量的下限能夠區(qū)分側柏葉藥材優(yōu)劣,即“量”。本研究所提出的側柏葉藥材的“質(zhì)-量”控制方法能夠有效判斷藥材的真?zhèn)蝺?yōu)劣,形成一個科學、可控的中藥質(zhì)量控制體系,旨在為中藥質(zhì)量控制和中藥產(chǎn)業(yè)持續(xù)發(fā)展提供探索性解決方案。
本研究將與對照藥材分離度和相似度良好、信噪比大于10作為特征峰的選取依據(jù),共確定了11個特征峰。采用質(zhì)譜技術指認出的側柏葉特征峰化學成分的基本母核為2-苯基色原酮[14-15]。扁柏雙黃酮對腫瘤細胞具有抑制作用[16];穗花杉雙黃酮具有抗金葡萄球菌作用[17];槲皮苷、楊梅苷與側柏葉的止血效果息息相關[18]。上述化學成分被認為是側柏葉中的主要活性成分,能全面科學地反映中藥側柏葉的內(nèi)在質(zhì)量[19]。
本實驗所收集的市面所售不同產(chǎn)地供試品,旨在建立基于“質(zhì)-量”雙標的側柏葉質(zhì)量分析方法,所收集的側柏葉供試藥材與側柏葉對照藥材的相似度均大于0.90[20],說明所收集的側柏葉供試藥材的特征峰化學成分基本一致,但僅采用10批不同產(chǎn)地的藥材規(guī)定特征峰相對含量下限,缺乏全面性,因此,需要更進一步大量收集不同產(chǎn)地、不同批次的藥材,完善該套方法,以期有效判斷藥材的真?zhèn)蝺?yōu)劣,形成一個科學、可控的中藥質(zhì)量控制體系,在滿足藥材多項質(zhì)量控制項的同時減輕企業(yè)需大量購買對照品的經(jīng)濟壓力,推動中醫(yī)藥事業(yè)可持續(xù)發(fā)展。
利益沖突 所有作者均聲明不存在利益沖突
[1] 張娟, 劉美, 李先寬, 等. 側柏葉的本草考證 [J]. 中國現(xiàn)代中藥, 2017, 19(9): 1318-1321.
[2] 陳志安, 吳芳. 以側柏葉為主治療咳嗽 [J]. 中醫(yī)臨床研究, 2013, 5(3): 87.
[3] 石典花, 張軍, 張樂林, 等. 不同采集季節(jié)、地點側柏葉飲片質(zhì)量考察及藥典相關標準的商榷 [J]. 時珍國醫(yī)國藥, 2017, 28(9): 2124-2127.
[4] 潘憲偉, 趙余慶. 側柏葉和果實中黃酮類和萜類物質(zhì)的現(xiàn)代藥學研究進展 [J]. 中草藥, 2012, 43(8): 1641-1646.
[5] 劉晨, 柳佳, 張麗, 等. 側柏葉炮制前后對血熱復合出血模型大鼠的止血作用比較 [J]. 中草藥, 2014, 45(5): 668-672.
[6] 石典花, 戴衍朋, 蘇本正, 等. 側柏葉“炒炭存性”科學內(nèi)涵初探 [J]. 中草藥, 2020, 51(23): 5963-5971.
[7] 張俊飛, 孫廣璐, 張彬, 等. 側柏葉藥理作用的研究進展 [J]. 時珍國醫(yī)國藥, 2013, 24(9): 2231-2233.
[8] 孟麗娟, 程松, 潘英妮, 等. HPLC法同時測定側柏葉中楊梅苷等4種黃酮的含量 [J]. 沈陽藥科大學學報, 2014, 31(2): 107-111.
[9] 梁統(tǒng), 覃燕梅, 梁念慈. 側柏葉醇提取物抗炎作用的研究 [J]. 中國藥科大學學報, 2001, 32(3): 224-226.
[10] 李遠輝, 文全泰, 張照平, 等. 側柏葉多糖的提取及其抗氧化活性的研究 [J]. 中國中醫(yī)藥科技, 2016, 23(1): 40-42.
[11] 姬翔宇, 張子雯, 陳姿伊, 等. 一測多評法同時測定雷公藤藥材及制劑雷公藤多苷片中7個質(zhì)控成分 [J]. 中草藥, 2022, 53(17): 5338-5347.
[12] 馮媛, 郭龍, 常雅晴, 等. 基于指紋圖譜和多成分含量測定的關黃柏及川黃柏差異性研究 [J]. 中草藥, 2022, 53(16): 5179-5184.
[13] 王夢林, 巴寅穎, 武秋紅, 等. 基于有效基準特征圖譜質(zhì)量表征的中藥荷葉質(zhì)量評價研究[J]. 環(huán)球中醫(yī)藥, 2022, 15(6): 40-948.
[14] 宗珊珊, 蘇本正, 石典花, 等. 側柏葉HPLC指紋圖譜建立及4種成分測定 [J]. 中成藥, 2019, 41(1): 114-118.
[15] 單鳴秋, 錢雯, 高靜, 等. UPLC-MS分析側柏葉中黃酮類化合物 [J]. 中國中藥雜志, 2011, 36(12): 1626-1629.
[16] 穆婉, 程學芳, 張雪, 等. 扁柏雙黃酮對肝細胞癌HepG2細胞增殖和凋亡的影響 [J]. 中南藥學, 2019, 17(3): 399-404.
[17] 蘇立燕. 穗花杉雙黃酮作為金黃色葡萄球菌MgrA抑制劑對小鼠肺炎的治療作用 [D]. 長春: 吉林大學, 2021.
[18] 石典花, 戴衍朋, 王麗鳳, 等. 基于UHPLC-QTOF-MS/MS辨識的側柏葉炒炭前后化學成分分析 [J]. 中國實驗方劑學雜志, 2021, 27(8): 107-116.
[19] 苗慧. 側柏葉的化學成分及藥理活性研究 [D]. 長春: 吉林農(nóng)業(yè)大學, 2018.
[20] 張智, 龍華, 曾羅, 等. 不同產(chǎn)地杜仲雄花指紋圖譜的建立及其化學模式識別研究 [J]. 中草藥, 2022, 53(22): 7207-7213.
Research on quality analysis method ofbased on “quality-quantity” double standard
YU Hao1, LI Tian-jiao1, 2, 3, BAO Yong-rui1, 2, 3, WANG Shuai1, 2, 3, MENG Xian-sheng1, 2, 3
1. College of Pharmacy, Liaoning University of Traditional Chinese Medicine, Dalian 116600, China 2. Liaoning Multi-dimensional Analysis of Traditional Chinese Medicine Technical Innovation Center, Dalian 116600, China 3. Liaoning Modern Traditional Chinese Medicine Research and Engineering Laboratory, Dalian 116600, China
To establish a “quality-quantity” double standard control method for Cebaiye(), which is qualitative based on the reference traditional Chinese medicinal materials (TCMM) as standard substances and quantitative without relying on multiple reference substances.HPLC technology was used to establish the characteristic chromatogram ofbased on the reference TCMM as standard substances. The chemical constituents of common peaks were identified by Q-TOF-MS technology, and the authenticity ofwas determined by the similarity of characteristic peaks of the reference TCMM and the tested TCMM. The above statement is “quality”. The relative content of each characteristic peak in different batches of the tested TCMM was calculated by accurate quantition of internal standard component naringin. The “average value-standard deviation” was taken as the lower limit of the relative content of characteristic peak chemical components relative to chemical composition of internal standard substance, and the quality ofwas determined according to the lower limit of the relative content of characteristic peak. The above statement is “quantity”.The characteristic chromatogram and content determination method met the requirements of methodology investigation. A total of 11 common chromatographic peaks were determined, and four chemical components were identified, which were myricetin, quercitrin, amentoflavone, hinokiflavone. The similarity between the tested TCMM and reference TCMM was greater than 0.90. The lower limit of relative content of chemical components ofcharacteristic peak was defined.The method can judge the authenticity of medicinal materials clearly and quickly without many reference substances, and provide reference for quality control of.
(L.) Franco; reference traditional Chinese medicinal materials; quality control; characteristic chromatogram; myricetin; quercitrin; amentoflavone; hinokiflavone
R286.2
A
0253 - 2670(2023)22 - 7319 - 06
10.7501/j.issn.0253-2670.2023.22.007
2023-05-06
遼寧省重點研發(fā)計劃項目(2020JH2/10300088):基于中醫(yī)典籍的經(jīng)典名方槐花散藥學研究
于 浩,男,碩士研究生,主要從事藥物分析研究。Tel: 18742572751 E-mail: y18742572751@163.com
通信作者:孟憲生,男,博士生導師,主要從事藥效物質(zhì)組學和作用機制整合研究。E-mail: mxsvvv@126.com
[責任編輯 時圣明]