替雷利珠單抗聯合培美曲塞、順鉑化療在晚期肺癌患者中的應用效果分析
王子慧,王永,王漢林
(1.蘭陵縣人民醫院腫瘤化療科,山東臨沂 277700;2.蘭陵縣人民醫院心內科,山東臨沂 277700)
肺癌是臨床常見惡性腫瘤,早期患者多無明顯癥狀,隨著病情進展,會出現呼吸困難、咳血等癥狀,此時病情多處于晚期,已失去最佳手術時機[1]。化療是晚期肺癌的首選方案,可殺死癌細胞,預防疾病進展,對延長患者生存期具有一定價值,但化療過程中會對正常組織細胞造成一定損傷,導致療效降低、免疫功能下降等,增加復發、轉移風險[2]。近年來,隨著靶向治療技術的持續發展,臨床發現腫瘤細胞轉移、復發與免疫逃逸能力緊密相關, 免疫治療愈發受到臨床重視。替雷利珠單抗是一種PD-1 抑制劑,可與腫瘤細胞表面PD-L1 結合,阻斷內源性PD-L1、PD-1 結合,以降低腫瘤細胞免疫力,現已在食管癌、肝細胞癌等治療中廣泛應用,但對于其在晚期肺癌患者中的應用效果尚需進一步研究[3]。 基于此,本研究選擇2020 年10月—2022 年12 月蘭陵縣人民醫院收治的92 例晚期肺癌患者為對象, 分析替雷利珠單抗聯合培美曲塞、順鉑化療的臨床效果。 現報道如下。
1 資料與方法
1.1 一般資料
選擇蘭陵縣人民醫院收治的晚期肺癌患者92 例為研究對象。納入標準:符合《中華醫學會肺癌臨床診療指南(2018 版)》[4]肺癌的診斷標準;腫瘤分期Ⅲ~Ⅳ期;凝血功能均正常;精神無障礙。 排除標準:合并其他惡性腫瘤者;存在急慢性感染者;合并肝、腎等器質性疾病者;對本研究所用藥物不耐受者。 本研究獲院醫學倫理委員會審批,患者、家屬均簽署同意書。按照隨機數字表法分為對照組和觀察組,各46 例。對照組男25 例,女21 例;年齡52~75 歲,平均年齡(63.54±3.61)歲;腺癌27 例,鱗癌19 例;腫瘤分期Ⅲ期30例,Ⅳ期16 例。觀察組男26 例,女20 例;年齡50~78歲,平均年齡(63.61±3.65)歲;腺癌25 例,鱗癌21 例;腫瘤分期Ⅲ期28 例,Ⅳ期18 例。兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性。
1.2 方法
1.2.1 對照組
對照組采用培美曲塞(湖南科倫制藥有限公司,國藥準字H20223539,規格:100 mg)、順鉑(齊魯制藥有限公司,國藥準字H20213819,規格:50 mL:50 mg)化療。化療第1 d,靜脈滴注培美曲塞500 mg/(m2?d);化療第1~3 d,靜脈滴注順鉑25 mg/(m2?d),化療前將培美曲塞、 順鉑溶于100 mL 0.9%氯化鈉注射液(陜西誠信制藥有限公司, 國藥準字H61023395,規格:100 mL:0.9 g)稀釋,滴注時間≥30 min,以21 d 為一個化療周期,共治療4 個周期。
1.2.2 觀察組
于對照組基礎上,觀察組聯合替雷利珠單抗(廣州百濟神州生物制藥有限公司,國藥準字S20190045,規格:100 mg/瓶)治療,200 mg/次,將其溶于200 mL 0.9%氯化鈉溶液中,進行靜脈滴注,第1 次滴注時間≥60 min,若患者耐受良好,后續滴注時間≥30 min即可,以21 d 為一個治療周期,共治療4 個周期。
1.3 觀察指標
(1)臨床療效。完全緩解(CR):患者經治療,腫瘤病灶完全消失,未出現新病灶。 部分緩解(PR):患者經治療,病灶最長徑總和減少幅度≥30%。穩定(SD):患者經治療,病灶最長徑總和減少幅度<30%,或增加幅度<20%。 進展(PD):患者經治療,病灶最長徑總和減少幅度≥20%,或出現新病灶。總有效率=(CR+PR)/總例數×100%。(2)腫瘤標志物。治療前后,抽取患者5 mL 空腹肘靜脈血,離心分離血清,通過酶聯免疫法檢測血清癌胚抗原 (CEA)、 細胞角蛋白19 片段(CYFRA21-1)、糖類抗原125(CA125)。 (3)免疫功能。 治療前后,抽取患者5 mL 空腹肘靜脈血,采用流式細胞儀(深圳邁瑞生物醫療電子股份有限公司,粵食藥監械20142400295,型號:BriCyte E6)檢測T 淋巴細胞亞群(CD3+、CD4+、CD8+)水平。 (4)不良反應。統計兩組惡心、貧血、疲乏、甲狀腺功能異常、皮疹等發生情況。
1.4 統計方法
采用SPSS 20.0 統計學軟件進行數據分析。 計數資料用[n(%)]表示,組間比較采用χ2檢驗;計量資料以(x依s)表示,組間比較采用t檢驗。P約0.05 為差異有統計學意義。
2 結 果
2.1 兩組臨床療效比較
觀察組治療總有效率高于對照組,差異有統計學意義(P<0.05)。 見表1。

表1 兩組晚期肺癌患者臨床療效比較[n(%)]
2.2 兩組腫瘤標志物水平比較
治療前,兩組腫瘤標志物水平比較,差異無統計學意義(P>0.05);治療后,觀察組CEA、CYFRA21-1、CA125 水平均低于對照組,組間差異有統計學意義(P<0.05)。 見表2。
表2 兩組晚期肺癌患者腫瘤標志物比較(±s)
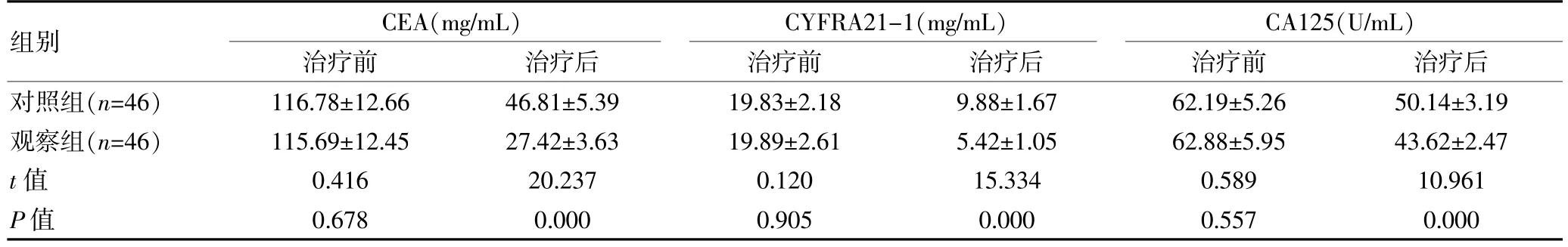
表2 兩組晚期肺癌患者腫瘤標志物比較(±s)
組別CEA(mg/mL)治療前治療后CYFRA21-1(mg/mL)治療前治療后CA125(U/mL)治療前治療后對照組(n=46)觀察組(n=46)t 值P 值116.78±12.66 115.69±12.45 0.416 0.678 46.81±5.39 27.42±3.63 20.237 0.000 19.83±2.18 19.89±2.61 0.120 0.905 9.88±1.67 5.42±1.05 15.334 0.000 62.19±5.26 62.88±5.95 0.589 0.557 50.14±3.19 43.62±2.47 10.961 0.000
2.3 兩組免疫功能比較
治療前,兩組免疫功能比較,差異無統計學意義(P>0.05);治療后,觀察組CD3+、CD4+水平均高于對照組,CD8+水平低于對照組, 組間差異有統計學意義(P<0.05)。 見表3。
表3 兩組晚期肺癌患者免疫功能比較[(±s),%]
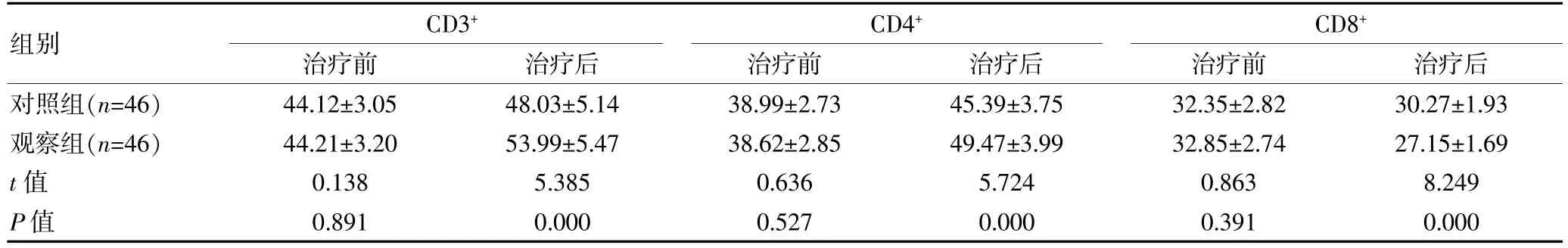
表3 兩組晚期肺癌患者免疫功能比較[(±s),%]
組別CD3+治療前治療后CD4+治療前治療后CD8+治療前治療后對照組(n=46)觀察組(n=46)t 值P 值44.12±3.05 44.21±3.20 0.138 0.891 48.03±5.14 53.99±5.47 5.385 0.000 38.99±2.73 38.62±2.85 0.636 0.527 45.39±3.75 49.47±3.99 5.724 0.000 32.35±2.82 32.85±2.74 0.863 0.391 30.27±1.93 27.15±1.69 8.249 0.000
2.4 兩組不良反應發生情況比較
對照組治療期間出現惡心3 例、貧血3 例、疲乏2 例、甲狀腺功能異常2 例、皮疹3 例,不良反應發生率為28.26%;觀察組治療期間出現惡心4 例、貧血4例、疲乏3 例、甲狀腺功能異常3 例、皮疹2 例,不良反應發生率為34.78%。兩組不良反應發生率對比,差異無統計學意義(χ2=0.453,P=0.501)。
3 討 論
肺癌是起源于肺部支氣管黏膜或腺體的惡性腫瘤,病因未明,臨床認為與吸煙、職業暴露、空氣污染等因素均相關,近年來發病率逐漸上升,嚴重威脅患者生命安全[5]。晚期肺癌患者病情較重,已錯過最佳手術時機,多采用化療治療,培美曲塞、順鉑是臨床常用化療方案,培美曲塞能夠催化葉酸多谷氨酸轉換為多聚谷氨酸鹽,使胸苷酸合成酶活性降低,拮抗葉酸生成,有效抑制腫瘤細胞繁殖;順鉑可損傷腫瘤細胞,促使腫瘤細胞DNA 變異,進而抑制其復制功能[6-7]。 然而,近年來臨床研究發現,腫瘤進展、轉移與免疫功能密切相關,免疫治療逐漸成為腫瘤研究的新方向。
CEA 是廣譜腫瘤標志物,在多種惡性腫瘤中均有表達;CYFRA21-1 在上皮細胞中廣泛存在,肺癌患者體內呈高表達水平;CA125 為非特異性腫瘤標志物,其水平變化可預測晚期肺癌患者生存期[8]。 本研究結果顯示,觀察組治療總有效率高于對照組,治療后CEA、CYFRA21-1、CA125 水平均低于對照組,CD3+、CD4+水平均高于對照組,CD8+水平低于對照組(P<0.05),兩組不良反應比較,差異無統計學意義(P>0.05),提示在晚期肺癌患者中采用替雷利珠單抗聯合培美曲塞、順鉑化療治療對降低血清腫瘤標志物水平、改善免疫功能效果顯著,且安全性高。其原因為PD-1 是免疫球蛋白家族成員,存在于激活T 細胞、B細胞中,能夠穩定機體正常免疫機制,防止發生免疫性疾病;PD-L1 作為PD-1 配體, 與PD-1 結合會阻滯招募蛋白酪氨酸酶-1,使下游信號通路受阻,影響細胞因子釋放,最終導致T 細胞失活。 替雷利珠單抗屬于PD-1 抑制劑,能夠阻斷腫瘤細胞PD-L1、PD-1結合,促進T 細胞增殖與分化,進而有效改善T 淋巴細胞亞群值,增強患者免疫功能[9-10]。 同時,替雷利珠單抗能夠提高T 細胞對腫瘤病灶的識別能力,增強其殺傷作用,從而提高抗腫瘤效果,降低血清腫瘤標志物水平。
綜上所述,替雷利珠單抗聯合培美曲塞、順鉑化療治療晚期肺癌患者效果顯著,能夠降低血清腫瘤標志物水平,改善免疫功能,且具有較高安全性。

