經皮耳迷走神經電刺激聯合經顱直流電刺激對腦卒中患者上肢功能的影響
王利凱,蕭禹,王立童
腦卒中是導致我國中老年人殘疾和死亡的首要因素,隨著醫療技術的進步,發病率和患病率逐年升高,且腦卒中患者致殘率極高,對康復的需求日益增加[1]。上肢功能恢復是腦卒中各種功能障礙康復的重點,對患者的功能獨立性至關重要[2]。隨著神經康復理念的發展,中樞干預技術在卒中康復中越來越不可或缺,已成為神經康復領域的關鍵技術。
經皮耳迷走神經電刺激(transcutaneous auricular vagus nerve stimulation,taVNS)作為一種無創神經刺激技術,通過電極刺激耳甲區激活基底核釋放神經遞質,增加神經可塑性,在改善腦卒中上肢功能康復中仍處于探索階段。由于其刺激效應存在時間依賴性,目前國內外研究多將taVNS與其他干預方法聯合使用,并已取得明顯的療效[3]。而經顱直流電刺激(transcranial direct current stimulation,tDCS)是一種非侵入性的腦功能刺激技術,利用恒定、低強度的直流電刺激干預大腦,通過提高患側或降低病灶對側大腦半球的興奮性改善半球間抑制失衡狀態,已作為腦卒中康復的一種治療策略[4]。目前,將這兩種干預方法聯合治療用于腦卒中治療的研究較少,故本研究采用taVNS聯合tDCS治療腦卒中偏癱患者,觀察其對上肢運動功能及日常生活能力的影響,現報道如下。
1 資料與方法
1.1 一般資料 收集2022年5月~2023年3月在大連醫科大學附屬第二醫院康復醫學科住院的腦卒中患者44例。納入標準:符合《中國各類主要腦血管診斷要點2019》有關腦卒中診斷標準[5],并經CT或MRI檢查證實;初次發病,單側肢體偏癱,病程2周~3個月;年齡25~80歲;Brunnstrom上肢運動功能分期≥2期;排除標準:既往有精神障礙、癲癇病史者;患視覺障礙、失語癥或癡呆者;簡易精神狀態評價量表評分(mini-mental state examination,MMSE)<17分;患有其他可能影響評估的神經性疾病、肌肉骨骼疾病者;合并心腦血管、消化系統、內分泌系統等疾病者;不宜接受耳部刺激者,如耳廓有感染、潰瘍或瘢痕者;不宜接受腦部刺激者,如顱內有金屬置入物、腦部有痛覺過敏、損傷或者炎癥;心率低于60次/min;體內裝有心臟起搏器、人工耳蝸等設備者;既往接受迷走神經手術或者顱內有金屬者。本研究方案通過大連醫科大學附屬第二醫院倫理委員會審批(倫審2023第058號)。所有受試者知曉本研究方案,并簽署知情同意書者。采用信封法患者隨機分為對照組和觀察組,每組22例。2組患者一般資料比較差異均無統計學意義。見表1。

表1 2組一般資料比較
1.2 方法 所有患者均接受藥物治療、物理治療、作業治療、針灸等常規康復訓練, 1次/d, 60min/次,5次/周,治療3周。對照組在常規治療的基礎上采用經顱直流電治療儀行經顱直流電刺激(transcranial direct current stimulation,tDCS)治療,在常規康復訓練之前30min進行。陽極刺激病灶側M1區,陰極刺激病灶對側眼眶上緣,選擇直流電刺激模式,電流強度為2.0mA,1次/d,30min/次,5次/周,治療3周[6]。觀察組患者在對照組治療的基礎上再進行taVNS,taVNS在tDCS治療前30min進行[3]。taVNS療法是通過低頻脈沖電刺激儀裝置實施的,該裝置連接2個電極(直徑5mm×5mm圓形金屬電極),將左耳耳甲區用酒精搽拭干燥后,放置電極于耳甲區的耳穴心、腎位置,見圖1。電刺激的頻率和脈沖寬度分別設置為25Hz和300μs,每個刺激持續30s,間歇30s,采用雙相正弦脈沖[7]。刺激電流從最低強度開始,逐漸增加,直到患者感覺到疼痛,將最終電流調整到略低于疼痛閾值。1次/d,30m in/次,5次/周,治療3周。
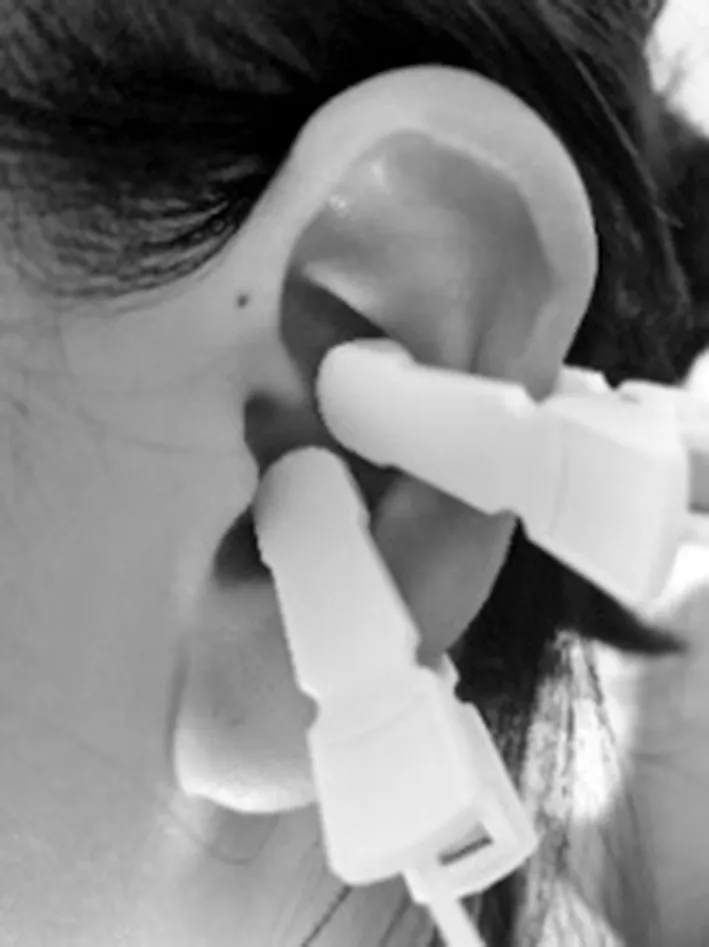
圖1 taVNS電極刺激部位
1.3 評定標準 治療前后對2組患者進行以下評定:①皮質潛伏期(cortical latency,CL)檢測[8]:選用經顱磁刺激儀,將參考電極貼于患側上肢拇短展肌肌腱,表面電極貼于拇短展肌處,地線電極片粘貼于腕部,電極片粘貼部位皮膚給予酒精脫脂處理以免產生干擾偽跡,選擇直徑70mm的“8”字形線圈,以80%運動閾值(motor thresshold,MT)磁刺激病灶側M1區,觸發后記錄運動誘發電位(motor evoked potential,MEP),選擇重復性好、波幅大的5條波形,測定MEP潛伏期并計算平均值,即為CL,反映大腦皮質手功能區的興奮性水平,CL縮短代表大腦皮質運動區到手的神經傳導功能變好[9]。②中樞運動傳導時間(central moter conduction time,CMCT)檢測:將經顱磁線圈放置在第7頸椎棘突處棘突旁(偏患側肢體),重復上述操作,記錄拇短展肌MEP。選擇5個具有重復性好、波幅大的波形,測定MEP潛伏期并計算平均值,即為脊髓潛伏期,反映脊髓水平的上肢運動神經傳導功能。皮質潛伏期與脊髓潛伏期的差即為CMCT,以評估神經脈沖從大腦皮質傳到脊髓的速度,CMCT縮短代表皮質脊髓束傳導功能好轉[10]。③上肢運動功能評定:采用Fugl-Meyer運動評定量表上肢部分(Fugl-Meyer assessment-upper extremity,FMA-UE)進行評分,該量表總分為66分,分數越高,表示上肢運動功能越好[11]。 ④日常生活活動能力評定:選用改良Barthel量表(Modified Barthel index,MBI)進行評分,滿分100分,得分越高表明患者日常生活能力越強[12]。⑤安全性指標監測:試驗組患者每次治療前后測量血壓,并用指脈氧夾監測心率;治療結束后詢問患者有無不適癥狀。
2 結果
2.1 2組患者治療前后CL、CMCT比較 治療3周后,2組患者CL、CMCT均較治療前減少(均P<0.05),觀察組CL、CMCT明顯低于對照組(均P<0.05)。見表2。
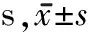
表2 2組患者治療前后CL、CMCT比較
2.2 2組患者治療前后FMA-UE、MBI評分比較 治療3周后,2組患者FMA-UE、MBI評分均較治療前增加(均P<0.05),觀察組FMA-UE、MBI評分均高于對照組(均P<0.05)。見表3。
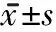
表3 2組患者治療前后FMA-UE、MBI評分比較 分,
2.3 治療過程中安全性指標 本試驗過程中,僅觀察組有1名患者出現耳甲區輕微瘙癢,未見泛紅等,治療結束后自行消失,其余患者均未出現耳廓局部疼痛、過敏、惡心、頭痛不適癥狀以及血壓心率明顯波動等反應。
3 討論
腦卒中后上肢往往會出現運動障礙、感覺障礙、疼痛和痙攣等不適癥狀,降低了日常生活能力,嚴重影響患者的生存質量。在上肢功能障礙的恢復過程中,各種功能障礙相互影響,所以對康復治療的干預方式提出了更高的要求[13]。“神經閉環”理論在傳統常規康復訓練基礎上引入中樞干預手段,是腦卒中上肢功能康復的重要理論[14]。不同于常規康復訓練,中樞干預技術通過調節大腦皮層興奮性或調控中樞神經元活動,改善大腦可塑性,以實現更加精準和有效的治療,逐漸成為腦卒中上肢功能恢復的重要手段[15]。
tDCS是一種非侵入性的神經調節技術,已經被廣泛研究和應用于腦卒中患者上肢功能康復[16]。tDCS通過在頭皮表面施加微弱電流來影響腦神經元的興奮性,從而促進運動功能的恢復。研究表明,tDCS能夠顯著提高腦卒中患者的上肢功能,改善運動靈敏度、協調性和手部功能[17]。tDCS可結合康復訓練使用,如手部功能訓練、肌肉電刺激、傳統物理治療等,能夠獲得更好的效果,且先進行tDCS再進行其他干預技術可能更優于同步進行[18]。一項網狀Meta分析顯示,在陽極、陰極、雙極3種經顱直流電刺激方案中,陽極刺激對腦卒中上肢偏癱患者的干預效果更佳[19]。因此,本試驗選用了先進行tDCS,且陽極刺激M1區,以期實現對上肢功能更加高效精準的康復。
近年來,taVNS成為治療腦卒中各種功能障礙康復的新方向[20]。耳廓上有豐富的神經末梢,而迷走神經大多分布在耳甲區,刺激迷走神經可以產生遠距離的治療效果。一些研究表明,taVNS與其他干預技術聯合使用,在腦卒中的上肢功能康復治療中的有效性得到了驗證[19-21]。這可能是因為taVNS可激活基底核,釋放乙酰膽堿和去甲腎上腺素神經遞質,從而實現大腦皮層的廣泛激活,增強大腦神經可塑性[22]。taVNS可以促進神經細胞的再生和重構,從而促進神經系統的恢復和康復。特別的是,皮層可塑性的觸發是受外界干預驅動的神經元特有的能力[23]。因此,taVNS和其他干預技術協同作用于多種神經途徑,增強運動皮層中與特定任務相關的神經可塑性,從而促進運動功能的恢復。taVNS作為一種新的治療方法,刺激部位、刺激參數尚無統一規范,其具體的應用場景和療效還需要更多的臨床研究來驗證和探究[3]。本研究參考目前大多數試驗參數設置,通過先taVNS預刺激后再進行tDCS,將taVNS與tDCS結合以增強M1區興奮性,以期優化卒中后肢體功能障礙干預方案。
本研究發現,治療3周后,2組患者CL、CMCT較治療前減少,且觀察組低于對照組;FMA-UE、MBI評分均較治療前增加,且觀察組高于對照組。表明tDCS、tDCS聯合taVNS均能促進腦卒中偏癱患者上肢功能和日常生活能力的恢復。在常規訓練基礎上輔以tDCS及taVNS聯合治療,能進一步促進腦卒中上肢功能和日常生活能力的恢復,有利于患者早日回歸家庭及社會。研究顯示,tDCS和taVNS協同刺激大腦反應,激活強度大于tDCS,可以喚起一系列皮質和皮質下大腦區域的激活,tDCS結合taVNS可能更具有調節腦網絡的潛力,是因為taVNS可能會將大腦活動調節到tDCS更容易工作的狀態[24]。此外,一項tDCS和taVNS組合對工作記憶影響的研究發現,與tDCS和taVNS的數值求和相比,組合技術具有更強的調節作用,特別是在改善一致性方面,使其具有了重要的臨床意義[25]。本研究將兩種無創性技術tDCS與taVNS相結合,采用taVNS刺激耳甲區無創性激活迷走神經,使用tDCS刺激上肢功能腦區M1區,通過兩種不同的作用機制,實現廣泛激活與精準刺激結合,相互補充相得益彰,為非侵入性神經調控治療手段提出了新的思路[21]。
在安全性方面,與tDCS類似,taVNS也是一種無創性調控技術,本研究選用了低頻25Hz、左側耳甲等常規參數,以避免右側耳甲迷走神經激活竇房結引起心動過緩[26]。盡管卒中患者合并癥較多,但是在研究過程中患者未有明顯的不適癥狀。在研究設置上,根據目前已發表的文獻來看,選用非同步協同治療項目較多[3]。本研究為充分保證試驗安全性和試驗嚴謹性,使taVNS在tDCS之前進行,以避免同步進行增強效應可能造成的風險,但是在保證安全的前提下,同步進行的有效性是否更強,刺激部位、持續時間、脈沖頻率等參數設置是否最佳仍值得進一步探索。
綜上所述,對于腦卒中上肢功能的恢復,taVNS與tDCS的協同刺激可能是一種有效的治療方法,可以更有效改善腦卒中上肢功能,提高日常生活能力,改善生活質量,同時減少不良反應的發生率。本研究的樣本量和觀察指標有限,仍需要大樣本多中心試驗,聯合治療最佳方案也仍需要進一步探索,以期未來規范地指導臨床應用。

