GnRHa黃體支持在IVF/ICSI-ET中的應用
王飛 曾湘暉
正常的黃體功能是妊娠成功的保證。控制性超促排卵(COH)作為輔助生殖技術(ART)的關鍵環節,通過藥物刺激多個卵泡同時發育并成熟,從而獲得多個卵和較高質量胚胎, 增加受孕率。育齡期女性在自然月經周期中,黃體功能不全(luteal phase defect,LPD)發生率為3%~10%,但在COH中,LPD則幾乎為100%[1]。通常因為在卵巢排卵后,出現黃體早退的現象,根本無法分泌夠劑量的孕激素,內膜分泌反應性因此出現延遲,未達到與胚胎發育徹底的同步,影響妊娠結局。迄今為止,臨床上對于行黃體支持藥物種類、劑量、劑型以及使用方案未達成統一共識。常用的黃體支持的藥物主要人絨毛膜促性腺激素(human chorionic gonadotropin,HCG)、P、雌激素(estradiol,E)。黃體酮直接使用或與HCG和E聯合使用是最常用的方案。使用促性腺激素釋放激素激動劑(gonadotropin releasing hormone agonist,GnRHa)行黃體支持治療,以期有效改善妊娠結局,其有效性和安全性正處于不斷探究過程中。國外有研究表明,GnRHa有類似避孕藥作用,可引發黃體溶解,不利于胚胎種植[2]。Balasch等[3]發現黃體中期添加GnRHa,妊娠率不僅沒有降低,反而胚胎著床率較前升高,猜測GnRHa可能通過刺激促黃體生成素(basal luteinizing hormone,LH)的作用,改善妊娠結局。2015年國內專家共識中首次提到,GnRHa作為新增黃體支持的藥物備選藥物之一,肯定了其療效,該藥物可通過增強黃體功能,明顯提升了胚胎植入成功率,從而改善妊娠結果[4]。一項研究發現黃體期添加GnRHa增加出生率、多胎率,有助于妊娠,且拮抗劑方案中效果更優[5]。近年來,GnRHa也被用于黃體支持,但因機制尚不明確,仍存在爭議。因此本課題擬探討在拮抗劑新鮮胚胎移植黃體期,于常規黃體支持(黃體酮+芬嗎通)基礎上添加不同劑量GnRHa對ART妊娠結局的影響,為有效標準提供參考。
1 資料與方法
1.1 一般資料 收集2020年1月至2023年2月于我院生殖中心行體外受精(in vitro fertilization-embryo transfer,IVF)/卵泡漿內單精子注射(intracytoplasmic sperm injection,ICSI)拮抗劑方案鮮胚移植314例患者臨床資料。該研究項目已于2021年10月通過人類遺傳資源與醫學倫理審查(2021SQCJ4499)與我院醫學倫理審查(2021-64),患者簽署了知情同意書。采用前瞻性對照臨床試驗,研究在拮抗劑新鮮胚胎移植黃體期于常規黃體支持(黃體酮+芬嗎通)基礎上再行添加不同劑量GnRHa,對ART妊娠結局的影響,按劑量依次分為A組:未添加GnRHa 95例;B組:添加0.1 mg GnRHa 92例;C組:添加0.3 mg GnRHa 55例;D組:添加0.4 mg GnRHa 72例。4組患者男女年齡、不孕年限、不孕類型、BMI、AMH、 AFC、FSH、LH、E2差異均無統計學意義(P>0.05)。見表1。
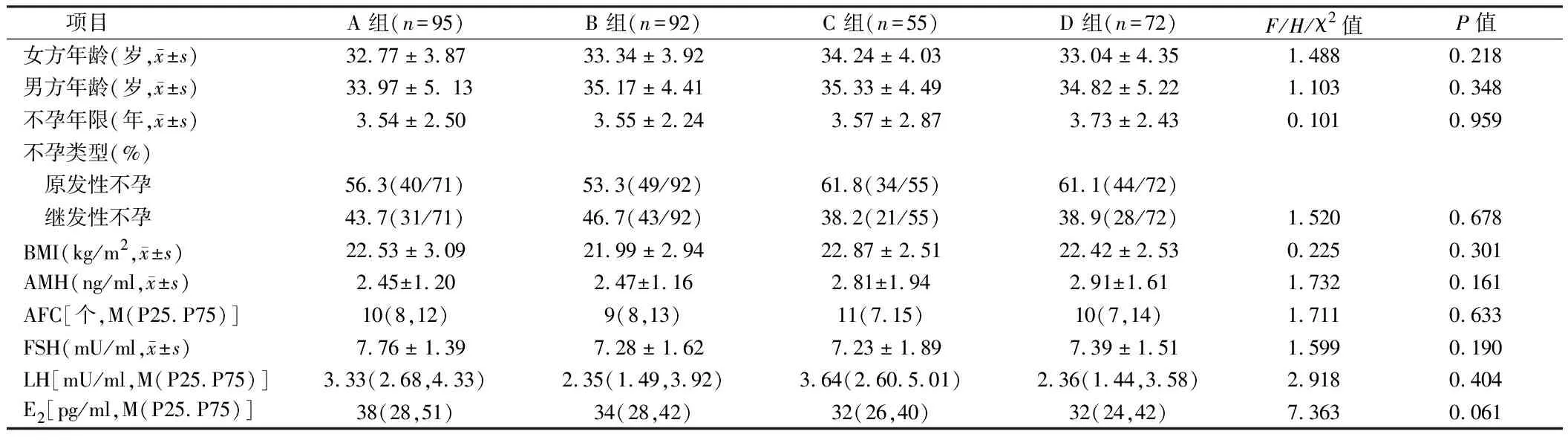
表1 4組患者一般情況比較
1.2 納入與排除標準
1.2.1 納入標準:①年齡20~40歲;②基礎促卵泡激素(FSH)<10 U/mL;③抗苗勒管激素(anti-Mullerian hormone,AMH)≥1.2 μg/L;④體重指數(Body mass index,BMI)正常;⑤移植周期數≤2,鮮胚移植胚胎為卵裂期胚胎(D3),且至少一個優質,且移胚總數≤3個;⑥拮抗劑方案,進行控制性超促排卵。
1.2.2 排除標準:①子宮器質性疾病(子宮肌瘤、子宮畸形、內膜息肉、內異癥、宮腔粘連等);②新鮮胚胎移植周期HCG日,患者血清孕酮值≥1.52 ng/ml;移植日B超示子宮內膜厚度<7 mm;③輸卵管中重度積水、輸卵管倒流、卵巢過度刺激綜合征(OHSS);④內分泌及代謝性疾病(如多囊卵巢刺激癥(PCOS)、甲亢、甲減、高泌乳素血癥等);⑤IVF/ICSI-ET禁忌證;⑥未簽署知情同意書的患者。
1.3 COH方案 使用拮抗劑方案,月經第2~3天測血FSH、LH、E2、P,依據性激素水平、竇卵泡數(basal antral follicle count,AFC)及大小決定是否開始啟動FSH,根據患者的卵巢功能(AFC和AMH)、年齡、BMI決定啟動劑量。當主導卵泡直徑達到12~14 mm時,根據LH值,決定是否使用GnRH-ant(思則凱,默克雪蘭諾,法國)0.25 mg/d,規律監測B超和血清E2、LH、P的激素水平變化情況。當雙側卵泡直徑>17 mm的數量>3 h,再根據患者血清中各性激素水平,選擇艾澤250 μg板機或雙扳機:注射用人絨毛促性腺激素(HCG,安徽豐原藥業)2 000 U+注射用醋酸曲普瑞林(達必佳,德國輝凌)0.2 mg。扳機后36 h B超檢查開始取卵,并在取卵的當天啟動黃體支持。取卵日取精,行IVF或ICSI常規體外受精,移植第3天卵裂期胚胎數目≥1個,至少有一個優質胚胎,對符合條件的剩余卵裂胚進行囊胚培養,并行囊胚冷凍保存。
1.4 鮮胚常規黃體支持方案 自取卵日開始,通過肌內注射提供黃體酮40 mg*1次,此后黃體酮60 mg(黃體酮軟膠囊600 mg/d,陰道放置,移植日給予芬嗎通(黃片2 mg/d,Abbott Biologicals B.V.),直至移植后14 d,妊娠者維持至移植后8~10周。
1.5 添加GnRHa的黃體支持方案 A組:常規黃體支持;B組:添加0.1 mg GnRHa,在常規黃體(地屈孕酮+芬嗎通)支持基礎上,取卵后第6天(移植后3 d)皮下注射0.1 mg GnRHa(醋酸曲普瑞林,0.1 mg/支,達必佳,德國輝凌);C組:添加0.3 mg GnRHa:(在常規黃體支持基礎上,分別于取卵第2、5、8天單次皮下注射0.1 mg GnRHa);D組:添加0.4 mg GnRHa,(在常規黃體支持基礎上,分別于取卵第2、4天單次皮下注射0.2 mg GnRHa)。移植后14 d測定血β-HCG,妊娠者維持至移植后8~10周。
1.6 胚胎移植 鮮胚取卵后72 h進行移植,移植胚胎為卵裂期胚胎(D3),至少一個優質,移胚總數≤3個。
1.7 觀察指標及隨訪 主要指標:種植率、臨床妊娠率、多胎率、早期流產率;次要指標:男女雙方年齡、不孕年限、不孕類型、BMI、AMH、AFC、bFSH、bLH、bE2、HCG日LH、E2、P水平及內膜厚度、獲卵數、MⅡ卵數、總受精數、卵裂數、2PN數、優質胚胎率、優質D3胚胎數、可利用D3胚胎數、囊胚形成數、優質囊胚數、移植日內膜厚度、平均移植胚胎數等。隨訪:于移植后14 d對血液中的β-HCG進行檢測,35 d B超可見孕囊和胎心跳動提示為臨床妊娠。
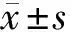
2 結果
2.1 4組促排卵情況 4組為IVF受精方式,HCG日LH、E2、P水平比較,差異均無統計學意義(P>0.05)。見表2。
2.2 4組實驗室數據及胚胎發育情況比較 4組患者在獲卵數、MⅡ數、總受精數、卵裂數、2PN數、優質D3胚胎數、可利用D3胚胎數、囊胚形成數、優質囊胚數比較差異無統計學意義(P>0.05)。見表3。
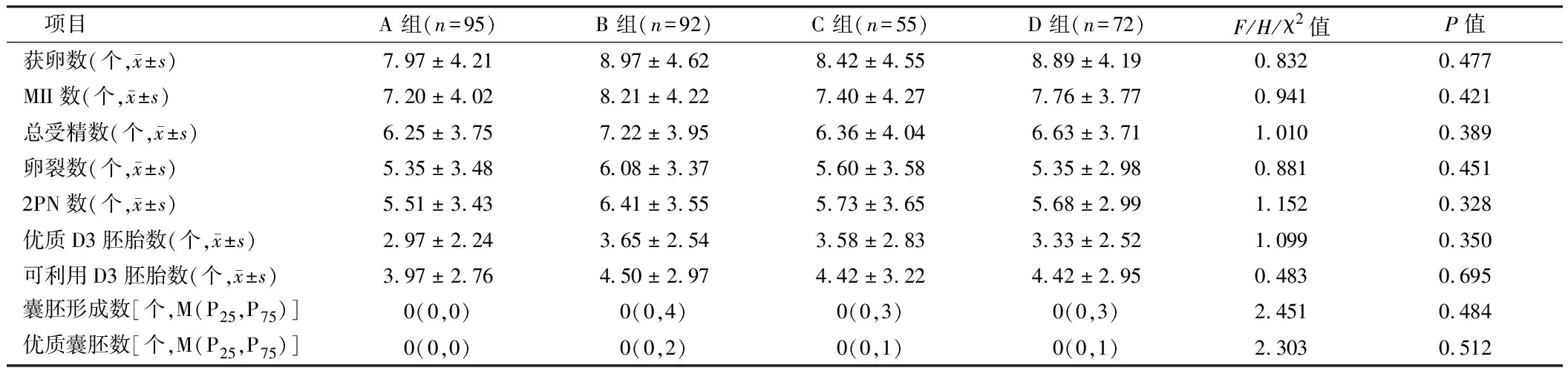
表3 4組患者實驗室數據及胚胎發育情況比較
2.3 4組患者妊娠結局情況比較 4組患者在胚胎種植率、早期流產率、多胎率等方面差異均無統計學意義(P>0.05),A組妊娠率低于B、C、D組,差異有統計學意義(P<0.05)。見表4。
2.4 與臨床妊娠結局有關的單因素分析 根據患者是否發生臨床妊娠,分為臨床妊娠組與非臨床妊娠組。2組在男女雙方年齡、不孕年限、不孕類型、 BMI、AMH、AFC、bFSH、bLH、bE2、HCG日LH、E2、P水平及內膜厚度水平方面差異均無統計學意義(P>0.05)。2組在獲卵數、MⅡ卵數、總受精數、卵裂 數、2PN數、優質D3胚胎數、可利用D3胚胎數、囊胚形成數、優質囊胚數、移植日內膜厚度等方面差異無統計學意義(P>0.05)。臨床妊娠組的平均移植胚胎數、GnRHa黃體支持占比均高于非臨床妊娠組(P<0.05)。見表5。
表5 臨床妊娠結局相關指標單因素分析
2.5 與臨床妊娠結局有關因素的Logistic回歸分析 將P值≤0.05的變量納入回歸分析模型。Logistic回歸分析結果發現:平均移植胚胎數對臨床妊娠結局影響具有統計學意義(P<0.05);GnRHa黃體支持占比對臨床妊娠結局影響具有統計學意義(P<0.01)。排除混雜因素后發現添加GnRHa、移植胚胎數均是影響拮抗劑方案鮮胚移植患者臨床妊娠結局的關鍵因素。見表6。

表6 臨床妊娠結局相關指標Logistic回歸分析
3 討論
3.1 GnRHa的結構及發揮黃體功能的機制 GnRHa是GnRH第6、10位的氨基酸替換形成的新型結構更穩定且半衰期更長的十肽化合物,同時其與GnRH受體親和力增加100~200倍。GnRH通過垂體門脈系統,作用于垂體前葉產生FSH和LH,而GnRHa通過持續性分泌,消耗了大量的GnRH受體,導致垂體脫敏,抑制了LH的產生,對黃體功能造成影響,同時也影響了子宮內膜的容受性。
GnRHa對于黃體支持的有效性和安全性的作用原理尚不清楚,可能與其多種不同作用機制有關。在現階段認為GnRHa用于黃體支持的可能機制為以下幾個方面:(1)GnRHa刺激垂,E、P分泌增多,接近于自然周期,更有利于妊娠的發生和維持。另外,GnRHa可能通過對黃體施加直接作用來產生雌孕激素。(2)研究發現人類胚胎、胎盤滋養層細胞及子宮內膜都有GnRHa受體mRNA,黃體期給藥GnRHa能加速已種植的胚胎產生HCG,有益于早期胎兒發育[6]。(3)釋放LH可以促進子宮內膜細胞血管生長因子,以及與胚胎種植有關的細胞因子的表達,從而有利于胚胎的著床和發育[7]。(4)GnRHa可明顯減低NK細胞的毒性,提高免疫功能,具有更有利于胚胎移植環境[8]。
3.2 添加GnRHa黃體支持在拮抗劑方案鮮胚移植周期中的作用 本研究中使用拮抗劑方案行鮮胚移植患者,在常規黃體支持方案中添加不同劑量(0.1 mg、0.3 mg、0.4 mg)GnRHa組的臨床妊娠率(61.96%,63.63%,62.50%)均明顯高于未添加GnRHa組(44.21%)。而添加不同劑量(0.1 mg、0.3 mg、0.4 mg)GnRHa種植率(39.77%,40.00%,36.59%)、早期流產率(14.04%,11.76%,11.11%),相較于未添加GnRHa組種植率(33.89%)、早期流產率(14.29%),雖無統計學差異,但種植率均有一定程度升高,早期流產率有下降的趨勢。
本研究結果提示,在拮抗劑方案鮮胚移植周期中,常規黃體支持(地屈孕酮+芬嗎通)的基礎上,加用GnRHa能明顯提高臨床妊娠率,改善妊娠結局,但添加3種不同劑量GnRHa的患者妊娠結局也略有差別。綜合本研究對使用不同劑量GnRHa的妊娠結局考慮,分別于取卵第2 d、5 d、8天單次皮下注射0.1 mg GnRHa,總劑量達0.3 mg時,種植率和臨床妊娠率在3組中效果最佳,這與曲丹妮等[9]研究結果相似,持續間斷給予GnRHa可改善ART妊娠結局。其可能原因為GnRHa雖抑制內源性的LH峰,但半衰期短,作用時間不長,僅可持續24~36 h,且取卵后6 d為體內黃體的最低期,加用GnRHa可再次刺激垂體LH的分泌,及時挽救了內源性黃體,安全并有效地發揮了黃體支持的作 用,對妊娠結局起到了積極的作用。
Oliveira等[10]發現拮抗劑方案加用GnRHa后,臨床結局的各項指標(種植率和臨床妊娠率)均有大幅度的升高。國內近期也有研究顯示,行IVF/ICSI患者,加用1次0.1 mg GnRHa(曲普瑞林)也顯著改善了妊娠結局[11],且有大樣本數據結果顯示,在低反應人群(FSH<8 mU/mL)中添加0.1 mg GnRHa,也達到了相同的效果[12]。一項納入行拮抗劑方案鮮胚移植的328周期ICSI患者的研究提示,于相同時機添加相同劑量GnRHa,提示添加GnRHa并未提高胚胎種植率、臨床妊娠率[13],與本研究結論不一致。分析其可能原因:雖抑制效應能快速消去,但黃體中期僅僅只是注射0.1 mg GnRHa刺激黃體,劑量太小,產生的孕酮未達到能發揮黃體支持的生理劑量的閾值,發揮效果顯微。有國外Meta分析顯示多劑量的GnRHa使用的活產率較單劑量高[14]。因此國內外學者研究多劑量的GnRHa黃體支持對妊娠結局的影響。
Qublan等[15]研究顯示移植著床率、臨床妊娠率、活產率也顯著升高。Aboulghar 等[16]發現不會提升繼續妊娠和臨床妊娠的機率,妊娠結局無影響。國外有RCT顯示選擇ICSI患者,分別移植日后3 d皮下注射1次1 mg GnRHa(亮丙瑞林100例),與移植日后第3、6天各注射1次(100例)比較,發現添加1次與2次妊娠結局無差異,且與未添加組相較,多胎率明顯升高[17]。因此可推測認為單次與多次添加GnRHa無差異,反而增加多胎率。各項研究的得出結論不一,但其研究報道少,周期數少,缺乏強有力臨床實驗數據反復驗證,因而對GnRHa用于黃體支持用法劑量存在爭議。
3.3 拮抗劑鮮胚移植周期中添加GnRHa的安全性 GnRHa的黃體支持作用可能有利于妊娠發生,但胚胎移植以后使GnRHa是否對母兒有不良影響,增加胎兒畸形的發生。理論上GnRHa半衰期較短,當皮下注射0.1 mg GnRHa后,其生物有效性大約持續24 h,可及時排泄。用藥后發生妊娠,此時的胚胎則不受GnRHa影響。
近年國外有研究指出,拮抗劑方案中添加GnRHa增加多胎妊娠的發生率[18]。國內余璐萍等[5]亦得到了相同的結果,添加GnRHa組的多胎率高于未添加組。李潔等[19]研究顯示,在移植后0、2 d分別添加GnRHa各0.1 mg,結果提示2組的自然流產率無差異,且出生的嬰兒中無畸形兒,表明GnRHa應用于拮抗劑方案的黃體期是相對安全的。國內前瞻性研究在黃體支持基礎上持續間斷皮下注射GnRHa,發現添加多劑量GnRHa長期隨訪安全性良好[9]。
國外前瞻性對照研究中顯示,于贈卵周期ICSI后的第6天注射單劑量的0.1 mg GnRHa,并未增加流產率[8],這與本研究的結論相一致。另有研究納入120例子宮內膜厚度不超過7 mm的患者,在GnRHa添加組中,內膜增厚的速度比常規黃體支持組更快,同樣胚胎種植率和臨床妊娠率亦有明顯提升[15]。在卵巢低反應(FSH<8 mU/mL)患者中也得出相同的結論[12]。還有學者發現,對第1次IVF失敗者,根據標準黃體支持方案取卵開始,連續14 d每日持續0.1 mg GnRHa注射,比OPU后6 d注射1次GnRHa更有效,多劑量組能取得較好的妊娠結局,可顯著提高妊娠率和活產率,提高妊娠率及活產率,且安全持久[20]。
既往研究發現,黃體期給藥GnRHa提示還未見能直接引起神經系統,消化系統和泌尿系統的損傷,進而導致胎兒畸形的發生,但并不排除不影響早期胚胎發育的可能性[8, 21]。國外研究表示,黃體期加入GnRHa,具有重要臨床價值[22],今后需進一步跟蹤調查其圍產期結局、胎兒神經系統、先天畸形等問題安全性。
目前大多數研究顯示鮮胚移植黃體中期添加GnRHa有利于臨床妊娠結局,且合適并安全的多劑量間斷給藥在胚胎著床率及臨床妊娠率方面效果較優,但添加時機及劑量尚無明確規定,且GnRHa用量超出安全范圍會導致垂體功能受到抑制,GnRHa黃體支持作用不僅無法發揮,反而帶來弊端[23-25]。目前國內進行的相關研究方法,多為取卵后第6天添加0.1 mg GnRHa。臨床上多根據經驗用藥,此時醫生更應熟練掌握藥物適應證及禁忌證,給ART助孕患者獲得良好結局打下基礎。
綜上所述,在黃體期加入GnRHa的拮抗劑方案中,可以改善此方案新鮮移植周期的妊娠結果。采用GnRHa扳機聯合黃體期應用,以增強黃體支持作用,降低OHSS的發生機率也是可行的。內膜較薄、反復IVF/ICSI-ET失敗的患者,贈卵周期等均可將于黃體期添加GnRHa作為黃體支持新型選擇。考慮到拮抗劑鮮胚添加GnRHa可能增加多胎率的風險及添加多劑量的效果更優,因此可相對減少移植胚胎的數量,增加GnRHa的劑量,從而降低多胎率,改善妊娠結局。

