實時心肌超聲造影結合二維應變評價急性心肌梗死介入術后心肌灌注與收縮功能
焦曉芳, 劉楠楠, 周微微, 李 陽, 王艷秋, 李貴申
北部戰區總醫院 心血管內科,遼寧 沈陽 110016
急性心肌梗死(acute myocardial infarction,AMI)是心血管疾病中最為嚴重的病癥之一,其高患病率、高病殘率和高病死率嚴重危害人類的生命安全[1-2]。目前,臨床上治療AMI最重要的措施之一是再血管化治療,經皮冠狀動脈介入(percutaneous coronary intervention,PCI)已經成為治療AMI最有效的方法之一[3]。已有研究證實,急診PCI術可以減輕左心室重構,提高患者存活率,改善遠期預后[2]。PCI術后對微循環灌注進行正確、有效的評價對治療及診斷具有重要意義。本研究旨在探討應用心肌超聲造影(myocardial contrast echocardiography,MCE)及二維應變成像(2-dimensional strain,2DS)評估PCI術后心肌梗死患者微循環灌注及左室收縮功能的變化。現報道如下。
1 對象與方法
1.1 研究對象 選取自2021年6月至2022年12月北部戰區總醫院胸痛中心收治的108例急性前壁心肌梗死患者為研究對象,排除26例存在其他冠狀動脈血管狹窄>50%的患者,22例失訪無法采集后期超聲參數的患者,2例透聲條件差不能完成圖像分析的患者,最終納入患者58例,其中,男性38例,女性20例;年齡35~81歲,平均年齡(59.8±9.5)歲。納入標準:(1)發病時間<12 h,心電圖ST段抬高>2 mm,肌鈣蛋白升高并行直接經皮冠狀動脈介入(primary percutaneous coronary intervention,PCI)術的AMI患者;(2)經冠狀動脈造影術確診為左前降支重度狹窄>90%并在狹窄處成功實施冠狀動脈支架置入,術后遠端血流達到心肌梗死溶栓試驗(thrombolysis test for myocardial infarction,TIMI)血流分級3級,余冠狀動脈動脈血管狹窄<50%的患者;(3)術后1周內完成MCE檢查,能完整清晰地顯示各節段心肌灌注情況的患者。排除標準:(1)透聲條件差,不能完成圖像分析及術后失訪的患者;(2)陳舊性心肌梗死、支架病史、嚴重瓣膜病變、先天性心臟病、心律失常、心肌病、重度肺動脈高壓的患者;(3)增強劑、白蛋白及其他血液制品過敏,過敏體質及嚴重肝功能不全的患者;(4)支架術后遠端血流未達到TIMI 3級的患者。所有患者檢查前均簽署知情同意書。本研究經醫院倫理委員會批準。
1.2 研究方法
Philips EPIQ 7C彩色多普勒超聲診斷儀,S5-1探頭,頻率1.0~5.0 MHz,內配有心肌聲學及2DS顯像程序軟件,并安裝Qlab 10.5工作站。
1.2.1 圖像采集 受試者取左側臥位,平靜呼吸連接同步導聯心電圖。依據美國超聲心動圖委員會推薦指南[4]測量二維超聲心動圖常規參數:左心室舒張末期內徑(left ventricular end diastolic dimension,LVDD)及左室射血分數(left ventricular ejection fraction,LVEF)。2DS記錄心尖四腔心、心尖三腔心及心尖兩腔心切面各3個心動周期動態圖像,儲存后脫機分析。MCE檢查,檢查前簽署知情同意書,建立靜脈通道,選用六氟化硫(聲諾維)增強劑,生理鹽水稀釋至5 ml,將機器設置為MCE模式,激活極低機械指數(指數<0.20)進行心肌造影,以1.0 ml/s速度勻速推注2.0~3.5 ml增強劑,隨后同樣速度推入生理鹽水5.0 ml,造影劑充盈均勻后應用高機械指數(MI 0.9)破壞心肌內微泡,再轉為低機械指數觀察心肌血流再灌注情況。連續采集包括爆破之前5個心動周期及之后15個心動周期的心尖四腔心、心尖三腔心及心尖兩腔心切面圖像,存儲脫機分析。
1.2.2 圖像分析 為保證研究結果的真實性及可靠性,在未知患者臨床資料的條件下,由兩名經驗豐富的超聲醫師依據超聲協會推薦的左心室17節段劃分法[4]對存儲圖像進行分析。2DS圖像分析啟用Qlab分析軟件,進入CMQ界面,分析心尖四腔、心尖三腔及心尖兩腔切面,選取二尖瓣前瓣瓣環、后瓣瓣環和心尖部3點,機器自動勾畫心內膜區域,手動微調,2DS軟件自動生成所追蹤心肌節段的應變曲線,將左室按基底段、中間段及心尖段共分為17節段,記錄心肌各節段的收縮期縱向峰值應變及左心室整體縱向應變(global longgitudinai strain,GLS)。MCE圖像分析,通過視覺目測法半定量評估室壁心肌灌注:1分,灌注良好,對比劑分布均勻;2分,灌注減弱、延遲,對比劑分布不均勻;3分,無灌注,對比劑缺損。
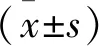
2 結果
2.1 心肌造影灌注結果 58例急診AMI患者支架術后均完成心肌造影檢查,其中,灌注良好22例(灌注良好組),灌注減弱19例(灌注減弱組),無灌注17例(無灌注組)。見圖1~3。

圖1 MCE檢查左室短軸顯示心肌灌注良好
2.2 3組間PCI術后1周內與術后3個月LVDD、LVEF、GLS比較 術后3個月,灌注良好組、灌注減弱組的LVEF、GLS均高于術后1周內,差異有統計學意義(P<0.05);灌注良好組、灌注減弱組的LVDD均低于術后1周內,但差異無統計學意義(P>0.05);無灌注組的LVEF、GLS均低于術后1周內,LVDD高于術后1周內,但差異均無統計學意義(P>0.05)。術后3個月,心肌灌注良好組的LVEF、GLS高于灌注減弱組和無灌注組,且灌注減弱組的LVEF、GLS高于無灌注組,差異均有統計學意義(P<0.05)。見表1。
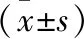
表1 3組間PCI術后1周內與3個月的LVDD、LVEF、GLS比較
3 討論
AMI發生后,心肌細胞在缺血、缺氧時間>6 h會出現壞死,心肌梗死發生12 h內為開通梗死相關動脈恢復動脈灌注挽救心肌細胞的最佳時機[5]。急診PCI是治療AMI的首選治療措施之一,但血管再通術后即使冠狀動脈造影檢查顯示冠狀動脈大血管已無狹窄,仍有30%的患者心肌缺乏再灌注[6],即部分AMI患者即使有效開通了心外膜大血管,若微循環完整性受損,遠端微血管仍無血液流入或血流緩慢,出現無再流現象[6],血管痙攣、血栓栓塞、炎癥細胞及壞死組織均可能導致開通血管無再流現象。冠心病患者再灌注治療的目的不是單純地恢復冠狀動脈血流,而是對有壞死風險的心肌進行完全和持續的再灌注[7]。
MCE是一種能實現在微循環水平觀察心肌及心內膜下灌注的新技術[8],其利用微氣泡作增強劑觀察某一區域心肌微循環的灌注情況,可用于檢測存活心肌與壞死心肌,MCE已成為研究AMI后冠狀動脈微循環再灌注的主要方法之一[9],尤其實時心肌造影能清晰地顯示各節段心肌灌注情況。MCE為預測微循環再灌注治療的成功與否提供了有用的信息,從而預測該區域心肌收縮功能恢復的潛能[10],為臨床判斷AMI患者術后左室功能恢復程度及臨床預后提供有價值的參考指標。2DS是一種無創性超聲檢查分析新技術,通過檢測單位時間內的心肌變形快速測量應變和應變率等值來反映心肌本身的組織特性和功能改變,能準確地反映局部心肌運動[11-12],定量評價心肌功能,更敏感地識別心肌功能異常[13]。
本研究聯合運用MCE與2DS兩種技術,探討AMI患者PCI術后心肌灌注水平預測心肌收縮功能恢復程度的可行性,應用MCE半定量評價AMI患者支架術后1周內的心肌灌注水平,并應用2DS對患者術后心肌收縮功能進行定量追蹤復查,GLS數值為負值,負值絕對值越大代表心肌應變越大,收縮功能越好,目前,正常心肌GLS尚無統一標準,本研究將GLS≤-20%[11]考慮為正常心肌。本研究所入選的患者為單支前降支冠狀動脈狹窄,避免了多支血管病變及陳舊性病變心肌低灌注對左室收縮功能及心肌應變恢復的影響。
本研究結果顯示,術后3個月,灌注良好組、灌注減弱組的LVEF、GLS均高于術后1周內,差異有統計學意義(P<0.05);灌注良好組、灌注減弱組的LVDD均低于術后1周內,但差異無統計學意義(P>0.05);無灌注組的LVEF、GLS均低于術后1周內,LVDD高于術后1周內,但差異均無統計學意義(P>0.05)。術后3個月,心肌灌注良好組的LVEF、GLS高于灌注減弱組和無灌注組,且灌注減弱組的LVEF、GLS高于無灌注組,差異均有統計學意義(P<0.05)。本研究結果提示,AMI患者術后心肌灌注水平直接影響患者心肌收縮功能恢復,心肌微循環灌注不足越嚴重,左心功能恢復越差;術后灌注水平越好,收縮功能恢復程度越高;心肌低灌注、無灌注與心肌持續缺血、梗死區擴大、心臟重塑的發生密切相關[14]。雖然,無復流心肌仍具備收縮功能恢復潛能,但心肌低灌注及無灌注仍是導致急診PCI術后患者不良預后的關鍵,因此,PCI術后應用MCE早期發現心肌低灌注及無灌注者,為臨床早進行藥物干預治療及治療方案的制定提供有價值的參考指標,為患者遠期預后提供預測參考。
本研究存在不足之處,患者例數較少,隨訪時間較短,后續將進一步擴大樣本量,延長隨訪時間。MCE半定量目測法很大程度上依賴患者的圖像質量及超聲醫師的經驗。2DS機器自動追蹤,手動微調存在一定的誤差。
綜上所述,MCE在評價AMI后心肌存活及預測心肌收縮功能恢復中起著重要作用,通過MCE定性、半定量分析,可以直觀、快捷地觀察節段性心肌灌注情況,AMI患者PCI術后心肌灌注情況可以反映心肌功能恢復情況,2DS可以定量評估整體及局部心肌收縮功能。

