骨質疏松椎體壓縮骨折患者MRI脂肪量化結果對經皮椎體成形術術后再骨折的預測價值
白賀威,曹晗
(1.漯河市婦幼保健院 放射科,河南 漯河 462000;2.漯河市第六人民醫院 放射科,河南 漯河 462000)
骨質疏松椎體壓縮骨折(osteoporotic vertebral compression fractures,OVCF)是中老年群體發生骨折的常見類型之一,臨床多采用經皮椎體成形術(percutaneous vertebroplasty,PVP)治療,此術式具有微創、操作簡單、安全性高、療程短等優點,可改善患者病情。但有研究指出,PVP術后患者再骨折發生風險仍高達10%~30%,一旦發生,患者的身體、心理遭受再次打擊,影響患者疾病治療積極性[1-2]。因此,做好早期PVP術后再骨折風險預測對改善患者預后尤為重要。研究發現,低骨量雖然是發生脆性骨折的重要指標,但仍有部分骨礦密度(bone mineral density,BMD)正常患者發生脆性骨折[3]。有研究證實,骨強度不僅與BMD有關,還取決于骨髓質量,隨著骨髓脂肪含量的升高骨強度也會逐漸降低[4]。近年來,磁共振成像(magnetic resonance imaging,MRI)脂肪量化技術應用逐漸廣泛,在評估腹部器官病變中有良好的評估價值[5]。基于此,本研究通過MRI技術量化椎體脂肪含量,并分析其對OVCF患者PVP術后再骨折的預測價值。
1 對象和方法
1.1 研究對象
前瞻性納入2020年3月至2022年3月漯河市婦幼保健院收治的OVCF患者為研究對象,本研究方案經醫院醫學倫理委員會批準。納入標準:(1)符合《骨質疏松性椎體壓縮性骨折的治療指南》[5]中OVCF診斷標準,并經影像學檢查確診;(2)新鮮椎體骨折;(3)有PVP手術適應證。排除標準:(1)合并椎體腫瘤,曾接受化療;(2)合并嚴重甲狀腺疾病、糖尿病等內分泌、代謝性疾病和肝、腎疾病;(3)合并爆裂性骨折;(4)存在麻醉禁忌或手術相關禁忌。
根據上述標準共納入2020年3月至2022年3月醫院收治的148例OVCF患者,其中男57例,女91例,年齡45~72歲,平均(57.89±5.23)歲;體重指數(body mass index,BMI)21.8~26.6 kg·m-2,平均(23.94±1.88)kg·m-2;椎體骨折階段T1129例,T1222例,L144例,L228例,L325例。
1.2 方法
1.2.1MRI脂肪量化檢測
患者取仰臥位,采用西門子MAGNETOM ESSENZA 1.5 T及CTL線圈進行掃描,掃描序列包括腰椎常規序列及矢狀位IDEAL-IQ序列,序列參數TR設置為6.4 ms,TE設置為Min full,NEX設置為0.5,FOV設置為25.0 cm×25.0 cm,層厚設置為10 mm,帶寬設置為111.11 kHz,層間距設置為0.5 mm,反轉角設置為40°,矩陣設置為256×256,共掃描38 s,掃描后生成的脂肪分數圖輸入AW 4.6工作站,對L1~4錐體的骨髓脂肪含量進行檢測,選擇錐體松質骨最大區域進行測量,面積293~329 mm2,避開骨皮質、終板、椎間盤以及解剖異常區域,在影像圖上勾選長方形感興趣區域,測量脂肪含量(fat fraction,FF),由兩名經驗豐富的放射科醫生進行3次重復測量,并取其平均值為最終結果。
1.2.2PVP術后再骨折判定
對患者PVP術后進行隨訪6個月,期間腰背部再次出現疼痛,在翻身時疼痛加劇,疼痛可向胸前、腹前區以及下肢放射,經影像檢查確診椎體骨折的患者納入發生組,其余則納入未發生組。
1.2.3臨床指標檢測
(1)BMD測量。采用雙能X線吸收計量檢測BMD,采用HOLOGIC Horizon W(S/N303039M)測量儀對L1~4椎體前后位進行掃描,去除骨折的椎體,獲得BMD。(2)骨形代謝標志物檢測 術前采集患者靜脈血3 mL,抗凝離心后,取上層血清,使用BIOBASE1000全自動酶免分析儀,采用酶聯免疫吸附法檢測血清骨鈣素(bone-γ-carboxyglutamic acid-containing protein,BGP)、骨特異性堿性磷酸酶(bone alkaline phosphatase,BALP)、Ⅰ型膠原交聯氨基末端肽(cross linked N-telopeptide of typeⅠcollagen,NTXⅠ)及Ⅰ型膠原交聯羧基端肽(cross linked C-telopeptide of typeⅠcollagen,CTXⅠ)水平。
1.3 統計學方法

2 結果
2.1 OVCF患者PVP術后再骨折情況
PVP術后隨訪6個月發現,OVCF患者中有30例患者出現再骨折,占比20.27%,納入發生組;118例患者未出現再復發,占比79.73%,納入未發生組。
2.2 一般資料
兩組患者年齡、性別、BMI等比較,差異無統計學意義(P>0.05)。見表1。

表1 兩組一般資料比較
2.3 FF、BMD水平及骨代謝指標
兩組術前BALP、NTXⅠ、CTXⅠ水平比較,差異無統計學意義(P>0.05);發生組患者術前FF、BMD、BGP水平高于未發生組,差異有統計學意義(P<0.05)。見表2。
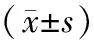
表2 兩組FF、BMD水平及骨代謝指標比較
2.4 OVCF患者PVP術后再骨折影響因素logistic回歸分析
將OVCF患者PVP術后再骨折的發生情況作為因變量(未發生=0,發生=1),將表2中差異有統計學意義的指標(FF、BMD、BGP)作為自變量,進行logistic回歸分析,結果顯示,BMD是OVCF患者PVP術后再骨折發生的保護因素(OR<1,P<0.05),FF是OVCF患者PVP術后再骨折發生的危險因素(OR>1,P<0.05)。見表3。

表3 OVCF患者PVP術后再骨折影響因素logistic回歸分析
2.5 術前FF水平預測OVCF患者PVP術后再骨折的ROC曲線分析
將OVCF患者PVP術后再骨折的發生情況作為狀態變量(未發生=0,發生=1),術前FF水平作為檢驗變量。繪制ROC曲線,結果顯示,術前FF水平預測OVCF患者PVP術后再骨折的AUC>0.7,具有一定預測價值。見表4。

表4 術前FF水平預測OVCF患者PVP術后再骨折的價值分析結果
3 討論
PVP治療可明顯改善OVCF患者骨折癥狀,恢復骨折椎體高度,但有研究發現,OVCF患者PVP術后的2~4個月的再骨折發生率達到10%~30%[6-7]。本研究中對OVCF患者PVP術后隨訪6個月發現,有30例患者出現再骨折,占比20.27%,與上述研究結果基本一致。對此,針對OVCF患者,在其行PVP手術治療后仍需要警惕術后再骨折的發生。因此,臨床尋找有效預測OVCF患者PVP術后再骨折的指標,對改善患者預后具有重要意義。
有研究顯示人體中的成骨細胞活性隨著年齡的增長而逐步下降,破骨細胞活性則升高,導致機體骨礦鹽的含量減少,造成骨退化及骨強度下降[8]。本研究結果顯示,術前BMD、BGP水平水平在OVCF患者PVP術后再骨折發生密切相關。分析原因在于,BMD是臨床用來確定骨質疏松相關的骨折發生風險的常規指標,在BMD水平較低時,患者的骨脆性較大,進而導致鄰近脊柱和椎體發生骨折,增加再骨折的發生風險[9-10]。BGP是成骨細胞分泌的非膠原蛋白,具有促進非結晶鈣磷酸鹽向羥磷灰石轉化的功能,進而有提高骨強度的作用,當其水平降低時,不利于骨的修復和在重建[11]。但上述指標預測PVP治療后復發存在特異性,故需尋求其他指標。
MRI中IDEAL-IQ技術是在IDEAL技術上改良3D掃描序列,通過采集不同TE時間的回波信號,獲得六組圖像信息,以此評估機體組織脂肪含量,并可通過脂肪比像進行定量分析,進而得到骨髓脂肪含量,其校正步驟簡單易處理,在臨床診斷中有較好的應用前景[12]。本研究結果顯示,再骨折發生組患者術前FF水平明顯高于未發生組,經logistic回歸分析結果顯示,FF是OVCF患者PVP術后再骨折發生的危險因素。分析原因在于,骨髓脂肪占骨髓體積的70%,其在造血干細胞功能維持、成骨分化與骨形成以及骨吸收中有重要的調控作用。骨質疏松癥患者骨髓內間充質干細胞產生成骨細胞和脂肪細胞的分化程序有利于脂肪生成和成骨細胞的形成,導致骨髓脂肪增加,骨形成減少,進而削弱骨質強度,導致OVCF患者PVP術后再骨折的發生[13]。此外,骨是由骨小梁及皮質等礦化成分及骨髓非礦化成分組成,骨髓對骨骼及機體代謝中起到重要作用,隨著椎間隙中的骨組織和骨髓的丟失,脂肪組織會逐漸填滿間隙,造成腰椎的骨小梁枯竭,造成脂肪沉積[14-15]。
為研究MRI脂肪量化結果對OVCF患者PVP術后再骨折的預測價值,繪制FF水平ROC曲線圖,結果顯示,術前FF水平預測OVCF患者PVP術后再骨折的AUC>0.7,具有一定預測價值。因此,FF水平是OVCF患者PVP術后再骨折發生的危險因素,對評估再骨折發生具有一定的預測價值,臨床可以通過監測OVCF患者的FF水平,及時采取干預措施,防止再骨折的發生,進而改善患者預后。
4 結論
FF、BMD水平是OVCF患者PVP術后再骨折的獨立影響因素,通過MRI技術量化椎體脂肪含量,預測OVCF患者PVP術后再骨折發生風險。

