原子吸收分光光度儀測定蔬菜維生素C 含量的研究
包蔚 朱曉蕓 徐樺 何鍇 余海芬
(上海市嘉定區農業技術推廣服務中心,上海 201800)
維生素C 又叫抗壞血酸,廣泛存在于植物組織中,尤其是在新鮮的水果、蔬菜中含量較多。同時,維生素C 是一種水溶性維生素,是人體需要量最大的一種維生素[1]。目前,國家標準中關于維生素C含量的測定方法有2,6-二氯靛酚滴定法(以下簡稱滴定法)和2,4-二硝基苯肼比色法[2],但是2,4-二硝基苯肼比色法操作復雜,且萃取液二甲苯為有機溶劑,具有較強的毒性,不利于操作人員的健康,故不推薦使用該方法。滴定法是根據維生素C 的氧化還原性質,通過樣品溶液由藍色轉變為粉紅色來辨別其滴定終點的到達,從而計算樣品中還原型抗壞血酸的含量[2]。由于多數水果、蔬菜樣品的提取液中含有一定的色素,導致采用滴定法滴定時,其終點不易辨認,影響了該方法的準確性。然而,原子吸收法(以下簡稱原吸法)是利用維生素C 在酸性介質中可將Cu2+定量地還原為Cu+,而Cu+與SCN-反應后可生成CuSCN 沉淀,沉淀經高速離心機有效分離出來后,可用原子吸收分光光度計測定含銅量,這樣即可推知樣品中維生素C 的含量[3]。在此背景下,筆者以滴定法為對照,以黃瓜、卷心菜、青椒、青菜4 種蔬菜為實驗材料,從實驗步驟、實驗結果、精密度、準確度4個維度,驗證了原吸法測定蔬菜中維生素C 含量的可行性。現將相關結果報道如下。
1 材料與方法
1.1 供試材料
選取新鮮、色澤正常、無腐爛變質的黃瓜、卷心菜、青菜、青椒4種蔬菜,每種蔬菜取不同可食部位若干混合作為蔬菜樣品。
1.2 試劑與儀器
1.2.1 滴定法
樣品提取液用質量濃度為2% 的草酸溶液。另外,稱取100 mg 維生素C 標準樣品,溶于草酸提取液中并稀釋至100 mL,配制成質量濃度為1 mg/mL的維生素C 標準溶液,現配現用。
滴定液的配制方法:稱取碳酸氫鈉52 mg 溶解在200 mL 熱蒸餾水中,然后稱取2,6-二氯靛酚溶液50 mg 溶解在上述碳酸氫鈉溶液中,冷卻后定容至250 mL,過濾至棕色瓶內,放在冰箱中保存。每次使用前,用標準抗壞血酸標定其滴定度。
1.2.2 原吸法
稱取草酸20 g,加冰醋酸80 mL,溶解后轉移到1 000 mL 容量瓶中,用蒸餾水定容后搖勻,作為樣品提取液備用。
準確稱取維生素C 標準樣品0.1 g,置于100 mL 棕色容量瓶中,用提取液稀釋至刻度線,即得到質量濃度為1 mg/mL 的維生素C 標準溶液。然后分別吸取5.0、10.0、20.0、30.0、40.0、50.0 mL標準溶液置于100 mL 容量瓶中,再分別定容至刻度線,即得到質量濃度為50、100、200、300、400、500 μg/mL 的維生素C 標準溶液。
稱取硫氰酸銨2 g,溶解后轉移到100 mL 容量瓶中定容,即得到質量濃度為2% 的硫氰酸銨溶液。量取1 mol/L 鹽酸50 mL、1 mol/L 醋酸鈉溶液50 mL,混合后移入250 mL 容量瓶中定容,即得到鹽酸-醋酸鈉緩沖液(pH 為1.99)。
實驗用的其他試劑和儀器:飽和氯化鉀溶液、飽和硫酸銅溶液、AAnalyst 800 型原子吸收分光光度儀、5 000 r/min 組織粉碎機等。
1.3 實驗方法
1.3.1 滴定法
稱取新鮮的蔬菜樣品10 g 放入研缽中,碾碎后加5 mL 樣品提取液,然后將樣品移入l00 mL 容量瓶,并稀釋至刻度后搖勻過濾。然后,吸取10 mL濾液放入蒸發皿中,用已標定過的2,6-二氯靛酚溶液滴定,直至溶液呈粉紅色30 s 不褪色為止。同時,做空白實驗。
1.3.2 原吸法
稱取新鮮的蔬菜樣品5 g,用組織粉碎機碎成糊狀,加入少許樣品提取液浸泡后過濾,將濾液轉移至250 mL 容量瓶中,用樣品提取液定容至刻度線。然后,分別吸取維生素C 標準溶液1 mL 和樣品提取液1 mL 于離心管中,再各加入飽和硫酸銅溶液1 mL、2% 硫氰酸銨溶液1 mL、緩沖液0.5 mL和飽和KCl 溶液0.5 mL,充分混合,稍后離心分離,去除上層清液,并用少量水洗滌沉淀2~3 次,加入硝酸0.5 mL 溶解后,轉移至100 mL 的容量瓶中加水定容至刻度線,搖勻。用原子吸收分光光度計測定其含銅量,根據所得的維生素C 含量的標準曲線即可得到樣品的測定結果。
1.3.3 精密度與準確度分析
實驗通過5次平行測定,計算相對標準偏差,來衡量實驗的精密度。同時,采用加標回收的方式,通過回收率的比較,來判定實驗的準確度。
2 結果與分析
2.1 實驗步驟比較
筆者在應用滴定法測定含有色素較多的茄子時發現,茄子樣品中含有花青素,濾液顯現出大紅色,較滴定后的標準溶液顏色深,無法判斷滴定終點。由此說明,不宜用滴定法測定含有可溶性色素的蔬菜。
筆者在應用原吸法測定時,在樣品提取液中加入飽和硫酸銅溶液和2%硫氰酸銨溶液后,待反應液變成綠色渾濁液體,離心,經沉淀后多次洗滌,再用濃硝酸溶解,最后上機測定。由此說明,原吸法需要反復離心、洗滌、沉淀,步驟較滴定法多。
2.2 實驗結果比較
由圖1可知,兩種方法的測定結果相差不大,且原吸法測得4 種蔬菜樣品的維生素C 含量均高于滴定法,其中,結果差異最大的為青椒,兩種方法每100 g 樣品相差5.84 mg;其次為青菜,兩種方法每100 g 樣品相差3.82 mg;第3 為黃瓜,兩種方法每100 g 樣品相差2.22 mg;差異最小的是卷心菜,兩種方法每100 g 樣品相差1.48 mg。分析其原因,可能是青椒、青菜、黃瓜含有較多的葉綠素,色素含量較多,干擾了滴定結果的判斷,導致這3種蔬菜樣品的維生素C 含量差異比卷心菜大。
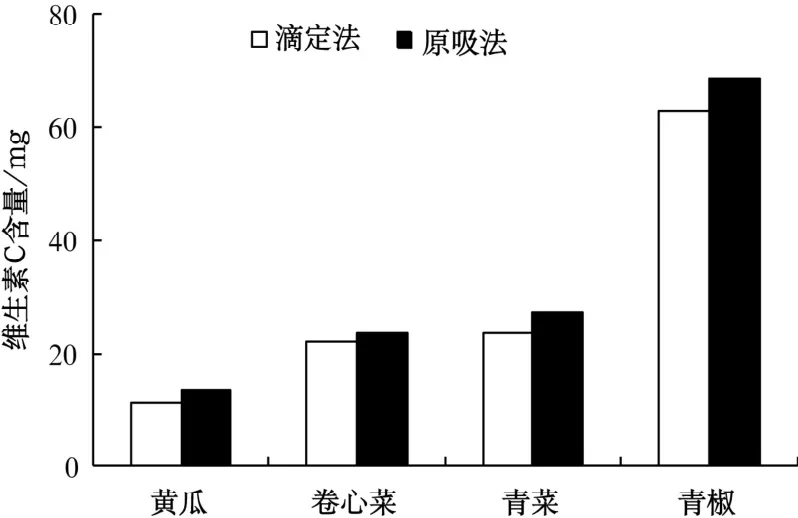
圖1 兩種檢測方法測定維生素C 含量結果比較
2.3 實驗精密度比較
采用兩種方法測定4種蔬菜樣品,其5次平行測定值的相對標準偏差結果見表1。由表1可知,滴定法的相對標準偏差為1.59%~4.67%,原吸法的相對標準偏差為0.89%~2.53%;精密度的要求都在標準要求的范圍內,且原吸法的精密度比滴定法高。分析其原因,可能是滴定法的終點判斷要滿足保持出現粉紅色30 s 內不褪色這一條件,主觀因素較強,而原吸法的測定結果由儀器讀取,人為誤差較小,且原吸法測定銅離子比較穩定。
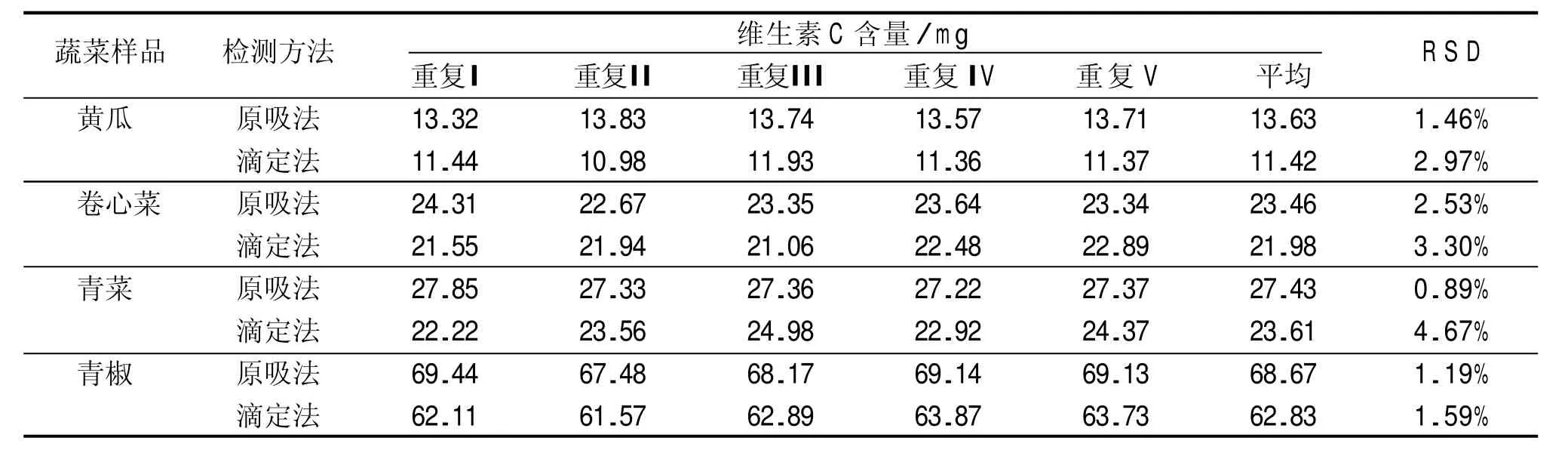
表1 兩種檢測方法精密度實驗結果比較
2.4 實驗準確度比較
由表2可知,原吸法的回收率為93.06%~105.29%,滴定法的回收率為97.38%~105.68%,回收率均在80%~120%的范圍內。從回收率的數值看,滴定法的準確度要優于原吸法,分析其原因,原吸法需經過多次離心和洗滌,其測定步驟較滴定法多,這對結果的準確性造成了一定影響。由表2還可知,在測定葉綠素含量較高的黃瓜、青菜、青椒等蔬菜時,滴定法的準確度不如原吸法。
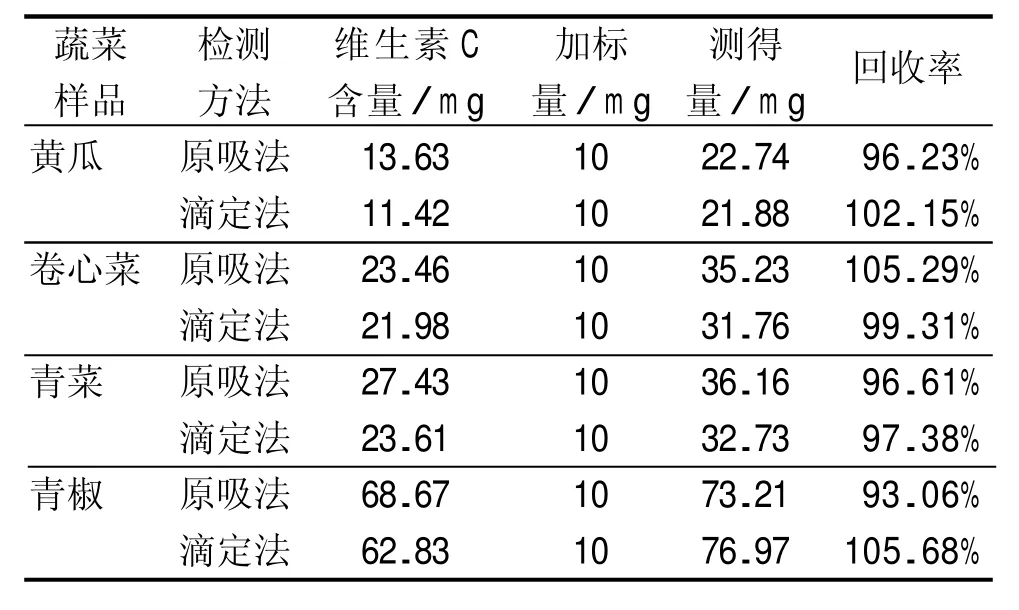
表2 兩種檢測方法加標回收率實驗結果比較
3 結論與討論
采用原吸法測定蔬菜中的維生素C 含量,其準確度和精確度均符合標準,故采用該方法測定蔬菜中維生素C含量具有一定的可行性。與滴定法相比,原吸法測定蔬菜中維生素C 含量的操作步驟較多,但是,在測定色素較多的蔬菜時,原吸法的準確性高于滴定法。因此,原吸法可作為測定蔬菜維生素C 含量的一種補充方法。

