腹腔鏡結直腸癌根治術治療結直腸癌臨床療效及對胃腸功能的影響
孔德勝,李忠信,張守凱
1.白銀市第三人民醫院外科,甘肅 白銀 730799;2.甘肅省第二人民醫院普外科,甘肅 蘭州 730000;3.甘肅省人民醫院外科,甘肅 蘭州 730000
結直腸癌是常見的消化道惡性腫瘤,其發病率逐年增加,嚴重影響人們的健康和生活質量[1]。腹腔鏡結直腸癌根治術作為一種新型的手術治療方法在臨床應用中逐漸得到推廣。腹腔鏡結直腸癌根治術具有創傷小、恢復快、美容效果好等優點,已逐漸成為結直腸癌手術治療的首選方法[2-3]。隨著手術技術的成熟和器械的改良,腹腔鏡手術已經可以完成淋巴結清掃、結直腸斷端吻合、術中造口等多種操作,提高了手術的完整性和徹底性,可更好地治愈結直腸癌。腹腔鏡結直腸癌根治術對胃腸功能的影響是存在的,但是其影響的程度和持續時間較小。研究顯示,腹腔鏡手術組與開腹手術組在胃腸功能恢復方面差異不大,術后恢復時間也沒有顯著差異[4]。研究表明,腹腔鏡手術與開腹手術在手術創傷、腫瘤清除率、術后生活質量等方面均無顯著差異[5]。基于此,本研究選取白銀市第三人民醫院2021年6月—2022年6月收治的60 例結直腸癌患者為研究對象,研究腹腔鏡結直腸癌根治術的療效優勢,現報道如下。
1 資料與方法
1.1 一般資料
選取本院收治的60 例結直腸癌患者,以隨機抽簽方法分為兩組,各30 例。其中開腹手術組施行常規開腹手術進行治療;腹腔鏡手術組行腹腔鏡結直腸癌根治術治療。開腹手術組中男16 例,女14例;年齡33~75 歲,平均(53.28±12.66)歲。腹腔鏡手術組中男17 例,女13 例;年齡32~76 歲,平均(53.44±12.57)歲。兩組一般資料對比,差異無統計學意義(P>0.05),具有可比性。本研究通過醫院醫學倫理委員會批準。本研究內容獲得患者或家屬知情同意。
1.2 納入與排除標準
納入標準:①年齡在18~76 歲的結直腸癌患者;②經組織學確診的結直腸腺癌患者,腫瘤位置在近端結腸、乙狀結腸或直腸部位;③臨床分期為I、II或III 期的患者;④沒有嚴重的心肺疾病或腹腔內其他惡性腫瘤。
排除標準:①腫瘤已經擴散至腹膜后、肝臟或其他遠處器官者;②大型腸梗阻或腸套疊等緊急情況,需要行緊急手術者;③大量或頑固性腹腔粘連者;④存在晚期肝硬化或高度脂肪肝者;⑤其他不適合手術治療的合并癥者。
1.3 方法
開腹手術組施行常規開腹手術進行治療。①麻醉:患者接受全身麻醉,確保手術期間無痛感。②切口開放:通常選擇腹部中線切口,手術醫生會根據具體情況選擇開腹的位置和長度。腹腔探查:醫生通過切開腹膜進入腹腔,以便觀察和評估腫瘤的大小、位置和周圍組織的情況。③結直腸切除:根據腫瘤的位置和術前評估的結果,醫生會切除患者的部分結直腸,包括腫瘤組織和周圍的健康組織。④淋巴結清掃:在結直腸切除的同時,醫生會清除與腫瘤相關的淋巴結,以確定是否有淋巴結轉移。⑤結腸重建:根據患者的具體情況,醫生會進行結腸重建,以確保消化道的正常功能。⑥傷口縫合:手術結束后,醫生會將腹部傷口進行縫合和護理。
腹腔鏡手術組行腹腔鏡結直腸癌根治術治療。①麻醉:患者經全身麻醉后被放置在仰臥位上,進行手術準備。手術切口:在患者腹部作3~4 個小切口,用于插入腹腔鏡和其他手術器械。②下腹腔檢查:通過腹腔鏡檢查腹腔內是否有轉移灶,確定手術范圍。檢查后解剖既往的手術切口。③結直腸暴露:操作醫生用特殊器械和技術將結直腸向上移動,暴露出術區。④結直腸切割和吻合:在結直腸癌腫瘤附近切下一段健康的腸管,然后在兩端進行吻合,恢復腸管連續性。⑤淋巴結清掃:清除結直腸附近的淋巴結,以探查有無淋巴結轉移。⑥結直腸切口閉合:遵循嚴格的無菌操作,將手術切口層層閉合。⑦術中控制出血:如果術中有出血,需要及時止血,確保手術安全。⑧抽取標本:將切除的組織標本送病理檢查。⑨術中控制疼痛:通過麻藥鎮痛等方式控制患者的術后疼痛。⑩結腸造口(如需):對需要造口的患者,術后可以在腹壁上開口,將結腸引至腹壁,使患者可以排便。
1.4 觀察指標
觀察并對比兩組患者治療前后血清腫瘤標志物水平:治療前后兩組患者的血清癌胚抗原(carcinoembryonic antigen, CEA)和血清胃腸癌相關抗原(carbohydrate antigen 19-9, CA19-9)水平應該是主要觀察的指標,這兩個指標是檢測胃癌患者的腫瘤標志物。
觀察并對比兩組患者治療前后肝腎功能以及血常規情況:通過檢測相關生化指標如谷丙轉氨酶(glutamic-pyruvic transaminase, ALT)、谷草轉氨酶(glutamic-oxaloacetic transaminase, AST)、總膽紅素(total bilirubin, TBIL)等來評估肝功能,通過檢測肌酐(creatinine, Cr)、尿素氮(blood urea nitrogen, BUN)等指標來評估腎功能,以觀察是否有明顯的異常。
觀察并對比兩組患者治療后不良反應發生情況:包括粒細胞減少、血紅蛋白減少等。
對兩組患者胃腸功能情況進行對比分析:胃腸功能的評估包括胃腸動力、胃動素以及胃泌素。通過觀察兩組患者的排便情況、排氣情況、食欲情況等,可以初步評估胃腸動力的改變。同時,觀察和比較胃動素和胃泌素的水平變化,可以得到對胃腸功能的更準確評估。
1.5 統計方法
本研究使用SPSS 23.0 統計學軟件對兩組患者治療前后的進行數據分析。計量資料符合正態分布以(±s)表示,進行t檢驗;計數資料用例數(n)和率(%)表示,進行χ2檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 兩組患者血清CEA 和CA19-9 水平變化對比
治療后,腹腔鏡手術組患者血清CEA 水平和CA19-9 水平顯著優于開腹手術組患者,差異有統計學意義(P<0.05),見表1。
表1 兩組患者治療前后血清CEA 和CA19-9 水平變化對比(±s)
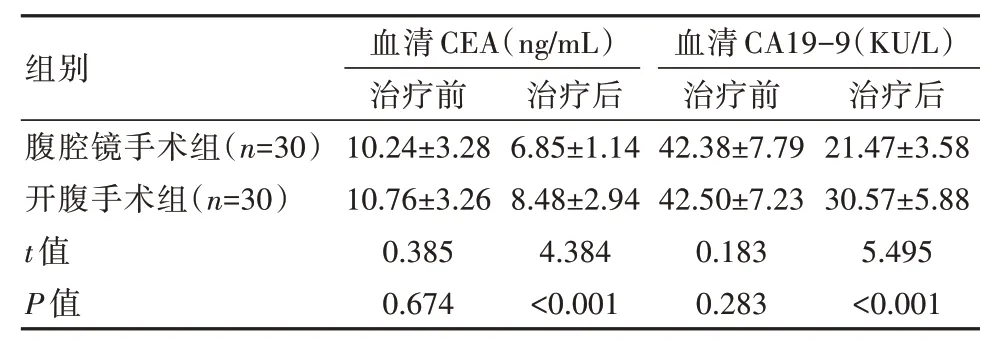
表1 兩組患者治療前后血清CEA 和CA19-9 水平變化對比(±s)
組別腹腔鏡手術組(n=30)開腹手術組(n=30)t 值P 值血清CEA(ng/mL)治療前10.24±3.28 10.76±3.26 0.385 0.674治療后6.85±1.14 8.48±2.94 4.384<0.001血清CA19-9(KU/L)治療前42.38±7.79 42.50±7.23 0.183 0.283治療后21.47±3.58 30.57±5.88 5.495<0.001
2.2 兩組患者肝腎功能對比
治療后,腹腔鏡手術組患者肝腎功能水平顯著優于開腹手術組患者,差異有統計學意義(P<0.05),見表2。
表2 兩組患者治療前后肝腎功能對比(±s)
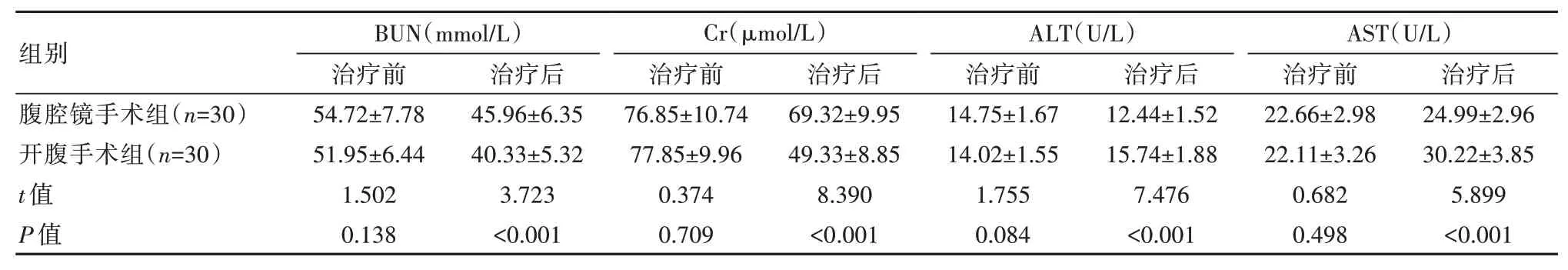
表2 兩組患者治療前后肝腎功能對比(±s)
組別腹腔鏡手術組(n=30)開腹手術組(n=30)t 值P 值BUN(mmol/L)治療前54.72±7.78 51.95±6.44 1.502 0.138治療后45.96±6.35 40.33±5.32 3.723<0.001 Cr(μmol/L)治療前76.85±10.74 77.85±9.96 0.374 0.709治療后69.32±9.95 49.33±8.85 8.390<0.001 ALT(U/L)治療前14.75±1.67 14.02±1.55 1.755 0.084治療后12.44±1.52 15.74±1.88 7.476<0.001 AST(U/L)治療前22.66±2.98 22.11±3.26 0.682 0.498治療后24.99±2.96 30.22±3.85 5.899<0.001
2.3 兩組患者血常規對比
治療后,腹腔鏡手術組患者血常規結果顯著優于開腹手術組患者,差異有統計學意義(P<0.05),見表3。
表3 兩組患者治療前后血常規情況對比(±s)
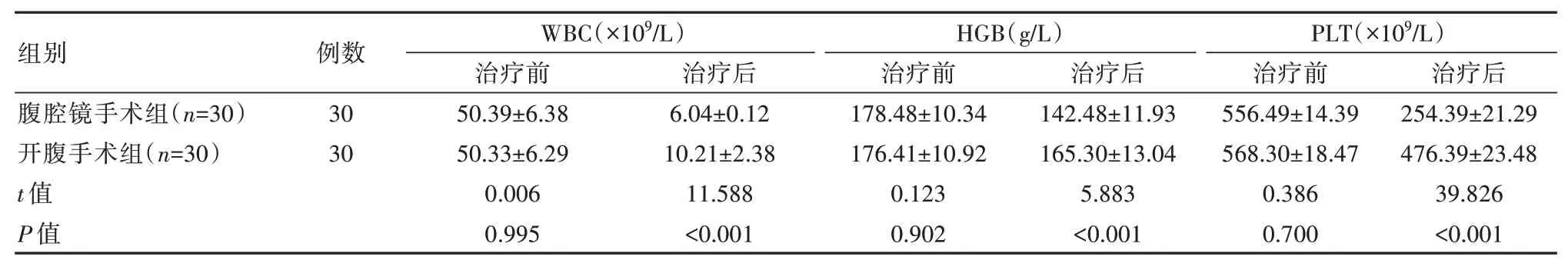
表3 兩組患者治療前后血常規情況對比(±s)
組別腹腔鏡手術組(n=30)開腹手術組(n=30)t 值P 值例數30 30 WBC(×109/L)治療前50.39±6.38 50.33±6.29 0.006 0.995治療后6.04±0.12 10.21±2.38 11.588<0.001 HGB(g/L)治療前178.48±10.34 176.41±10.92 0.123 0.902治療后142.48±11.93 165.30±13.04 5.883<0.001 PLT(×109/L)治療前556.49±14.39 568.30±18.47 0.386 0.700治療后254.39±21.29 476.39±23.48 39.826<0.001
2.4 兩組患者不良反應發生情況對比
腹腔鏡手術組患者不良反應發生情況顯著低于開腹手術組患者,差異有統計學意義(P<0.05),見表4。
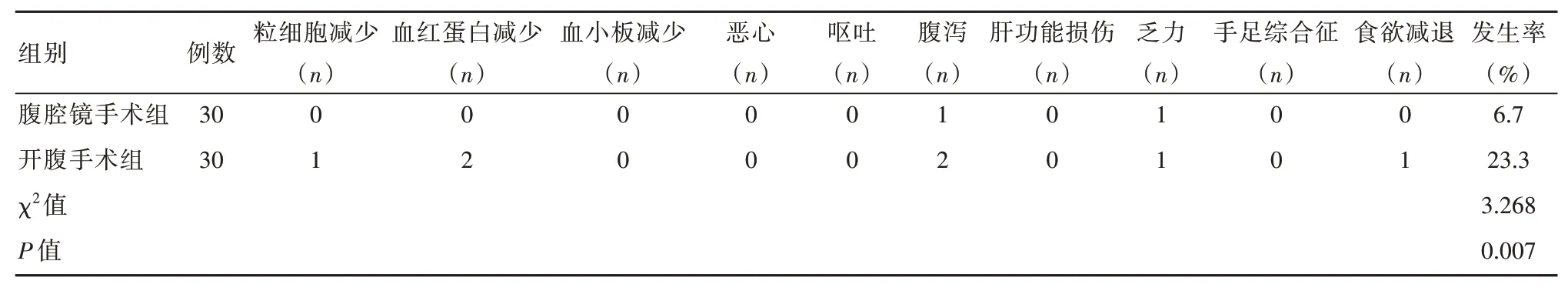
表4 兩組患者不良反應發生情況對比
2.5 兩組患者胃腸功能情況對比
腹腔鏡手術組患者胃腸功能以及術后恢復情況顯著優于開腹手術組患者,差異有統計學意義(P<0.05),見表5。
表5 兩組患者胃腸功能情況對比(±s)
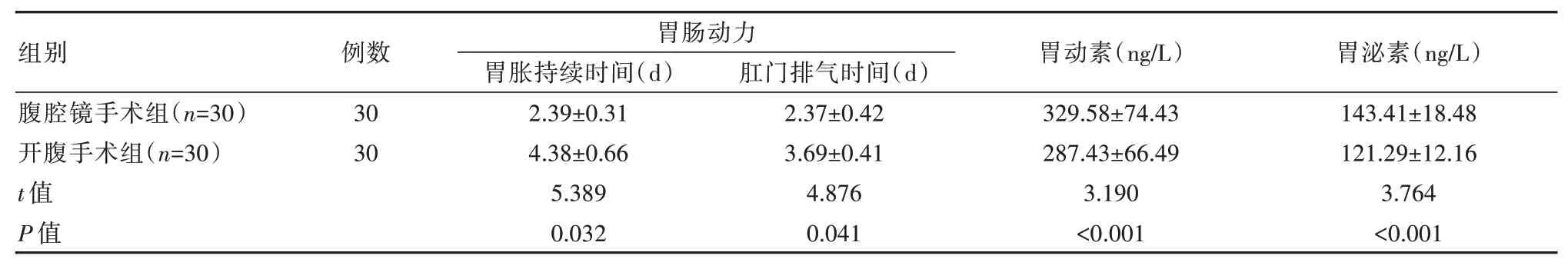
表5 兩組患者胃腸功能情況對比(±s)
組別腹腔鏡手術組(n=30)開腹手術組(n=30)t 值P 值例數30 30胃腸動力胃脹持續時間(d)2.39±0.31 4.38±0.66 5.389 0.032肛門排氣時間(d)2.37±0.42 3.69±0.41 4.876 0.041胃動素(ng/L)329.58±74.43 287.43±66.49 3.190<0.001胃泌素(ng/L)143.41±18.48 121.29±12.16 3.764<0.001
3 討論
常規的開腹手術一直是結直腸癌主要的治療方式[6]。然而,該手術存在一定的弊端,因此腹腔鏡結直腸癌根治術作為一種微創手術技術應運而生。
結直腸癌是一種惡性腫瘤,其發病與多種因素相關,包括年齡、遺傳基因、飲食習慣、炎癥性腸病等。其早期癥狀不明顯,臨床表現主要包括腹痛、便血、排便習慣改變等。發展到晚期,可出現腹瀉、貧血、腹脹等癥狀,并可能產生腸梗阻、腹膜播散等嚴重并發癥[7]。常規開腹手術作為一種傳統治療結直腸癌的方式,其作用機制主要包括徹底切除腫瘤、清除淋巴結、阻斷腫瘤供血和排除腫瘤轉移等[8]。然而,常規開腹手術存在一些明顯的弊端,這些弊端極大地影響了患者的心理和生理狀態。首先,常規開腹手術需要切開患者的腹腔,導致術后的傷口較大。這個大傷口需要一定時間來愈合,給患者帶來了長時間的疼痛和不適。術后疼痛使得患者難以進行常規的生活活動和工作,同時也加重了患者的心理負擔。在尚未康復的情況下,患者必須依賴藥物來緩解疼痛,這可能導致藥物成癮和其他不良反應。其次,常規開腹手術的術后恢復速度較慢。由于手術切口較大,患者需要更長的時間來康復。術后恢復緩慢使患者長時間處于體弱多病的狀態,對于長期臥床休息的患者來說,還可能導致肺部感染和深靜脈血栓等并發癥發生的風險增加。患者也可能因為康復過程中的不適和身體的虛弱而感到絕望和壓力,這對于心理的恢復同樣具有負面影響。最后,常規開腹手術切口的愈合也可能出現困難。盡管現代醫學技術已經取得了很大的進步,但仍然有一部分患者可能面臨著傷口感染、瘢痕增生等并發癥發生的風險。這些并發癥不僅會延緩傷口愈合的時間,還可能導致更大的疼痛和不適。腹腔鏡結直腸癌根治術作為一種微創手術技術,通過腹腔鏡器械在腹腔內進行手術。其作用機制與常規開腹手術相似,但相比之下有以下優勢:①創傷小:腹腔鏡手術只需進行3~4 個小切口,相比于常規開腹手術而言,創傷更小,術后疼痛明顯減輕,恢復較快。②普適性強:腹腔鏡手術適用于大部分結直腸癌患者,包括老年患者、肥胖患者、合并其他疾病的患者等。③相關合并癥風險低:相比于常規開腹手術,腹腔鏡手術的相關合并癥風險,如感染、出血等,明顯降低。④準確性高:腹腔鏡手術可以放大顯微鏡下視野,有助于醫生準確找到淋巴結,并且可以通過腹腔鏡進行探查,提高手術的準確性[9]。⑤美觀性好:常規開腹手術的切口較大,術后容易留下明顯的疤痕,而腹腔鏡手術的切口較小,疤痕相對不明顯,美觀性好。腹腔鏡結直腸癌根治術已經成為一種較為成熟的微創手術技術,其臨床療效已經得到廣泛認可。然而,也需要注意的是,腹腔鏡手術在技術要求上更高,需要醫生具備豐富的經驗和高超的操作技巧[10]。一方面,手術后可能導致胃腸道的運動功能發生改變,從而影響食物的順利通過腸道,可能出現胃脹、腹瀉等消化系統不適感[11]。另一方面,手術后還可能導致胃腸道的吸收功能受損。例如,術后可能出現胃酸過多、膽汁反流等情況,影響食物的消化和吸收。這些影響胃腸功能的狀況在術后一段時間內可能會持續存在,但通常隨著時間的推移會逐漸恢復正常。為了減少手術對胃腸功能的影響,術后的營養支持和康復非常重要。手術后應給予患者合理的飲食建議,其內容包括逐漸恢復飲食、避免食用油膩、刺激性食物,鼓勵適量運動等[12]。此外,還可以使用藥物來調節胃腸功能。例如,可以使用胃腸動力藥物來促進胃腸道的蠕動,改善食物通過腸道的速度和順利度;對于胃酸過多的患者,可以使用胃酸抑制劑等藥物。
綜上所述,腹腔鏡結直腸癌根治術相比于常規開腹手術具有明顯的優勢,可以有效治療結直腸癌,并減輕患者的術后痛苦。但是,醫生需要在具體操作中根據患者的病情和術前評估結果,權衡利弊選擇適合的手術方式。

