24h鹽酸嗎啡緩釋片與市售品在比格犬體內的藥代動力學對比研究*
闕 曉,蔣 猛,張玲玲,曾令高,蒲 婷,熊莉平,蒲道俊△
(1.西南藥業股份有限公司,重慶 400038;2.重慶市食品藥品檢驗檢測研究院·國家藥品監督管理局麻醉精神藥品質量監測重點實驗室,重慶 401121)
世界衛生組織(WHO)推薦的癌癥三階梯止痛方案指出,重度癌痛患者推薦使用嗎啡[1-4]。嗎啡是一種阿片受體激動藥,可通過模擬內源性抗痛物質腦啡肽的作用,激動中樞神經阿片受體而產生強效鎮痛作用,對持續性鈍痛的效果強于間斷性銳痛和內臟絞痛[5-8]。24 h嗎啡緩釋制劑在國外已上市多年,而國內現僅有注射劑、普通片劑、口服液、12 h 緩釋片等劑型[9-10]。嗎啡制劑陣痛作用時間較短,患者血藥濃度波動較大,毒副作用明顯;且為了達到鎮痛效果,每日需多次服用或注射,患者順應性差,醫護人員工作量大。前期研究中,自制使用以零級釋藥為基本特征的24 h 鹽酸嗎啡緩釋片,以醋酸纖維素為成膜材料,通過加入一種水溶性致孔劑形成微孔型滲透泵片。該制劑在體內經過片芯浸潤、溶解后,可借助膜內外滲透壓差緩慢從孔中釋放藥物,達到24 h 長效緩釋作用。為此,本研究中建立了測定比格犬血漿中鹽酸嗎啡濃度的液相色譜串聯質譜(LC-MS/MS)法,并比較了自制24 h 鹽酸嗎啡緩釋片與2種市售品的藥代動力學行為,以評價該制劑的緩釋特征。現報道如下。
1 儀器、試藥與動物
1.1 儀器
Acquity UPLC 型超高效液相色譜系統(美國Waters公司);TRIPLE QUAD 6500+型三重四極桿液質聯用儀(美國應用生物系統公司),處理系統為Analyst軟件;XP26型微量分析天平(精度為百萬分之一),S210型pH計,均購于梅特勒-托利多儀器<上海>有限公司;SIA256 型渦旋振蕩器(Scientific Industries,Inc);5417R 型高速冷凍離心機(德國Eppendorf公司);EQ7000型超純水機(美國Millipore公司);。
1.2 試藥
嗎啡對照品(中國食品藥品檢定研究院,批號為171201-201324,含量為99.1%);磷酸可待因對照品(內標,青海制藥廠有限公司,批號為20170213,含量為99.4%);鹽酸嗎啡片(市售品1,東北制藥集團沈陽第一制藥有限公司,批號為1170102,規格為每片10 mg);鹽酸嗎啡緩釋片(市售品2,批號為15080028,規格為每片30 mg),24 h 鹽酸嗎啡緩釋片(自制,批號為170604,規格為每片60 mg),均購于西南藥業股份有限公司;甲醇、乙腈(色譜純,Burdick&Jackson);檸檬酸三鈉(分析純,上海泰坦科技股份有限公司);檸檬酸(分析純,國藥集團化學試劑有限公司);β-葡萄糖醛酸酶(美國Sigma 公司,濃度為85 000 U/mL);二甲基亞砜(DMSO,分析純,永華化學科技<江蘇>有限公司);甲酸(J&K百威靈公司);水為超純水。
1.3 動物
健康比格犬12 只,普通級,8 月齡,體質量8.0~8.6 kg,雌雄各半。購自上海新岡實驗動物場,動物生產許可證號為SCXK(滬)2017-0006,實驗動物質量合格證號為31161910000012,飼養期間自由飲水和進食。
2 方法與結果
2.1 色譜與質譜條件
2.1.1 色譜條件
色譜柱:ACE Phenyl 柱(100 mm×2.1 mm,5μm);流動相:0.1%甲酸水溶液(A)-0.1%甲酸乙腈溶液(B),梯度洗脫(0 min 時98%A,1.20 min 時50%A,1.50 min時10%A,1.80 min 時10%A,1.81 min 時98%A);流速:500μL/min;柱溫:40 ℃;進樣量:1μL。
2.1.2 質譜條件
電噴霧離子源(ESI);正離子模式,多反應監測模式(MRM);離子源電壓(IS):5 500 V;離子源溫度(TEM):500 ℃;掃描時間:0.2 s;監測離子對參數:質荷比(m/z)286.1~165.3(嗎啡),m/z300.2~165.1(可待因)。
2.2 樣品處理
取磷酸可待因對照品適量,加甲醇或DMSO 使溶解,混勻,即得可待因貯備液;取適量,加乙腈制得質量濃度為100 ng/mL 的內標溶液。取血漿樣品,放至室溫,渦旋,混勻,量取50μL,置1.5 mL離心管中,加稀釋后的β-葡萄糖醛酸酶(濃度為5 000 U/mL)50μL,混勻,37 ℃水浴16 h,加400μL 內標溶液,渦旋,混勻,離心(轉速為14 000 r/min)5 min,取上清液,備用。
2.3 方法學考察
專屬性試驗:取6 只比格犬的空白血漿,按2.2 項下樣品處理方法處理(用相同體積的乙腈替換內標溶液),得空白基質樣品;取6只比格犬的空白血漿,按2.2項下樣品處理方法處理,加入一定濃度的內標溶液,得含內標的空白基質樣品;取6 只比格犬的空白血漿,按2.2項下樣品處理方法處理,加入一定濃度的內標溶液和含定量限濃度水平的待測物,得定量限空白基質樣品。吸取上述3種溶液各適量,按2.1項下色譜與質譜條件進樣測定,待測物和內標物的出峰處均無干擾峰或影響定量的干擾峰,表明方法專屬性良好。色譜圖見圖1。
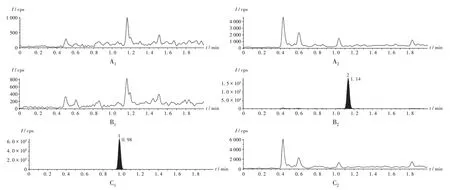
1.嗎啡 2.可待因A1,A2.空白基質樣品 B1,B2.含內標的空白基質樣品 C1,C2.定量限空白基質樣品圖1 專屬性試驗液相色譜串聯質譜圖1.Morphine 2.CodeineA1,A2.Blank matrix samples B1,B2.Blank matrix samples containing internal standards C1,C2.Quantitative limit blank matrix samplesFig.1 LC-MS/MS chromatograms of the specific test
線性關系考察:取嗎啡對照品適量,加甲醇或DMSO 使溶解,混勻,即得嗎啡貯備液,用乙腈稀釋為質量濃度為200 μg/mL 的標準溶液,再用空白血漿稀釋為質量濃度為5 000 ng/mL 的標準曲線樣品,繼續用空白血漿依次稀釋至嗎啡質量濃度分別為2 000,1 000,500,250,100,50,10,5 ng/mL,按2.2 項下樣品處理方法進行處理,按2.1 項下色譜與質譜條件進樣測定,以待測物質量濃度(X,ng/mL)為橫坐標、待測物與內標的峰面積比值(Y)為縱坐標,采用加權最小二乘法(W=1/X2)進行線性回歸,得回歸方程Y=0.001 94X+0.001 09(r=0.998 4,n=8)。結果表明,嗎啡的質量濃度在5~2 000 ng/mL 范圍內與待測物和內標峰面積比值的線性關系良好。且各濃度標準曲線樣品的相對誤差(RE)在±15.0%范圍內,定量下限(LLOQ)為5 ng/mL。
準確度和精密度試驗:按線性關系考察項下操作,配制嗎啡質量濃度分別為5,15,200,1 600 ng/mL 的LLOQ 及低、中、高質量濃度的質控樣品,按2.2 項下樣品處理方法進行處理,每個濃度平行制備6 份,按2.1項下色譜與質譜條件進樣測定。結果所有樣品批內(n=6)和批間(n=18)結果的RSD均低于15%,LLOQ樣品的平均RE在±20.0%范圍內,低、中、高質量濃度樣品的平均RE在± 15.0%范圍內,均符合標準,表明方法精密度和準確度良好。
提取回收試驗:取比格犬空白血漿適量,以1∶8(V/V)分別加入乙腈,渦旋,離心(轉速為14 000 r/min)5 min,取上清液,混勻,待用。加入嗎啡貯備液的上清液進行稀釋,配制嗎啡質量濃度分別為1 600,200,15 ng/mL的基質樣品,按2.2 項下樣品處理方法進行處理,每個濃度平行制備6 份。同時,按準確度和精密度試驗項下方法制備相同濃度的質控樣品,按2.1項下色譜與質譜條件進樣測定。結果在同一分析物濃度水平下,嗎啡低、中、高質量濃度每個分析物峰面積的RSD均不超過4.63%(≤15.0%),不同質量濃度水平間分析物峰面積的RSD為3.94%(≤20.0%),均符合標準要求;內標可待因的低、中、高質量濃度每個分析物峰面積的RSD≤2.11%(≤20.0%),不同質量濃度水平間分析物峰面積的RSD為1.89%(≤15.0%),均符合標準。
穩定性試驗:采用低、高質量濃度的質控樣品(15,1 600 ng/mL),每個濃度平行制備6 份,分別于-80~-70 ℃冷凍至少24 h,室溫解凍,重復4 次,按2.2 項下樣品處理方法進行處理,評價冷凍/解凍穩定性;室溫放置6 h 后進樣分析,評價室溫放置穩定性;將其提取處理后,于自動進樣器(4 ℃)放置52 h 后進樣分析,評價自動進樣器穩定性;于-80~-70 ℃冰箱中分別凍存8 d及32 d后進樣分析,評價短期/長期穩定性。結果低、高質量濃度質控樣品在冷凍/解凍4 次、室溫放置6 h、自動進樣器放置52 h、凍存8 d 及32 d 后的穩定性均良好。詳見表1。
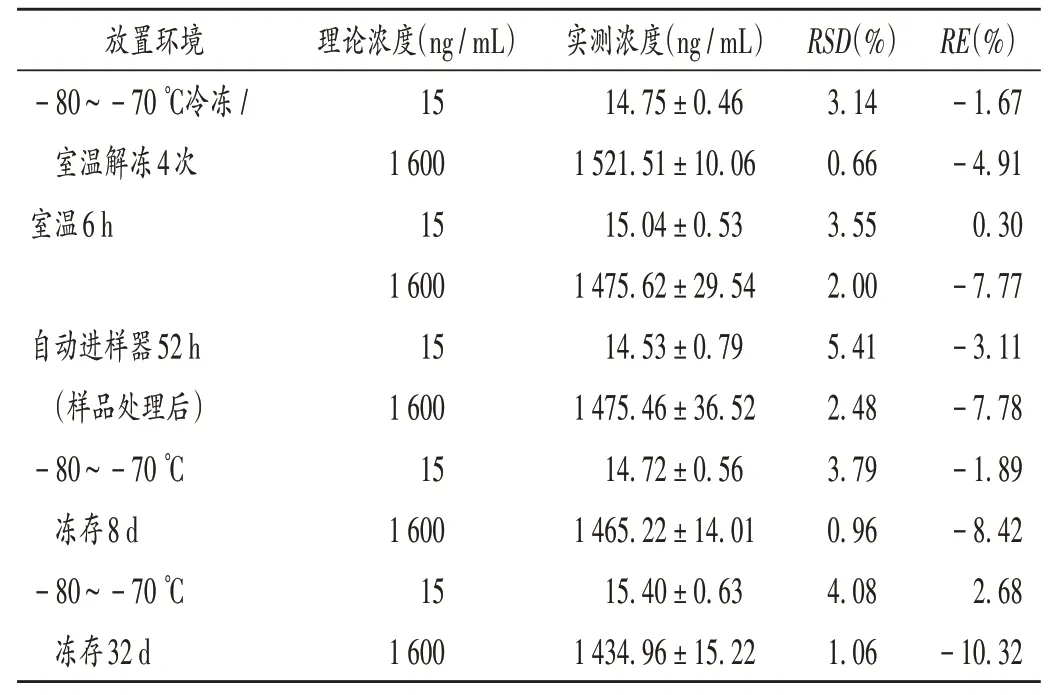
表1 穩定性試驗結果(n=6)Tab.1 Results of the stability test(n=6)
2.4 藥代動力學行為
2.4.1 給藥方案
將12 只比格犬分為自制品組、市售品1 組、市售品2 組,各4 只(雌雄各半),進行單劑量、三周期交叉口服給藥試驗,清洗期為7 d。3 組均口服給藥,每次1 片,其中自制品組1次/天,市售品1組6次/天(每次間隔4 h),市售品2 組2 次/天(每次間隔12 h)。首次給藥前禁食16~17 h,試驗期間自由飲水,給藥后約4 h 進食。給藥方案見圖2。

圖2 試驗給藥方案Fig.2 Administration plans for Beagle dogs
血樣采集時間點為自制品組給藥前(0 h)及給藥后0.25,0.5,1,2,3,4,5,6,8,12,14,16,24,28,32,48 h共17個點;市售品1組給藥前(0 h)及給藥后0.25,0.5,1,2,4,4.25,4.5,5,6,8,8.25,8.5,9,10,12,12.25,12.5,13,14,16,16.25,16.5,17,18,20,20.25,20.5,21,22,24,28,32,48 h 共34 個點;市售品2 組給藥前(0 h)及給藥后0.25,0.5,1,2,4,6,8,12,12.25,12.5,13,14,16,18,24,28,32,48 h 共19 個點。每只動物每個時間點經頸靜脈采血約1 mL,置肝素鈉抗凝離心管中,離心(轉速為3 500 r/min)10 min,分離血漿(2~8 ℃),-80 ℃保存,備用。
2.4.2 數據分析與結果
根據藥物的血藥濃度數據,采用Phoenix WinNonlin 7.0 藥代動力學計算軟件非房室模型分別計算受試物的藥代動力學參數,包括0-t、0-∞時的血藥濃度曲線下面積(AUC0-t、AUC0-∞)、平均駐留時間(MRT0-∞)、最大血藥濃度(Cmax)、達峰時間(tmax)、半衰期(t1/2),以及自制品較市售品1、市售品2 的生物利用度(F),Cmax和AUC0-t經對數轉換后采用方差分析進行統計學分析。數據均以表示,P<0.05為差異有統計學意義。
3 組血藥濃度-時間曲線見圖3,藥代動力學參數見表2。鹽酸嗎啡自制品較市售品1、市售品2 的相對F分別為(80.05±55.18)%、(100.47±67.34)%。自制品與市售品1、市售品2 的AUC0-t無顯著差異(P>0.05);自制品的Cmax是市售品1、市售品2的1.05倍和1.07倍,3 種制劑的Cmax無顯著差異(P>0.05);自制品的tmax是市售品1、市售品2的13.9倍和7.1倍,較市售制劑有明顯的緩釋作用;自制品24 h內給藥1片(60 mg)時藥物的暴露量與市售品1(24 h 內給藥6 次,每次10 mg,間隔4 h)和市售品2(24 h內給藥2次,每次30 mg,間隔12 h)無顯著差異(P>0.05),但暴露量的比格犬間個體差異較大。
表2 比格犬口服不同鹽酸嗎啡制劑的藥代動力學參數()Tab.2 Pharmacokinetic parameters of different morphine hydrochloride preparations after oral administration in Beagle dogs()
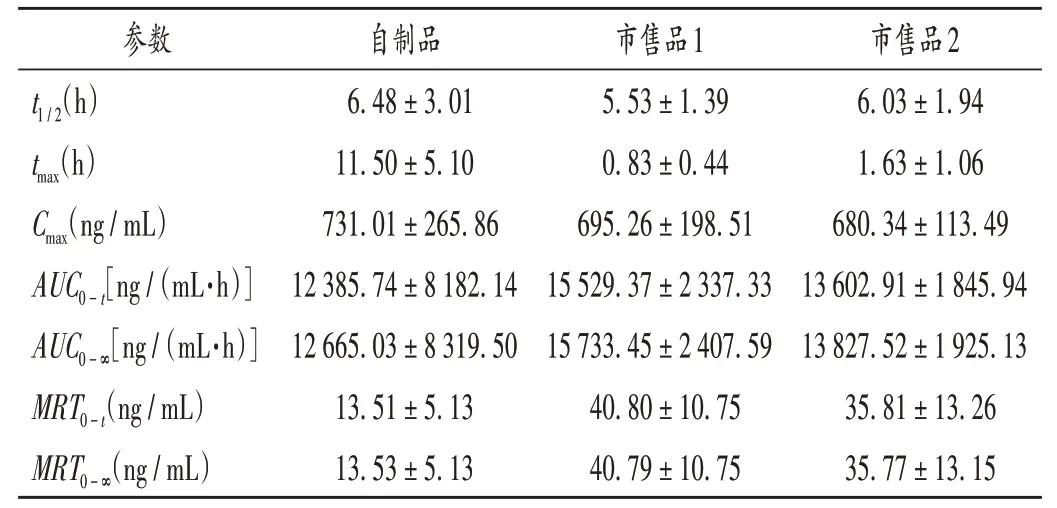
表2 比格犬口服不同鹽酸嗎啡制劑的藥代動力學參數()Tab.2 Pharmacokinetic parameters of different morphine hydrochloride preparations after oral administration in Beagle dogs()
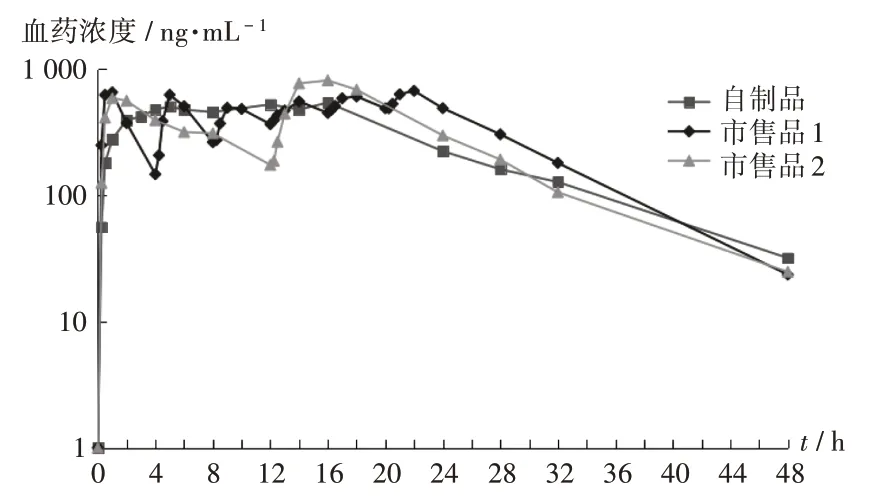
圖3 比格犬口服不同鹽酸嗎啡制劑后的血藥濃度-時間曲線Fig.3 Plasma concentration-time curves of different morphine hydrochloride preparations after oral administration in Beagle dogs
3 討論
滲透泵給藥系統是以膜內外的滲透壓差為釋藥動力、以恒定的零級釋藥為基本特征的一種新型釋藥系統[11-13]。與傳統口服制劑相比,滲透泵給藥系統的釋藥行為不受胃腸道pH 值、酶、胃腸蠕動、食物等生理因素影響,具有良好的體內外相關性,可最大限度地避免血藥濃度的峰谷波動現象,減少服藥次數,減輕全身毒副作用,提高藥物制劑的安全性、有效性和患者的順應性,是目前緩控釋效果最理想的給藥系統之一[14-17]。滲透泵主要分為單室滲透泵和雙室滲透泵,其中易溶性藥物主要制備成單室滲透泵,難溶性藥物主要制備成雙室滲透泵。滲透泵片主要由片芯和半透膜組成,片芯中含有活性成分、促滲劑等,半透膜材料含有增塑劑、致孔劑等。目前,常以醋酸纖維素/聚乙二醇、乙基纖維素/聚乙二醇、醋酸纖維素/鄰苯二甲酸酯等半透膜材料制備滲透泵控釋片。在放置過程中,隨著儲存時間的延長,滲透泵控釋片的釋放性能下降明顯。越臨近效期,越接近溶出度下限。聚乙二醇、鄰苯二甲酸酯等材料同時具備致孔劑和增塑劑作用,放置過程會不斷與纖維素相結合,造成膜通透性下降,使釋放變慢,稱作老化效應[18-20]。老化效應在單層及雙層滲透泵中均會出現,對僅依賴膜釋放的單層滲透泵,老化效應對藥物釋藥速率的影響更顯著。BAYER 公司的硝苯地平控釋片、OSMOTICA 公司的鹽酸文拉法辛緩釋片等都存在半透膜的老化效應。本研究中的自制24 h鹽酸嗎啡緩釋片以單室滲透泵為基礎,通過優化處方和工藝參數來調整藥物釋放曲線,如致孔劑、促滲劑的類型和用量,半透膜的厚度,釋藥孔的大小,均可使制劑避免半透膜的老化效應和藥物突釋現象,確保制劑在效期內的穩定性。
早期的國內市售嗎啡主要為普通速釋片(以市售品1 為代表),需反復給藥,存在漏服風險,降低了患者的順應性,且增加了醫護人員的工作量。目前,市售嗎啡口服制劑多為12 h鹽酸嗎啡緩釋片(以市售品2為代表),每日給藥2 次。本研究結果顯示,自制24 h 鹽酸嗎啡緩釋片較國產普通片(市售品1)和12 h 緩釋片(市售品2)的tmax有所延長,減少了普通制劑血藥濃度的波動。
綜上所述,本研究中建立的方法靈敏度高、重復性好、準確度高,且無干擾,自制24 h 鹽酸嗎啡緩釋片具有顯著的緩釋特征。本研究為單劑量探索性試驗,后續研究中將進一步通過臨床人體耐受性和藥代動力學研究進行24 h鹽酸嗎啡緩釋片的人體安全性評價。

