藥品網絡銷售現狀分析及監管對策
蔣 磊
(河南省安陽市食品藥品審評中心,河南 安陽 455000)
目前,我國醫藥零售行業傳統銷售模式分為醫療終端和社會零售藥店,其中社會零售藥店采取的是面對面銷售。隨著騰訊、微信、融媒體直播帶貨、電商平臺App等互聯網銷售新模式的發展,藥品零售行業發生了巨大變化。企業也逐漸意識到互聯網新經營模式對藥品零售行業帶來的重大機遇,均轉向網上銷售,對藥品經營質量管理監管提出更高要求。為此,本研究中分析了新模式藥品監管執法中發現的問題,并提出相應的監管對策。現報道如下。
1 現狀
1.1 監管不足
1)互聯網銷售具有虛擬性、隱匿性、發散性、跨地域性等特點,尤其是藥品網絡銷售存在主體類型多,不同類型主體風險差異、管理方式不同,為監督管理、執法管轄、案件調查、證據固定等監管行為帶來挑戰[1]。無論是直播平臺管理者還是監管部門,無法及時甄別直播帶貨的內容,對違規銷售的監管還有管轄權模糊的問題。
2)通過騰訊、微信違法銷售藥品隱蔽性極強。如在新型冠狀病毒感染疫情期間,在QQ、微信或朋友圈總能看到標有“貨源充足”的稀缺藥品和醫療器械等防疫物資。QQ 和微信出現的違法銷售行為往往都是“點對點”銷售,很難被發現,即使發現了線索也無法收集違法證據,極大地影響監管公信力,造成用藥安全隱患。《中華人民共和國藥品管理法》(以下簡稱《藥品管理法》)、《醫療器械監督管理條例》等規定,經營藥品、醫療器械需取得藥品經營許可證、醫療器械經營備案證、醫療器械經營許可證,藥品、醫療器械屬特殊商品,嚴禁個人以任何形式經營。直播帶貨式的銷售、QQ、微信中均應禁止售賣藥品和醫療器械。
1.2 銷售亂象
《藥品管理法》第五十七條規定,藥品經營企業購銷藥品,應當有真實、完整的購銷記錄。《藥品經營質量管理規范》(GSP)第六十六條、第六十七條、第九十二條規定,經營企業在采購藥品時,應當向供貨單位索取發票;做到發票上的購進金額與財務賬目內容相對應,并做好銷售記錄。個別企業在線下采購過程中通過少部分藥品的合法手續以掩蓋真實的采購數量,達到非法牟利的目的。通過對轄區經營有網店的藥品零售企業的實地調查發現,這類行為在網上銷售的情況更加嚴重。特別是在電商平臺或直播間為了提高品牌價值更高的傭金、提成等,往往會借助流量造假及“水軍”“刷單”等方式獲取銷量榜的位置[2];更有甚者聘請沒有相關醫藥學專業知識及資格的人氣主播,直播時普遍存在宣傳誤導、夸大功效等情況,虛設銷售業績,博取消費者的關注。監管部門無法查證交易是否真實,更難以獲取企業的真實銷售數據。
1.3 儲存條件不符合GSP 要求
藥品是一種特殊的商品,空氣、光、溫度、相對濕度等外界因素對藥效的穩定性具有較大影響。即使未過藥品包裝上標定的有效期,貯存不當也會導致藥品變質而失效[3]。科學、有效的保存條件是保證藥效的必要條件。
《中國藥典》規定:常溫環境10~30 ℃,陰涼環境不超過20 ℃,冷藏環境2~10 ℃,冷凍環境在0 ℃以下,常溫下相對濕度應控制在35%~75%。GSP 第八十三條規定,企業應當根據藥品的質量特性對藥品進行合理儲存,并按符合包裝標識的溫度要求儲存藥品,包裝上沒有標識具體溫度的,按《中國藥典》規定的貯藏要求進行儲存。
而在GSP 檢查及跟蹤檢查中發現,線下藥房可做到符合GSP 要求的儲存和養護條件;網上銷售的藥品在實際儲存過程中幾乎未按GSP 要求的條件進行儲存和養護,而是按普通商品堆放儲存,需要陰涼保存甚至冷藏保存的藥品與常溫保存的藥品堆放在同一空間,而且違法企業委托的物流公司都是按普通商品進行包裝和運輸,很難做到按藥品溫控或冷鏈運輸要求運輸,完全忽視了藥品作為一種特殊商品的屬性。電商對藥品的儲存和養護條件還是物流過程中的運輸條件,都無法保證嚴格按《藥品經營質量管理規范附錄6:藥品零售配送質量管理》(以下簡稱《附錄6》)所要求的標準執行。不符合GSP 要求的保存和運輸存在質量風險[3],增加了藥效不穩定的可能性。
1.4 銷售流向與實際不符
個別批發企業或連鎖總部未獲取零售經營資格,但在疫情期間藥械物資極度稀缺時,企業為了尋求經濟效益最大化而不惜鋌而走險。GSP 第五十七條規定,企業應當建立能夠符合經營全過程管理及質量控制要求的計算機系統,實現藥品可追溯;第五十九條規定,各類數據的錄入、修改、保存等操作應當符合授權范圍、操作規程和管理制度的要求,保證數據原始、真實、準確、安全和可追溯。某些違法企業為規避在計算機管理系統中出現藥品從批發企業直接流向個人消費者的違法、違規風險,利用自身擁有的上游供貨資源及下游銷售網絡的優勢,通過本企業員工的微信或新媒體社交平臺(如抖音視頻、快手視頻等)渠道散布貨源信息并進行銷售(表1),通過虛構銷售記錄,隱瞞真實的銷售流向,造成賬貨實際流向不一致。外省市還存在個別連鎖企業總部利用總部的電商平臺,先將藥品郵寄給消費者,再通過電商平臺從旗下連鎖門店做銷售處理,看似符合要求,但藥品流向路徑與實際不符[4]。
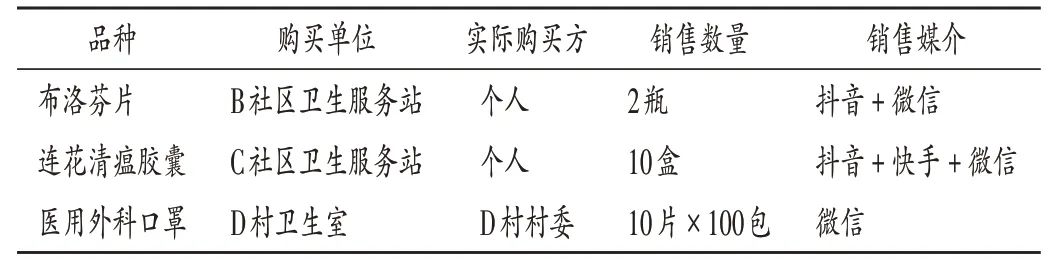
表1 批發企業A銷售調查情況Tab.1 Sales survey of wholesale company A
1.5 售后
1)服務不完整。線下購買可根據消費者的購買需要,很直觀地挑選藥品,且實體藥店在營業場所內設置有顧客意見簿,并在顯著位置懸掛有轄區監管部門的投訴舉報電話。消費者如果對門店藥學服務不滿意或對藥品質量有異議,可直接找商家反饋問題或向轄區監管部門投訴。《藥品管理法》第六十二條也規定了第三方平臺提供者應當對發生在平臺的藥品經營行為進行管理(表2)。部分大型電商消費平臺頁面標注了消費者維權熱線電話,并設立了投訴客服,但實際消費過程中,消費者遇到藥品質量問題或消費糾紛時,平臺往往要求消費者自行與入住電商協商或推諉拖延,售后服務效率往往很低;個別直播類的平臺主頁或直播間未設置相關售后維權的聯系方式或不明顯,消費者只能求助12315投訴平臺。

表2 2021年至2022年河南省安陽市藥品和醫療器械投訴、舉報情況(次)Tab.2 Complaints and reports on drugs and medical devices in Anyang City,Henan Province from 2021 to 2022(case)
2)不良反應信息收集難。GSP第一百七十五條明確要求企業應進行不良反應信息收集和反饋,消費者在實體店自行購買或在執業藥師指導下購買非處方藥,出現不良反應和用藥風險時可及時反饋至藥品經營企業,而網上購買藥品則嚴重缺乏這方面的措施和渠道。電商平臺和入駐企業忽視不良反應信息收集環節,鮮有設置專門部門或配備專門人員負責收集不良反應信息,中斷了入駐企業與消費者間的關聯[5]。
2 存在問題與監管對策
2.1 藥品網絡銷售監管難
《藥品網絡銷售監督管理辦法》第二十八條對違法銷售行為的監管權限進行劃分[6],監管部門對電商平臺及平臺內的入駐企業可做到有法可依、違法必究[1]。針對直播或網絡視頻銷售中內容無法及時、準確甄別等情形,建議借鑒全國“掃黃打非”辦公室部署的“凈網行動”聯合整治網絡專項行動成功經驗,以現有國家藥品監督管理局構建的藥品網絡交易監測系統為載體,建立一支專業的國家級網絡巡查隊伍,利用多部門信息大數據一體化[4]和聲訊自動捕捉類軟件等方式,開展涉及銷售藥品、化妝品、醫療器械直播、網絡視頻閱評和監測等線上綜合監管工作,重點監控熱門直播或短視頻平臺,即時通信類社交平臺也可通過技術升級,充分利用現有科技手段,如對關鍵字、詞或同音的內容進行過濾并實時篩查。國家級巡查部門及時或定期將收集到的違法信息及證據移送相關省級藥品監管部門查處。既解決了各級監管部門對直播或網絡視頻內容無法及時甄別的困難,有效管控QQ、微信等“點對點”隱蔽性極強的違法銷售藥品行為,又理清了屬地監管權責的劃分。
2.2 網絡“水軍”虛假交易
2023 年“清朗”系列專項行動中對網絡“水軍”進行整治并取得了良好成效,但網絡“水軍”仍然存在,包括操縱信息、刷量控評、惡意營銷等[7]。隨著我國計算機及網絡科技應用技術的發展,利用群控軟件、發帖AI機器人等智能程序、新技術進行刷量刷評的現象也層出不窮。應壓實網站平臺主體責任,不斷提升網站平臺對抗機器人“水軍”的技術手段,強化自媒體賬號專業資質認證管理,對于從事醫療、司法、教育等專業領域信息內容生產的自媒體,務必要從嚴審核認證材料并加注標識[8]。
《藥品網絡銷售監督管理辦法》第九條、第十三條明確規定,如有需要購買處方藥或進行線上醫師診療。建議相關電商平臺在現有技術和審核辦法下,可通過視頻進行網絡確認再為消費者開具處方,平臺將整個過程截圖并按規定存檔保存,從技術和審核制度上避免網絡“水軍”或機器人“水軍”進行虛假交易。
2.3 無法有效實施GSP
1)各級、各地尚未建立基于《附錄6》的相關配套認證檢查方案。國家藥品監督管理部門首先應組織專家對國內知名或大型電商平臺自營藥品銷售的企業,按規范要求進行系統化的檢查和審評,確保電商平臺在實施規范要求和網絡運營中不會出現質量管理疏漏,并制訂對應的現場檢查指導原則,供下級監管單位比照執行。由國家藥品監督管理部門提供業務指導,相關電商平臺通過網絡技術升級改造,加強平臺對入住藥品經營企業資質和能否滿足《附錄6》要求的審核,同時建立監管部門與平臺的協查通報渠道。
2)省級藥品監督管理部門按照《附錄6》的要求,組織對本轄區內有網絡經營行為的批發或連鎖企業進行認證檢查或報告審查,必要時要求企業簽訂不違反網絡銷售管理規范承諾書,充分發揮大型網絡銷售企業的自律性,確保能依法、依規開展經營行為。
3)省轄市藥品監督管理部門依照《藥品網絡銷售監督管理辦法》的要求,對轄區內已報告的企業或經投訴舉報的企業,根據GSP、《附錄6》的要求進行飛行檢查或專項檢查,如有發現違規經營行為責令限期整改,逾期不整改除按相關法律法規處罰外,所在電商平臺還應做下架或封號處理。
2.4 售后和不良反應信息收集難
1)《藥品廣告審查辦法》《藥品廣告審查發布標準》等法規文件自頒布以來,藥品廣告形式已發生了巨大變化,針對新業態、新模式下的售前和售后,應規范網上藥店宣傳頁面內容和布局,并結合消費者用藥行為和風險因素,編制藥品廣告遵循的要件規則及藥品廣告新應用場景的市場監管策略,可參照平臺企業責任落實等指標[9]。
2)應依據《藥品管理法》《消費者權益保護法》《電子商務法》等法律加快制訂并完善包括但不限于藥品售后主體責任,每個售后環節都應有承擔責任及賠償損失的制度。因交易信息誤導導致的售后糾紛,應在平臺運營監管中避免,如未采取應對措施,消費者可根據損失要求交易平臺賠償或代償。交易平臺應對入住的藥品經營企業進行形式審查,對其相關的合法證照、藥品質量管理體系等信息進行確認,盡到平臺的監管義務。若發生嚴重的售后事件,平臺應及時向入駐企業所在地的行政監管部門報告,則可不承擔法律責任[10]。
3)《藥品不良反應報告和監測管理辦法》第二條規定:“國家實行藥品不良反應報告制度。藥品生產企業、藥品經營企業、醫療衛生機構應按規定報告所發現的藥品不良反應。”依托國家藥品不良反應監測系統,電商平臺應按《藥品網絡銷售監督管理辦法》的要求,不斷完善網絡銷售藥品的藥品不良反應監測制度及召回制度[11],加快制訂能有效追溯藥品質量售后服務及投訴的管理制度,加強對入駐企業和自營業務的質量監督和管控。
3 建議
藥品網絡銷售已成為快速發展的新業態,成為提升群眾用藥可及性的重要手段。我國可借鑒歐洲國家的典型做法,推行兼具政府行政監管和協會行業自律的互聯網藥品銷售共治管理模式,即以政府主導管理為基礎,以協會管理互聯網經營全過程為抓手,充分發揮既有行業協會如執業藥師協會的作用,明確其在互聯網藥品銷售過程中應承擔的職能,形成“政府+行業”的管理新格局[12]。堅持安全與發展并重,按國家藥品監督管理局探索“以網管網”“以快制快”的監管措施加強監管力度[13]。同時,第三方平臺企業要統籌考慮發展與安全問題,牢固樹立安全風險意識和質量安全第一的意識;以《藥品網絡銷售監督管理辦法》為抓手,切實履行企業主體責任,持續提升藥品流通全過程質量安全管理能力;持續守法合規,采取多種措施規范藥品網絡銷售市場秩序[14],切實保障公眾的用藥安全和合法權益。

