HPLC-MS/ MS 法同時測定微量血漿中甲氨蝶呤、左乙拉西坦、拉莫三嗪濃度及其臨床應用
秦亞彬 張古英 趙德運
河北省兒童醫院藥學部,河北石家莊 050031
甲氨蝶呤是抗葉酸類抗腫瘤藥,廣泛應用于急性淋巴細胞白血病、淋巴瘤等疾病的化療[1-2]。研究顯示,常規監測甲氨蝶呤血藥濃度可以有效降低不良反應發生率[3-5]。左乙拉西坦和拉莫三嗪為第二代抗癲癇藥,在患兒中有較好的療效[6-8]。左乙拉西坦和拉莫三嗪聯合應用或用于兒童、孕婦和肝腎功能異常的患者時,建議監測血藥濃度[9-10]。
甲氨蝶呤、左乙拉西坦和拉莫三嗪均屬于兒童治療藥物監測的常規品種[11-12]。實際臨床治療過程中存在癲癇患者聯合使用兩種抗癲癇藥的現象,癲癇合并白血病患者有兩種藥物聯用的可能。甲氨蝶呤和左乙拉西坦均為P-糖蛋白底物,兩者聯用可導致甲氨蝶呤的藥動學參數發生變化,繼而影響其濃度,增加腎毒性[13]。
HPLC-MS/MS 法具有良好的分離能力和選擇性,可以同時檢測多種藥物,近年來被廣泛用于治療藥物的監測工作[14-15]。兒童血管細小,采血困難。故本研究嘗試采用微量血漿樣本,建立同時測定甲氨蝶呤、左乙拉西坦、拉莫三嗪濃度的HPLC-MS/MS 法,以用于患兒血藥濃度監測,為合理用藥提供保障。
1 儀器與試藥
1.1 儀器
Agilent 1260 高效液相色譜儀(美國安捷倫公司);Agilent Ultivo 三重四極桿質譜儀(美國安捷倫公司);低溫高速離心機(北京白洋醫療器械有限公司);渦旋混合器(杭州佑寧儀器有限公司)。
1.2 藥品與試劑
甲氨蝶呤對照品(中國食品藥品檢定研究院,批號:100138-201704,純度:99.4%);內標甲氨蝶呤-D3(上海源葉生物有限公司,批號:H17M9Q56012,純度>98.0%);左乙拉西坦(成都德思特生物技術有限公司,批號:DST-190223-028);內標左乙拉西坦-D6,(深圳海思安生物技術有限公司,批號:30001101,純度:98%);拉莫三嗪(中國食品藥品檢定研究院,批號:100775-201902,純度:99.7%);內標拉莫三嗪-13C3-D3(深圳海思安生物技術有限公司,批號:30002385,純度:98%);甲醇為色譜純(賽默飛世爾科技有限公司);甲酸為色譜純(美國MREDA 公司);純凈水(杭州娃哈哈集團有限公司);血漿均來源于河北省兒童醫院。
2 方法與結果
2.1 色譜及質譜條件
2.1.1 色譜條件 分析柱為Agilent C18(50mm×2.1mm,1.8μm);流動相0.1%甲酸水(A)和甲醇(B)梯度洗脫(0.00~0.50 min,98%→95%A;0.50~1.50 min,95%→5%A;1.50~2.40 min,5% A;2.41~2.50 min,95% →98% A;2.50~3.50 min,98%A);柱溫:45℃;自動進樣器溫度:8 ℃;流速為0.4 ml/min;進樣體積:3 μl。
2.1.2 質譜條件 離子源:電噴霧離子源,正離子模式;鞘氣溫度:280 ℃,鞘氣體積流量:11 L/min;噴嘴電壓:500 V;霧化器壓力:15 psi;毛細管電壓:正電壓4 000 V;干燥氣溫度:300 ℃,干燥氣體積流量7 L/min;多反應監測掃描分析。
離子通道選擇:甲氨蝶呤m/z 455.1→308.2,內標甲氨蝶呤-D3 m/z 458.1→311.1;左乙拉西坦m/z 171.1.4→126.2,內標左乙拉西坦-D6 m/z 177.2→132.2;拉莫三嗪m/z 256.1→211,內標拉莫三嗪-13C3-D3 m/z 262.1→217.1。碰撞能均為20 eV。
2.2 溶液配制
2.2.1 對照品及內標溶液制備 準確稱取甲氨蝶呤10.3 mg 置于50 ml 容量瓶中,左乙拉西坦、拉莫三嗪各20 mg 置于5 ml 容量瓶中,甲氨蝶呤-D3、左乙拉西坦-D6、拉莫三嗪-13C3-D3 各1 mg 用甲醇/ 水(V/V=1/1)分別溶解,超聲助溶并稀釋至刻度,獲得儲備液。用甲醇/水(V/V=1/1)對儲備液逐級稀釋獲得一系列濃度對照品的標準溶液及500 ng/ml 甲氨蝶呤-D3、30 μg/ml 左乙拉西坦-D6 和15 μg/ml 拉莫三嗪-13C3-D3 的混合內標溶液,-80℃冷凍保存。
2.2.2 標準曲線和質控樣品制備 精密吸取50 μl 甲氨蝶呤、50 μl 左乙拉西坦和50 μl 拉莫三嗪各濃度標準溶液加入離心管中,再加入1 850 μl 空白血漿渦旋混勻,制成6 個濃度系列的混合標準曲線。甲氨蝶呤的濃度為25、50、100、500、1 000、1 500 ng/ml,左乙拉西坦的濃度為1、2、5、10、25、50 μg/ml,拉莫三嗪的濃度為0.5、1.0、2.5、5.0、12.5、25.0 μg/ml。
另取適量儲備液用空白血漿稀釋制得3 個濃度水平的混合質控樣品。其中甲氨蝶呤的質量濃度為75、300、1 200 ng/ml,左乙拉西坦的質量濃度為3、20、40 μg/ml、拉莫三嗪的質量濃度為1.5、10.0、20.0 μg/ml。
2.3 樣品前處理
精密吸取10 μl 血漿樣本,加入10 μl 混合內標溶液和100 μl 甲醇,渦旋1 min,11360 r/min 離心10 min,離心半徑為50 mm,取50 μl 上清液,用水稀釋5 倍后轉移至進樣瓶供進樣分析。
2.4 方法學驗證
根據《中華人民共和國藥典》[14]生物樣品定量分析方法驗證指導原則,從選擇性、殘留、定量下限、校準曲線、準確度和精密度、稀釋可靠性及穩定性方面對方法進行驗證。
2.4.1 特異性考察 取6 個不同批次的空白血漿以等體積的甲醇/水(50/50)替代內標溶液,按“2.3”項下方法處理分析,記錄空白血漿樣品色譜圖。另取上述6 份空白血漿配制成分析物標準血漿溶液,按“2.3”項下方法處理后進樣,記錄待測物和內標物的色譜圖。結果顯示,血漿中內源性物質不干擾甲氨蝶呤、左乙拉西坦和拉莫三嗪及其內標物的測定。見圖1。
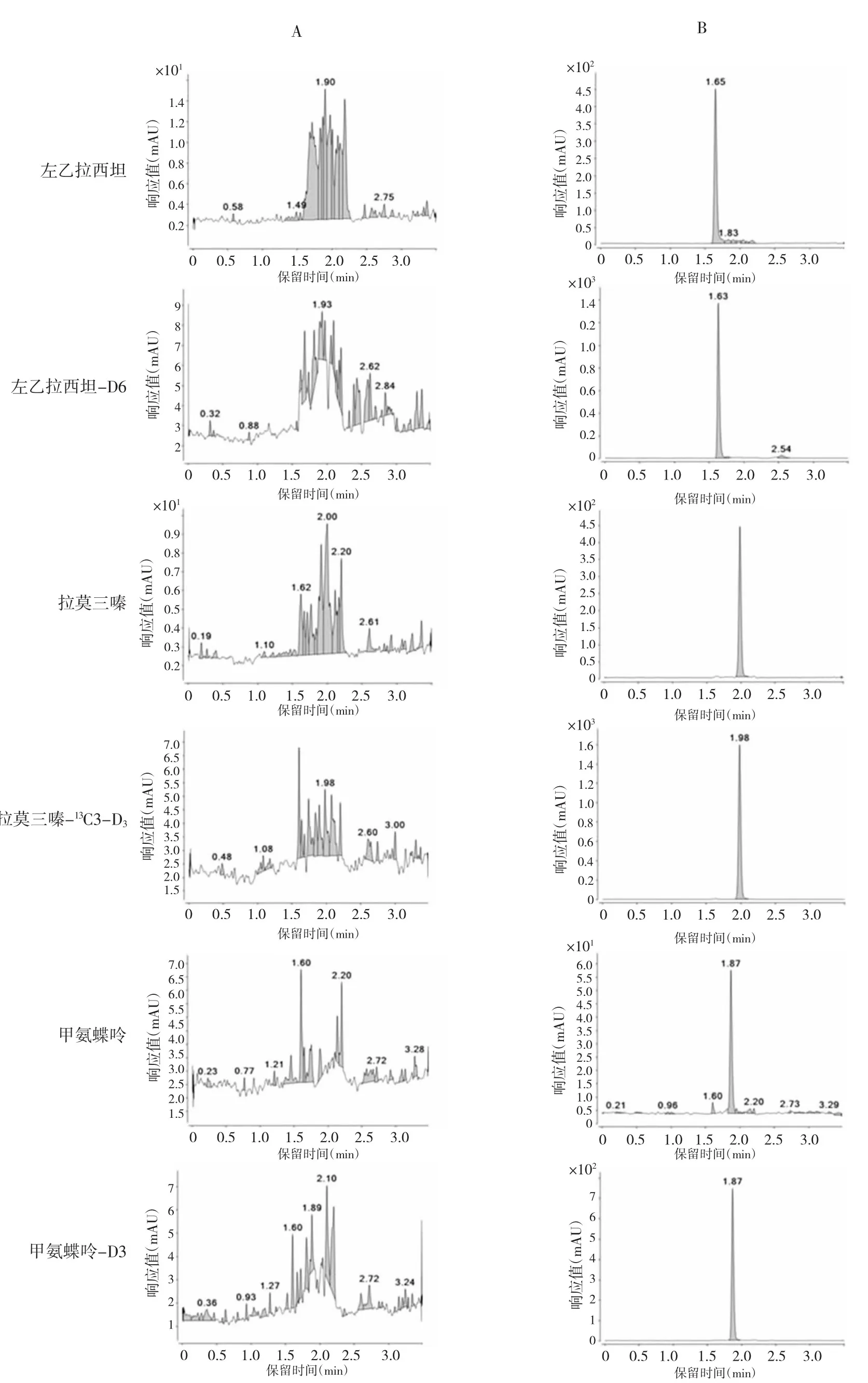
圖1 左乙拉西坦、拉莫三嗪和甲氨蝶呤及內標物的典型色譜圖
2.4.2 標準曲線與定量下限 將“2.2.2”項下6 個濃度的樣品,按“2.3”項下方法處理后進樣檢測。采用最小二乘法進行回歸擬合,求得直線回歸方程并計算校正標樣濃度。甲氨蝶呤在25~1 500 ng/ml 線性關系良好,標準曲線方程:Y=0.251 6X+0.003 4(r=0.998 9),定量下限為25 ng/ml;左乙拉西坦在1~50 μg/ml 線性關系良好,標準曲線方程:Y=16.687 6X+0.000 2(r=0.991 1),定量下限為1 μg/ml;拉莫三嗪在0.5~25.0 μg/ml 線性關系良好,標準曲線方程:Y=46.369 5X-0.059 9(r=0.999 1),定量下限為0.5 μg/ml。定量下限信噪比均>5,符合定量要求。
2.4.3 精密度與準確度 混合質控樣品和定量下限濃度樣品按“2.3”項下方法處理后進樣測定,每個濃度平行測定5 份,批內及批間準確度和精密度結果均符合要求。見表1。
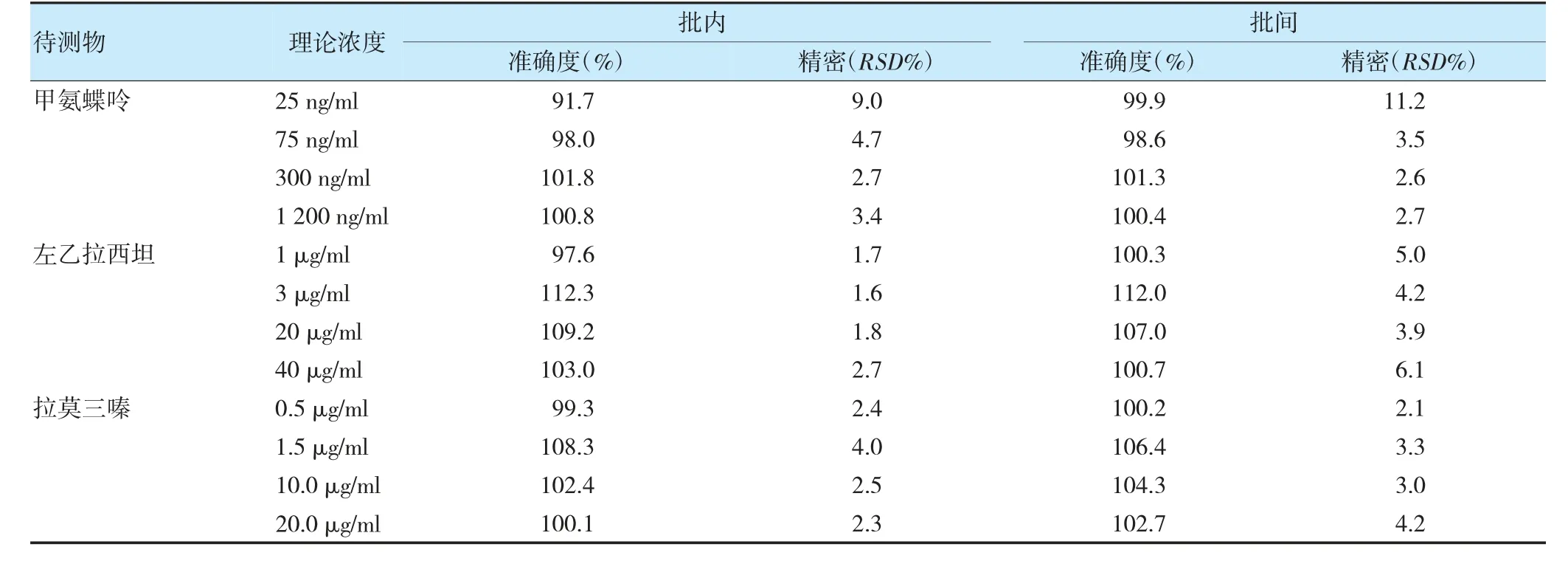
表1 批內及批間精密度及準確度結果
2.4.4 基質效應取6 個不同個體來源的空白血漿,按“2.3”項下方法配置低、高濃度的混合質控樣品,分別計算經內標歸一化后的基質效應因子及變異系數(coefficient of variation,CV)。結果顯示,經內標歸一化后,各化合物基質效應因子的CV 均<15%,樣品測定不受基質的影響。見表2。
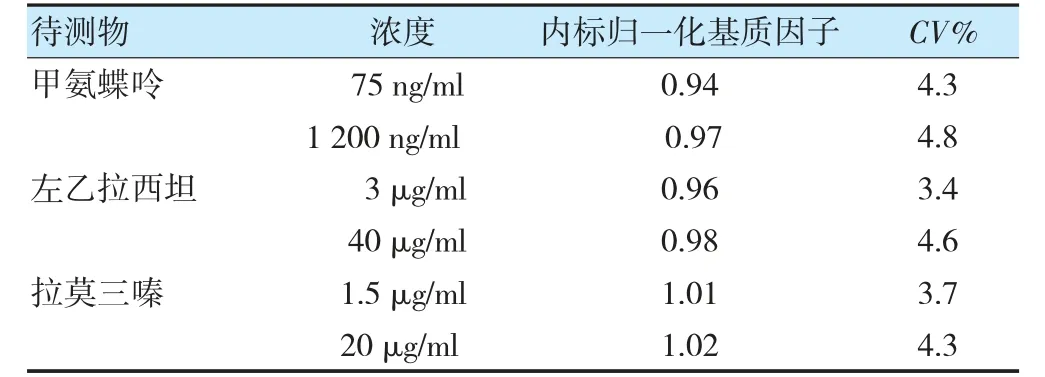
表2 各待測藥物在人血漿中的基質效應
2.4.5 殘留效應 系統殘留分析是對定量上限樣品分析后立即分析空白血漿樣品。要求殘留不超過待測物定量下限的20%,不超過內標峰面積的5%。結果顯示,殘留符合接受標準。
2.4.6 稀釋可靠性 分別配制高于定量上限的標準樣品,其中甲氨蝶呤質量濃度為30 μg/ml、左乙拉西坦和拉莫三嗪濃度均為100 μg/ml,用空白血漿稀釋上述樣品,使稀釋后樣品質量濃度在標準曲線的線性范圍內,平行5 份,計算稀釋后樣品測定結果的準確度和精密度。結果均<15%,符合標準。
2.4.7 穩定性 制備低、高濃度水平的混合質控樣品,分別考察室溫放置24 h、-20 ℃凍存2 周、反復凍融3次及自動進樣器保存12 h 的穩定性。結果顯示,甲氨蝶呤、左乙拉西坦和拉莫三嗪在以上條件下均不影響其測定準確度。見表3。
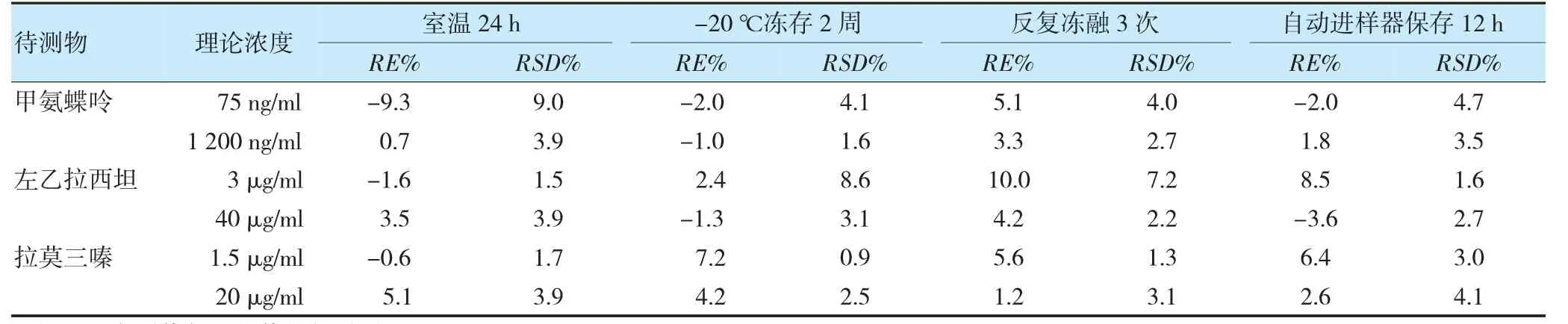
表3 穩定性結果
2.5 臨床應用
建立的檢測方法經驗證后應用于治療藥物監測。2022 年10 月至2023 年3 月共檢測了1 348 例患兒樣本。患兒采血后置于EDTA 抗凝采血管,4 000 r/min離心10 min,離心半徑為100 mm,取血漿;按“2.3”項下方法處理后檢測。共檢測甲氨蝶呤360 例,均為腫瘤維持性化療患兒,大劑量輸注甲氨蝶呤后24、48、72 h采血,其測定范圍在0.055~132.350 μmol/L。左乙拉西坦830 例、拉莫三嗪158 例,均為癲癇患兒,口服左乙拉西坦或拉莫三嗪1 周以上(達穩態后),于清晨服藥前采血(谷濃度),左乙拉西坦測定范圍在1.00~44.19 μg/ml;拉莫三嗪測定范圍在0.50~17.68 μg/ml。本研究經河北省兒童醫院醫學研究倫理委員會批準(醫研倫審第202210 號)。
3 討論
文獻報道,HPLC-MS/MS 法主要用于同時測定多種理化性質相似的同類藥物[15-17]。而本研究嘗試同時檢測理化性質相差較大不同類藥物。在優化色譜和質譜條件時,嘗試了不同比例的流動相和添加劑,最終采用梯度洗脫并且流動相添加甲酸的方法,使甲氨蝶呤、左乙拉西坦和拉莫三嗪均有合適的保留時間,峰形較好,無拖尾現象,可以滿足檢測要求。另外,與已知方法比較,本研究只需要10 μl 血漿,非常適用于兒童等采血困難群體[18-21]。
在生物樣本分析的前處理方法中,蛋白沉淀法因其處理簡便,易于操作,廣受青睞[22]。本研究選擇甲醇作為沉淀劑,待測物有足夠的提取回收率,可以滿足檢測需求。樣品前處理采用蛋白沉淀法,往往不能完全去除蛋白、鹽類和磷脂,這些內源性干擾能引起基質效應[23]。本研究中采用與待測物結構相似的同位素標記作為內標,以降低基質效應的干擾。同位素內標具有與待測物相同的色譜行為,是HPLC-MS/MS 法最合適的內標[24]。另外,樣品經蛋白沉淀法后的上清液,加水稀釋5 倍后再進樣,以降低基質干擾[25]。
本研究建立了可以同時測定血漿中甲氨蝶呤、左乙拉西坦和拉莫三嗪的HPLC-MS/MS 法,該方法可以用于治療藥物監測,也適用于藥物相互作用及藥動學研究,為藥物的合理使用提供參考依據。
利益沖突聲明:本文所有作者均聲明不存在利益沖突。

