促性腺激素釋放激素類似物治療下丘腦錯構瘤導致性早熟5例臨床分析
伊 鵬,李翠玲,黃新疆,曾春華
(廣州醫科大學附屬婦女兒童醫療中心 廣東省兒童健康與疾病臨床醫學研究中心,廣東 廣州 510623)
下丘腦錯構瘤(hypothalamic hamartoma,HH)又稱灰結節錯構瘤、下丘腦神經元錯構瘤。錯構瘤不是真正的腫瘤,是器官內正常組織的錯誤組合與排列。錯構瘤生長緩慢,可發生在全身任何部位,極少惡性變。HH主要由異位腦灰質、神經元、神經膠質細胞和纖維束等組成。發病率約為 1/50萬~1/100萬,多數在嬰幼兒期發病,男女比例約1.52∶1[1]。2007年世界衛生組織在關于中樞神經系統腫瘤的分類中,將HH歸于類腫瘤病變[2]。其臨床表現主要為中樞性性早熟和癡笑樣癲癇。此外,也有部分HH患兒伴發認知功能障礙和其他類型癲癇(如癲癇大發作、全身發作等),也見無癥狀病例報道[3]。
既往主張表現為單純性早熟的HH患兒首選手術治療。自1980年,促性腺激素釋放激素類似物 (gonadotropin releasing hormone analogue, GnRHa)成為中樞性性早熟的首選治療方案[3-4]。本文通過對GnRHa治療HH導致性早熟患兒5例進行回顧性分析,旨在為臨床提供依據。
1 資料與方法
1.1病例選擇 選取2017年5月至2021年5月廣州醫科大學附屬婦女兒童醫療中心診治的HH患兒5例。納入標準:①有性早熟的臨床表現:女孩表現為乳腺發育,陰道出血,陰毛生長等。男孩表現為睪丸陰莖增大,陰毛生長等。②頭顱磁共振成像(magnetic resonance imaging,MRI)檢查明確診斷HH。③排除其他疾病因素以及飲食藥物因素導致的性早熟的可能。
1.2資料收集和治療方案 收集患兒的一般資料和臨床表現(性別、身高、體重、初診年齡、主要癥狀、主要體征、初診骨齡、頭顱MRI檢查)、實驗室檢查、療效評價。
1.2.1實驗室檢查 GnRHa激發試驗采用的藥物是醋酸曲普瑞林注射液0.1 mg,靜脈注射,劑量按照2.5 μg/kg,最大不超過0.1 mg。若促黃體生成素(luteinizing hormone,LH)基礎值大于10 IU/L,不再進行性激素激發實驗。于注射前(基礎值)和注射后30、60、90、120 min分別采血測定血清促卵泡激素(follicle stimulating hormone, FSH)和LH。當LH峰值大于10 IU/L認為性腺軸功能已經啟動,判定為中樞性性早熟。當患兒使用GnRHa治療3次后復查簡易GnRHa激發試驗,只采集注射前(基礎值)和注射后60 min的血,測定血清FSH和LH。
1.2.2治療方案 ①使用醋酸亮丙瑞林注射液(3.75 mg)或醋酸曲普瑞林注射液(3.75 mg)抑制性發育治療, 起始劑量約為100 μg/kg,每月1針。根據后續性發育的變化情況,調整藥物的劑量。維持劑量100 μg/kg,如果性發育明顯減緩,將給以藥物減量至60~80 μg/kg。根據每個患兒的情況,給以復查子宮卵巢超聲,性激素,骨齡。②避免服用人參、燕窩、鹿茸、動物卵巢胎盤等。避免大量使用糖皮質激素類藥物,避免誤服避孕藥物。
2 結 果
2.1一般資料和臨床表現 5例患兒中,女性3例,男性2例。初診年齡為6月~8歲。女童主要表現為乳腺發育和陰道出血,男童主要表現為陰莖睪丸增大。初診骨齡均有超前,頭顱MRI檢查均發現下丘腦灰結節區有占位性病變。見表1。
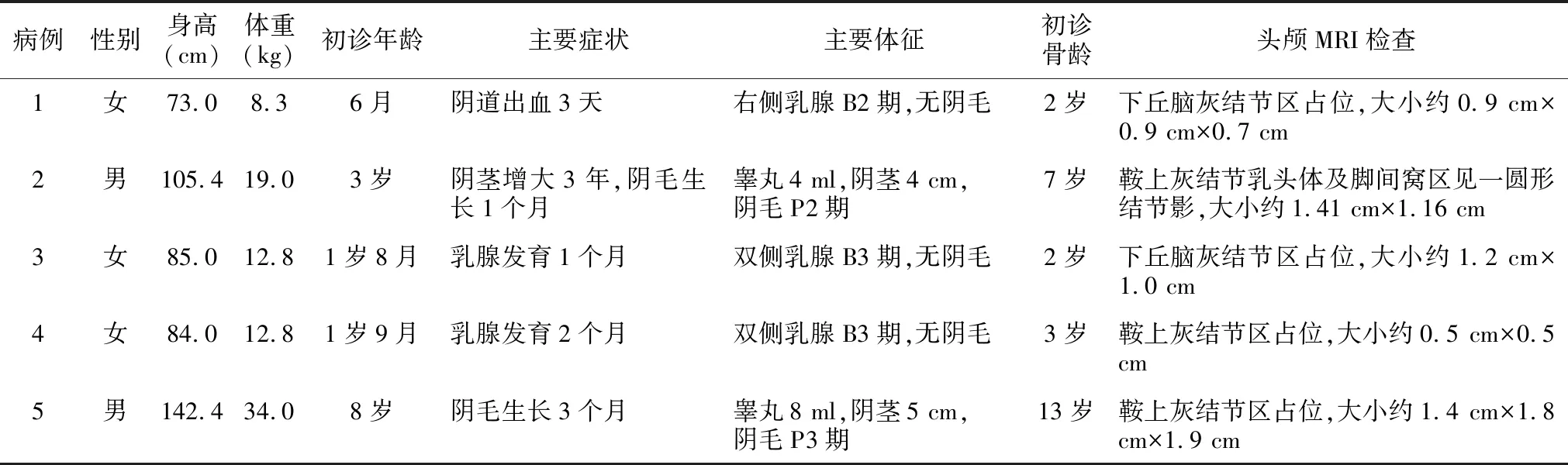
表1 患兒一般資料
2.2實驗室檢查 5例患兒均行GnRHa激發試驗和簡易GnRHa激發試驗,見表2~3。
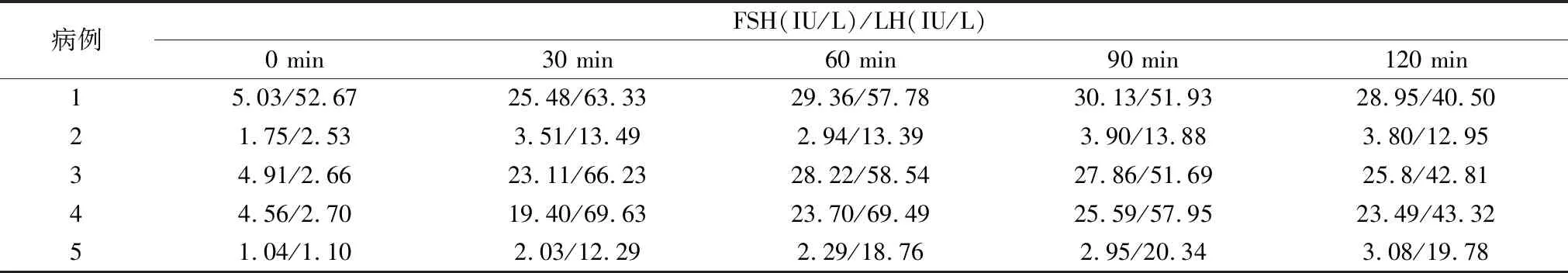
表2 GnRHa激發試驗
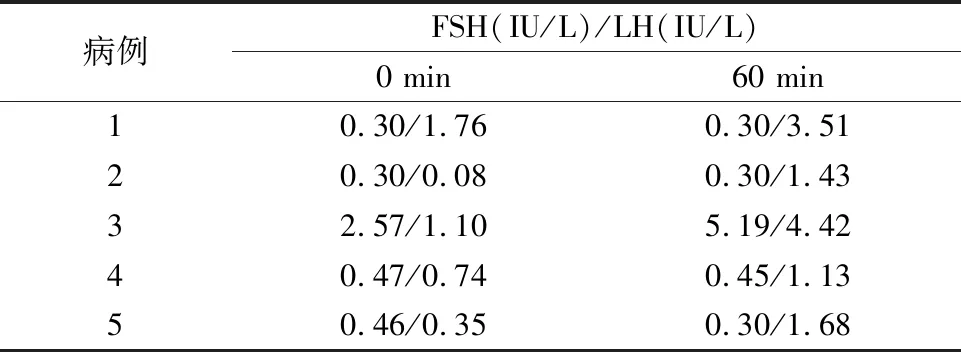
表3 簡易GnRHa激發試驗
2.3療效評價 5例患兒性激素水平均明顯下降。病例1月經消失,乳腺從B2期減小到B1期。病例2和5的陰莖睪丸沒有進一步增大。病例3和4乳腺從B3期減小到B2期。見表4。
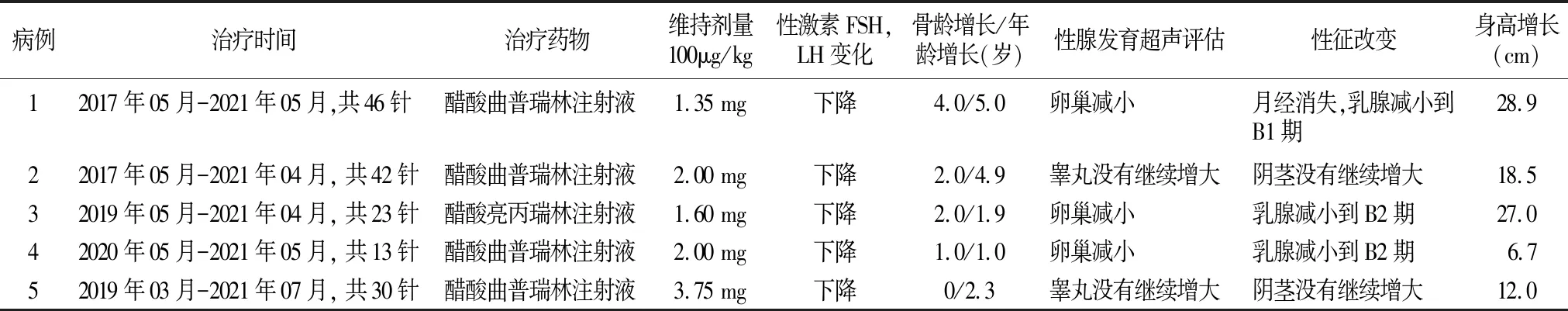
表4 治療藥物效果評價
經過治療3次以后,總體FSH和LH值均獲得明顯下降。除LH 0 min,治療后FSH 0 min,FSH 60 min及LH 60 min較治療前降低,差異均具有統計學意義(P<0.05)。見表5。
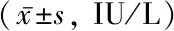
表5 FSH和LH治療前后比較
3 討 論
HH并非真正的腫瘤,而是一種異位的神經組織塊,起源于下丘腦乳頭體和灰結節間,向下生長至腳間窩的蛛網膜下腔,由內分泌神經元纖維和膠質細胞構成[5]。國外報道女性多于男性。本病多在兒童期發病,主要臨床表現為癡笑樣癲癇,性早熟,行為異常及智力低下等[6]。癡笑樣癲癇表現為發作性傻笑,持續數秒或者數十秒,發作時意識清醒,每天可反復發作。女孩性早熟表現為乳腺發育,陰毛生長,月經初潮等。男孩性早熟表現為陰囊陰莖增大,外陰色素沉著,陰毛生長等。性早熟是由于錯構瘤可釋放促性腺激素釋放激素,進而刺激垂體分泌促性腺激素所導致。癡笑樣癲癇與錯構瘤有異常放電或錯構瘤分泌致癇神經肽有關。也要注意HH少見的臨床表現,比如陣發性強直性眼偏斜[7],糖尿病[8],嬰兒痙攣[9],神經纖維瘤[10]。
HH發病原因可能為中線神經管閉合不全所致。它可單獨存在,也可以同時伴有其他發育異常,如胼胝體缺如,視隔發育不良,灰質異位和大腦半球發育不良等。MRI檢查顯示腳間池內相當于乳頭體,灰結節和垂體柄處有等信號腫物。HH分為2個類型:Ⅰ型為“有蒂型”,表現為HH附著于灰結節、乳頭體或兩者間,下丘腦無變形,此類患者表現為性早熟或無癥狀,首選藥物治療;Ⅱ型為“無蒂型”,指HH有廣泛的基底面并長入下丘腦和第三腦室,導致下丘腦和第三腦室變形,此類患者表現為癡笑樣癲癇及認知功能障礙,首選手術切除病灶[11]。
通過全外顯子測序的方式檢測切除的錯構瘤標本和外周血,在37%的HH導致的癡笑樣癲癇患者中,可發現位于Hedgehog信號通路上的基因突變[12],例如GLI3基因突變[13]。GLI3基因突變會導致pallister hall綜合征,其臨床表現包括HH,垂體功能減退,會厭分叉,肛門閉鎖,并指(趾)及多指(趾)畸形。有學者在HH患者中發現了染色體6p25.1-25.3區域的序列重復,考慮可能為致病的遺傳因素[14]。
自1980年,如HH患兒只表現為性早熟,未合并癲癇等其他癥狀,首選治療方案為單獨使用GnRHa,不建議手術治療[15-16]。但是藥物治療的缺點是費用高,每年需要2萬元左右。每個月需要打針,用藥時間長,需要持續到正常的青春期年齡。手術治療適用于以下性早熟患者:①GnRHa治療不能控制性早熟者;②雖然GnRHa治療可以控制性早熟,但是患者在用藥期間,又出現了癡笑樣癲癇等神經系統癥狀;③患者家庭無法承擔長期藥物治療的經濟成本和時間成本。如果HH患兒一開始就表現為癲癇,則就首選手術治療[17-18],另外也有多種新的手術方式可供選擇,如神經內鏡離斷術、伽瑪刀照射、射頻熱凝術、激光間質熱療等。
有研究報道14例HH導性早熟患兒接受GnRHa治療后,追蹤到成人期,均達到了正常的成年身高,未合并生殖系統疾病[19]。楊培蓉等[20]使用醋酸曲普瑞林注射液治療4例HH致性早熟患兒,患兒的性發育均獲得明顯的抑制。本研究5例患兒癥狀均獲得了良好控制,家長對于治療效果滿意,患兒成年期的身高還需要進一步的追蹤。

