密度泛函理論研究富勒烯C70對偏二甲肼與NO2的抽氫反應機制
趙子航,慕曉剛,王生輝,馬海霞,
(1.西北大學 化工學院/西安市特種能源材料重點實驗室,陜西 西安 710069;2.火箭軍工程大學,陜西 西安 710025)
引 言
液體燃料作為動力源在航天航空和軍事領域被廣泛使用[1]。其中,肼類燃料和四氧化二氮(NTO)組成的雙組元推進劑具有很強的可靠性,可應用于多種火箭發動機中[2,3]。此外,肼類燃料具有短點火延遲時間、高比沖、良好的自燃特性等優點,是作為液體推進劑的較好選擇。目前肼類燃料主要包括肼、甲基肼、偏二甲肼(UDMH)。研究人員針對不同肼類燃料進行了理論及實驗研究[4-11],結果表明肼類燃料與NTO發生熱分解反應產生NO2,是氣相反應之初最主要且能參與后續反應的自由基。趙建爍等[12]通過前線軌道理論分析3種肼類燃料與NO2的反應過程后發現UDMH反應活性最佳,UDMH是3種肼類燃料中最容易與NO2發生反應的物質。因此,選擇適宜的UDMH燃燒催化劑,加速UDMH的分解,可以提高液體推進劑的性能。采用理論計算方法研究可用于促進UDMH分解的催化劑,能夠避免實驗中UDMH的高毒性對試驗人員的危害,并且為后續的實驗研究提供參考。
相比于傳統碳材料,富勒烯特殊的電子性質、多孔結構和較大的比表面積使其具有更好的催化作用[13],在能源工業、材料科學、生物醫藥等領域具有極高的應用價值[14-19]。自1990年突破了毫克級富勒烯的制備技術[20],研究人員針對富勒烯制備出一系列富勒烯分子及其衍生物。因此,C60、C70成為最穩定且最廣泛生產的兩種富勒烯。趙楊等[12]研究了富勒烯及其衍生物作為不同組分在含能材料中的應用,闡述了富勒烯作為含能組分、催化劑等的優秀表現,并且研究中提到C70具有良好的化學活性以及多種功能衍生化的可能性。
本研究建立了UDMH在C70表面的不同吸附構型,通過密度泛函理論(DFT)對其吸附行為進行研究,以探究C70對UDMH性能的影響。
1 計算方法
采用Material Studio (Version 8.0)軟件的DMol3模塊[21-22]進行模型優化,該軟件基于密度泛函理論開發。在對模型進行幾何優化時,泛函選用廣義梯度近似(GGA)[23]中的Perdew-Burke-Ernzerh (PBE)[24]交換關聯勢,以描述體系中電子交換相關作用。在搜索穩定模型的過程中,分別設置能量、受力和位移的收斂標準為2×10-5Ha (1Ha=27.21eV)、2×10-3Ha/nm和5×10-4nm;熱占位中Smearing的參數設置為0.01Hatree。弱相互作用修正采用Tkatchenko-Scheffler[24]方法。價電子波函數采用雙數值極化函數展開(DNP),截斷半徑為0.44nm。布里淵區采樣k點設置為1×1×1[25],研究中所有化學物質模型的原子核處理方式均為All electron,對物質中所有電子都進行處理。
在研究基元反應的過程中,采用完全線性同步聯合二次同步(LST/QST)方法進行過渡態搜索[26],以探究反應機理、計算C70加入前后UDMH分解的反應勢壘和反應熱。
吸附質在催化劑表面的吸附能可由公式(1)計算獲得[26]:
Eads=EUDMH/C70-(EC70+EUDMH)
(1)
式中:Eads為吸附能;EUDMH/C70為吸附后UDMH/C70體系的總能量;EC70、EUDMH分別為吸附前C70和UDMH單獨物質的能量。根據式(1)吸附能計算結果可以快速判斷吸附過程的吸放熱情況以及吸附的穩定性。
圖1為C70和UDMH的三維結構。C70富勒烯是一個對稱的碳分子,它是由70個碳原子組成的一個球形團簇。UDMH分子主要由兩個非極性基團—CH3和一個極性基團—NH2組成。因此,本研究將UDMH放置于C70附近進行幾何優化且沒有虛頻的穩定吸附構型作為研究對象。
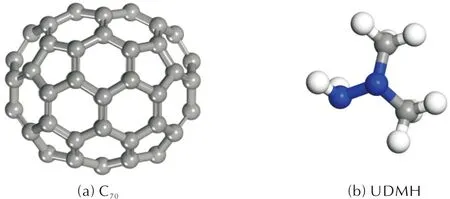
圖1 C70和UDMH的三維結構Fig.1 The three-dimensional structures of C70 and UDMH
2 結果與討論
2.1 UDMH分子C70上的吸附行為
C70團簇的分子結構存在一定的對稱性[18,19],故僅考慮少數位點作為吸附位點。經結構優化得到兩種不同的吸附構型如圖2所示。規定圖1(a)為C70正面圖像,圖2中(1)、(2)分別為A構型的正視圖與側視圖;(3)、(4)為B構型的正視圖與側視圖。
如圖2所示,相對于C70分子,A構型中UDMH分子的NH2基團和CH3基團均位于C70六元環的上方;B構型中NH2基團位于C70分子中六元環上方,CH3基團則位于五元環上方。此外,A構型中UDMH分子中NH2基團上N原子與C70分子的最短距離為3.396?,B構型中的最短距離為3.645?,較長的距離意味著兩個分子之間的氫鍵較弱。

圖2 兩種不同C70-UDMH吸附優化構型Fig.2 Two different kinds of optimized conformations of C70-UDMH
對兩種構型中UDMH的吸附能進行計算,結果顯示,UDMH在C70上的吸附能分別為:A構型-0.1392eV、B構型-0.1422eV。較低的吸附能表明UDMH分子可能以物理吸附的形式吸附于C70上。通過對純C70、UDMH以及兩種構型進行態密度和分子間距離計算,進一步證明C70和UDMH二者之間的吸附為物理吸附。各個結構的局域態密度(LDOS)如圖3所示。由圖3(a)、(c)和(d)可知,UDMH與C70形成穩定吸附構型后,C70中的態密度峰發生變化,主要發生在-9~-2eV范圍內,說明UDMH和C70之間發生了電子轉移。N原子的DOS峰分布于C70分子分布能級的-20~0.5eV范圍內,并且在-7~-4eV存在部分重疊。將圖3(c)、(d)兩種構型的DOS圖像相比,在-7~-3eV能級范圍內,A構型中C70的DOS峰的峰值比B構型更高,且圖2(b)中N原子的DOS峰形和能級并無改變。盡管兩種分子間的DOS峰有部分重疊,但是分子間距離較遠,不具備形成共價鍵的條件(采用兩個成鍵原子半徑之和的0.6~1.5倍長度來判斷共價鍵的形成與斷裂)[27]。
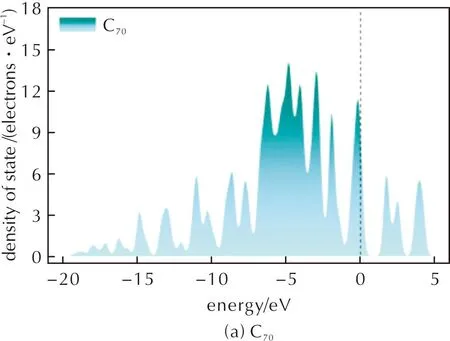
圖3 各個結構的局域態密度圖像Fig.3 Local density of states of different structures
2.2 C70與UDMH的相互作用
基于文獻研究[9,12]確定無C70作用時UDMH在NO2自由基存在時的初始分解及次級分解路徑。將NO2自由基分別放置于CH3和NH2基團并進行抽氫反應過渡態(TS)搜索。計算結果表明,在NH2基團上發生的抽氫反應勢壘為34.1kJ/mol,反應熱為31.4kJ/mol,在CH3基團上的反應勢壘為83.0kJ/mol,反應熱為82.9kJ/mol。NH2基團上抽氫反應具有較低的反應勢壘,與文獻報道一致[11]。
基于上述結果,次級反應仍選擇NH基團上發生,以NO2靠近NH基團并發生H原子轉移的結構分別作為基元反應的始態(IS)、終態(FS)結構。在NH2上發生的兩步抽氫反應中IS、TS、FS結構如圖4所示,相應的反應能量曲線如圖5所示。UDMH分解初始及次級反應過渡態搜索結果均符合過渡態的搜索結果。
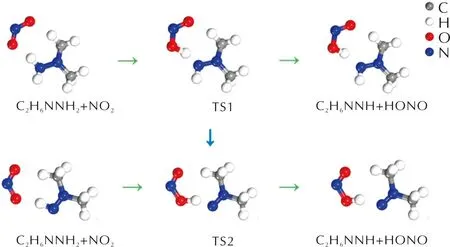
圖4 UDMH分解的兩步基元反應結構示意圖Fig.4 Schematic diagram of two-step elementary reaction structure for UDMH decomposition

圖5 UDMH分解的兩步基元反應的能量曲線Fig.5 Energetic profiles of two-step elementary reaction for UDMH decomposition
當NO2自由基靠近UDMH分子,NH2基團上H原子會發生解離,并轉移至NO2自由基上,從而生成C2H6NNH和HONO,反應活化能為34.1kJ/mol,反應熱為31.4kJ/mol。第二步抽氫反應以同樣的方式進行,經過NO2自由基在NH基團上抽氫,形成C2H6NN和HONO(圖4),該基元反應的活化能和反應熱分別為28.7kJ/mol和22.8kJ/mol。從數值上分析,第一步抽氫反應的活化能和反應熱都明顯高于第二步,由此說明第一步抽氫反應對于UDMH分解的發生具有決定性。
加入C70后,首先研究UDMH分解的起始反應位點可否發生在甲基,故研究了NO2從甲基上發生抽氫的可行性。在嘗試優化多種模型之后,都不能得到穩定的IS結構,無法進行后續的過渡態搜索和反應熱計算,表明加入C70后,NO2自由基在UDMH甲基上發生抽氫反應的位置仍然在NH2上。進一步計算獲得了A、B兩種構型與NO2相互作用的穩定構型,如圖6所示。
將NH2基團作為UDMH分解初始及次級反應的反應位點,分別選取在此基團附近吸附NO2自由基及對應的H原子轉移后的穩定結構作為反應的IS、FS結構。
對NH2基團上兩步抽氫反應進行過渡態搜索,得到的反應過渡態均只有一個虛頻,證明過渡態的搜索結果正確。C70吸附UDMH體系中兩步抽氫反應的IS、TS以及FS結構如圖6所示,對應的反應能量曲線如圖7所示。

圖6 兩種吸附體系中UDMH分解的基元反應結構圖Fig.6 The elementary reactions structuresdiagrams of UDMH decomposition in two adsorption systems
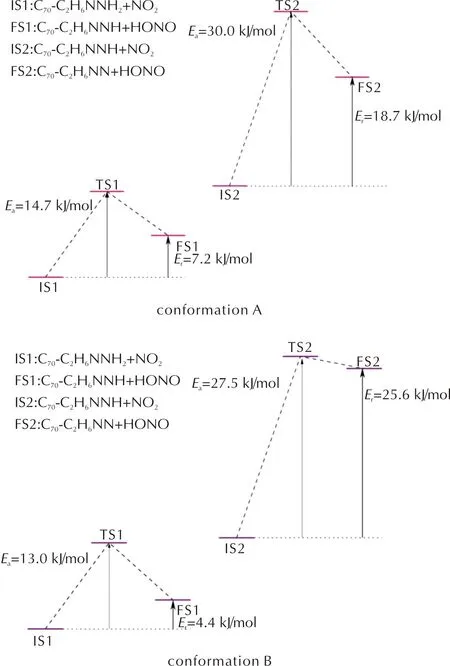
圖7 不同吸附構型UDMH分解的基元反應能量曲線Fig.7 Energetic curves of the elementary reactions for UDMH decomposition in different adsorption systems
當NO2自由基進入反應體系并發生反應時,反應形式與純UDMH分解相同,均為NO2自由基從NH2基團上抽取氫離子。隨著NO2自由基靠近UDMH分子,NH2基團上一個H原子轉移至NO2自由基上,形成C2H6NNH分子和HONO。由圖7可知,該基元反應在A構型體系中的活化能為14.7kJ/mol,反應熱為7.2kJ/mol;在B構型體系中活化能(13.0kJ/mol)和反應熱(4.4kJ/mol)相對更低。在第二步反應發生前,兩種構型中的C2H6NNH分子均發生了旋轉(圖6),但這并沒有影響抽氫反應的發生。其中A構型中抽氫反應的反應勢壘為30.0kJ/mol,反應熱為18.7kJ/mol,而B構型中反應勢壘為27.5kJ/mol,反應熱為25.6kJ/mol。相較于A構型,第二步反應中B構型反應的活化能更高,而反應熱更低。結果表明,在C70存在時UDMH分子分解的前兩步基元反應仍為吸熱反應,與純UDMH分解不同的是,C70的加入會使第二步反應的反應勢壘和反應熱都明顯高于第一步。
此外,在對C70吸附體系UDMH第一步分解產物(圖9(b)、(e))直接進行優化時,考慮到UDMH中NH2基團在經歷了抽氫反應后轉變為NH基團,且N—N沒有發生改變,故在幾何優化前將分子總價態設置為-1進行優化,得到的結果表明該結構可以穩定存在且分子總價態為-1。對第二步反應產物(圖9(c)、(f))進行優化時將分子總價態設置為-2、0分別進行優化,結果表明分子總價態設置為0時能量更低,原因可能是在失去了兩個H原子后N—N轉化為N═N,分子價態重新歸零。
為了從反應熱方面具體說明C70用于催化UDMH分解的可行性,表1列出3種體系中兩步基元反應的活化能以及反應熱數據,相應能量曲線如圖8所示。

表1 純UDMH體系以及兩種C70體系中UDMH分解基元反應的活化能及反應熱Table 1 Activation energies and heat of reaction of the elementary reactions for UDMH decomposition in the pure UDMH system and in two C70 systems
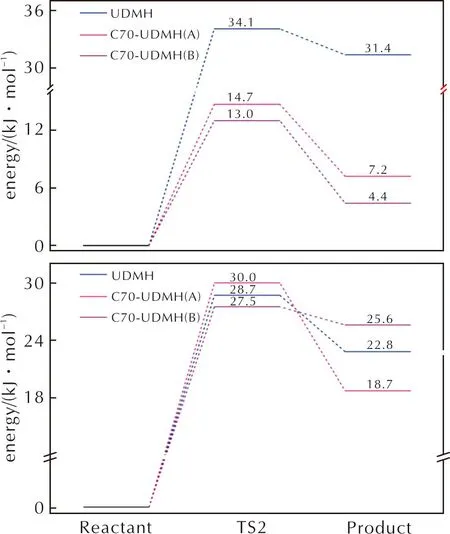
圖8 純UDMH與C70-UDMH體系中前兩步抽氫反應的能量曲線Fig.8 Energetic curves of the first two steps of hydrogen extraction reaction in the pure UDMH and C70-UDMH systems
C70的加入會顯著降低UDMH分解的第一步反應的反應勢壘和反應熱。相比于純體系中第一步反應34.1kJ/mol的反應勢壘,兩種構型中第一步反應的反應勢壘分別降至14.7kJ/mol(A)、13.0kJ/mol(B);反應熱從31.4kJ/mol減小到7.2kJ/mol(A)、4.4kJ/mol(B)。這意味著C70的加入對于UDMH第一步分解反應在動力學和熱力學上都是有利的。而在第二步反應中,不同的吸附構型C70對UDMH反應的反應熱影響不同。計算結果顯示,構型A在降低4.1kJ/mol反應熱的同時會提高1.3kJ/mol的反應活化能;而構型B在反應熱和反應活化能的改變上與構型A恰恰相反,構型B中第二步基元反應的反應活化能減少了0.8kJ/mol,反應熱增加了2.8kJ/mol。結合反應勢壘分析,構型A中C70對于第二步反應的發生具有輕微的抑制作用,構型B則有輕微的催化作用。
Mulliken布局電荷分布是考察電子結構的一個重要參數,一般來說,電荷值越負,所帶電子越多。表2列出了不同構型中UDMH及C70部分原子的Mulliken電荷數。Mulliken電荷分析表明在發生吸附后UDMH中的N、C原子失去部分電子,A構型中N原子失去了0.028e電子,B構型中失去更多的電子(0.032e);且相較于A構型(0.612e),B構型中的兩個C原子失去更多的電子(0.65e)。同時C70中距離UDMH分子最近的一個六元環會得到大部分電子。這說明C70作為催化劑吸附UDMH后,可能會使UDMH分子失去部分電荷,從而使其發生分解反應的能壘降低。
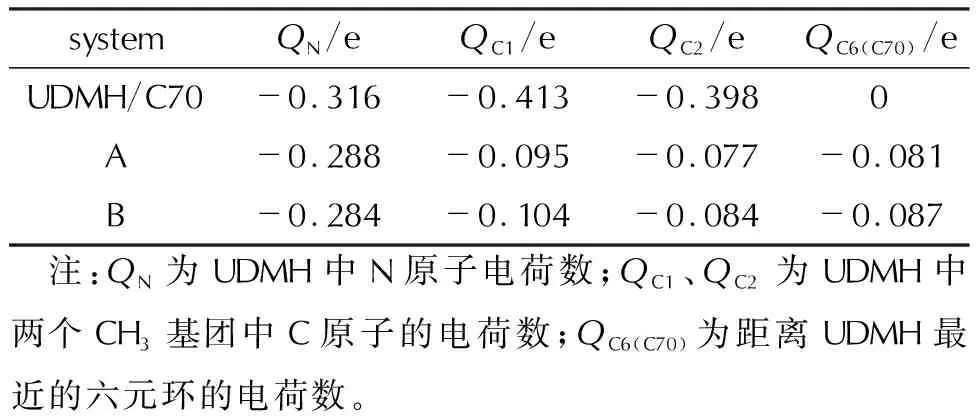
表2 純UDMH、C70及兩種吸附體系的Mulliken電荷Table 2 Mulliken charges of pure UDMH, C70 and two adsorption systems
綜合上述分析,C70的加入對于UDMH的分解具有催化作用。且在第一步抽氫反應中非常明顯,A、B兩種吸附構型分別降低了19.4kJ/mol和21.1kJ/mol的反應勢壘以及24.2kJ/mol、27.0kJ/mol的反應熱。計算結果表明,C70的加入會將第一步的反應熱和反應勢壘降低至比第二步更低的水平。其中,B構型更傾向于降低反應的活化能,A構型對于反應熱的降低則更為明顯。
當UDMH在吸附體系發生分解時,其中間產物與C70分子之間的距離會不斷變化。通過計算獲得了兩種吸附構型—NH2發生兩步抽氫反應的優化吸附構型如圖9所示,其中(a)~(c)為A構型的初始狀態及中間體;(d)~(f)為B構型對應的結構。UDMH及不同階段抽氫反應產物與C70團簇分子之間的距離如表3所示。
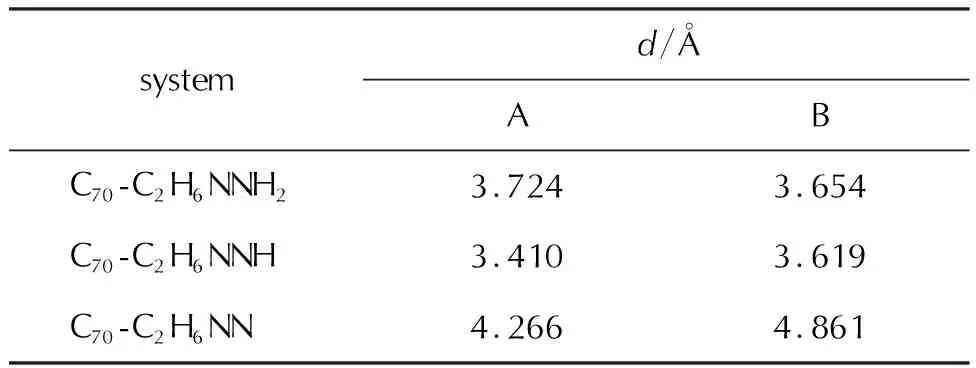
表3 UDMH以及分解反應中間體中N原子與C70中一個C原子的距離Table 3 Distances between N atoms in UDMH and its decomposition reaction intermediates and one C atom in C70
相對C70中的碳原子,A構型的UDMH分子在第一步反應結束后輕微向C70分子靠近,N原子和C原子間距離縮短至3.410?,在下一步反應結束時距離增加至4.266?。并且UDMH分子會以N—N鍵為軸發生逆時針旋轉。B構型中UDMH與C70在距離上的變化趨勢與A構型相同,然而B構型體系中UDMH的分解產物在第一步反應結束相對于C70移動的距離相較于A構型更少,在第二步反應結束相對A構型更多。分子間距離的增加意味著UDMH可能會在其中一步抽氫反應結束后發生脫附,從而進行后續的分解。

圖9 (a~f)UDMH及其分解反應中間體;(g)、(h)測距時參考C70選定的C原子Fig.9 (a—f) UDMH and its intermediates of decomposition reactions; (g)、(h) C atoms selected with reference to C70 during ranging
此外,為探究在反應過程中C70對于UDMH分子和NO2自由基及其產物中化學鍵的影響,測量了不同體系中NO2的兩個N═O鍵以及UDMH中的N—N鍵的鍵長,結果見表4。

表4 UDMH分解過程中部分化學鍵鍵長Table4 Partial chemical bond lengths during UDMH decomposition process
隨著UDMH分解反應的進行,N—N鍵會逐漸縮短,且NO2自由基中不同的N═O鍵鍵長也會發生輕微的變化。在NO2自由基進入體系時,其中兩個N═O鍵鍵長在1.235~1.252?;而形成HONO自由基后,連接H原子的N═O鍵被拉長至1.368~1.383?,沒有連接H原子的N═O鍵會縮短至1.214~1.216?。并且不同體系中化學鍵的鍵長在數值以及變化趨勢上幾乎相同。這說明在UDMH分解過程中,C70對于UDMH分子及NO2、HONO自由基中化學鍵的影響并不明顯。
進一步研究發現,純UDMH經歷兩步抽氫反應并向體系中加入NO2后,(CH3)2NN中的N原子會吸收自由基中的O原子,轉化為(CH3)2NNO,隨著NO2含量的增加,N—N鍵斷裂生成(CH3)2N。而在C70體系中卻沒有發生這種現象,此時UDMH分解產物與C70的分子間距離達到4.27?(A)、4.86?(B),因此推測可能發生了UDMH脫附,C70對于后續反應的影響需要進一步深入研究。
3 結 論
(1)采用密度泛函理論研究了UDMH在C70團簇分子上的吸附行為,獲得兩種吸附構型,UDMH最初以分子形態吸附,兩種物質之間主要發生物理吸附。吸附能為負值且較低,該吸附是放熱過程。C70存在時,UDMH第一步分解生成的中間體會呈現電負性,價態為-1價。
(2)在C70的作用下,UDMH與NO2反應時,第一步抽氫反應傾向于在NH2基團上發生,且C70的加入不會改變UDMH分解初始反應的位置。同時,C70的加入降低了UDMH分解過程的第一步抽氫反應的反應勢壘和反應熱。對于不同的吸附構型,A構型傾向于降低反應熱,B構型則會降低反應勢壘。對于第一步抽氫反應,C70對反應勢壘和反應熱的降低尤為明顯,A、B兩種吸附構型分別降低了19.4kJ/mol和21.1kJ/mol的反應勢壘以及24.2kJ/mol、27.0kJ/mol的反應熱。
(3)反應勢壘研究結果表明,加入C70后加速了UDMH分解的引發反應,并且在B構型中,C70對UDMH分解的反應勢壘的催化作用更為明顯。

