采空區(qū)碳封存條件下CO2-水界面特性及溶解傳質(zhì)規(guī)律
李樹(shù)剛 , 張靜非 , 林海飛 , 包若羽 , 丁 洋 , 白 楊 , 周雨璇 , 朱 冰
(1.西安科技大學(xué) 安全科學(xué)與工程學(xué)院, 陜西 西安 710054;2.西安科技大學(xué) 西部礦井開(kāi)采及災(zāi)害防治教育部重點(diǎn)試驗(yàn)室, 陜西 西安 710054;3.煤炭行業(yè)西部礦井瓦斯智能抽采工程研究中心, 陜西 西安 710054;4.應(yīng)急管理部信息研究院, 北京 100029)
碳排放導(dǎo)致的全球氣候變暖問(wèn)題日益顯著,加快了能源行業(yè)低碳化結(jié)構(gòu)調(diào)整的進(jìn)程[1-3]。CO2排放作為溫室效應(yīng)加劇的主要源頭,與煤炭等化石能源使用密切相關(guān)[4-5]。“雙碳”戰(zhàn)略目標(biāo)的推行要求在煤炭綠色低碳發(fā)展的基礎(chǔ)上,應(yīng)同時(shí)積極探索碳捕集、封存和利用(CCUS)技術(shù),最大限度實(shí)現(xiàn)CO2的捕捉封存、回收循環(huán)及資源化利用[6-8]。對(duì)煤礦而言,CO2封存目標(biāo)地質(zhì)體主要為深部不可采煤層,而采空區(qū)作為非常規(guī)潛在封存地質(zhì)體前景同樣不容小覷[9-10]。采空區(qū)CO2封存作為解決煤炭行業(yè)碳排放難題的重要負(fù)碳技術(shù)儲(chǔ)備,在采空區(qū)廢棄資源二次利用、碳減排等方面具有廣泛的應(yīng)用價(jià)值[11-13]。
CO2在采空區(qū)碳封存的主要形式包括物理封存(構(gòu)造封存、殘余氣封存)與化學(xué)封存(溶解封存、礦化封存)[14-15]。就安全性而言,化學(xué)封存尤其是礦化封存被認(rèn)為是安全性最高的封存方式。其中,CO2的擴(kuò)散溶解傳質(zhì)是化學(xué)封存發(fā)生的首要條件[16-17]。采空區(qū)上部覆巖與側(cè)向封閉墻(煤柱+注漿封堵墻)形成封存空間,注入的游離態(tài)CO2會(huì)擴(kuò)散溶解形成CO2-水體系[18-19],打破地層的地球化學(xué)平衡,經(jīng)歷CO2(g)→CO2(aq)→ H CO-3→C O23-的一系列動(dòng)態(tài)化學(xué)轉(zhuǎn)化過(guò)程[20-21]。溶解度和反應(yīng)程度受氣液界面張力、環(huán)境溫壓、地層水離子質(zhì)量分?jǐn)?shù)等因素影響。
CO2充注進(jìn)入采空區(qū)后的擴(kuò)散傳質(zhì)效率受到氣液界面張力較大影響。CHOW 等[22]通過(guò)實(shí)驗(yàn),在298~488 K 和0~50 MPa 條件下測(cè)量了(N2+CO2)+H2O 的界面張力(Interfacial Tension,以下簡(jiǎn)稱為IFT),并改進(jìn)了經(jīng)驗(yàn)系數(shù);美合日阿依·穆太力普等[23-24]重點(diǎn)對(duì)封存地層溫度、壓力條件下的CO2-咸水/油相間IFT、巖石接觸角(CA)、CO2溶解度及溶解CO2的咸水pH、CO2-油混相壓力等相界面特性進(jìn)行了實(shí)驗(yàn)和數(shù)值分析;邸夢(mèng)瑤等[25]開(kāi)展了深部咸水層環(huán)境下CO2-水界面張力模型計(jì)算研究,并指出了界面張力測(cè)定對(duì)CO2安全封存的應(yīng)用價(jià)值。CO2在地層水中的溶解度直接影響化學(xué)封存效率,研究點(diǎn)主要包括多尺度實(shí)驗(yàn)室研究及溶解度模型重構(gòu)等[26]。實(shí)驗(yàn)研究方面,龍震宇等[27]利用高溫高壓反應(yīng)釜等設(shè)備,測(cè)量不同溫度、壓力、礦化度下CO2在水中的溶解度,明確了CO2在水中的溶解規(guī)律;馬麗麗等[28]通過(guò)恒溫水浴振蕩器使靜態(tài)溶解平衡的CO2-水體系中的流體產(chǎn)生回旋運(yùn)動(dòng),以此研究流體的流速對(duì)CO2-水體系靜態(tài)溶解平衡的影響;溶解度模型研究方面,幾乎所有的建模原理都是從熱力學(xué)基本原理出發(fā)[29],DUAN 等[30-31]建立了預(yù)測(cè)CO2在純水和NaCl 水溶液中溶解度的模型;MAO 以及LI 等[32-33]均采用基于Pitzer 電解質(zhì)理論的活度系數(shù)和Peng-Robinson 狀態(tài)方程的方法建立了CO2在不同條件下的溶解度熱力學(xué)模型。
雖然前期探索CO2地下封存技術(shù)的方式較多,但多是基于CO2的超臨界態(tài)處理,對(duì)采空區(qū)儲(chǔ)層環(huán)境下氣態(tài)CO2氣液界面擴(kuò)散-溶解機(jī)理的探索有待進(jìn)一步分析。筆者利用原位界面張力測(cè)定儀開(kāi)展了不同溫壓、地層水礦化度及陽(yáng)離子溶液種類對(duì)CO2-地層水系統(tǒng)的IFT影響規(guī)律實(shí)驗(yàn),明晰了CO2注入含水碎脹煤巖體中的氣液界面擴(kuò)散效應(yīng),并將基于統(tǒng)計(jì)締合理論結(jié)合蘭納-瓊斯勢(shì)能模型的狀態(tài)方程(SAFT-LJ 狀態(tài)方程)與密度梯度理論(DGT)結(jié)合預(yù)測(cè)了IFT理論值;其次利用自主研發(fā)的地質(zhì)封存地化反應(yīng)模擬實(shí)驗(yàn)平臺(tái)對(duì)相同條件下的CO2溶解性進(jìn)行了探究實(shí)驗(yàn),得到了采空區(qū)儲(chǔ)層環(huán)境下CO2溶解度變化特征,采用DS 模型計(jì)算了對(duì)應(yīng)CO2溶解度理論值,進(jìn)一步闡明了CO2-地層水界面效應(yīng)與溶解傳質(zhì)的耦合關(guān)系,以期為采空區(qū)CO2安全高效封存提供理論依據(jù)。
1 實(shí)驗(yàn)流程及設(shè)備
1.1 地質(zhì)背景
本次實(shí)驗(yàn)以黃陵礦區(qū)某礦采空區(qū)為研究對(duì)象,該礦區(qū)位于鄂爾多斯盆地南緣,主要含煤地層為侏羅系中統(tǒng)延安組,目標(biāo)區(qū)儲(chǔ)層埋深628~632 m,實(shí)測(cè)研究采空區(qū)溫度處于24~38 ℃,采空區(qū)積水的水化學(xué)類型以SO4·Cl—Na、Cl·SO4—Na 為主。
1.2 實(shí)驗(yàn)系統(tǒng)
(1)界面張力測(cè)定系統(tǒng)。CO2-地層水系統(tǒng)界面張力測(cè)定采用自主研發(fā)的原位界面張力測(cè)定儀,如圖1(b)②所示。

圖1 整體研究思路、實(shí)驗(yàn)設(shè)備及流程Fig.1 Overall research ideas, experimental equipment and flow chart
設(shè)備主要包括密閉釜體、進(jìn)氣控壓裝置、溶液/釜體控溫裝置、進(jìn)液裝置、高分辨率攝像頭以及抽真空裝置等。可實(shí)現(xiàn)CO2氣氛環(huán)境中不同溫度(25~60 ℃)、壓力(0~6 MPa)條件的參數(shù)測(cè)定。
1.3 實(shí)驗(yàn)流程
(1)根據(jù)目標(biāo)采空區(qū)儲(chǔ)層環(huán)境確定實(shí)驗(yàn)參數(shù),并采集現(xiàn)場(chǎng)水樣進(jìn)行水質(zhì)檢測(cè)(圖1(a)①),具體選取依據(jù)如1.4 部分(關(guān)鍵實(shí)驗(yàn)參數(shù)選取)所示。
(2)利用自主研發(fā)的原位界面張力測(cè)定儀進(jìn)行不同模擬儲(chǔ)層環(huán)境下,CO2-水界面張力變化規(guī)律實(shí)驗(yàn)研究。首先進(jìn)行實(shí)驗(yàn)系統(tǒng)的氣密性測(cè)試,以保證實(shí)驗(yàn)設(shè)備的可靠穩(wěn)定性,并開(kāi)展不同溫度(25~45 ℃)、壓力(0.5~2.5 MPa)、礦化度(0.5%~2.5%)、離子溶液類型(NaCl、MgCl2、KCl、CaCl2)條件下,自變量對(duì)IFT變化影響規(guī)律實(shí)驗(yàn)。
(3)利用CO2地質(zhì)封存地化反應(yīng)模擬實(shí)驗(yàn)平臺(tái)進(jìn)行不同模擬儲(chǔ)層環(huán)境下,CO2溶解特性變化規(guī)律探究實(shí)驗(yàn)。首先進(jìn)行實(shí)驗(yàn)系統(tǒng)的氣密性測(cè)試,以保證實(shí)驗(yàn)設(shè)備的可靠穩(wěn)定性,并開(kāi)展不同溫度(25~45 ℃)、壓力(0.5~2.5 MPa)、礦化度(0~2.5%)、離子溶液類型(NaCl、MgCl2、KCl、CaCl2)條件下,自變量對(duì)溶液離子變化及溶解度影響規(guī)律實(shí)驗(yàn)。攪拌轉(zhuǎn)速設(shè)定200 r/min,模擬動(dòng)態(tài)條件下的平衡狀態(tài)。實(shí)驗(yàn)平臺(tái)外接PXS-CO2型多參數(shù)離子計(jì)與離子色譜,對(duì)反應(yīng)液中的離子進(jìn)行測(cè)定(圖1(c)⑤)。
(4)IFT可由原位界面張力測(cè)定儀直接測(cè)得,CO2溶解度采用平衡取樣測(cè)試法計(jì)算[23]。
1.4 實(shí)驗(yàn)方案及參數(shù)確定
本實(shí)驗(yàn)的目的是開(kāi)展CO2注入采空區(qū)后氣液間擴(kuò)散-溶解的復(fù)雜物理化學(xué)過(guò)程,著重開(kāi)展探究溫度、壓力、礦化度以及不同陽(yáng)離子對(duì)CO2-水界面張力及CO2溶解性的影響規(guī)律。根據(jù)目前已開(kāi)展的調(diào)研探究結(jié)果,綜合確定實(shí)驗(yàn)?zāi)M環(huán)境溫度T、環(huán)境壓力P、礦化度Kt、離子溶液類型,采用控制變量法設(shè)計(jì)實(shí)驗(yàn)方案,見(jiàn)表1。純水條件下僅改變單一變量(溫度或壓力),共25 組實(shí)驗(yàn);NaCl 溶液條件下,設(shè)置溫度梯度2組(25、45 ℃),分別改變單一變量(礦化度或壓力),共50 組;不同離子溶液類型條件下,固定礦化度1.5%,設(shè)置溫度梯度2 組(25、45 ℃),分別改變單一變量(溶液類型或壓力),共40 組。
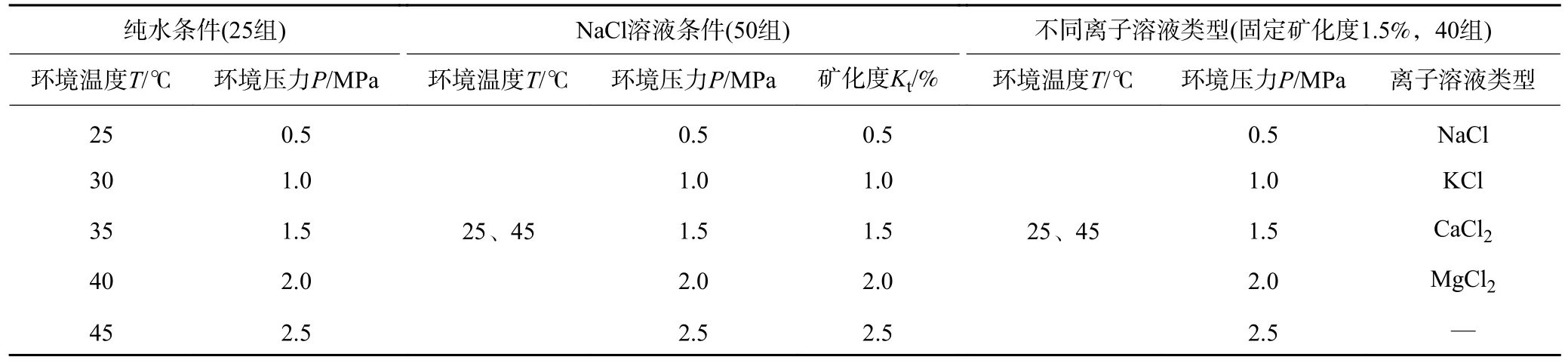
表1 實(shí)驗(yàn)研究方案設(shè)計(jì)Table 1 Experimental research scheme design
關(guān)鍵實(shí)驗(yàn)參數(shù)選取依據(jù)如下:
(1)溫度壓力確定。實(shí)測(cè)研究采空區(qū)溫度處于24~38 ℃,平均31℃,為了便于考察不同溫度梯度對(duì)實(shí)驗(yàn)的影響,選用25、30、35、40、45 ℃五組溫度作為實(shí)驗(yàn)參數(shù),包含了實(shí)測(cè)數(shù)據(jù)范圍并進(jìn)行了擴(kuò)展;目標(biāo)儲(chǔ)層埋深628~632 m,平均壓力梯度0.70 MPa/hm,估算儲(chǔ)層壓力4.4 MPa,考慮采空區(qū)欠壓實(shí)狀態(tài)及應(yīng)力重新分布等影響,設(shè)定實(shí)驗(yàn)壓力梯度為0.5、1.0、1.5、2.0、2.5 MPa。
(2)離子溶液類型及質(zhì)量分?jǐn)?shù)確定。通過(guò)采集目標(biāo)采空區(qū)水樣,進(jìn)行水質(zhì)檢測(cè)得到了水樣離子類型及濃度參數(shù)(圖2①),主要離子類型包括K+、Na+、Ca2+、Mg2+、Cl-等,礦化度為1.315%~1.924%。由于陽(yáng)離子對(duì)水分子的吸引力強(qiáng)于陰離子,且離子溶液對(duì)氣液界面張力的影響主要是由于陽(yáng)離子價(jià)態(tài)的影響,相同條件下,陽(yáng)離子對(duì)氣液間IFT增加的貢獻(xiàn)率排序?yàn)椋篘H4+< K+< Na+< Li+< Ca2+< Mg2+,這在其他學(xué)者研究成果中也得到了驗(yàn)證;而CO2在離子溶液中的溶解度影響主要也是陽(yáng)離子價(jià)態(tài)。因此筆者僅以陽(yáng)離子價(jià)態(tài)為變量進(jìn)行實(shí)驗(yàn)探究,設(shè)定實(shí)驗(yàn)用離子溶液類型分別為NaCl、MgCl2、KCl、CaCl2,礦化度梯度0.5%、1.0%、1.5%、2.0%、2.5%。
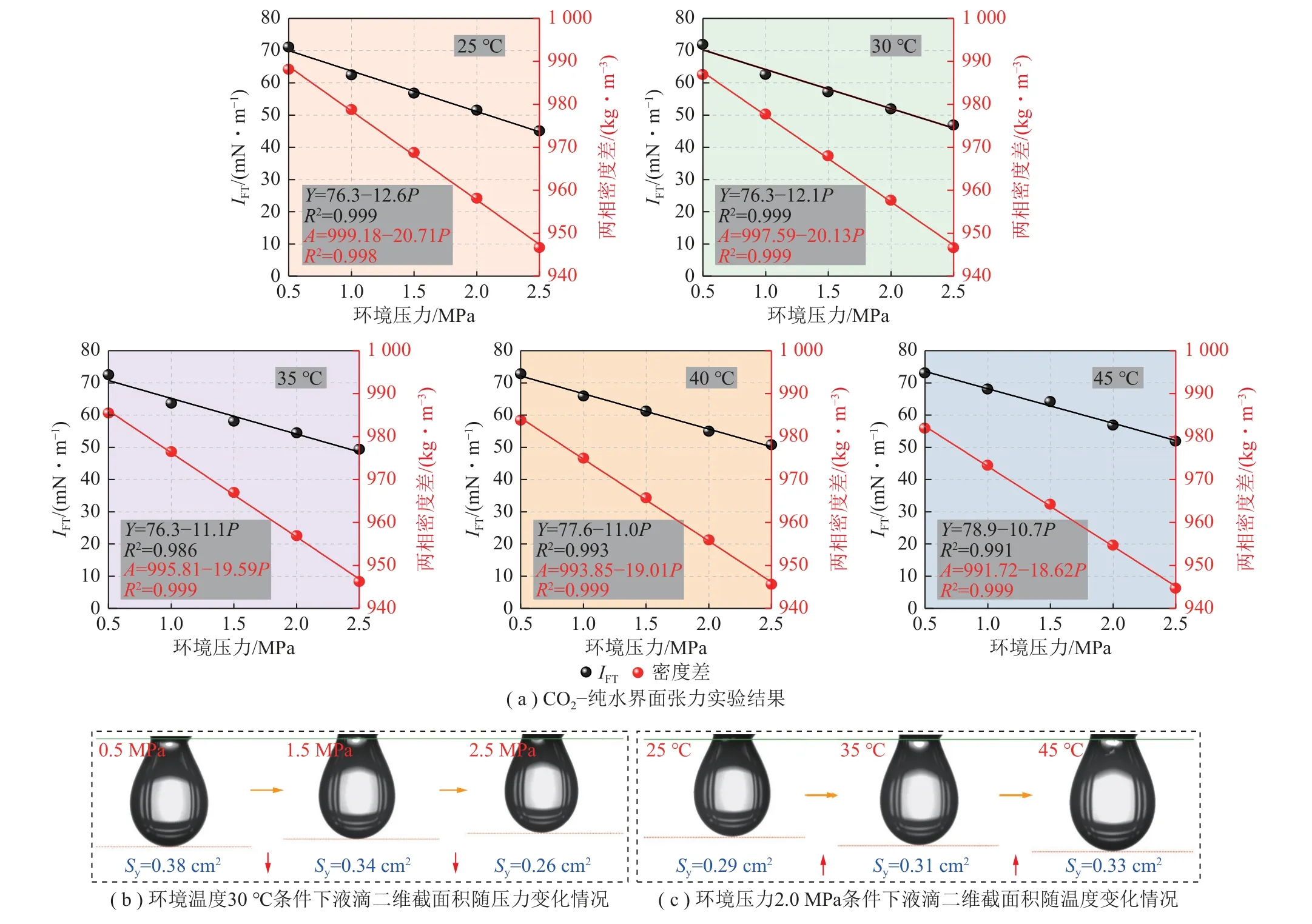
圖2 不同溫度、壓力條件下CO2-純水界面張力變化情況Fig.2 Change of interfacial tension of CO2-pure water under different temperature and pressure
2 結(jié)果與討論
2.1 不同環(huán)境因素對(duì)CO2-水界面張力的影響規(guī)律
2.1.1 溫壓條件對(duì)界面張力的影響
本部分開(kāi)展了不同溫度(25、30、35、40、45 ℃)、不同環(huán)境壓力(0.5、1.0、1.5、2.0、2.5 MPa)條件下CO2-純水界面張力探究實(shí)驗(yàn)。圖2(a)為CO2-純水界面張力實(shí)驗(yàn)結(jié)果,圖2(b)、(c)分別為環(huán)境壓力0.5 MPa 下液滴二維截面積隨溫度變化情況及環(huán)境溫度30 ℃時(shí)液滴二維截面積隨壓力變化情況。
根據(jù)圖2(a)實(shí)驗(yàn)結(jié)果可知,采空區(qū)碳封存條件下,CO2與水的兩相密度差Δρ與環(huán)境壓力具備負(fù)相關(guān)性,同時(shí)IFT整體上隨著壓力增大顯著減小。當(dāng)溫度為25 ℃、純水條件下,壓力由0.5 MPa 增至2.5 MPa,IFT由71.1 mN/m 降低至45.1 mN/m;當(dāng)溫度為30 ℃、壓力由0.5 MPa 變化至1.0 MPa 時(shí),其最大IFT絕對(duì)變化量(|ΔIFT|)達(dá)到9.3 mN/m(圖3)。在CO2-水實(shí)驗(yàn)體系中,環(huán)境壓力升高時(shí),CO2分子的分壓也會(huì)增加,氣態(tài)CO2被壓縮直接導(dǎo)致其密度ρg的發(fā)生顯著增大,同時(shí)CO2的溶解也會(huì)改變純水密度ρl,但改變幅度較小,因此最終會(huì)導(dǎo)致兩相密度差Δρ減小(Δρ=ρl-ρg),根據(jù)Young-Laplace 方程理論可知,當(dāng)密度差Δρ減小時(shí),它會(huì)導(dǎo)致界面上液體和氣體之間的壓力差ΔP降低,從而進(jìn)一步降低界面張力。
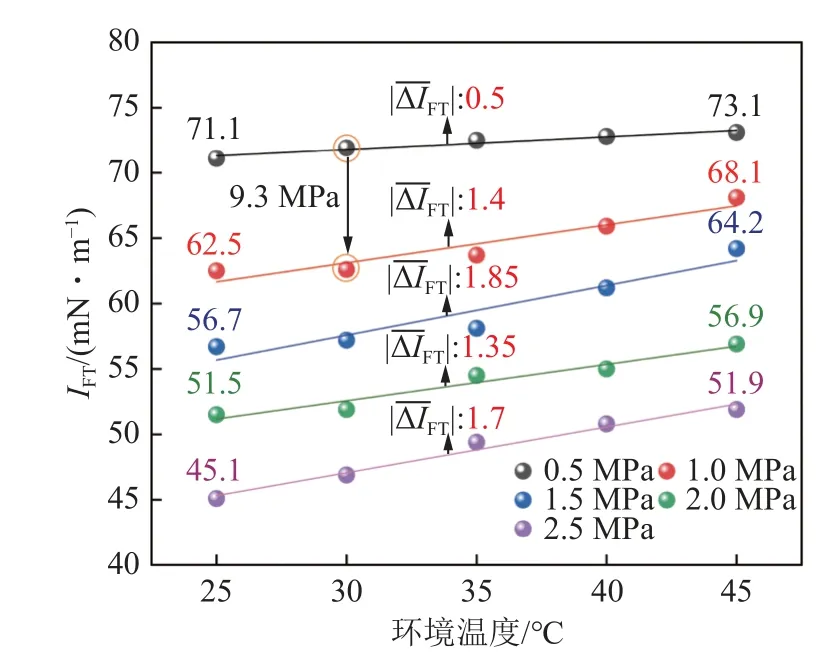
圖3 溫壓效應(yīng)對(duì)IFT 的影響Fig.3 Influence of temperature and pressure on IFT value
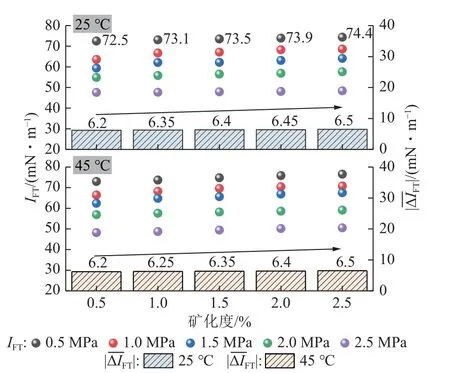
圖4 不同礦化度條件下CO2-鹽水界面張力變化情況Fig.4 Variation of interfacial tension of CO2-brine under different salinity conditions
由圖2(b)可得,溫度一定時(shí),壓力越高,IFT逐漸減小,液滴整體形態(tài)逐漸變小。采用MATLAB 軟件通過(guò)對(duì)液滴形態(tài)照片進(jìn)行二值化處理,計(jì)算了其液滴二維截面積(Sy)的數(shù)據(jù)變化情況,隨著壓力由0.5 MPa 升高至2.5 MPa,對(duì)應(yīng)Sy變化為:0.38 cm2→0.34 cm2→ 0.26 cm2,數(shù)值逐漸減小。這點(diǎn)可從熱力學(xué)原理出發(fā),用Gibbs 自由能(G)來(lái)解釋溫度和壓力對(duì)氣液界面張力的影響,如式(1)所示:
其中,H為系統(tǒng)的焓;S為系統(tǒng)的熵。從體系能量角度來(lái)說(shuō),環(huán)境壓力升高,CO2溶解在液滴內(nèi)部時(shí),這會(huì)導(dǎo)致液滴內(nèi)部的分子之間相互作用增強(qiáng),增加了液滴的焓(ΔH增加);而壓力升高會(huì)減少氣體分子的自由度,系統(tǒng)的熵(ΔS)會(huì)減小,根據(jù)式(1)可以看出,ΔH增加,ΔS減小增加了系統(tǒng)的自由能,使液滴不穩(wěn)定。為了使系統(tǒng)更趨向平衡,減小的液滴體積和界面表面積有助于減小總自由能,因此隨著環(huán)境壓力升高,液滴會(huì)逐漸收縮,降低IFT,以此保證系統(tǒng)穩(wěn)定[34]。
限于實(shí)驗(yàn)條件及參數(shù)范圍選取差異,溫度效應(yīng)對(duì)IFT的影響存在不同結(jié)論。CHIQUET 等[35]認(rèn)為環(huán)境壓力一定時(shí),溫度升高會(huì)使氣液兩相體系的IFT減小,但減小幅度不大。BIKKINA[36]和CHALBAUD[37]則認(rèn)為,當(dāng)壓力較低時(shí)二氧化碳為氣態(tài),界面張力會(huì)隨著溫度的升高而增大,而當(dāng)壓力較高時(shí),界面張力值幾乎不再隨溫度的變化而改變。

2.1.2 地層水礦化度及陽(yáng)離子價(jià)態(tài)對(duì)界面張力的影響

礦化度對(duì)CO2-鹽水界面張力的影響主要包括密度差Δρ變化以及分子間作用力兩方面。首先本實(shí)驗(yàn)采用懸滴輪廓法測(cè)試界面張力,通過(guò)液滴形態(tài)測(cè)量結(jié)果計(jì)算界面張力,計(jì)算公式為
其中,η為液滴形狀參數(shù)。礦化度升高,導(dǎo)致氣液兩相密度差Δρ增大,從而增加CO2-鹽水界面張力。
從分子間作用力方面分析,CO2-鹽水界面張力與體系中每個(gè)組分的貢獻(xiàn)相關(guān),如圖5 所示,液滴在CO2氣氛下形成后,分子間作用力會(huì)促使水分子會(huì)在氣液界面上有序排列,當(dāng)提高液相礦化度后(加入NaCl),NaCl 會(huì)在水中完全電離(圖5(a)),由于Na+和Cl-離子具有相反的電荷,它們可能會(huì)形成電荷分層結(jié)構(gòu),這意味著在界面附近,Cl-離子可能更傾向于靠近液滴表面,而Na+離子更傾向于留在溶液內(nèi)部。這種電荷分層可以減少電荷之間的排斥作用,導(dǎo)致界面附近的水分子形成更緊密、更有序的結(jié)構(gòu),增加了表面張力[38](圖5(b))。除此之外,外加離子的進(jìn)入,會(huì)對(duì)離子-分子相互作用力(Cl-—H2O、Na+—H2O)、離子-離子相互作用力(Cl-—Na+)以及水分子之間的作用產(chǎn)生影響,這些因素共同導(dǎo)致了氣液界面張力的增加。
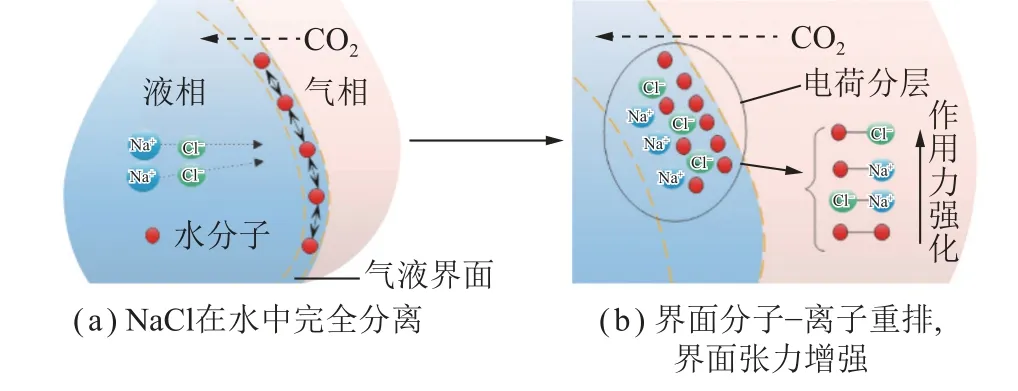
圖5 NaCl 對(duì)氣液界面分子-離子重新分布的影響Fig.5 Effect of NaCl on the molecular-ion redistribution at the gas-liquid interface
由圖6 可得,溫度、礦化度一定時(shí),環(huán)境壓力與不同離子溶液類型條件下的IFT具備較好的正相關(guān)性,而溫度對(duì)IFT的正效應(yīng)較弱。進(jìn)一步分析可發(fā)現(xiàn),存在一價(jià)陽(yáng)離子的鹽溶液(NaCl、KCl)對(duì)IFT的影響整體小于存在二價(jià)陽(yáng)離子的鹽溶液(CaCl2、MgCl2),當(dāng)環(huán)境溫度25 ℃、壓力0.5 MPa 時(shí)(圖5 標(biāo)記處),NaCl、KCl 溶液條件下的IFT分別為73.4、72.5 mN/m,而CaCl2、MgCl2溶液條件下的IFT分別為75.8、76.1 mN/m,其他情況與此結(jié)果一致。
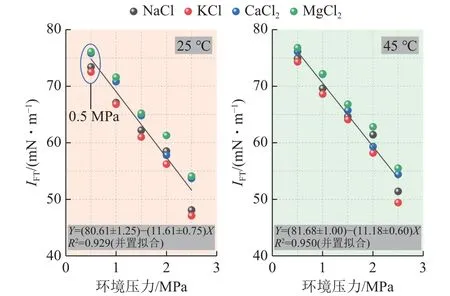
圖6 不同離子溶液類型條件下CO2-純水界面張力變化情況(礦化度統(tǒng)一為1.5%)Fig.6 Change of CO2-brine interfacial tension under different ionic solution types (the salinity is 1.5%)
如圖7 所示,為不同類型鹽溶液中陽(yáng)離子價(jià)態(tài)對(duì)IFT值的影響分析。首先可以看出當(dāng)溫度為25 ℃和45 ℃時(shí),不同CO2-鹽溶液之間的最大IFT(IFTmax)與最小IFT(IFTmin)均呈現(xiàn)出隨著陽(yáng)離子價(jià)態(tài)升高而增大的現(xiàn)象,且二價(jià)陽(yáng)離子溶液與CO2的IFT大于一價(jià)陽(yáng)離子溶液,這與圖6 表現(xiàn)的規(guī)律一致。同時(shí),不同離子溶液與CO2的平均界面張力變化絕對(duì)值也存在類似規(guī)律。經(jīng)過(guò)實(shí)驗(yàn)探究得出,在環(huán)境條件一致時(shí),單一陽(yáng)離子(在相同質(zhì)量分?jǐn)?shù)條件下)對(duì)IFT增加的影響強(qiáng)度排序?yàn)椋篕+< Na+< Ca2+< Mg2+。
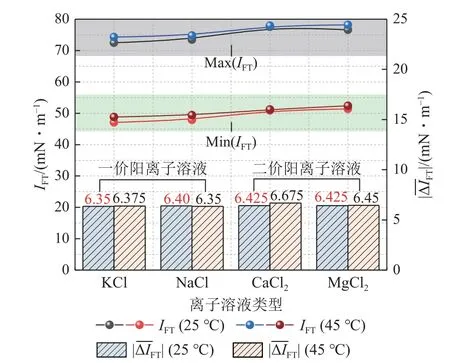
圖7 陽(yáng)離子類型及價(jià)態(tài)對(duì)IFT 的影響Fig.7 Effect of cation type and valence on IFT
根據(jù)前述內(nèi)容可知,鹽溶液引起的界面張力增加是由于排斥了結(jié)構(gòu)形成離子(陽(yáng)離子),而破壞結(jié)構(gòu)的陰離子一般聚集在界面上,并在其周圍產(chǎn)生離子強(qiáng)度梯度,促進(jìn)水分子對(duì)水相主體的吸引,這最終導(dǎo)致了界面面積的擴(kuò)大和界面張力的增加(圖5)。
二價(jià)陽(yáng)離子具有比一價(jià)陽(yáng)離子更高的電荷,其構(gòu)型能力更強(qiáng),這意味著它們?cè)谝后w中能夠引入更多的電荷,在液體-氣體界面附近,這些額外的電荷會(huì)導(dǎo)致更強(qiáng)的靜電相互作用力。針對(duì)二價(jià)陽(yáng)離子來(lái)說(shuō),Mg2+的半徑大于Ca2+,電荷密度更高,Mg2+在氣液界面上的排布可能更加緊密,從而對(duì)界面性質(zhì)產(chǎn)生更顯著的影響[39]。但相關(guān)學(xué)者經(jīng)過(guò)實(shí)驗(yàn)得出,在給定的物質(zhì)的量濃度下,對(duì)于含有二價(jià)陽(yáng)離子的溶液,界面張力的平均變化至少是含有一價(jià)陽(yáng)離子的溶液(NaCl)的2 倍[40]。這在本研究中并未得到顯著體現(xiàn),這是因?yàn)椴煽諈^(qū)碳封存的環(huán)境條件跨度較小,對(duì)比大跨度的實(shí)驗(yàn)結(jié)果存在一定局限,但總體規(guī)律具有一致性。
2.1.3 氣液界面張力預(yù)測(cè)模型及誤差分析
前述部分開(kāi)展了CO2-水界面張力探究實(shí)驗(yàn),但眾多學(xué)者所采用的實(shí)驗(yàn)設(shè)備、實(shí)驗(yàn)條件等不盡相同,所得出的結(jié)果也存在差異,因此本研究除了開(kāi)展相關(guān)實(shí)驗(yàn)之外,還通過(guò)構(gòu)建氣液界面張力預(yù)測(cè)模型計(jì)算了理論值,以便更好驗(yàn)證本次實(shí)驗(yàn)的準(zhǔn)確性。
根據(jù)相關(guān)學(xué)者研究發(fā)現(xiàn),CO2-水界面張力存在的實(shí)質(zhì)是兩相密度差Δρ所引起,因此大部分理論模型都是基于密度函數(shù)所得,如密度梯度理論(DGT)和密度泛函理論(DFT)等[41]。本研究將文獻(xiàn)[30]改進(jìn)后的SAFT-LJ 方程與DGT 理論結(jié)合,對(duì)CO2-H2O/鹽水界面張力進(jìn)行建模研究,該狀態(tài)方程除分子間締合力外還考慮了排斥力、色散力、氫鍵力、多極相互作用力和離子間相互作用力對(duì)體系亥姆霍茲自由能的貢獻(xiàn)。基于密度梯度理論得到的界面張力IFT計(jì)算模型[42]為

SAFT-LJ 狀態(tài)方程利用Lennard-Jones 勢(shì)能模型模擬短程作用力及多極作用力(偶極分子和四極分子之間)對(duì)體系亥姆霍茲自由能αres的貢獻(xiàn),如式(4)[43]所示
式中,α為體系的總自由能;αideal為理想氣體自由能;最右邊5 項(xiàng)分別代表以Lennard-Jones 勢(shì)能模型描述的短程作用、成鏈作用、締合作用、多極作用和離子作用貢獻(xiàn)的亥姆霍茲自由能。
式(4)中 ΔΩ[ρ1(z),ρ2(z)]時(shí),可采用式(5)計(jì)算:

如圖8 所示,為純水及NaCl 溶液條件下,界面張力IFT的預(yù)測(cè)模型理論值(ml)、實(shí)驗(yàn)值(ms)分布及偏差率F分析,當(dāng)采用DGT 理論結(jié)合SAFT-LJ 狀態(tài)方程預(yù)測(cè)CO2/NaCl 水溶液界面張力,此處需引入平均球近似理論(MSA),以考慮離子間遠(yuǎn)程靜電力(庫(kù)侖力)對(duì)體系能量的貢獻(xiàn)。可以看出,數(shù)據(jù)分布于45°對(duì)角線附近,整體預(yù)測(cè)精度較高。純水條件下的實(shí)驗(yàn)偏差率F為-2.65%~3.68%,NaCl 溶液條件下的實(shí)驗(yàn)偏差率F為-5.08%~7.77%。利用該模型預(yù)測(cè)氣液界面張力考慮模型適用度情況還有待進(jìn)一步驗(yàn)證。
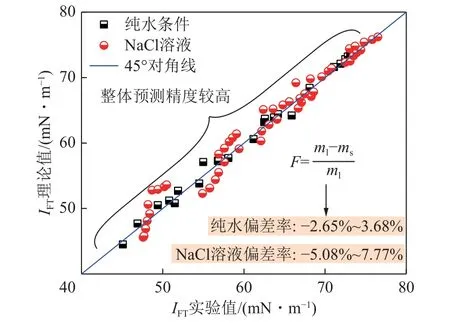
圖8 IFT 的預(yù)測(cè)模型理論值與實(shí)驗(yàn)值誤差分析Fig.8 Error analysis between the theoretical value and the experimental value of the IFT prediction model
2.2 不同環(huán)境因素對(duì)CO2 溶解性的影響規(guī)律
2.2.1 溫壓條件對(duì)溶解度的影響
本部分開(kāi)展了不同溫度(25、30、35、40、45 ℃)、不同環(huán)境壓力(0.5、1.0、1.5、2.0、2.5 MPa)下CO2在純水中的溶解性探究實(shí)驗(yàn)。由圖9 和表2 可得,隨著壓力升高,CO2溶解度均呈現(xiàn)上升趨勢(shì),而壓力一定時(shí),溫度與CO2溶解度存在負(fù)相關(guān)性。
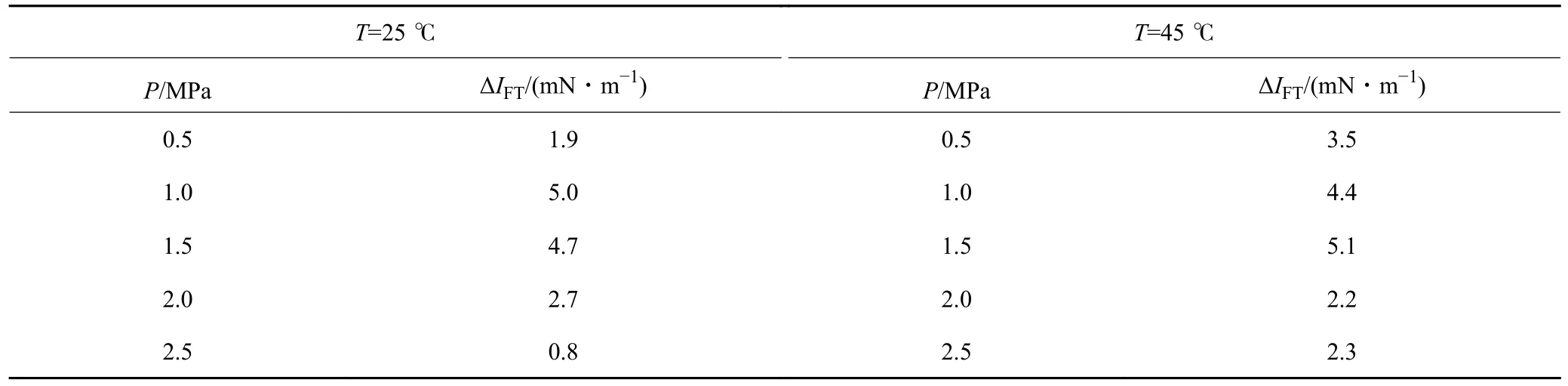
表2 不同溫壓條件下ΔIFT 數(shù)值(礦化度:0.5%→2.5%)Table 2 ΔIFT values under different temperature and pressure conditions (salinity: 0.5%→2.5%)
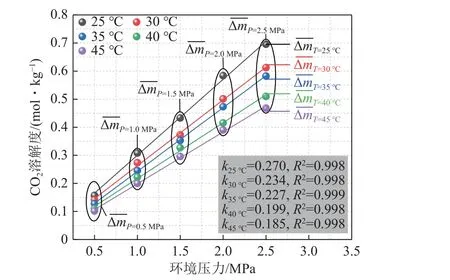
圖9 溫壓條件對(duì)CO2 溶解度的影響(純水)Fig.9 Effect of temperature and pressure conditions on CO2 solubility (pure water)
不同溫度梯度下,CO2溶解度隨壓力變化數(shù)據(jù)擬合斜率k分布于0.185~0.270,壓力變化引起的溶解度平均變化量 ΔmT分布于0.091 6~0.134 5 mol/kg,由此可以看出,溫度升高會(huì)減弱壓力效應(yīng)對(duì)CO2溶解度的改變。壓力一定時(shí),溫度變化引起的溶解度平均變化量 ΔmP處于0.014 0~0.056 8 mol/kg,壓力升高會(huì)加劇溫度效應(yīng)對(duì)CO2溶解度的改變,見(jiàn)表3。
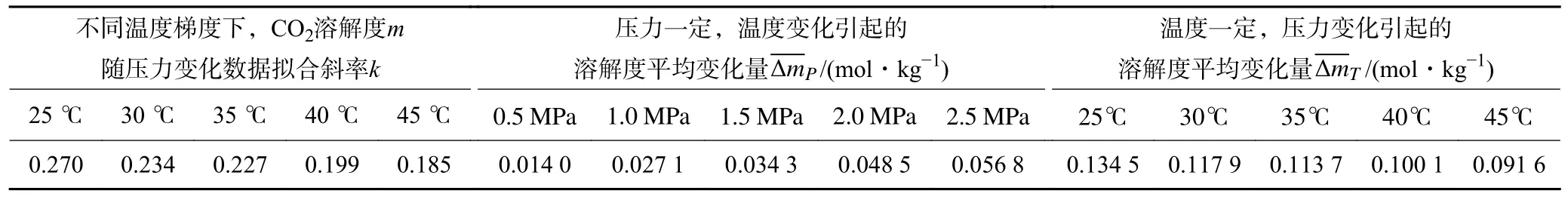
表3 溫壓效應(yīng)與CO2 溶解度變化關(guān)系分析Table 3 Analysis of the relationship between temperature-pressure effect and CO2 solubility
壓力對(duì)CO2溶解度的影響可根據(jù)Henry 定律來(lái)解釋。根據(jù)亨利定律[44],溶解度與氣體分壓之間存在線性關(guān)系,即溶解度m與P成正比。數(shù)學(xué)上可以表示為
其中,KH為亨利常數(shù),是與特定氣體和液體組合有關(guān)的常數(shù),每種氣體在每種液體中都有自己的亨利常數(shù),它與溫度相關(guān)。溫度一定時(shí),當(dāng)壓力升高時(shí),這會(huì)導(dǎo)致氣體更多地溶解到液體中。而從化學(xué)平衡的角度來(lái)看,當(dāng)外部條件發(fā)生變化時(shí),系統(tǒng)會(huì)傾向于通過(guò)相應(yīng)的反應(yīng)來(lái)減輕這種變化。在這種情況下,增加壓力會(huì)導(dǎo)致氣液界面上的CO2從氣相向液相移動(dòng),以減少對(duì)壓力變化的響應(yīng)反饋。
當(dāng)環(huán)境壓力(即CO2分壓P)一定時(shí),隨著溫度升高,亨利常數(shù)KH通常會(huì)減小,這是因?yàn)樵诟邷叵拢后w分子的熱運(yùn)動(dòng)增加,液體分子更容易逸出液體表面,導(dǎo)致氣體分子離開(kāi)液體,因此溶解度降低。
2.2.2 地層水礦化度及陽(yáng)離子價(jià)態(tài)對(duì)溶解度的影響
該部分開(kāi)展了不同礦化度(0.5%、1.0%、1.5%、2.0%、2.5%)及不同離子溶液類型(NaCl、MgCl2、KCl、CaCl2)對(duì)CO2溶解度影響的探究實(shí)驗(yàn),為了便于對(duì)比分析,選取2 個(gè)溫度梯度(25、45 ℃)進(jìn)行。
如圖10 所示,以NaCl 溶液為例,環(huán)境溫壓條件一定時(shí),CO2溶解度隨溶液礦化度增大而降低,當(dāng)溫度25 ℃、壓力2.5 MPa 時(shí),礦化度由0.5%升高至2.5%,對(duì)應(yīng)溶解度由0.675 1 mol/kg 降低為0.635 3 mol/kg,降幅達(dá)5.9%。同樣可以看出,溫壓條件對(duì)CO2溶解度的影響與純水情況一致,溫度與溶解度呈負(fù)相關(guān)性,與壓力呈正相關(guān)性。
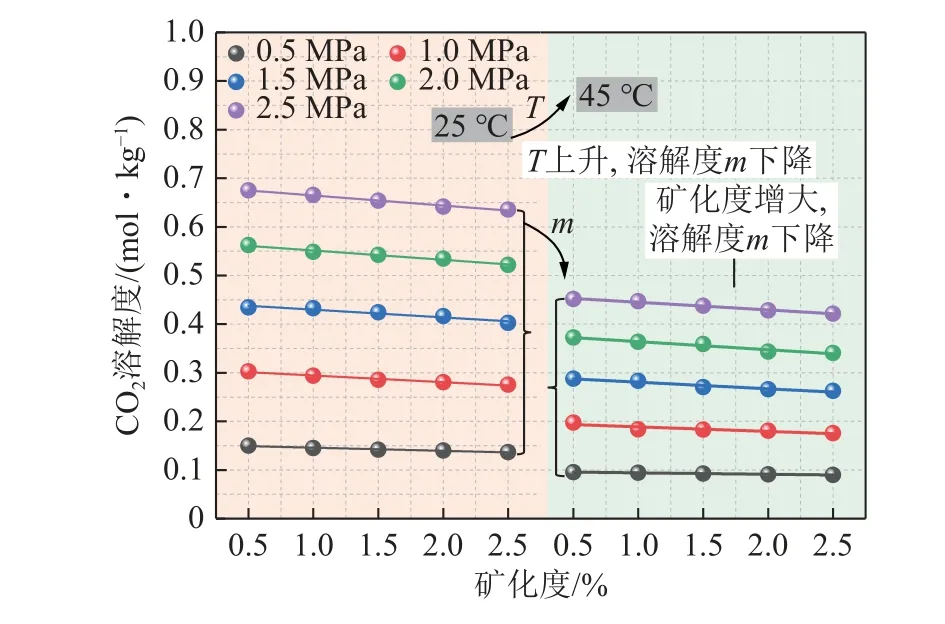
圖10 礦化度對(duì)CO2 溶解度的影響Fig.10 Effect of salinity on CO2 solubility
礦化度對(duì)CO2溶解度的影響主要體現(xiàn)在電解質(zhì)效應(yīng)、溶解平衡與碳酸平衡等方面[45]。如圖11 所示,Na+和Cl-的存在會(huì)增大IFT(2.1.2 節(jié)已解釋),進(jìn)一步弱化CO2的氣液擴(kuò)散傳質(zhì)作用;而采空區(qū)水中礦化度的增加會(huì)造成其電導(dǎo)率變化,導(dǎo)致溶液更加電解質(zhì)化,影響水分子的極性和氫鍵形成,進(jìn)而影響碳酸平衡,促使CO2轉(zhuǎn)為 HCO-3和 CO23-,從而影響CO2的溶解度[46];同時(shí),礦化度的增加會(huì)提高溶液的黏度,限制CO2分子在水中的擴(kuò)散,導(dǎo)致CO2分子更難以從氣相轉(zhuǎn)移到水相。

圖11 礦化度對(duì)CO2 溶解度的影響機(jī)制Fig.11 Effect of salinity on CO2 solubility
圖12 為不同類型離子溶液對(duì)CO2溶解度的影響規(guī)律分析。整體而言,CO2在一價(jià)陽(yáng)離子溶液(NaCl、KCl)中的溶解度大于二價(jià)陽(yáng)離子溶液(CaCl2、MgCl2),例如,當(dāng)環(huán)境溫度為25 ℃、壓力為0.5~2.5 MPa時(shí),CO2在KCl、NaCl 溶液中的溶解度分別為0.152 6~0.664 7、0.143 4~0.653 6 mol/kg,而在CaCl2、MgCl2溶液中的溶解度分別為0.139 7~0.629 0、0.138 2~0.624 5 mol/kg。不同離子溶液對(duì)CO2的吸收率排序?yàn)椋篕+> Na+> Ca2+> Mg2+。
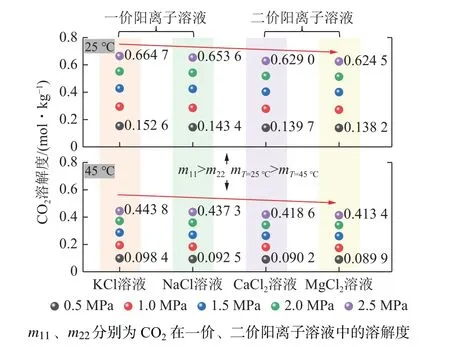
圖12 離子溶液類型對(duì)CO2 溶解度的影響Fig.12 Effect of ionic solution type on CO2 solubility
離子價(jià)態(tài)對(duì)CO2溶解度的影響主要體現(xiàn)在電荷數(shù)及離子半徑差異方面。首先二價(jià)陽(yáng)離子(Ca2+、Mg2+)所帶電荷高于一價(jià)陽(yáng)離子(Na+、K+),當(dāng)CO2吸附于水表面后,二價(jià)陽(yáng)離子具有2 個(gè)正電荷,可以更強(qiáng)烈地與CO2分子中的負(fù)電荷部分相互吸引,但也使CO2分子在水中更難溶解;其次,K+和Na+的電荷相同,都是+1 電荷。但鉀離子的半徑(220 pm)比鈉離子(190 pm)大,導(dǎo)致電荷分布較為分散,即電荷密度較低,這使得鉀離子與CO2分子之間的電荷相互作用相對(duì)較弱,有助于CO2分子更容易溶解在水中。
2.2.3 CO2溶解度預(yù)測(cè)模型及誤差分析
進(jìn)一步通過(guò)理論模型計(jì)算理論數(shù)值,以便更好驗(yàn)證本次實(shí)驗(yàn)的準(zhǔn)確性。常用的CO2溶解度計(jì)算模型包括D-S 模型、PR-HV 模型、Chang 模型和Furnival 模型等[26]。其中D-S 模型(式(7))適用于溫度0~260 ℃、壓力0~200 MPa、礦化度0~4 mol/kg 的條件,同時(shí)考慮了不同礦物離子對(duì)CO2溶解度的影響,因此選用該模型進(jìn)行理論計(jì)算[30-31]:
式中,m(CO2) 為溶解度,mol/kg;y(CO2)為CO2在本體相(氣相)中的摩爾分?jǐn)?shù);φ(CO2)為逸度系數(shù);μ(CO2)l(0)/(RT) 為無(wú)因次標(biāo)準(zhǔn)化學(xué)勢(shì);λ為二級(jí)交互系數(shù); ζ為三級(jí)交互系數(shù);mi為該離子的礦化度,mol/kg;c和a分別為不同的陽(yáng)離子和陰離子。
圖13 為CO2在純水以及NaCl 溶液中溶解度的預(yù)測(cè)模型理論值(ml)、實(shí)驗(yàn)值(ms)分布及偏差率F分析,純水條件下的實(shí)驗(yàn)偏差率F為-1.18%~5.64%,NaCl 溶液條件下的實(shí)驗(yàn)偏差率F為2.15%~8.35%,總體精度較高。純水條件下不考慮離子交互影響,簡(jiǎn)化模型后主要利用液相化學(xué)勢(shì)(μ(CO2)L)與氣相化學(xué)勢(shì)(μ(CO2)V)平衡的關(guān)系進(jìn)行預(yù)測(cè)。
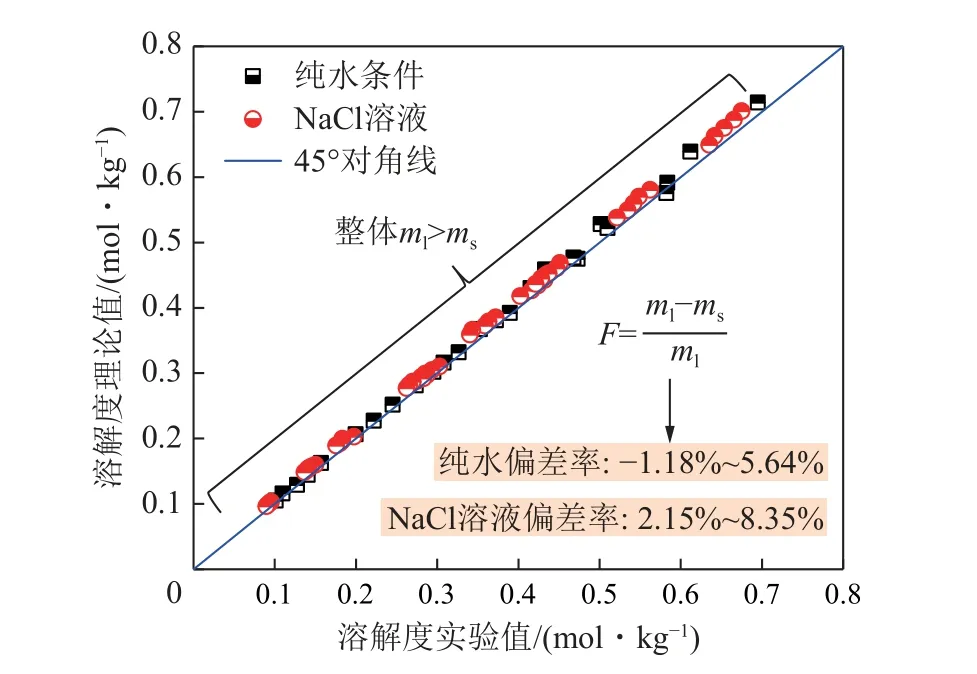
圖13 溶解度的預(yù)測(cè)模型理論值與實(shí)驗(yàn)值誤差分析Fig.13 Error analysis between the theoretical value and the experimental value of the solubility prediction model
3 CO2-地層水氣液界面效應(yīng)及溶解傳質(zhì)耦合機(jī)理
界面張力與溶解度分別為束縛氣封存及溶解封存的重要評(píng)價(jià)參量,對(duì)闡明CO2-地層水氣液界面效應(yīng)與其溶解傳質(zhì)效應(yīng)具有重要意義。首先應(yīng)當(dāng)進(jìn)一步明晰采空區(qū)CO2-地層水氣液界面效應(yīng)及溶解傳質(zhì)過(guò)程,如圖14 所示,當(dāng)CO2注入采空區(qū)后發(fā)生的擴(kuò)散傳質(zhì)-溶解效應(yīng)是研究束縛氣封存及溶解封存的重要基礎(chǔ),氣態(tài)CO2(CO2(g))克服界面張力通過(guò)擴(kuò)散傳質(zhì)作用進(jìn)入采空水,轉(zhuǎn)變?yōu)槿芙鈶B(tài)CO2(CO2(aq))后進(jìn)一步溶解反應(yīng)生成 HCO-3與 CO23-,此過(guò)程的封存效率受到環(huán)境溫度、環(huán)境壓力、采空水礦化度、采空水陽(yáng)離子類型等因素影響。
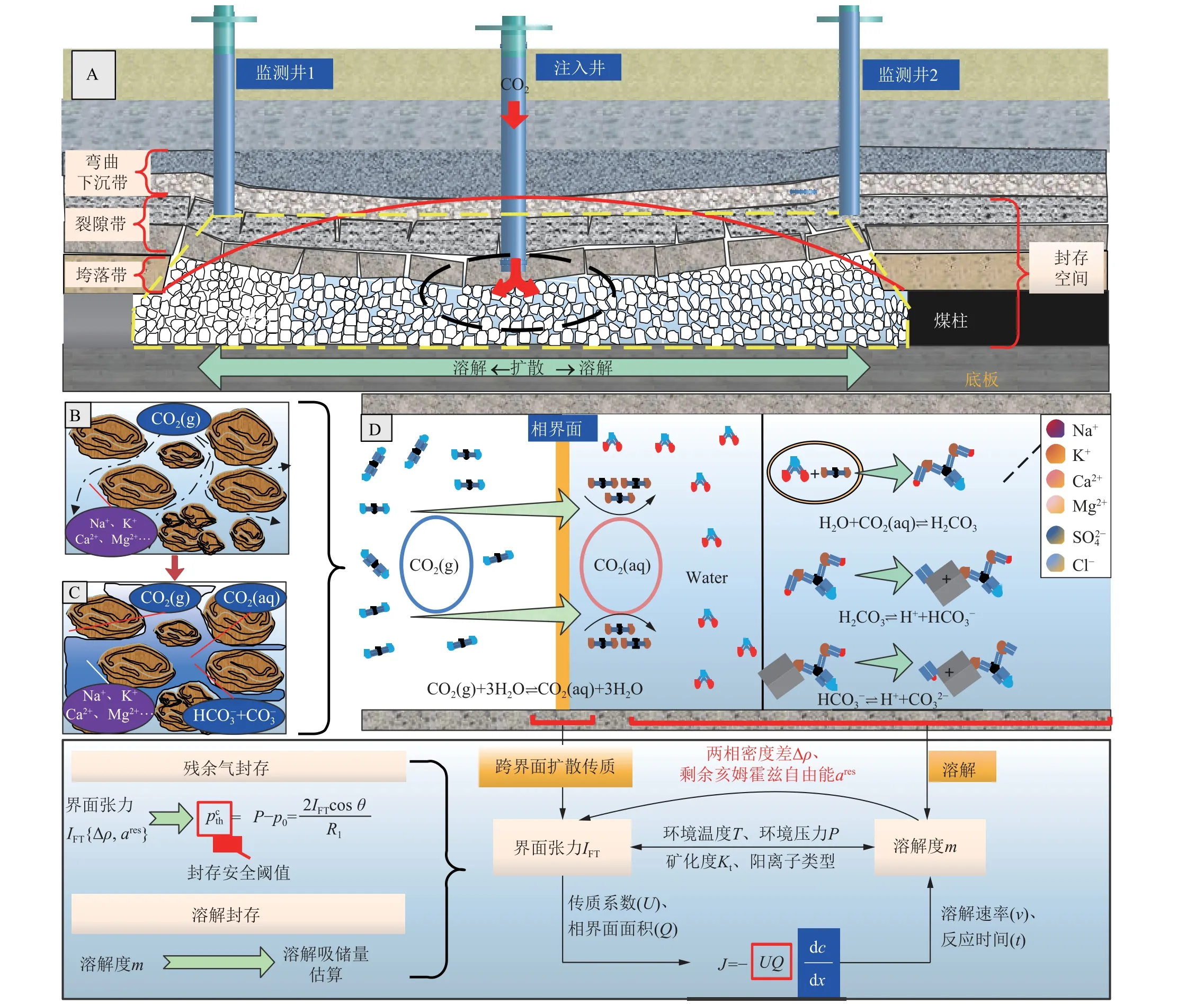
圖14 采空區(qū)CO2-地層水氣液界面效應(yīng)及溶解傳質(zhì)機(jī)理Fig.14 Mechanism of CO2 diffusion-dissolution across the interface in goaf of closed mine
如圖15 所示,為不同自變量與CO2-水界面張力、溶解度之間的變化規(guī)律。采空區(qū)碳封存實(shí)驗(yàn)條件下,界面張力與溶解度始終保持負(fù)相關(guān)關(guān)系,壓力升高,IFT增大,CO2溶解度降低(圖15(a));溫度、礦化度以及溶液陽(yáng)離子價(jià)態(tài)升高,IFT降低,CO2溶解度增大(圖15(b)~(d))。

圖15 自變量與界面張力-溶解度-溶解度變化規(guī)律Fig.15 Independent variables and interfacial tension-solubility change rule
界面張力與溶解度之間的互饋關(guān)系可以根據(jù)前述2 個(gè)參量的預(yù)測(cè)模型來(lái)初步解釋。由式(3)~(5)的界面張力預(yù)測(cè)模型可以發(fā)現(xiàn),界面張力求解的核心是獲取熱力學(xué)平衡條件下界面中2 組分的密度分布,要得到密度分布需要計(jì)算CO2-地層水體系的交互作用因子、亥姆霍茲自由能等參量,這些因素與環(huán)境溫壓、礦化度、采空水陽(yáng)離子類型有關(guān);同樣由式(6)、式(7)的預(yù)測(cè)模型看出,溶解度也受到環(huán)境溫壓、礦化度、采空水陽(yáng)離子類型的共同作用,通過(guò)溶解度的改變控制密度分布,進(jìn)而影響界面張力,反之亦然。而從物理模型(圖14)、自變量與界面張力-溶解度變化規(guī)律(圖15)可知,界面張力變化會(huì)改變氣液傳質(zhì)系數(shù)與相界面面積,根據(jù)菲克第二定律可得出,以上2 項(xiàng)參數(shù)會(huì)直接作用于氣液界面的傳質(zhì)效率(J),進(jìn)而改變CO2溶解速率、反應(yīng)時(shí)間等,對(duì)CO2在采空水中的溶解度產(chǎn)生影響;反過(guò)來(lái),CO2溶解度的改變會(huì)對(duì)氣液兩相密度差Δρ、剩余亥姆霍茲自由能ares產(chǎn)生影響(短程作用、成鏈作用、締合作用、多極作用和離子作用),從而改變界面張力。
進(jìn)一步可從分子間作用力角度闡述界面張力與溶解度之間的影響機(jī)理。界面張力是液體表面上分子間相互作用的結(jié)果,界面張力越大,水分子更加緊密地相互排列,形成一個(gè)相對(duì)難以滲透的屏障,使CO2分子較難進(jìn)入水中并與水分子相互作用,因此溶解度下降[47]。同時(shí)可以看出,環(huán)境壓力對(duì)界面張力及溶解度的影響效應(yīng)遠(yuǎn)大于溫度、礦化度,當(dāng)其他環(huán)境條件一致時(shí),壓力由0.5 MPa 升高至2.5 MPa,對(duì)應(yīng)IFT由71.1 mN/m 降至45.1 mN/m,溶解度由0.157 2 mol/kg升高至0.695 2 mol/kg;而溫度由25 ℃升高至45 ℃,對(duì)應(yīng)IFT只由71.1 mN/m 降至73.1 mN/m,溶解度由0.152 6 mol/kg 升高至0.101 4 mol/kg,幅度較小。這種現(xiàn)象除了實(shí)驗(yàn)取值跨度較小之外,還由于壓力能夠直接影響CO2氣體分子進(jìn)入液體的能力,以及液體分子在液體-氣體界面上的排列,而溫度升高會(huì)導(dǎo)致液體分子動(dòng)能增加,分子間相互作用減弱,從而增加CO2分子進(jìn)入液體的趨勢(shì),但這個(gè)影響通常不如壓力的影響顯著[48];礦化度變化可以影響液體中的離子強(qiáng)度,從而影響溶解度,但對(duì)界面張力的影響較小。因此,低溫、高壓、低礦化度能夠更有效強(qiáng)化溶解封存效能,提升采空區(qū)碳封存安全性。
從采空區(qū)CO2地質(zhì)封存安全性來(lái)說(shuō),一旦獲得較為準(zhǔn)確的CO2-地層水界面張力IFT,可求解封存地質(zhì)體蓋層的毛管壓力閾值pcth(封存安全性系數(shù)),如式(8)所示[24],為CO2注入?yún)?shù)提供依據(jù)。其次,CO2在采空區(qū)水中溶解度的大小直接決定化學(xué)封存效能,對(duì)安全性評(píng)估及化學(xué)封存強(qiáng)化機(jī)理研究奠定基礎(chǔ)。
式中,p0為儲(chǔ)層流體壓力;R1為蓋層中最大的孔喉或者裂縫的直徑; θ為接觸角。
CO2在水中的溶解和擴(kuò)散影響著CO2從氣相向采空區(qū)水體的遷移,而CO2與水中溶解的鹽類反應(yīng)則可能導(dǎo)致地質(zhì)封存巖層的溶解與巖石結(jié)構(gòu)改變,進(jìn)而影響儲(chǔ)存系統(tǒng)的完整性和穩(wěn)定性。此外,CO2溶解還可能引發(fā)地下水的酸化,增加了地層巖石溶解的風(fēng)險(xiǎn),從而潛在影響地質(zhì)封存的安全性。因此,在采空區(qū)地質(zhì)封存的安全性評(píng)估與實(shí)施中,必須深入研究CO2-水界面效應(yīng)與溶解傳質(zhì)的關(guān)系,以充分理解這些過(guò)程對(duì)封存系統(tǒng)的影響,確保CO2長(zhǎng)期穩(wěn)定儲(chǔ)存,最大限度地減少潛在的環(huán)境風(fēng)險(xiǎn)。
4 結(jié) 論
(1)采空區(qū)碳封存條件下,CO2與水之間的IFT整體上隨著壓力增大顯著減小,對(duì)應(yīng)的氣液兩相密度差與環(huán)境壓力具備負(fù)相關(guān)性;隨著環(huán)境溫度由25 ℃升高到45 ℃后,同等壓力條件的IFT稍有增加;在溫壓條件一定時(shí),溶液礦化度與IFT存在正相關(guān)性,且在本實(shí)驗(yàn)范圍內(nèi),低壓、高溫、高礦化度會(huì)促使IFT的升高;CO2-鹽溶液之間的IFT呈現(xiàn)出隨著陽(yáng)離子價(jià)態(tài)升高而增大的現(xiàn)象(K+< Na+< Ca2+< Mg2+);將SAFT-LJ 狀態(tài)方程與DGT 理論結(jié)合預(yù)測(cè)的IFT理論值,整體預(yù)測(cè)精度較高,純水條件下的實(shí)驗(yàn)偏差率為-2.65%~3.68%,NaCl 溶液條件下的實(shí)驗(yàn)偏差率為-5.08%~7.77%。
(2)隨著儲(chǔ)層環(huán)境壓力升高,CO2溶解度均呈現(xiàn)上升趨勢(shì),而壓力一定時(shí),溫度與CO2溶解度存在負(fù)相關(guān)性。環(huán)境溫壓條件一定時(shí),CO2溶解度隨溶液礦化度增大而降低,溶解度作為溶解封存量估算的重要參數(shù),低溫、高壓、低礦化度能夠更有效強(qiáng)化溶解封存效能。整體而言,CO2在一價(jià)陽(yáng)離子溶液(NaCl、KCl)中的溶解度大于二價(jià)陽(yáng)離子溶液(CaCl2、MgCl2),不同離子對(duì)CO2的吸收率排序?yàn)椋篕+> Na+> Ca2+>Mg2+。采用D-S 模型計(jì)算了對(duì)應(yīng)CO2溶解度理論值,純水條件下的實(shí)驗(yàn)偏差率為-1.18%~5.64%,NaCl 溶液條件下的實(shí)驗(yàn)偏差率為2.15%~8.35%。(3)從采空區(qū)CO2地質(zhì)封存安全性來(lái)說(shuō),界面張力與溶解度分別為束縛氣封存及溶解封存的重要評(píng)價(jià)參量。界面張力變化會(huì)改變氣液傳質(zhì)系數(shù)與相界面面積,根據(jù)菲克第二定律可得出,以上2 項(xiàng)參數(shù)會(huì)直接作用于氣液界面的傳質(zhì)效率,進(jìn)而改變CO2溶解速率、反應(yīng)時(shí)間等,對(duì)CO2在采空水中的溶解度產(chǎn)生影響;反過(guò)來(lái),CO2溶解度的改變會(huì)對(duì)氣液兩相密度差、剩余亥姆霍茲自由能產(chǎn)生影響(短程作用、成鏈作用、締合作用、多極作用和離子作用),從而改變界面張力,因此,低溫、高壓、低礦化度能夠更有效強(qiáng)化溶解封存效能,提升采空區(qū)碳封存安全性。

