H2SO4-Fe2(SO4)3浸出銅精礦過程中鐵形態轉化研究
張明峂 羅仙平 李曉東 沈樓燕 趙紅波
〔摘 要〕 H2SO4-Fe2(SO4)3浸出體系因其具有成本低、腐蝕性較低等特點,被廣泛應用于銅精礦的浸出。由于溶液中Fe的形態變化決定著浸出工藝的經濟效益,因此針對浸出液中不同條件下的鐵形態進行了研究。研究表明,Fe3+與Fe2+之間的轉化主要涉及電子轉移,不會改變H+ 濃度;當浸出液pH值達到2時,會產生大量黃鉀鐵礬沉淀,并夾雜著質量分數為1.0%的Cu和質量分數為0.5%的Zn;當浸出液中Fe2+質量濃度超過46.5 g/L時,在常溫下會產生FeSO4·7H2O結晶,并夾雜著質量分數為1.9%的Cu和質量分數為1.0%的Zn。
〔關鍵詞〕銅精礦;H2SO4-Fe2(SO4)3浸出體系;浸出條件;硫酸鐵;氧化
中圖分類號:TF811;TF803.21? ? 文獻標志碼:A? 文章編號:1004-4345(2024)02-0001-04
Study on Iron Species Transformation in the Leaching of Copper Concentrate by H2SO4-Fe2(SO4)3
ZHANG Mingtong1, LUO Xianping2, LI Xiaodong3, SHEN Louyan4, ZHAO Hongbo1
(1. Central South University, Changsha, Hunan 410083, China; 2. Jiangxi University of Science and Technology, Ganzhou, Jiangxi 341099, China; 3. Hunan Research Institute for Nonferrous Metals, Changsha, Hunan 410100, China;
4. China Nerin Engineering Co., Ltd., Nanchang, Jiangxi 330038, China)
Abstract? ?The H2SO4-Fe2(SO4)3 leaching system is widely used for the leaching of copper concentrate due to its low cost and low corrosivity. The species change of iron in solution determine the economic benefits of the leaching process. This study investigates the iron species in the leach solution under different conditions on a basis of the process. It has been shown that the conversion between Fe3+ and Fe2+ mainly involves electron transfer and does not alter the H+ concentration. When the pH value of the leach solution rises to 2, a large amount of jarosite will be generated, with Cu of a mass fraction of 1.0% and Zn of a mass fraction of 0.5%. When the concentration of Fe2+ in the leach solution exceeds 46.5 g/L, heptahydrated ferrous sulphate crystals will be generated at room temperature, with Cu of a mass fraction of 1.9% and Zn of a mass fraction of 1.0%.
Keywords? copper concentrate; H2SO4-Fe2(SO4)3 leaching system; leaching conditions; iron sulfate; oxidation
銅是一種重要的工業金屬原料,具有優異的導熱性、導電性和延展性,被廣泛應用于電力、建筑、國防工業等領域[1]。中國的銅資源約占世界銅儲量的3%,具有人均占有量少、資源品質差、分布廣、開采難度大等特點[2-3]。黃銅礦是主要的銅礦資源,世界上70%以上的銅以黃銅礦的形式存在。由于持續開采,國內的黃銅礦呈現出“貧、細、雜”的特點[4-5],且黃銅礦與閃鋅礦、方鉛礦、黃鐵礦等的伴生關系復雜,在浮選過程中受到“表面活化”的影響難以實現深度分離,導致銅精礦中含閃鋅礦、方鉛礦等其他硫化礦[6]。因此,近年來復雜銅精礦的綜合利用問題越來越受到關注。
目前,從銅精礦中提取銅的方式仍然以火法冶煉為主,而銅精礦中夾雜的其他硫化礦不僅會降低銅產品的品位,還會造成熔爐堵塞等問題[7]。此外,銅精礦的火法冶煉過程中會產生大量SO2煙氣,吸收、處理這些SO2增加了火法冶煉工藝的成本[8]。相比之下,濕法工藝能夠避免產生SO2,對礦物的品位要求也低,因此更適合用于從復雜銅精礦中提取金屬銅。
濕法工藝浸出銅的方式有很多,其中H2SO4-Fe2(SO4)3浸出體系因成本低、腐蝕性小,受到了廣泛的關注[9]。但截至目前,研究工作集中在銅鋅精礦在該體系中的溶解機理、溶解動力學、鈍化現象和產物等內容上[10-11],關于浸出液中鐵形態變化的研究還比較少。實際上,H2SO4-Fe2(SO4)3浸出體系中含有高濃度的鐵離子,礦物的浸出反應以鐵離子的氧化還原反應為主,且溶液中的鐵離子會發生絡合、沉淀、結晶等形態變化[12]。浸出液中鐵離子的不同形態不但會對礦物浸出效果造成影響,還會對浸出液中有價金屬的存在形態產生影響,從而影響復雜銅精礦在H2SO4-Fe2(SO4)3體系中溶解浸出的經濟效益。因此,對H2SO4-Fe2(SO4)3浸出銅精礦工藝中鐵形態進行分析具有重要意義。
經過前期浸出實驗條件的探索和優化,得到銅精礦在H2SO4-Fe2(SO4)3體系中的最優浸出條件為:Fe2(SO4)3濃度為1 mol/L、H2SO4質量濃度為10 g/L,t=95 ℃。本文擬對Fe濃度為2 mol/L、S濃度為3 mol/L的Fe-S-H2O體系浸出液在25 ℃和95 ℃條件下,不同形態的鐵的分布情況進行研究,探討溶液氧化還原電位、pH值以及FeSO4濃度對鐵形態的影響。
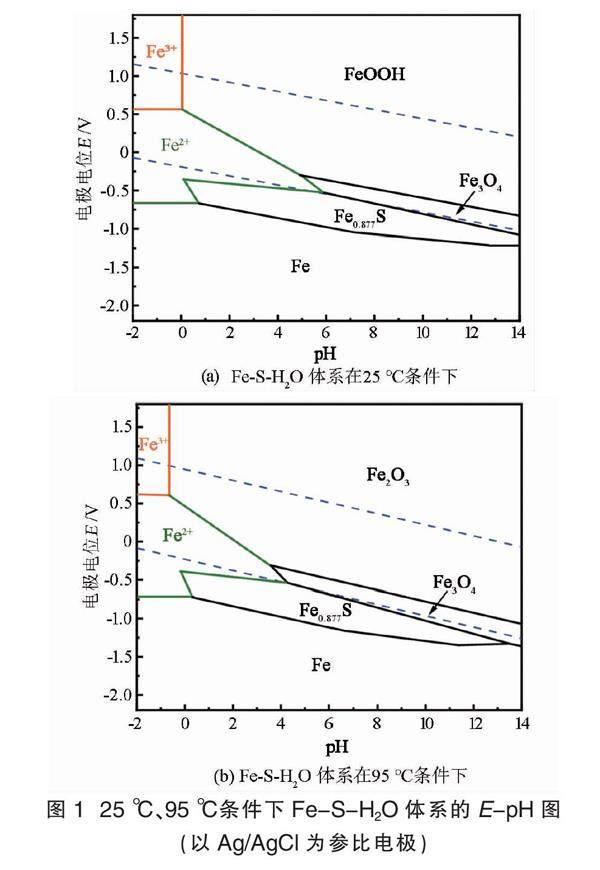
通過熱力學分析軟件HSC Chemistry分析得到的在25 ℃和95 ℃條件下,Fe濃度為2 mol/L、S濃度為3 mol/L的Fe-S-H2O體系浸出液中不同形態的鐵的分布優勢區間如圖1所示。
1? ?溶液氧化還原電位的影響
由圖1可以看到,溶解態的Fe3+位于E-pH圖的左上角,說明Fe3+更容易存在于酸性高電位的環境中。在該體系中,當氧化還原電位低于0.6 V(vs. Ag/AgCl)時,Fe3+ 會得到電子生成Fe2+。該過程不涉及H+ 濃度的變化,所以Fe3+ 與Fe2+ 優勢區間的分隔線為水平線。隨著氧化還原電位繼續降低,Fe2+會與硫生成Fe0.877S,然后再被還原生成鐵單質。但是,Fe0.877S優勢區間的氧化還原電位已經低于氫線,即在該條件下,H2O會被還原產生H2。因此,在H2SO4-Fe2(SO4)3浸出工藝中考慮的氧化還原電位主要包括Fe3+與Fe2+ 優勢區間和水穩定區域。H2SO4-Fe2(SO4)3浸出液保持在酸性高氧化還原電位狀態,加入硫化銅精礦以后,由于硫化礦表面電位較低,接觸到礦物的Fe3+ 會得到電子生成Fe2+。所以,浸出結束后,大量的Fe2(SO4)3被還原成了FeSO4。同樣,在酸性條件下,隨著氧化還原電位的升高,Fe2+ 又會失去電子生成Fe3+。該過程也不涉及H+ 濃度的變化。
2? ?pH的影響
為研究pH值升高后鐵的形態變化及其影響,實驗反應液由FeSO4和Fe2(SO4)3以4∶1的摩爾比配成,用于模擬浸出液。反應液總鐵濃度為1.6 mol/L,含Cu2+、Zn2+離子各10 g/L。采用3 mol/L的KOH溶液調節pH值,反應裝置為錐形瓶。實驗時,將錐形瓶被放置于恒溫水浴搖床中,控制溫度和攪拌速率。
由圖1可知,Fe3+ 在pH升高過程中會產生羥基氧化鐵(FeOOH)。在自然界中,FeOOH存在4種晶型,分別為α-FeOOH、β-FeOOH、γ-FeOOH、δ-FeOOH,其中最穩定的是α-FeOOH(針鐵礦)。作為一種水合鐵氧化礦,α-FeOOH加熱失水后會生成Fe2O3 [13]。
酸性反應液的初始pH值為0.8,在滴加KOH溶液的同時,通過pH計監測溶液酸度變化。在pH值低于1.4時,溶液中幾乎無沉淀產生;當pH值升至1.6時,溶液中有較多沉淀產生;當pH值升至2時,溶液中有大量沉淀產生。
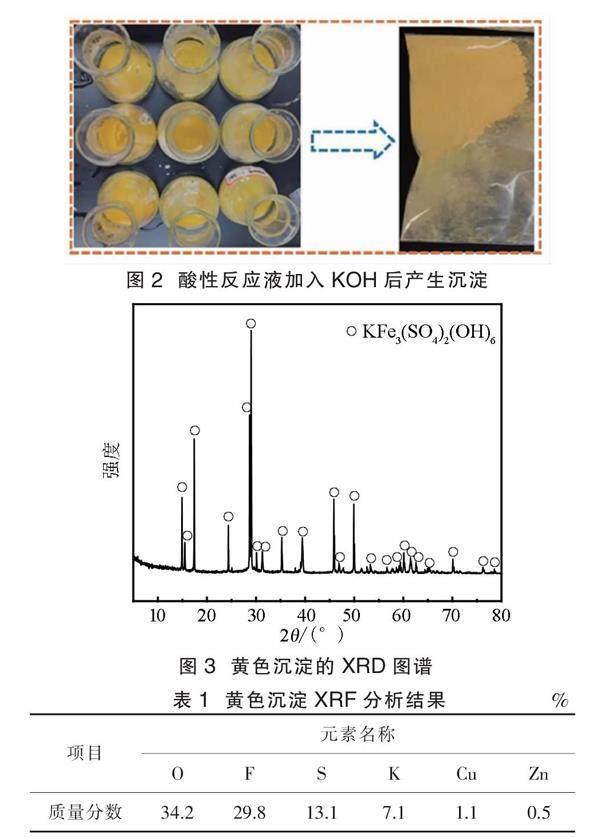
此外,溫度對沉淀的形成也具有重要影響。實驗表明,當溫度由室溫上升到60 ℃ 時,沉淀速度明顯加快;當升至95 ℃ 時,沉淀不僅生成迅速,而且顆粒已堆積在錐形瓶底部,見圖2。將沉淀分離、沖洗、烘干、研磨后,用于XRD檢測和XRF分析。黃色沉淀XRD圖譜見圖3,XRF分析結果見表1。
圖3中幾乎只有KFe3(SO4)2(OH)6的衍射峰,再結合表1的分析結果,可以判定黃色沉淀的物相主要為KFe3(SO4)2(OH)6。
由表1可知,黃鉀鐵礬沉淀中含有質量分數為1.1%的銅和質量分數為0.5%的鋅,表明生成黃鉀鐵礬的過程中會造成Cu2+和Zn2+的共沉淀,這勢必會影響含鋅銅精礦在H2SO4-Fe2(SO4)3體系中浸出的經濟效益。
Bigham、Schwertmann等[14]對28個礦區水環境中的沉淀物進行分析:當pH≥6.5時,沉淀物主要為水鐵礦(Fe5HO8·4H2O)或與針鐵礦(α-FeOOH)的混合物;當pH在2.8~4.5范圍內時,沉淀物主要為施威特曼石[理想化學式為Fe8O8(OH)6SO4]和極少量的針鐵礦;當pH=2.6時,形成了大量的含鈉黃鉀鐵礬,即(H, K, Na) Fe3(SO4)2(OH)6。Pina、Frenay等[15]提到黃鉀鐵礬生成速率隨溫度升高而明顯加快。當溫度低于60 ℃時,沉淀生長較慢;在pH=2時,沉淀形成最快;pH小于1或大于3時,沉淀形成明顯被抑制。Graf [16]提出溶液中SO42-/K+ 濃度越高,黃鉀鐵礬的穩定性越好。Majzlan則提出Fe3+與SO42- 之間存在較強絡合作用[12],而H+ 或OH- 濃度過高時會抑制這種作用。
根據上述研究成果,本研究第3章中浸出液的pH值為1,且SO42-濃度極高,需要警惕黃鉀鐵礬的產生,其可能會抑制礦物浸出,造成溶液中Cu2+、Zn2+的損失。
3? ?硫酸亞鐵濃度的影響
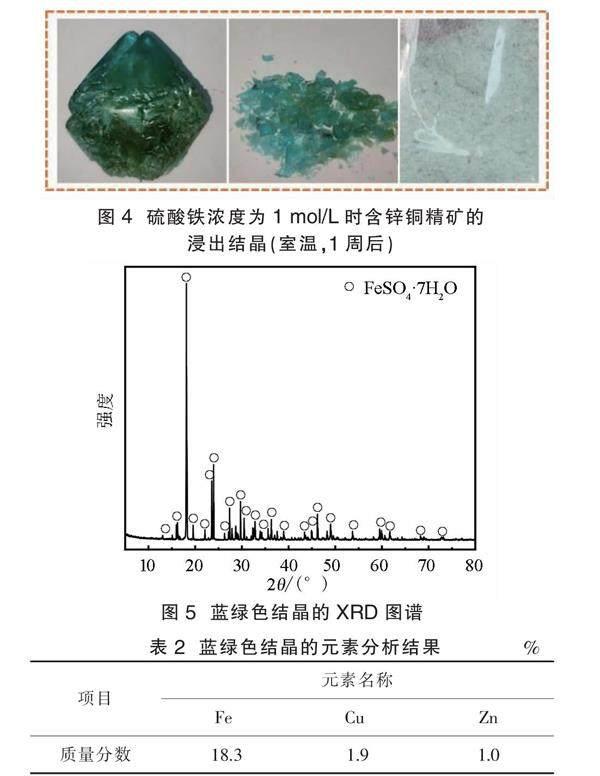
在之前的工作中,研究了不同硫酸鐵濃度(0.2 mol/L、0.4 mol/L、0.6 mol/L、0.8 mol/L和1.0 mol/L)中含鋅銅精礦的浸出情況。浸出結束后,不同溶液中Fe2+ 離子濃度分別為9.0 g/L、18.1 g/L、25.3 g/L、38.7 g/L和46.5 g/L。這些浸出液在室溫中靜置1周后,在含46.5 g/L Fe2+ 離子的浸出液中發現了藍綠色結晶,如圖4所示。將該結晶取出,經去離子水沖洗、常溫晾干、研磨后進行XRD檢測和元素分析。XRD圖譜見圖5,元素分析結果見表2。
圖5中幾乎只有七水合硫酸亞鐵(FeSO4·7H2O)的衍射峰,這表明是高濃度硫酸亞鐵發生了結晶。
Bullough、Canning等[17]研究發現FeSO4結合水數量隨溫度升高而減少,FeSO4·7H2O存在于較低溫度下(低于45 ℃)。FeSO4在H2SO4溶液中的溶解度隨溫度的降低、硫酸濃度的升高而降低。在25 ℃時,質量分數為0.6 %的硫酸溶液中,FeSO4的溶解度僅為22.5%。含鋅銅精礦浸出液中FeSO4產生結晶會夾雜Cu2+、Zn2+,由表2可知,該結晶中含有1.9 %的Cu和1.0 %的Zn。因此,以H2SO4-Fe2(SO4)3浸出含鋅銅精礦需要關注溶液中Fe2+的濃度,并預測在所有工藝的溫度和酸度中是否會產生結晶,以免影響浸出效益。
4? ?結論
本研究采用H2SO4-Fe2(SO4)3體系浸出含鋅銅精礦,對浸出液中Fe的形態進行研究,得到以下結論:1)Fe3+更容易穩定存在于酸性、氧化還原電位高的溶液中(以Ag/AgCl為參比電極時,E>0.6 V),Fe2+更容易穩定存在于酸性、氧化還原電位較低的溶液中(以Ag/AgCl為參比電極時,E<0.6 V,高于氫線),Fe2+和Fe3+之間的轉化主要涉及電子得失,不涉及H+ 濃度變化。2)用3 mol/L KOH溶液調節硫酸鐵溶液的pH值到2,會有大量黃鉀鐵礬沉淀生成,且生成速度隨溫度升高而加快。沉淀中含有質量分數為1.0%的Cu和質量分數為0.5%的Zn。3)常溫下,銅精礦在
1 mol/L硫酸鐵中浸出得到的浸出液會發生結晶,結晶成分主要為FeSO4·7H2O,結晶中含有質量分數為1.9%的Cu和質量分數為1.0%的Zn。
參考文獻
[1] 張楠.2023年中國銅工業供需形勢分析 [J].中國礦業,2024,33(2): 20.
[2] 孫傳堯, 宋振國, 朱陽戈, 等. 中國銅鋁鉛鋅礦產資源開發利用現狀及安全供應戰略研究 [J]. 中國工程科學, 2019, 21(1): 133.
[3] BERNHARDT D R I J. Mineral commodity summaries 2020 [R]. Reston, VA, 2020.
[4] LI X, MONNENS W, LI Z, et al. Solvometallurgical process for extraction of copper from chalcopyrite and other sulfidic ore minerals[J]. Green Chemistry, 2019, 22(2):417.DOI:10.1039/c9gc02983d.
[5] ZHAO H, ZHANG Y, ZHANG X, et al. The dissolution and passivation mechanism of chalcopyrite in bioleaching: An overview [J]. Minerals Engineering, 2019,136-140.
[6] EJTEMAEI M, NGUYEN A V. Characterisation of sphalerite and pyrite surfaces activated by copper sulphate [J].Minerals Enginee-ring, 2017, 100: 223.
[7] BELLEMANS I, DE WILDE E, MOELANS N, et al. Metal losses in pyrometallurgical operations-a review [J]. Adv Colloid Interfac, 2018, 255: 47-63.
[8] KARPPINEN A,SEISKO S, LUNDSTR M M. Atmospheric leaching of Ni, Co, Cu, and Zn from sulfide tailings using various oxidants [J]. Minerals Engineering, 2024, 207: 108576.
[9] LI Y, KAWASHIMA N, LI J, et al. A review of the structure, and fundamental mechanisms and kinetics of the leaching of chalcopy-rite [J]. Adv Colloid Interfac, 2013, 197: 32.
[10] MARTíNEZ-GóMEZ V J, FUENTES-ACEITUNO J C, PéREZ-GARIBAY R, et al. A phenomenological study of the electro-assisted reductive leaching of chalcopyrite [J]. Hydrometallurgy, 2016, 164: 54-63.
[11] WINARKO R, DREISINGER D B, MIURA A, et al. Characteriz-ation of the solid leach residues from the iodine-assisted chalco-pyrite leaching in ferric sulfate media[J].Hydrometallurgy,2024: 106302.
[12] MAJZLAN J, MYNENI S C B. Speciation of iron and sulfate in acid waters: aqueous clusters to mineral precipitates [J]. Environmental Science & Technology, 2005, 39(1): 188.
[13] 藺祖弘. 改性羥基氧化鐵用于含砷毒劑污染場地修復的性能評價及機理研究 [D].北京:北京化工大學,2021.
[14] BIGHAM J M, SCHWERTMANN U, TRAINA S J, et al. Schwertmannite and the chemical modeling of iron in acid sulfate waters [J].Geochimica et Cosmochimica Acta, 1996, 60(12): 2111.
[15] PINA P D S, FRENAY J, LE O V A, et al. A critical review of the chemical leaching of sphalerite in ferric sulfate and chloride solution[J/OL].Chemistry, Environmental Science,2003[2023-10-23]. https://www.semanticscholar.org/paper/A-critical-review-of-the-chemical-leaching-of-in-Pina-Frenay/be6ee645ec76ba19fc
22d7f1072cdf809a3c2253.
[16] GRAF D L. Chemical equilibria in soils [J]. Clays and Clay Minerals, 1979, 28(4): 319.
[17] BULLOUGH W S, CANNING T A, STRAWBRIDGE M. The solubility of ferrous sulphate in aqueous solutions of sulphuric acid [J]. Journal of Chemical Technology & Biotechnology, 2010, 2(12):703-707.
收稿日期:2023-10-29
作者簡介:張明峂(1997—),男,主要研究方向為復雜硫化礦常壓濕法浸出。

