高中化學實驗題的解題技巧研究
劉冬

摘要:在高中化學解題中,實驗題解題備受廣大師生的關注.實驗題涉及的知識較多,綜合性較強,題型靈活多變,是高考化學中的熱門考點之一,對學生的解題能力有著較高的要求.如何有效提升學生化學實驗題解題能力已經成為眼下教育領域普遍關注的熱點問題之一,本文據此展開深入分析與研究,以供參考.
關鍵詞:高中化學;實驗題;解題技巧
中圖分類號:G632文獻標識碼:A文章編號:1008-0333(2024)11-0126-03
實驗題是化學、物理與生物考試中的必考題型之一,通常涉及實驗裝置、反應原理、操作流程、實驗現象以及結論等內容,具有復雜性與綜合性.在實驗題教學中,教師應注重對解題技巧與思路的講授,根據不同實驗題題型,采用不同解題技巧,幫助學生掌握多種實驗題解題技巧,使其學會舉一反三,能夠做到遷移應用,結合題目題型選用相應的解題技巧,提高解答實驗題的效率.
1? 高中化學實驗題解題原則
高中化學實驗題一般是從實驗原理、操作目的、操作流程、現象與結果的分析等各個方面進行設計的,在平常的實驗操作中,儀器安裝需遵循“從下到上,先左后右”的基本原則.在解答實驗題時,首先需找到題干中的已知條件,分析實驗儀器的功能和使用方法,以此為基礎綜合分析實驗裝置與操作流程,根據相關規范展開解題.同時,教師應要求學生將實驗步驟進行簡化處理,從已知條件中找出關鍵詞句,將復雜繁瑣的實驗步驟拆分成若干個小步驟,降低試題難度,使其深化理解題干信息,從中找到解題方法,減少出現錯誤的概率,提升學生解題準確度[1].
2 高中化學實驗題的具體解題技巧
例1在乙酸乙酯制備與純化的化學實驗之中,裝置與操作如圖1所示,其中用不上的操作是( ).
分析在這道基礎性實驗題中,主要考查學生對化學實驗基本操作的掌握,學生需要準確掌握在制備乙酸乙酯的實驗中所使用儀器、試劑,理解實驗原理與操作步驟等,結合學習的理論知識,明確在濃硫酸作用下乙酸和乙醇會發生酯化反應,但是在生成物中會有一些雜質,需進一步純化處理.
詳解針對A選項,是在加熱乙醇、濃硫酸與冰醋酸的混合物,有乙酸乙酯生成,實驗是在加熱條件下,而且混合物均是液體,所以試管口輕微朝上傾斜是正確的,故正確;針對B選項,要想實現乙酸乙酯的純化,需除去生成物中混有的乙酸與乙醇,結合乙酸乙酯不能溶于水的性質,可采用飽和碳酸鈉來吸收乙酸、溶解乙醇,為了避免倒吸,不能把導管插入液體中,故操作正確;針對C選項,
因乙酸乙酯不溶于水,分液可達到分離的目的操作正確;針對D選項,裝置是一個蒸發和濃縮溶液的實驗裝置,在該實驗中用不到此操作,D錯誤.答案D.
在高中化學實驗題中,基礎操作和基本原理類的試題較為常見,主要考查學生對基礎性化學理論知識、實驗基本操作規范與流程的掌握情況.解答化學基礎實驗試題時,要準確找到解題的突破口,巧妙運用基礎知識對題目進行解答[2].
例2將一定量的鎂粉加到適量的溴水中,一段時間以后,溴水的顏色就會慢慢消失,對于這一現象,同學們產生不一樣的見解:(1)有的同學指出鎂粉與溴水在水中會發生如下化學反應:
①Br2+H2OHBr+HBrO
②Mg+2HBrMgBr2+H2↑
③Mg+2HBrOMg(BrO)2+H2↑
由于反應②、③的進行,促進了反應①往右移動,致使溴水的顏色慢慢消失;(2)有的同學則指出并非上述原因導致溴水的顏色慢慢消失.那么請自主制定實驗方案,分析以上兩種說法正確與否?
分析此實驗題目主要考查學生對鎂粉與溴水這一化學反應原理的理解程度與掌握情況.根據化學反應原理找到解題思路,對以上實驗方案展開研究驗證,確定說法是否正確.
(1)將鎂粉加到溴水中,會發生一系列的化學反應,如果在整個化學反應過程中出現大量氣體,則說明(1)中同學的看法正確,反之則說明(2)中同學的看法正確;(2)向含有溴的四氯化碳溶液中加入一定量的鎂粉,如果溶液的顏色慢慢消失,則說明(2)中同學的看法是正確的.
實驗原理題是一種常見的題型,主要考查學生對化學反應原理的理解與掌握情況.此類試題涉及的知識點比較多,以及各類化學反應類型,包括復分解反應、氧化還原反應和離子反應及化學反應與能量變化、方向、條件、速率與限度等.針對有關化學反應原理的實驗題,高中化學教師指導學生明確題目中的化學反應原理,結合實驗目的、操作流程和注意事項等知識,完成解題[3].
例3牙膏摩擦劑的主要成分為氫氧化鋁和碳酸鈣,其中一些成分遇到鹽酸時會有無色氣體的產生,現在通過定性實驗來檢驗牙膏的成分.把一定量的牙膏放到水中進行溶解,然后加以攪拌和過濾,請求:(1)將得到的濾渣放到氫氧化鈉溶液中,再進行過濾操作,寫出氫氧化鋁和氫氧化鈉溶液反應的離子方程式;(2)將二氧化碳氣體通入到(1)中的濾液之中,然后注入過量的稀鹽酸,將會出現什么實驗現象?
分析此實驗題的綜合性強,難度系數較大,但是在解題時,依然是利用課本中的知識.學生需要認真閱讀和分析題干信息,根據具體實驗操作計算,結合誤差分析完成解題.題目中問的是離子方程式的書寫與出現的實驗現象,都是比較熱門的化學試題形式,準確使用所學知識,上述問題即可迎刃而解.
(1)氫氧化鋁和氫氧化鈉溶液反應的離子方程式是:
Al(OH)3+OH-[Al(OH)4]-
或者Al(OH)3+OH-AlO-2+2H2O
(2)結合題目的具體要求,遷移和應用基礎化學知識,在(1)中得到的濾液為NaAlO2(偏鋁酸鈉)溶液,向溶液內通入二氧化碳氣體,發生的化學反應是:
CO2+3H2O+2NaAlO2
2Al(OH)3↓+Na2CO3
出現的白色沉淀為氫氧化鋁,同時還會生成碳酸鈉,再加入過量的稀鹽酸后,發生如下化學反應:
Al(OH)3+3HClAlCl3 + 3H2O
Na2CO3+2HCl2NaCl+CO2↑+H2O
白色的氫氧化鋁沉淀會被溶解掉,且有大量二氧化碳氣體產生.
綜合性實驗題背景一般是日常生活或者工業生產情境,對學生的創新能力和綜合能力要求較高.考查學生的基礎實驗技能、操作技巧、檢驗物質、運算等能力.
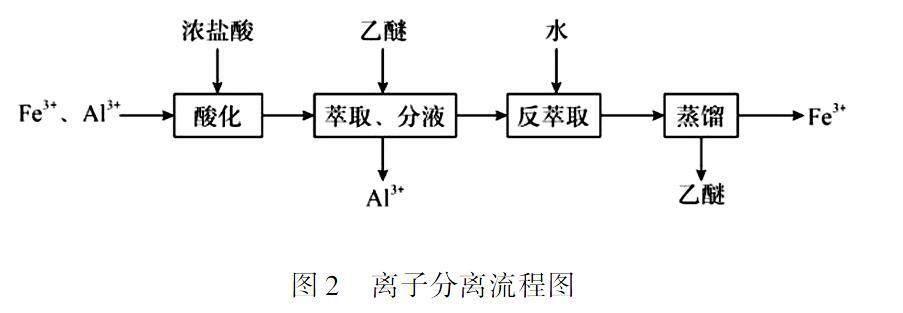
例4實驗室分離Fe3+和Al3+的流程如圖2所示,已知Fe3+在濃鹽酸中生成黃色配離子[FeCl4]-,該配離子在乙醚(Et2O,沸點34.6 ℃)中生成締合物Et2O·H+·[FeCl4]-,以下說法不正確的有().
A.進行萃取振蕩操作時,分液漏斗下口需傾斜向下
B.進行分液操作時,需先把下層液體從分液漏斗下口放出
C.分液后水相是無色的,這說明已經達到分離的目的
D.蒸餾時需使用直形冷凝管
分析本題是有關工藝流程的實驗題,應著重分析實驗操作流程的規范性,如裝置是否漏水、分液漏斗的震蕩、檢查氣密性、萃取、洗滌、分液和過濾等操作,找出4個選項中的不規范操作.
A選項,萃取振蕩時,分液漏斗下口需傾斜向上,所以不正確; B選項,進行分液操作時,密度大的液體位于下層,密度小的液體則位于上層,下層液體從分液漏斗下口放出,當下層液體放完后,密度小的上層液體從分液漏斗上口倒出,故正確; C選項,Fe3+在濃鹽酸中生成黃色配離子,該離子在乙醚中生成締合物,乙醚與水互不相溶,所以分液后水相是無色的,說明水相中沒有Fe3+,此時已經達到分離目的,也是正確的; D選項,蒸餾時使用直形冷凝管,可以讓餾分全部轉移至接收瓶里面,不會在冷凝管中殘留,同樣是正確的.答案:A.
3 結束語
通常來說,高中化學實驗題一般集中在化學實驗基礎.物質檢驗、分離與提純,綜合實驗設計與評價等方面,也有貼近生活、生產方面的試題,其中工藝流程類試題是一種常見的題目類型.高中化學教師需要認真研究最近幾年高考化學試卷中流程類實驗題特征,帶領學生分析題目中的工藝生產流程,分析涉及的化學反應、實驗原理以及操作規范等,幫助學生掌握解題技巧,鍛煉其解題能力[4].
參考文獻:
[1]邱長恩.新高考背景下高中化學實驗解題的探究[J].數理化解題研究,2022(28):143-145.
[2] 王秀丹.高中化學實驗設計與探究題的解題技巧研究[J].中學生數理化(教與學),2021(01):49.
[3] 盛惲博.高中化學實驗題的幾種常見解法淺析[J].高中數理化,2021(24):65.
[4] 史洪偉.淺析高中化學實驗題解題方法的研究[J].數理化解題研究,2021(27):104-105.
[責任編輯:季春陽]

