基于新課程新教材的“結構課堂”的研究與構建


一、“結構課堂”內涵、理論指導與實施策略的支持
1.“結構課堂”的內涵
“結構課堂”是指把課堂與教學統一在結構之中,形成內在的邏輯與進階上升,達到教學形式與教學內容相輔相成、形式邏輯與內容邏輯緊密結合之美。筆者提出的化學“結構課堂”是將形式之美與邏輯之美統攝在一起,合二為一,構建成高效開放的教學模式。
2.“結構課堂”的理論指導
吉登斯提出的結構化理論強調行動與結構相互制約而形成的結構二重性關系,吉登斯認為,能動性的發揮滲透在個體行動流中,即在動機的激發過程、行動理性化再到行動的反思性監控三者之間的流動過程中。現當代課堂教學結構必須重建:(1)現當代課堂教學中的師生能動者的身份“重塑”;(2)現當代課堂教學中規則的“重建”:(3)現當代課堂教學資源的“再造”;(4)現當代課堂教學活動中的二重性——特別強調和突出教師和學生、學生之間的相互溝通、相互激勵、啟發和分享,它以發展學生的多種才能為目的,是既有競爭又有合作的一種教學方法,在教學中確立“主體一客體、主體一主體、主體一客體一主體”之新型多元關系,很好地解放了學生,發展了學生素養。
3.“結構課堂”實施策略的支持
問題化的實踐策略:這是統領全過程的策略,基于真實情境所引發的思維沖突,或是對于實踐成果的質疑批判、遷移發展所引發的需要解決的新問題。
結構化的引導策略:結構化引導是邏輯化和主體化的統一,要依據學科的內在邏輯、主體的原生態思維,預設、生成由表及里、由淺入深的結構化問題,才能展示內隱的、包含失敗的豐富結構。
變化式的發展策略:在前述實踐基礎上開展對變式性、創新性問題的再研究,推進學習的深入,實現認識的轉化,促進價值認同和自我認同。
思想化的凝練策略:一是學習過程所包含的科學方法、學科思想;二是學習過程中主體的科學審美、情感態度;三是學習內容包含的價值觀念、家國情懷。
二、“結構課堂”的具體操作與實施
筆者提出的“結構課堂”的實踐框架由5大環節構成:1.確立教學目標,2.篩選關鍵要素,3.優化教學結構,4.促進過程共生,5.強化反饋調節。
三、“結構課堂”——原電池原理課堂教學實施過程
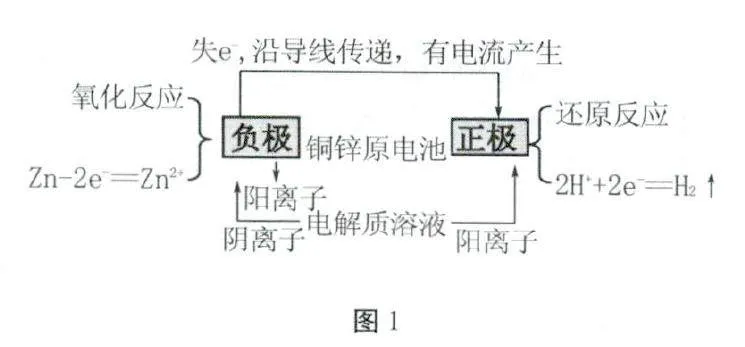
情境導入一:(科學史話1)公元1799年,科學家伏打(伏特)以含食鹽水的濕抹布,夾在銀和鋅的圓形板中間,堆積成圓柱狀,制造出最早的電池——伏打電池。將不同的金屬片插入電解質水溶液形成的電池,通稱伏打電池。今天把它的原理模型提煉出來就是我們曾在必修課程中學過的原電池,也稱單液原電池。單液電池原理模型如圖1所示(回顧必修課程學過的相關內容——第一次模型引入)。
教材從一開始就說這種原電池的缺點,同學們通過動手實驗來探究下它有哪些缺點呢?
學生小組實驗探究一:討論分析單液電池在實際應用中有何弊端。
實驗步驟:
1.按照圖2所示連接好數字化傳感器。
2.紅色導線夾鏈接銅片,黑色導線夾鏈接鋅片,采集數據2 min。
3.觀察鋅片、銅片、平板電腦電流示數的變化并如實記錄。
4.實驗結束,將電極從電解質溶液中取出,用濾紙擦干;如實書寫實驗現象。
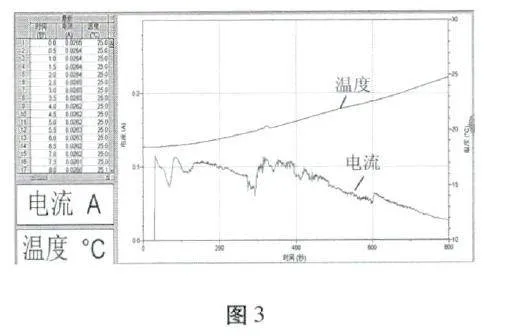
單液電池實驗現象歸納分析:(單液原電池溫度傳感器與電流傳感器采集實驗數據圖如圖3所示)
電極現象:鋅片、銅片上有均有紅色物質析出。
電流曲線:電流曲線不穩定,逐漸減小。
溫度變化:溫度曲線明顯升高,說明部分化學能未能轉化為電能,而是變成了熱能。
猜想原因:①Zn與Cu2+直接接觸發生反應,Zn片、附著在Zn上的Cu以及CuSO4溶液局部形成了原電池,促進了Cu在鋅片表面析出。②轉移的電子沒有經過導線,電流逐漸衰減;Cu2+、Zn2+混在一起,降低了電極電勢差。③因氧化劑與還原劑直接接觸(會發生非原電池反應),放電時間短,轉化為電能的效率不高。
該裝置能量轉化率低的原因是什么?如何解決?(第一次翻轉進階)
小組討論,解決問題的關鍵:還原劑Zn與氧化劑CuSO4不直接接觸,即分成雙液。
這樣行嗎?不行,2個溶液間缺少離子導體,無法形成閉合回路。
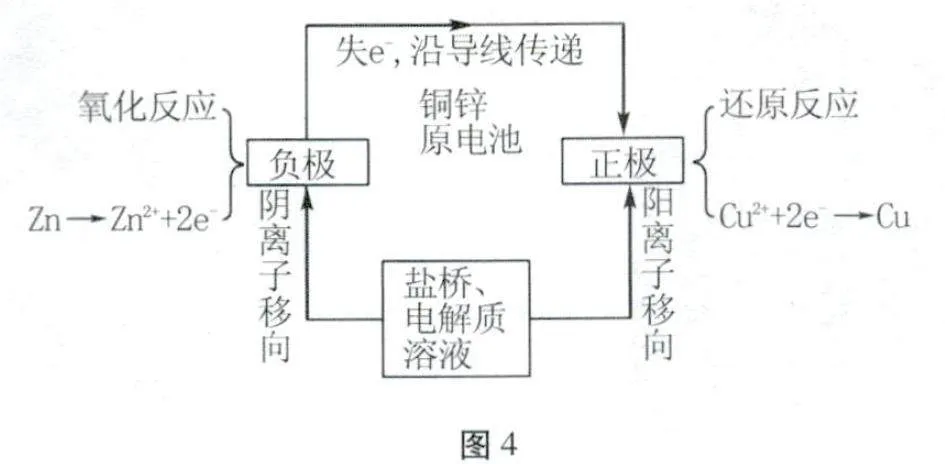
情境導入二:(科學史話2)1836年,丹尼爾根據伏打電堆發明世界上第一個實用電池,并用于早期鐵路的信號燈。丹尼爾電池就是今天所要學習的帶鹽橋的雙液電池。帶鹽橋的雙液電池相比于傳統的單液電池,在能量密度、使用壽命、安全性等方面都有所提高。雙液電池原理模型如圖4所示(第二次建模)。
鹽橋的作用:(略)。但我們測量后發現,教材上的U型管雙液原電池電流并不比單液原電池電流大,反而變小了!說明盡管雙液電池比單液電池有很多優點,但也不是完美的!
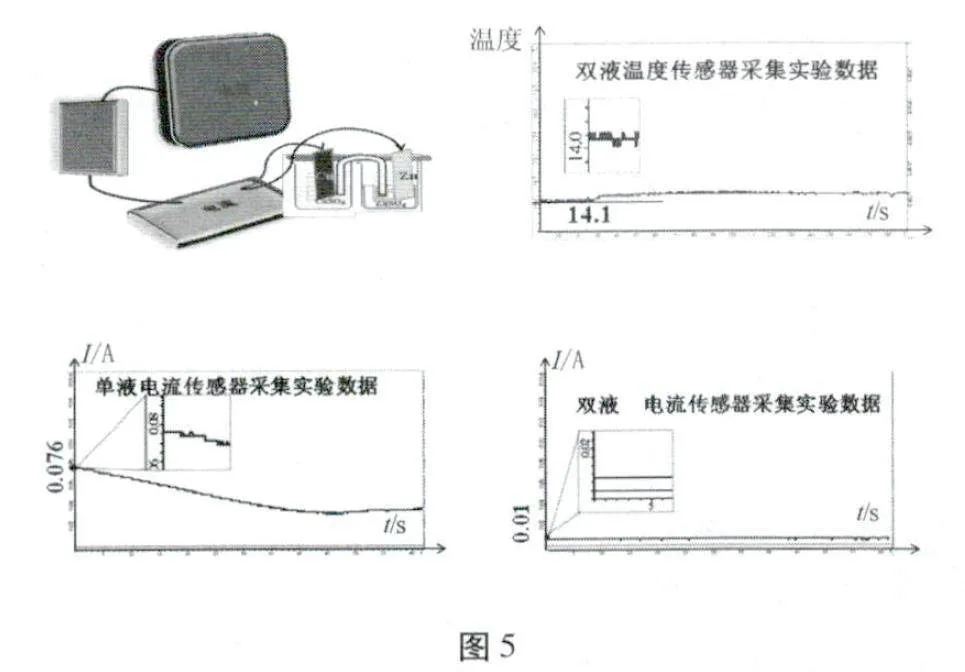
學生小組實驗探究二:雙液電池在實際應用中有何優缺點。
實驗及所得數據如圖5所示。
電極現象:鋅片上無明顯變化;銅片上有紅色物質析出。
電流曲線:電流曲線平穩,但示數較小。溫度變化:
溫度曲線變化不明顯,說明化學能基本全部轉化為電能。
小組討論歸納:大家先從理論角度討論變小的原因是什么?(從鹽橋內離子移動距離和離子運動通道2個方面思考對原電池內阻的影響。)
一是鹽橋距離長,離子運動距離變長,二是鹽橋與電解質溶液接觸面積小,離子運動通道變窄,導致原電池內阻變大電流變小。
如何改進?(第二次翻轉進階)
①將鹽橋加寬變短!②藥品用量依然較大,能否設計更微型化的原電池?
小組討論研究微型化創新方案:
1.濾紙條作為反應池;
2.蘸有飽和KCl液濾紙當作鹽橋。
實驗步驟:
1.如圖6所示,在銅片上放一層濾紙滴加5滴CuSO4;鋅片上放濾紙滴加5滴ZnSO4;用鑷子夾取蘸有飽和KCI溶液的濾紙,再與2塊金屬片緊貼好,用小玻璃片壓住濾紙,用魚尾夾同定好。
2.讀取數據2 min,測完請及時斷開電路。
3.導線夾與金屬片接觸即可,避免接觸溶液。
趣味實驗:將電極插入兩瓣未分開的橘子,為何兩瓣未分開的橘子也能產生電流?
強調“膜”的功能:分區但又允許離子通過。相對于鹽橋,上面2例中的“浸了KCl溶液的隔板”和“兩瓣未分開的橘子中的膜”優勢在哪?
情境導入三:(科學史話3)1950年W.朱達首先合成了離子交換膜,應用時主要是利用它的離子選擇透過性。高中化學中常見的有:陽離子交換膜,陰離子交換膜,質子交換膜。
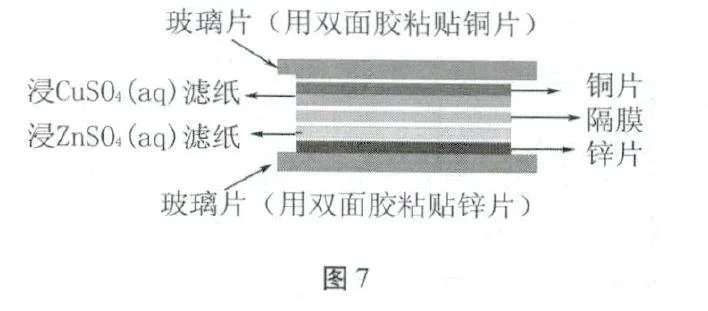
學生小組實驗探究三:原電池的高效化與微型化創新改進——帶離子交換膜的微型化電池。
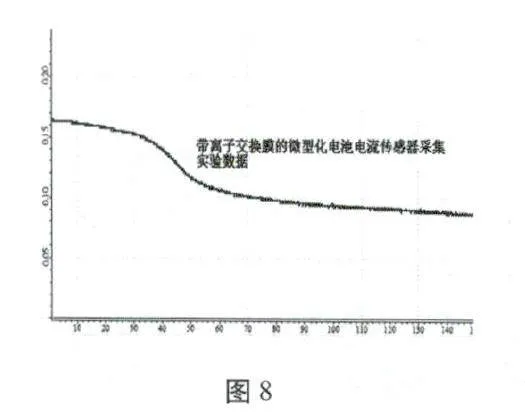
經過分析、設計與討論,按照圖7組裝原電池裝置,并連接傳感器與平板電腦進行數據采集。
采集完數據(如圖8所示)后,對離子交換膜的微型化電池有哪些優勢做出分析歸納和總結(對照單液電池和雙液電池)。
帶離子交換膜的微型化電池優點:體積小、藥品用量少(1 mL)、電流持久較穩定、實驗操作簡便快速、陽膜可重復使用、廢棄濾紙無污染綠色化學等優點。
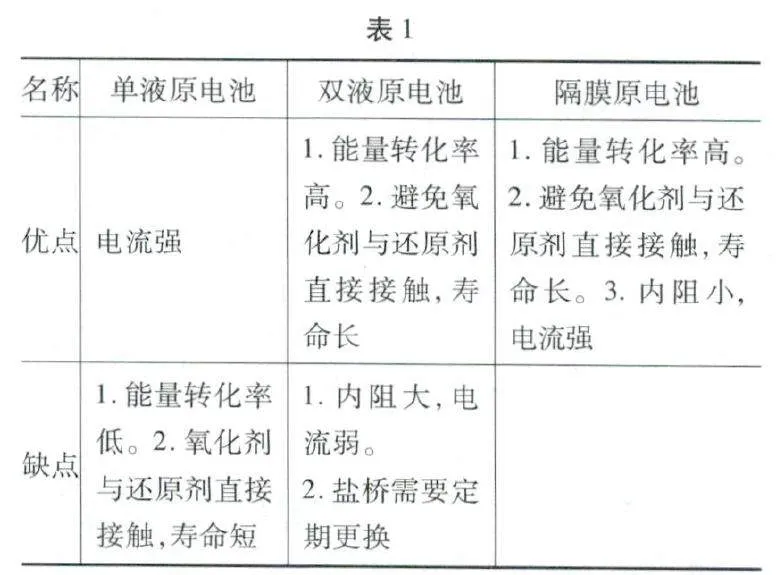
對比分析:其分析見表1。
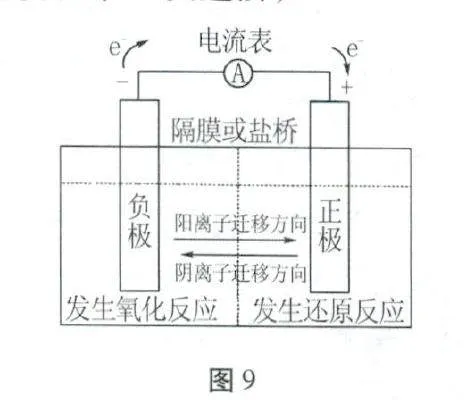
至此,建立起原電池理想化模型如圖9所示。(第三次建模和第三次進階)
(構成原電池四要素及其功能略。)
課堂反饋調節——精選有關陌生電池的原理分析題讓學生演練(過程略)。
基金項目:本論文系中國教師教育發展研究院科研活動綜合委員會“重點規劃課題”2022年度立項課題“基于新課程新教材的高中化學探究性實驗案例及應用效果評價研究”(課題號:JYF2104628)的階段性研究成果。
(收稿日期:2024 -04 - 26)

