加速超分割放療聯合PD-1抑制劑在小細胞肺癌誘導化療后的應用價值


【摘要】 目的:分析加速超分割放療聯合程序型死亡受體-1(PD-1)抑制劑在小細胞肺癌(SCLC)誘導化療后的應用價值。方法:回顧性選取2021年4月—2023年3月新余市人民醫院收治的82例SCLC患者的臨床資料,依據治療方式分為觀察組(n=42)、對照組(n=40),對照組采用依托泊苷+順鉑/卡鉑(EP)或者伊立替康+順鉑/卡鉑(IP)方案進行誘導化療,同時聯合加速超分割放療,觀察組在對照組基礎上聯合新型PD-1抑制劑。對比兩組臨床療效及治療前后血清腫瘤標志物、Karnofsky評分、生存情況與不良反應發生情況。結果:觀察組客觀緩解率(ORR)明顯高于對照組,差異有統計學意義(P<0.05)。治療后,兩組血清胃泌素釋放肽前體(ProGRP)、神經元特異性烯醇化酶(NSE)、細胞角蛋白-19的可溶性片段(Cyfra21-1)、癌胚抗原(CEA)水平均低于治療前,且觀察組均低于對照組,差異均有統計學意義(P<0.05)。治療后1、6、12個月,兩組Karnofsky評分均高于治療前,且觀察組Karnofsky評分均高于對照組,差異均有統計學意義(P<0.05)。觀察組1年內無進展生存率、總生存率均略高于對照組,但差異均無統計學意義(P>0.05)。兩組各項不良反應發生率比較,差異均無統計學意義(P>0.05)。結論:加速超分割放療聯合PD-1抑制劑用于SCLC患者誘導化療后,可明顯地提高臨床療效,下調腫瘤標志物水平,安全可靠。
【關鍵詞】 加速超分割放療 PD-1抑制劑 小細胞肺癌 誘導化療 安全性
Application Value of Accelerated Hyperfractionated Radiotherapy Combined with PD-1 Inhibitor after Induction Chemotherapy for Small Cell Lung Cancer/LI Lifang, LIU Xiaohong, YUAN Chuanping, AI Dongdong. //Medical Innovation of China, 2024, 21(26): 0-028
[Abstract] Objective: To analyze the application value of accelerated hyperfractionated radiotherapy combined with programmed death receptor-1 (PD-1) inhibitor after induction chemotherapy in small cell lung cancer (SCLC). Method: Clinical data of 82 SCLC patients admitted to Xinyu People's Hospital from April 2021 to March 2023 were retrospectively selected, and divided into observation group (n=42) and control group (n=40) according to treatment methods. The control group received induction chemotherapy with Etoposide + Cisplatin/Carboplatin (EP) or Irinotecan + Cisplatin (IP) regimen combined with accelerated hyperfractionation radiotherapy, the observation group was combined with new PD-1 inhibitor on the basis of control group. The clinical efficacy, serum tumor markers, Karnofsky score before and after treatment, survival and adverse reactions were compared between the two groups. Result: The short-term objective response rate (ORR) in the observation group was significantly higher than that iTIbFe7oMqNN3J54jtoylFQ==n the control group, the difference was statistically significant (P<0.05). After treatment, serum levels of pro-gastrin releasing peptide (ProGRP), neurone-specific enolase (NSE), soluble fragment of cytokeratin-19 (Cyfra21-1) and carcinoembryonic antigen (CEA) in two groups were lower than those before treatment, and those in observation group were lower than those in control group, the differences were statistically significant (P<0.05). At 1, 6 and 12 months after treatment, the Karnofsky scores of the two groups were higher than those before treatment, and the Karnofsky scores of the observation group were higher than those of the control group, the differences were statistically significant (P<0.05). The progression-free survival rate and overall survival rate during the past year in the observation group were slightly higher than those in the control group, but there were no statistical significance between the two groups (P>0.05). There were no significant differences in the incidence of adverse reactions between the two groups (P>0.05). Conclusion: Accelerated hyperfractionated radiotherapy combined with PD-1 inhibitor for induction chemotherapy in SCLC patients can significantly improve the clinical efficacy, reduce the level of tumor markers, and is safe and reliable.
[Key words] Accelerated hyperfractionated radiotherapy PD-1 inhibitor Small cell lung cancer Induction chemotherapy Safety
First-author's address: Department of Oncology, Xinyu People's Hospital, Xinyu 338000, China
doi:10.3969/j.issn.1674-4985.2024.26.006
小細胞肺癌(SCLC)屬于一種神經內分泌腫瘤,有高度侵襲性、生長迅速及伴癌旁內分泌與早期廣泛轉移等特點[1]。目前治療SLCL的方案以放化療為主,但大多數患者于初始治療之后不久即出現復發情況,多數預后不佳,開展持久而有效的一線治療有重要意義。在臨床上胸部放療和免疫治療聯合具備協同增效作用,原因為免疫和傳統腫瘤放療化療聯合可有效激活人體的自身免疫反應,最終特異而持續地識別全身腫瘤細胞,因此胸部放療聯合免疫治療SCLC具有良好的理論基礎,但目前仍需更多臨床數據[2]。放療可縮小及消除癌灶,加速超分割放療中采用的超分割劑量有一定的臨床療效,且治療時間短頻次少,患者耐受性好,但SCLC在既往研究中經免疫治療用于二線后,與胸部放療聯合者較少[3]。近年來國產免疫檢測點抑制劑程序型死亡受體-1(PD-1)不斷增多,在許多實體腫瘤中已納入醫保適應證,價格實惠,患者可及性大,其中信迪利單抗為新型PD-1抑制劑之一,已被證實可提高非小細胞肺癌的總生存率及無進展生存率[4],本研究擬探索PD-1抑制劑聯合加速超分割放療對SCLC的療效及安全性,明確局部放療與免疫聯合治療的最佳時機。
1 資料與方法
1.1 一般資料
回顧性選取2021年4月—2023年3月新余市人民醫院收治的82例SCLC患者的臨床資料。納入標準:(1)均滿足相關診斷[5],經病理與影像學檢測確診;(2)年齡18~71歲,臨床分期Ⅲb、Ⅳ期;(3)未見其他類型的癌癥或遠處轉移。排除標準:(1)合并嚴重的心腦血管性病變、其他惡性腫瘤;(2)既往存在肺部手術的情況或對于本研究所采用的藥物有過敏史;(3)免疫性疾病、器官衰竭、精神異常。依據治療方式分為觀察組(n=42)、對照組(n=40),本研究經新余市人民醫院醫學倫理委員會批準。
1.2 方法
對照組采用依托泊苷+順鉑/卡鉑(EP)或者伊立替康+順鉑/卡鉑(IP)方案進行誘導化療,同時聯合加速超分割放療,(1)誘導化療:EP方案為,第1~3天予以依托泊苷注射液(生產廠家:福州基石醫藥科技有限公司,批準文號:國藥準字H35021396,規格:2 mL︰40 mg)80~100 mg/m2靜脈滴注;第1~3天給予順鉑注射液(生產廠家:齊魯制藥有限公司,批準文號:國藥準字H20213819,規格:50 mL︰50 mg)75 mg/m2靜滴或者僅在第1天給予卡鉑注射液(生產廠家:齊魯制藥有限公司,批準文號:國藥準字H20227083,規格:15 mL︰150 mg)300 mg/m2。每21天為1個周期,每治療2個周期評估病灶,共持續4~6個周期。IP方案,在第1天、第8天靜滴鹽酸伊立替康注射液(生產廠家:江蘇恒瑞醫藥股份有限公司,批準文號:國藥準字H20061276,規格:5 mL︰100 mg)100 mg/m2;第1~3天靜脈滴注順鉑75 mg/m2或僅在第1天給予卡鉑300 mg/m2,每21天為一個周期,每治療2個周期評估病灶,共持續6個周期。(2)胸部加速超分割放療方法:在2或3個療程的誘導化療后行胸部放療。觀察組另予以信迪利單抗注射液[生產廠家:信達生物制藥(蘇州)有限公司,批準文號:國藥準字S20180016,規格:10 mL︰100 mg]200 mg/次,靜脈滴注,每3周使用1次。
1.3 觀察指標與評價標準
(1)根據實體瘤療效評估標準評價治療6周期結束時的效果,分為完全緩解(CR)、部分緩解(PR)、病情穩定(SD)、病情進展(PD),客觀緩解率(ORR)=(CR+PR)例數/總例數×100%[6]。(2)治療前及治療結束時,采集3 mL的晨空腹靜脈血,采用Eppendorf離心機在3 500 r/min速率下離心(離心半徑=8 cm,濕度55%~60%)10 min,分離血清,-70 ℃冰箱保存,采用全自動化學發光免疫分析儀及其配套試劑盒測定胃泌素釋放肽前體(ProGRP)、神經元特異性烯醇化酶(NSE)、細胞角蛋白-19的可溶性片段(Cyfra21-1)、癌胚抗原(CEA)水平。(3)治療前及治療后1、6、12個月采用Karnofsky量表評估兩組生活質量,該表評分為0~100分,得分越高表明患者健康狀況越好。(4)記錄兩組1年內無進展生存期(PFS)、總生存期(OS)情況。(5)記錄治療期間的不良反應發生情況,包括放射性食管炎、放射性肺炎、肝損傷、骨髓抑制、乏力、血小板減少、消化道反應等。
1.4 統計學處理
本研究數據采用SPSS 23.0統計學軟件進行分析和處理,計量資料以(x±s)表示,采用獨立/配對樣本t檢驗、重復測量數據的方差分析及LSD-t檢驗;計數資料以率(%)表示,采用字2檢驗/連續校正字2檢驗,繪制Kaplan-Meier曲線分析生存情況。以P<0.05為差異有統計學意義。
2 結果
2.1 兩組基線資料比較
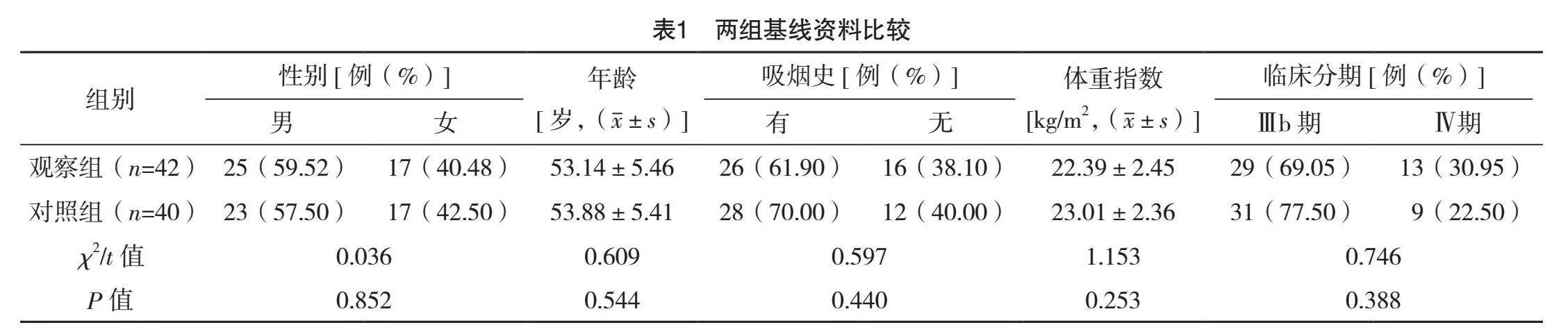
兩組基線資料比較,差異均無統計學意義(P>0.05),有可比性,見表1。
2.2 兩組臨床療效比較
觀察組ORR達78.57%,明顯高于對照組的57.50%,差異有統計學意義(字2=4.201,P=0.040),見表2。
2.3 兩組腫瘤標志物水平比較
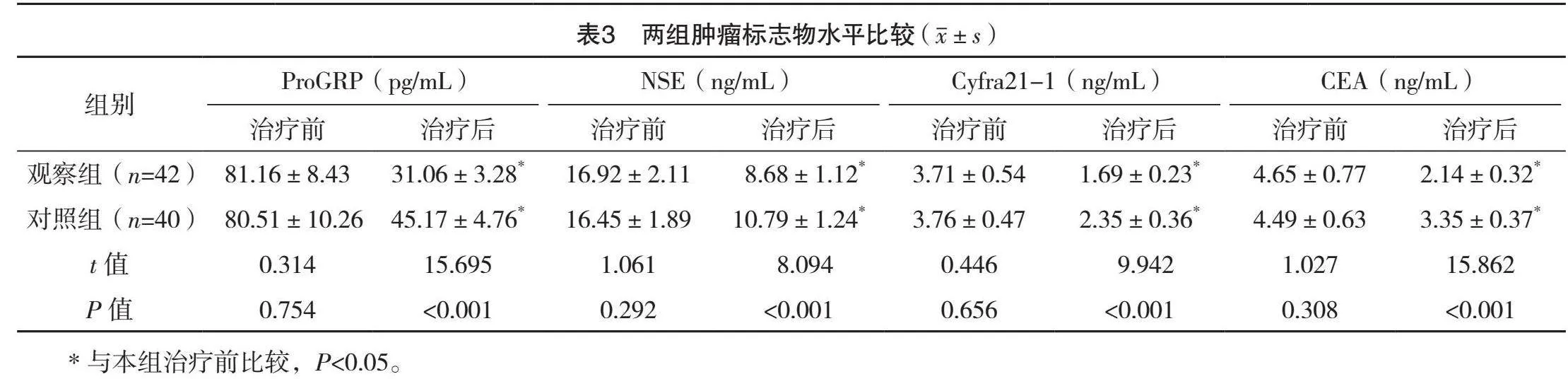
治療前,兩組各腫瘤標志物水平比較,差異均無統計學意義(P>0.05);治療后,兩組ProGRP、NSE、Cyfra21-1、CEA水平均低于治療前,且觀察組均低于對照組,差異均有統計學意義(P<0.05)。見表3。
2.4 兩組不良反應發生情況比較
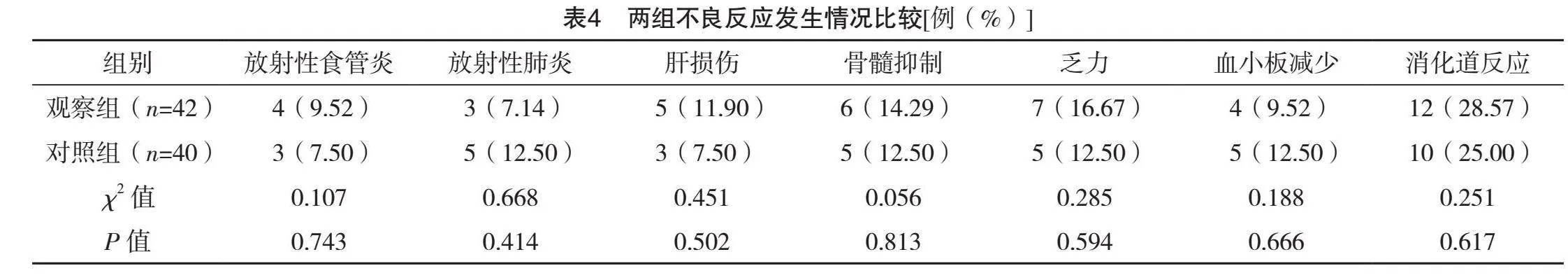
兩組各項不良反應發生率比較,差異均無統計學意義(P>0.05),見表4。
2.5 兩組Karnofsky評分比較
觀察組有4例在11個月時達終點事件,對照組1例在9個月時達終點事件,2例在10個月時達終點事件,2例在11個月時達終點事件,1例在12個月時達終點事件,因此治療12個月時兩組樣本量分別為36、34例。治療后1、6、12個月,兩組Karnofsky評分均高于治療前,且觀察組Karnofsky評分均高于對照組,差異均有統計學意義(P<0.05);兩組Karnofsky評分的交互、組間、時點效應比較,差異均有統計學意義(F交互=11.476,F組間=13.942,F時點=62.985,P交互<0.001,P組間<0.001,P時點<0.001)。見表5。
2.6 兩組生存情況比較
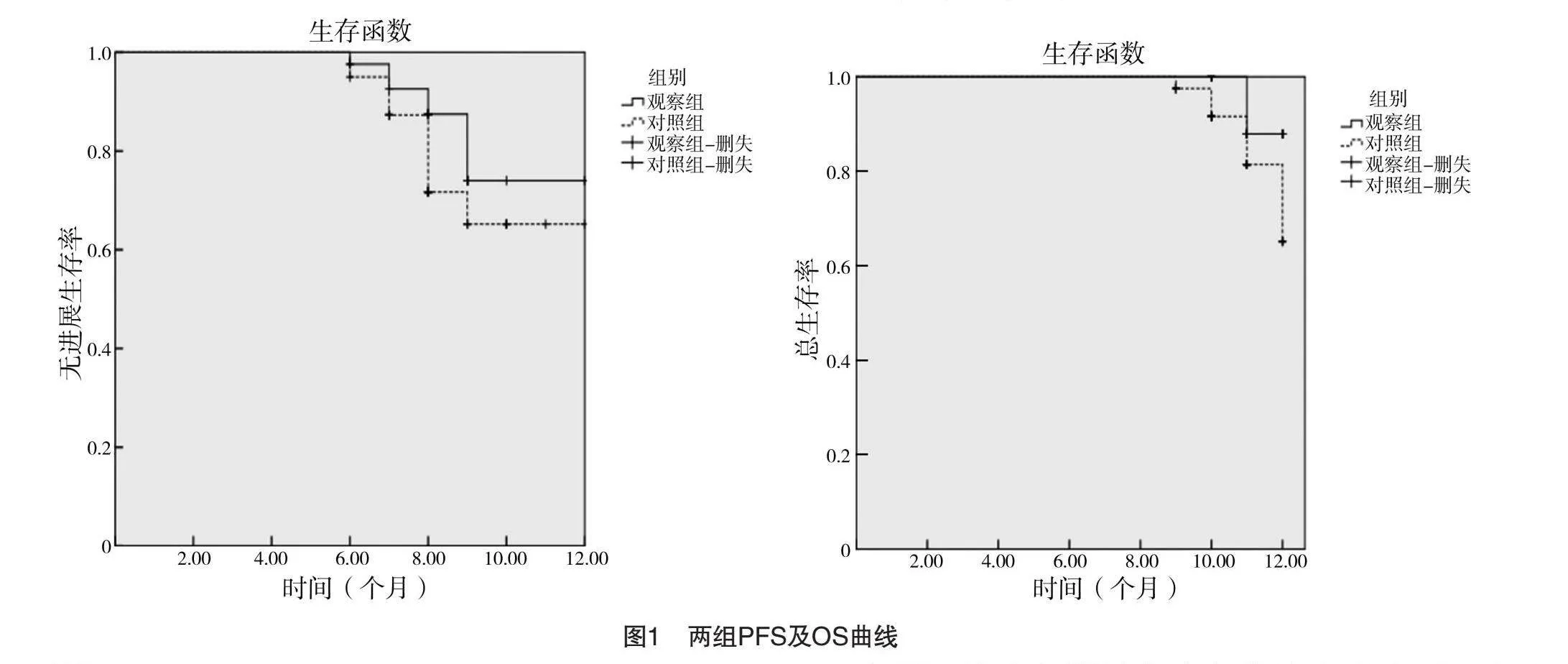
觀察組平均PFS、OS分別為11.00、11.88個月,均長于對照組的10.53、11.70個月;Kaplan-Meier檢驗顯示,觀察組1年內的無進展生存率為79.64%,總生存率為83.24%,均略高于對照組的65.20%、75.10%,但差異均無統計學意義(Log rank字2=1.482,P=0.224;Log rank字2=2.171,P=0.141)。見圖1。
3 討論
SCLC具有較高的發病率、致死率,臨床應及時采取治療措施。目前主要采用以順鉑為主的誘導化療方案對SCLC進行治療,可在一定程度上延長患者生存期,并改善預后,但其有較多副作用[7]。放療可降低癌細胞的遠處播散,其中超分割放療時單日總照射劑量較大,照射相對較為頻繁,這會造成正常組織器官及免疫系統恢復減慢,免疫系統受損[8]。PD-1為主的免疫治療則會使腫瘤血管正常化,改善腫瘤微環境乏氧,使腫瘤對放射線更加敏感,其中信迪利單抗為常用PD-1抑制劑[9],但目前仍缺乏PD-1抑制劑聯合放療在SCLC中的大型臨床研究數據。
在采用放療與誘導化療方案治療癌癥時,由于藥物及放射線對于正常組織、器官具備一定殺傷作用,可能損傷臨近靶區食管、正常肺組織及免疫細胞[10]。本次觀察組采用超分割放療聯合信迪利單抗、常規誘導化療,結果顯示其ORR達78.57%,明顯高于對照組的57.50%,表明聯合方案對于SCLC有一定療效。放療可促進抗原的識別及提呈、激活免疫相關通路、重塑腫瘤免疫抑制微環境;而信迪利單抗能有效地激活機體中抗腫瘤免疫效應,提高其免疫水平[11-12]。
隨SCLC病情進展,患者體內血清腫瘤標志物分泌增多,其中Cyfra21-1屬于肺組織腫瘤上皮中含量最高的細絲蛋白,可作為檢測肺癌的敏感性指標[13]。本次發現,觀察組Cyfra21-1、CEA水平均低于對照組,與周蓓燁等[14]的研究相近,但本研究也發現觀察組治療后血清ProGRP、NSE水平均低于對照組,因此聯合方案能有效地調節SCLC腫瘤標志物。原因可能是信迪利單抗可阻斷與配體PD-L1/2的結合,減少腫瘤細胞的免疫逃逸狀態,并活化CD4+T細胞,提高靶向癌細胞殺傷力,最終改善腫瘤的微環境狀態[15-16],提升生活質量,這也是觀察組治療后各隨訪時點Karnofsky評分均高于對照組的原因。在生存獲益上,本次兩組PFS、OS及1年內無進展生存率、總生存率未見明顯差異,與文獻[17-20]研究結果有出入,可能與本次隨訪時間較短,病例數較少有關,關于在生存方面的影響后期需要進一步展開長期隨訪觀察和研究。
PD-1抑劑治療可能在激活機體抗腫瘤免疫效應的同時也誘發免疫相關的毒副反應[21-23]。柳家榮等[24]的研究發現,信迪利單抗聯合鹽酸安羅替尼二線治療晚期SCLC的不良反應均可耐受。本次發現,觀察組各項不良反應發生率與對照組差異無顯著性,提示聯合用藥后會引起SCLC病例一定的毒副反應風險,但通過采取對癥干預/調整藥物等措施后,不良反應均在可控范圍,耐受性良好。
綜上所述,加速超分割放療與PD-1抑制劑用在SCLC患者誘導化療后,可明顯地提升療效,下調各項腫瘤標志物,延長生存期,安全性可靠。
參考文獻
[1]彭春艷,劉勇,易琰斐,等.撳針預埋療法防治小細胞肺癌EP方案所致惡心嘔吐的療效觀察[J].中國醫學創新,2022,19(11):81-84.
[2]孫軍霞,李宏亮.大分割放療治療非小細胞肺癌的療效觀察和毒副作用[J].沈陽藥科大學學報,2021,38(S1):128-128.
[3]李錫清,趙尊蘭,候夢琳,等.惡病質對信迪利單抗免疫治療非小細胞肺癌療效的影響[J].中華腫瘤雜志,2021,43(12):1292-1297.
[4] LU S,WU L,JIAN H,et al.Sintilimab plus Bevacizumab biosimilar IBI305 and chemotherapy for patients with EGFR-mutated non-squamous non-small-cell lung cancer who progressed on EGFR tyrosine-kinase inhibitor therapy (ORIENT-31): first interim results from a randomised,double-blind,multicentre,phase 3 trial[J].Lancet Oncol,2022,23(9):1167-1179.
[5]石遠凱,孫燕,于金明,等.中國晚期原發性肺癌診治專家共識(2016年版)[J].中國肺癌雜志,2016,19(1):1-15.
[6] EISENHAUER E A,THERASSE P,BOGAERTS J,et al.New response evaluation criteria in solid tumours: revised RECIST guideline(version 1.1)[J].Eur J Cancer,2009,45(2):228-247.
[7] ZHANG F,BAI H,GAO R,et al.Dynamics of peripheral T cell clones during PD-1 blockade in non-small cell lung cancer[J].Cancer Immunol Immunother,2020,69(12):2599-2611.
[8] REESE S W,CONE E,MARCHESE M,et al.Lessons from pharmacovigilance: pulmonary immune-related adverse events after immune checkpoint inhibitor therapy[J].Lung,2021,199(2):199-211.
[9] FU L,CHEN P,WANG S,et al.Complete pathological response with diabetic ketoacidosis to the combination of sintilimab and anlotinib in an unresectable hepatocellular carcinoma patient: a case report[J].Anticancer Drugs,2022,33(1):e741-e746.https://pubmed.ncbi.nlm.nih.gov/34338239/.
[10]何宜生,鮑亮亮,余嘉文,等.大分割放療聯合EP方案化療治療局限期小細胞肺癌的臨床療效及安全性[J].腫瘤防治研究,2023,50(2):170-174.
[11]王澤偉,王偉佳,張洪巖.超分割放療對局限期小細胞肺癌患者T淋巴細胞亞群和腫瘤標志物的影響[J].臨床肺科雜志,2023,28(12):1788-1792.
[12] LU S,WU L,JIAN H,et al.Sintilimab plus chemotherapy for patients with EGFR-mutated non-squamous non-small-cell lung cancer with disease progression after EGFR tyrosine-kinase inhibitor therapy (ORIENT-31): second interim analysis from a double-blind, randomised, placebo-controlled, phase 3 trial[J].Lancet Respir Med,2023,11(7):624-636.
[13]蔚曉勇,李曉鳳,史婉婷,等.信迪利單抗聯合紫杉醇、多西他賽二線治療晚期非小細胞肺癌效果分析[J].腫瘤研究與臨床,2024,36(1):6-10.
[14]周蓓燁,王芳,劉銀.安羅替尼聯合信迪利單抗對晚期非小細胞肺癌的臨床療效分析[J].中國現代醫學雜志,2022,32(23):28-33.
[15]楊艷莉,劉紅梅,余靜麗.信迪利單抗對晚期非小細胞肺癌患者T淋巴細胞亞群的影響及其治療效果研究[J].癌癥進展,2023,21(3):301-304,308.
[16] XU J,JIANG H,PAN Y,et al.Sintilimab plus chemotherapy for unresectable gastric or gastroesophageal junction cancer: the orient-16 randomized clinical trial[J].JAMA,2023,330(21):2064-2074.
[17]宋慧勝,李志英,王馨,等.局限期小細胞肺癌常規分割放療與加速超分割放療的臨床療效觀察[J].廣東醫學,2020,41(12):1259-1262.
[18]劉文揚,韓梓銘,王健仰,等.廣泛期小細胞肺癌誘導治療后胸部放療序貫PD-1/PD-L1抑制劑的安全性研究[J].中華放射腫瘤學雜志,2022,31(3):236-241.
[19]武陽,陸翰杰,水會鋒.既往免疫經治的晚期非小細胞肺癌患者接受安羅替尼聯合PD-1單抗的療效及安全性[J].實用醫學雜志,2023,39(5):572-578.
[20]白悅,孫大強,張遜,等.PD-1單抗聯合化療在ⅢA期非小細胞肺癌術前新輔助治療中的應用[J].中華胸心血管外科雜志,2022,38(2):96-101.
[21]何維清.抗程序性死亡因子-1/程序性死亡配體1單抗治療進展期非小細胞肺癌療效及對腫瘤浸潤T細胞密度和分布的影響[J].黑龍江醫學,2022,46(1):17-19.
[22]王廉.信迪利單抗聯合替莫唑胺治療膠質母細胞瘤的效果及對p53蛋白、BMP、TPX2的影響[J].中國醫學創新,2022,19(35):5-9.
[23]王桂英.程序性細胞死亡蛋白-1抑制劑聯合紫杉醇+順鉑化療方案治療肺鱗癌患者的近遠期效果觀察[J].黑龍江醫學,2023,47(1):31-34.
[24]柳家榮,段玲,王文義,等.信迪利單抗聯合鹽酸安羅替尼二線治療晚期小細胞肺癌的前瞻性、單臂Ⅱ期臨床研究[J].實用癌癥雜志,2023,38(5):839-842.
(收稿日期:2024-07-09) (本文編輯:馬嬌)

