三個(gè)實(shí)驗(yàn)的改進(jìn)及教學(xué)

摘 要: 分析學(xué)生可能暴露的錯(cuò)誤或不完整的認(rèn)知結(jié)構(gòu),在原有實(shí)驗(yàn)基礎(chǔ)上,分別設(shè)計(jì)、改進(jìn)氫氧燃料電池的制備、氯水成分的探究以及NOx的制備和性質(zhì)等實(shí)驗(yàn),較好地引導(dǎo)學(xué)生進(jìn)行實(shí)驗(yàn)探究。通過(guò)實(shí)驗(yàn)操作、數(shù)據(jù)分析和反思討論,提高了學(xué)生的科學(xué)素養(yǎng)和實(shí)驗(yàn)?zāi)芰Α?/p>
關(guān)鍵詞: 氫氧燃料電池; 氯水成分; 氮氧化物; 教學(xué)案例; 實(shí)驗(yàn)改進(jìn)
文章編號(hào): 1005-6629(2024)11-0071-05
中圖分類(lèi)號(hào): G633.8
文獻(xiàn)標(biāo)識(shí)碼: B
由感性認(rèn)識(shí)得出的結(jié)論常常會(huì)偏離科學(xué)現(xiàn)象的本質(zhì)[1]。通過(guò)針對(duì)性地創(chuàng)新實(shí)驗(yàn),可以有效輔助學(xué)生暴露錯(cuò)誤或者不完整的認(rèn)知結(jié)構(gòu),使學(xué)生感受到原有概念的局限[2]。本文以氫氧燃料電池的制備、氯水成分的探究、NOx制備和性質(zhì)的實(shí)驗(yàn)教學(xué)為案例,設(shè)計(jì)符合學(xué)情的創(chuàng)新實(shí)驗(yàn),有效指導(dǎo)學(xué)生進(jìn)行科學(xué)探究。通過(guò)實(shí)驗(yàn)操作和數(shù)據(jù)分析引導(dǎo)學(xué)生逐步上升到理性認(rèn)識(shí),真正發(fā)揮實(shí)驗(yàn)的育人價(jià)值。
1 氫氧燃料電池實(shí)驗(yàn)改進(jìn)
1.1 教材實(shí)驗(yàn)
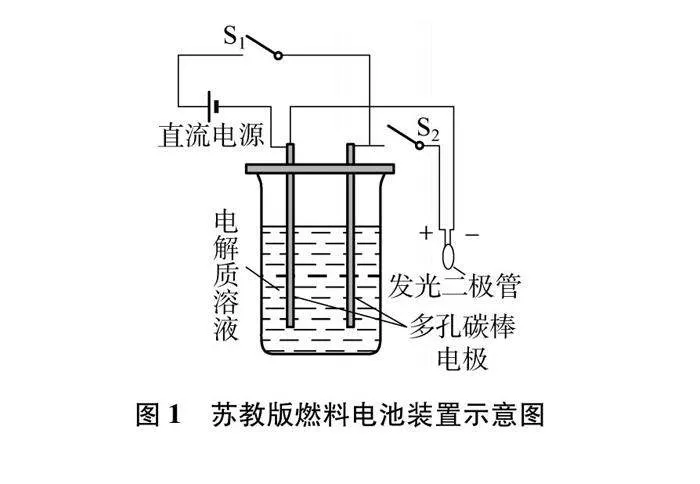
2020年版的蘇教版化學(xué)必修二中的實(shí)驗(yàn)裝置如圖1所示。
(1) 按下開(kāi)關(guān)S1,接通電源,電解溶液約半分鐘,碳棒上分別產(chǎn)生明顯的氣泡。
(2) 斷開(kāi)開(kāi)關(guān)S1,按下開(kāi)關(guān)S2,可以觀察到二極管的發(fā)光現(xiàn)象。
1.2 實(shí)驗(yàn)改進(jìn)的動(dòng)機(jī)
2017年版《普通高中化學(xué)課程標(biāo)準(zhǔn)》(以下簡(jiǎn)稱(chēng)“新課標(biāo)”)將“制作簡(jiǎn)易的燃料電池”列為學(xué)生必做實(shí)驗(yàn)。
學(xué)生對(duì)鋅銅-稀硫酸原電池的認(rèn)識(shí)是具體的:鋅失去電子,電子通過(guò)導(dǎo)線移動(dòng)到銅極,所以銅極產(chǎn)生氫氣;學(xué)生對(duì)燃料電池的認(rèn)識(shí)是抽象的:氣體不能做電極,外電路如何產(chǎn)生電子的定向移動(dòng)形成電流,是學(xué)生對(duì)燃料電池的最大困頓。針對(duì)性地改進(jìn)實(shí)驗(yàn),通過(guò)實(shí)驗(yàn)對(duì)比使學(xué)生主動(dòng)意識(shí)到外部電流的產(chǎn)生主要有兩種方式:一是電極本身可以失去電子;二是電極本身作為催化劑,使覆在活性位點(diǎn)上的氣體失去電子[3]。常見(jiàn)的燃料電池就是利用了第二種方式。
1.3 改進(jìn)實(shí)驗(yàn)
1.3.1 實(shí)驗(yàn)用品
器材:9V方塊電池、3mm LED發(fā)光二極管、兩個(gè)碳棒、兩支8cm長(zhǎng)的中華牌2B鉛筆芯、鎳泡電極、硬紙板
藥品:10%硫酸溶液和飽和Na2SO4的混合溶液
1.3.2 實(shí)驗(yàn)裝置
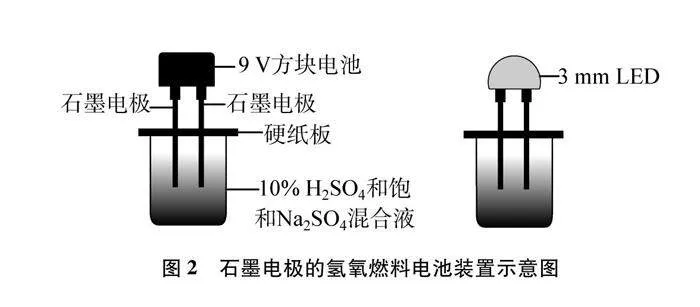
改進(jìn)后的實(shí)驗(yàn)裝置如圖2所示。
1.3.3 實(shí)驗(yàn)步驟和現(xiàn)象
(1) 選擇與9V方塊電池電極直徑相當(dāng)?shù)奶及簟?/p>
(2) 以9V電池的正負(fù)極之間的寬度作為標(biāo)準(zhǔn)把兩支碳棒固定在硬紙板上。
(3) 在燒杯中注入10%的硫酸和飽和Na2SO4的混合溶液為電解質(zhì)溶液。
(4) 將9V的方塊電池的正負(fù)極充分接觸兩支碳棒。兩支碳棒都產(chǎn)生大量的氣泡,與電源負(fù)極相連的一端產(chǎn)生的氣體比另一端產(chǎn)生的氣體更多。
(5) 當(dāng)氣體非常多的時(shí)候,取下方塊電池。
(6) 迅速將3mm LED發(fā)光二極管連接到電路中,3mm LED發(fā)光二極管亮了。
1.3.4 實(shí)驗(yàn)注意事項(xiàng)
(1) 如果碳棒太粗,可以用小刀將碳棒的頭部削一下,確保碳棒與電池的正負(fù)極充分接觸。
(2) 可以彎曲3mm LED的電極,固定3mm LED和碳棒,保證碳棒與之充分接觸。
(3) 電解的時(shí)間以90秒為宜。
(4) 移走電池后,要迅速連接好3mm LED和碳棒。
1.3.5 對(duì)比實(shí)驗(yàn)
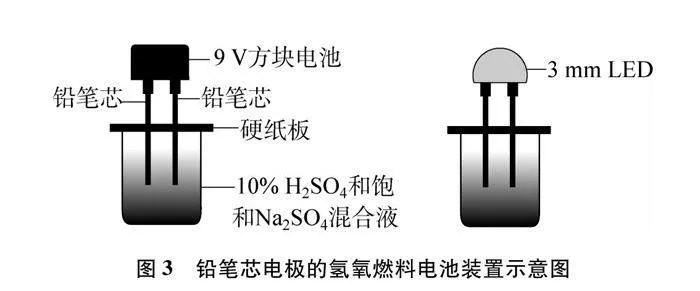
(1) 更換電極,采用兩支8cm長(zhǎng)的2B鉛筆芯為電極,如圖3所示。操作同上,小燈泡不亮。
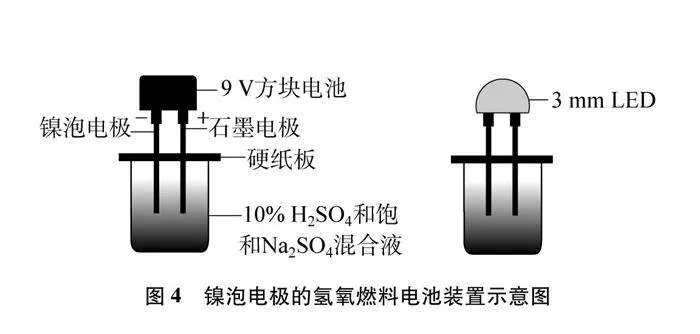
(2) 更換電極,采用鎳泡電極與電池的負(fù)極相連,如圖4所示。操作同上,小燈泡亮的時(shí)間明顯比碳棒長(zhǎng)。
1.4 實(shí)驗(yàn)改進(jìn)的意義
“講”燃料電池是中學(xué)最普遍的實(shí)驗(yàn)教學(xué)現(xiàn)象。化學(xué)家傅鷹說(shuō)過(guò):“提出一個(gè)機(jī)理來(lái)解釋一種現(xiàn)象并不困難,困難的是如何以實(shí)驗(yàn)證明這是正確的,而且是唯一正確的機(jī)理。在未達(dá)到這個(gè)地步之時(shí),我們對(duì)于任何理論都應(yīng)該持保留態(tài)度。只有如此,才是實(shí)事求是的科學(xué)精神。”
通過(guò)對(duì)比實(shí)驗(yàn),觀察到采用鉛筆芯電極有氣泡產(chǎn)生,氣泡少,小燈泡不亮;采用石墨電極,有大量的氣泡產(chǎn)生,小燈泡可以亮2~4秒;采用鎳泡電極[4],同樣有大量的氣泡產(chǎn)生,小燈泡可以亮5~6秒。通過(guò)此實(shí)驗(yàn)現(xiàn)象,學(xué)生不但可以得出燃料電池的電極材料扮演兩個(gè)角色,一是催化劑,氫氣覆蓋在電極材料的活性位點(diǎn)上,就可以失去電子;二是充當(dāng)導(dǎo)線,傳輸電子,還可以得出不同的電極催化效果是不同的,氫氧燃料電池中鎳泡電極優(yōu)于石墨電極[5,6]。
2 氯水成分探究實(shí)驗(yàn)改進(jìn)
2.1 教材實(shí)驗(yàn)
2020年版的蘇教版化學(xué)必修一中,沒(méi)有實(shí)驗(yàn)裝置圖,通過(guò)三個(gè)小實(shí)驗(yàn)探究氯水的成分[7]。
(1) 實(shí)驗(yàn)1:將干燥的有色布條和濕潤(rùn)的有色布條分別放入兩瓶干燥的氯氣中,觀察并比較實(shí)驗(yàn)現(xiàn)象。
(2) 實(shí)驗(yàn)2:分別用玻璃棒蘸取新制氯水和稀鹽酸,滴在pH試紙上,觀察并比較實(shí)驗(yàn)現(xiàn)象。
(3) 實(shí)驗(yàn)3:在潔凈的試管中加入1mL新制氯氣,再向試管中加入幾滴硝酸銀溶液和稀硝酸,觀察實(shí)驗(yàn)現(xiàn)象。
2.2 實(shí)驗(yàn)改進(jìn)的動(dòng)機(jī)
氯氣有毒,課堂演示該實(shí)驗(yàn)的教師少之又少。教材的實(shí)驗(yàn)設(shè)計(jì)想達(dá)成三個(gè)教學(xué)目標(biāo):一是通過(guò)對(duì)比實(shí)驗(yàn)讓學(xué)生意識(shí)到氯水中真正具有漂白作用的是次氯酸,氯氣不具有漂白性;二是氯水呈酸性,可以用pH計(jì)測(cè)定,但不宜用pH試紙測(cè)量;三是氯氣與水會(huì)發(fā)生反應(yīng),且反應(yīng)是可逆的。氯水的漂白性、氯水的酸性測(cè)量是近幾年高考考查的熱點(diǎn),也是學(xué)生最普遍的失分項(xiàng)。轉(zhuǎn)變思維,氯氣雖然有毒卻是增強(qiáng)學(xué)生“綠色化學(xué)”觀念的契機(jī)。作為一名化學(xué)教師有責(zé)任教會(huì)學(xué)生正確處理有毒氣體,降低有毒氣體的危害且利用它的性質(zhì)造福人類(lèi)社會(huì)。
2.3 改進(jìn)實(shí)驗(yàn)
2.3.1 實(shí)驗(yàn)用品
器材:2個(gè)50mL的注射器、10個(gè)紅色的采血管、干燥的有色布條、濕潤(rùn)的有色布條
藥品:濃鹽酸、高錳酸鉀、飽和食鹽水、濃硫酸、稀硝酸、稀硝酸銀溶液、紫色石蕊溶液
2.3.2 實(shí)驗(yàn)裝置
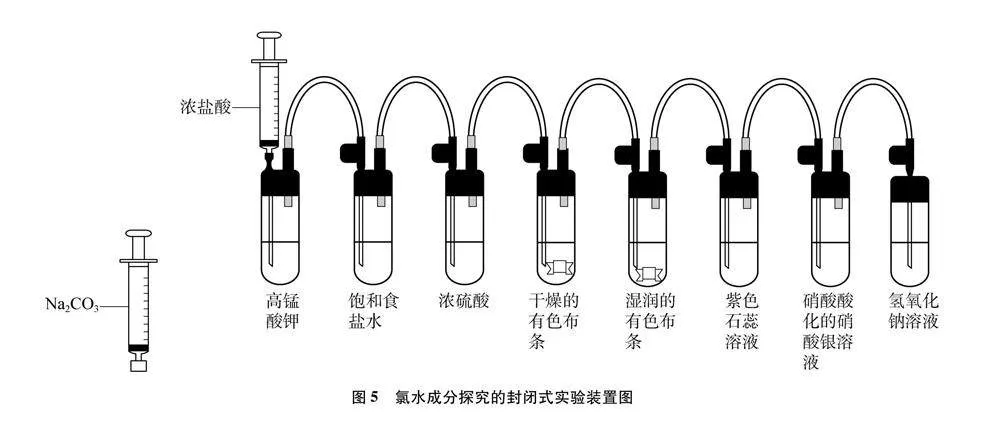
改進(jìn)的實(shí)驗(yàn)裝置如圖5所示。
2.3.3 實(shí)驗(yàn)步驟及現(xiàn)象
(1) 推動(dòng)注射器活塞,少量多次地推入濃鹽酸。
(2) 可以觀察到有黃綠色氣體產(chǎn)生、干燥的有色布條不變色、濕潤(rùn)的有色布條退色,紫色石蕊先變紅、然后退色,硝酸銀溶液中出現(xiàn)白色沉淀。
(3) 更換注射器,將飽和Na2CO3溶液推入濃鹽酸與高錳酸鉀反應(yīng)后的體系中,利用HCl與Na2CO3反應(yīng)產(chǎn)生CO2氣體,從而將裝置中的氯氣趕入氫氧化鈉溶液中,增強(qiáng)學(xué)生的環(huán)保意識(shí)。
(4) 由現(xiàn)象得出實(shí)驗(yàn)結(jié)論。
① Cl2+H2OHCl+HClO
② Cl-+Ag+AgCl↓
③ 干燥的氯氣沒(méi)有漂白性,濕潤(rùn)的氯氣具有漂白性
尾氣處理:Cl2+2NaOHNaCl+NaClO+H2O
2.3.4 實(shí)驗(yàn)注意事項(xiàng)
(1) 高錳酸鉀需少量,確保全部反應(yīng)掉。
(2) 濃鹽酸要少量多次地加入,防止反應(yīng)太劇烈。
(3) 反應(yīng)后的裝置中有氯氣,反應(yīng)最后要將飽和Na2CO3溶液推入發(fā)生裝置中,排出裝置中的氣體,對(duì)尾氣進(jìn)行處理。
2.4 實(shí)驗(yàn)改進(jìn)的意義
掌握概念須理解其內(nèi)涵,明其外延。紫色石蕊變紅,氯水中有H+,符合學(xué)生的常規(guī)認(rèn)知。后來(lái)退色,這一反常現(xiàn)象與學(xué)生的認(rèn)知是相悖的。這種碰撞可以讓學(xué)生認(rèn)識(shí)到任何一個(gè)概念都是內(nèi)涵與外延的統(tǒng)一。通過(guò)對(duì)比實(shí)驗(yàn),自然得出氯氣不具有漂白性的結(jié)論。教師要有意識(shí)地培養(yǎng)學(xué)生敢于質(zhì)疑、去偽存真的科學(xué)態(tài)度,這與“新課標(biāo)”提出化學(xué)學(xué)科核心素養(yǎng)也是一致的。封閉式實(shí)驗(yàn)設(shè)計(jì)探究氯水成分可以提高實(shí)驗(yàn)的安全性和教學(xué)效果。
3 NOx制備和性質(zhì)的實(shí)驗(yàn)改進(jìn)
3.1 教材實(shí)驗(yàn)
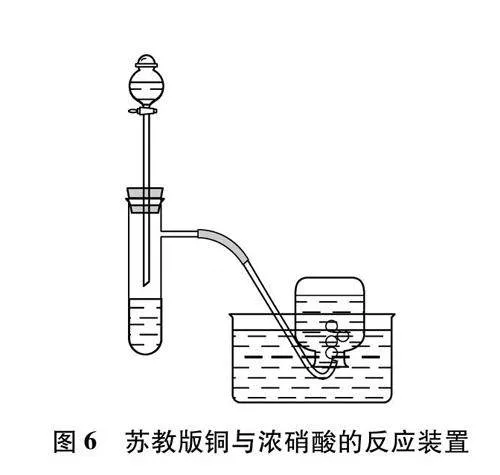
2020年版的蘇教版化學(xué)必修二中的實(shí)驗(yàn)裝置如圖6所示。
(1) 實(shí)驗(yàn)1:將銅片置于具支試管的底部,通過(guò)分液漏斗加入2mL濃硝酸,將產(chǎn)生的氣體通入倒置于水槽充滿水的集氣瓶中,觀察實(shí)驗(yàn)現(xiàn)象。
(2) 實(shí)驗(yàn)2:向分液漏斗內(nèi)加入5mL水,稀釋硝酸,繼續(xù)收集產(chǎn)生的氣體,觀察實(shí)驗(yàn)現(xiàn)象[8]。
3.2 實(shí)驗(yàn)改進(jìn)的動(dòng)機(jī)
銅與硝酸的反應(yīng)是高中化學(xué)教學(xué)中的一項(xiàng)重要內(nèi)容,教材的實(shí)驗(yàn)設(shè)計(jì)是有優(yōu)勢(shì)的,體現(xiàn)硝酸濃度不同的反應(yīng)產(chǎn)物也隨之不同。因?yàn)闆](méi)有排除空氣的干擾,銅與濃硝酸反應(yīng)產(chǎn)生的是NO2還是NO具有爭(zhēng)議性;學(xué)生易混淆NO2和NO;銅與硝酸的反應(yīng)產(chǎn)物取決于硝酸的濃度,這種由反應(yīng)物濃度不同導(dǎo)致產(chǎn)物不同也增加了學(xué)生理解和記憶的難度。
3.3 改進(jìn)實(shí)驗(yàn)
3.3.1 實(shí)驗(yàn)用品
儀器:10mL螺口注射器5個(gè)、50mL的螺口注射器1個(gè)、20mL注射器2個(gè)、6個(gè)三通閥、雙目魯爾管
藥品:銅片、濃硝酸、稀硝酸、蒸餾水、氫氧化鈉的酚酞溶液、氧氣
3.3.2 實(shí)驗(yàn)裝置
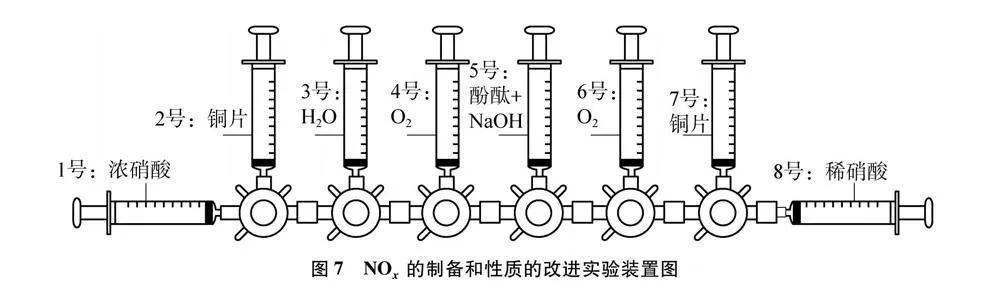
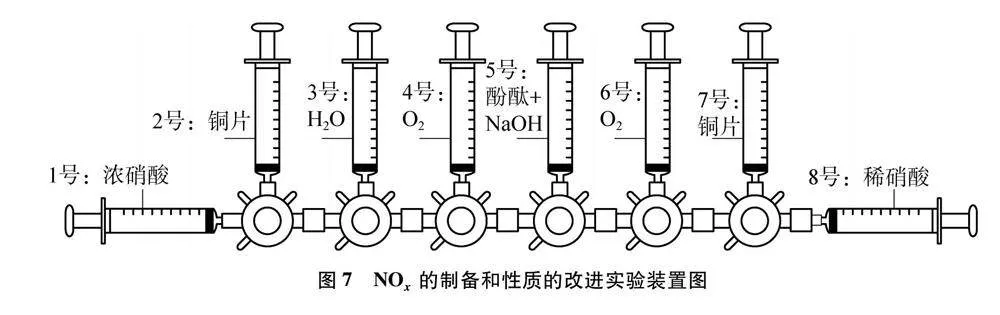
改進(jìn)的實(shí)驗(yàn)裝置如圖7所示。
3.3.3 實(shí)驗(yàn)步驟及現(xiàn)象
(1) 旋轉(zhuǎn)三通閥閥門(mén),將8號(hào)注射器中稀硝酸推入7號(hào)注射器中,關(guān)閉7號(hào)注射器閥門(mén)。
(2) 旋轉(zhuǎn)三通閥閥門(mén),將1號(hào)注射器中濃硝酸推入2號(hào)注射器中,關(guān)閉2號(hào)注射器閥門(mén)。
(3) 2號(hào)注射器里溶液變藍(lán)綠色,有紅棕色氣體產(chǎn)生,推動(dòng)2號(hào)注射器的活塞緩緩向上移動(dòng),直至銅片消失,活塞停止上升。
(4) 反應(yīng)停止后,旋轉(zhuǎn)活塞,將2號(hào)注射器中的溶液推入1號(hào)注射器,關(guān)閉1號(hào)的注射器閥門(mén)。
(5) 7號(hào)注射器中,產(chǎn)生氣泡,溶液變?yōu)闇\藍(lán)色。
(6) 旋轉(zhuǎn)閥門(mén),將2號(hào)中紅棕色氣體緩慢推入3號(hào)注射器中,紅棕色氣體消失,產(chǎn)生無(wú)色氣體,體積大約為紅棕色氣體的13。
(7) 待3號(hào)注射器中反應(yīng)完全,旋轉(zhuǎn)閥門(mén),將4號(hào)注射器中O2通入3號(hào)注射器中,無(wú)色的氣體快速變?yōu)榧t棕色,時(shí)間久了紅棕色又變?yōu)闊o(wú)色氣體。
(8) 7號(hào)注射器中銅片消失,溶液變成藍(lán)綠色,產(chǎn)生無(wú)色的氣體,旋轉(zhuǎn)閥門(mén),將7號(hào)注射器中溶液擠入8號(hào)注射器中,關(guān)閉8號(hào)注射器的閥門(mén)。
(9) 旋轉(zhuǎn)活塞,將6號(hào)中O2緩慢推入7號(hào)注射器中,7號(hào)注射器中無(wú)色氣體迅速變?yōu)榧t棕色。
(10) 調(diào)節(jié)閥門(mén),將3號(hào)注射器中液體和氣體擠入5號(hào)注射器中,將7號(hào)注射器中的氣體擠入5號(hào)注射器,5號(hào)注射器中紅色消失。
(11) 由現(xiàn)象得出實(shí)驗(yàn)結(jié)論(略)。
3.3.4 實(shí)驗(yàn)注意事項(xiàng)
(1) 3號(hào)、7號(hào)采用20mL的注射器,5號(hào)采用50mL的注射器,其他為10mL的注射器。
(2) 因?yàn)榛瘜W(xué)反應(yīng)速率較慢,旋轉(zhuǎn)閥門(mén)先將稀硝酸擠入銅片中。
(3) 銅片需少量,確保全部反應(yīng)掉。
(4) 緩慢充入氣體,防止氣體的總體積超過(guò)注射器的總體積。
3.4 實(shí)驗(yàn)改進(jìn)的意義
第一個(gè)對(duì)比實(shí)驗(yàn),銅與濃硝酸反應(yīng)產(chǎn)生紅棕色的氣體,銅與稀硝酸反應(yīng)產(chǎn)生無(wú)色氣體,得出反應(yīng)物濃度的不同,產(chǎn)物也不同的結(jié)論;第二個(gè)對(duì)比實(shí)驗(yàn),2號(hào)注射器中的紅棕色氣體遇到水會(huì)變成無(wú)色氣體,無(wú)色氣體遇到氧氣又變成紅棕色氣體。7號(hào)注射器中的無(wú)色氣體遇到氧氣變成紅棕色氣體。得出紅棕色氣體和無(wú)色氣體可以相互轉(zhuǎn)化的結(jié)論。最后把氣體都充入加有酚酞的氫氧化鈉溶液中,紅色溶液的顏色變淺直至消失,得出氫氧化鈉溶液可以對(duì)NOx進(jìn)行尾氣處理的結(jié)論。針對(duì)性創(chuàng)新實(shí)驗(yàn)的教學(xué)效果優(yōu)于“講”實(shí)驗(yàn),對(duì)促進(jìn)學(xué)生正確認(rèn)知的建立、提高教學(xué)質(zhì)量具有重要價(jià)值。
參考文獻(xiàn):
[1]張永康. 學(xué)生“相異構(gòu)思”的展現(xiàn)與激發(fā)[J]. 基礎(chǔ)教育研究, 2019, (2): 18~19.
[2]畢華林. 亓英麗. 化學(xué)教學(xué)論[M]. 北京: 北京師范大學(xué)出版社, 2022: 239.
[3]朱明建. 自制液壓儲(chǔ)氣式氫氧燃料電池[J]. 化學(xué)教學(xué), 2022, (4): 87~88.
[4]王新福. 用多孔泡沫金屬改進(jìn)中學(xué)化學(xué)實(shí)驗(yàn)的若干案例[J]. 化學(xué)教學(xué), 2024, (1): 71~73.
[5]盛榮. 對(duì)簡(jiǎn)易氫氧燃料電池實(shí)驗(yàn)的商榷及重制[J]. 化學(xué)教學(xué), 2017, (5): 56~57.
[6]陳靜, 陳懿. 氫氧燃料電池演示實(shí)驗(yàn)的改進(jìn)[J]. 化學(xué)教學(xué), 2022, (4): 74~75.
[7][8]鄒麗平, 林海斌. 教材實(shí)驗(yàn)類(lèi)欄目的教學(xué)建議[J]. 化學(xué)教學(xué), 2013, (3): 62~65.

