科學家開發智能計算生物醫學顯微成像技術提升成像精度和信息獲取能力
近日,浙江大學劉智毅研究員、劉文杰博士合作課題組開發定量智能計算成像(ADQ)框架,該框架提供了一種生物醫學顯微成像的新范式,通過智能計算輔助傳統光學顯微鏡幫助科學家找回數據中錯失的信息。
自埃里克·白茲格等相關學者于2014年獲得諾貝爾化學獎以來,超分辨顯微成像技術近十年得到了蓬勃發展,大量新技術不斷涌現,突破現有技術的成像分辨率、速度、深度等限制。但是每種技術均有其優缺點和適用范圍,選擇哪一種技術應對特定的問題是科學家們的困擾之一。
此外,超分辨顯微成像技術的發展最終服務于相關生物應用,但是如何將技術發展和生物應用更緊密地結合,幫助生物學家更好地觀察、發現和解釋新現象,仍然是長期以來的難題。
面對上述問題,ADQ框架通過智能計算輔助傳統光學顯微鏡充分挖掘潛藏的生物學信息,更好地助力生物學應用。
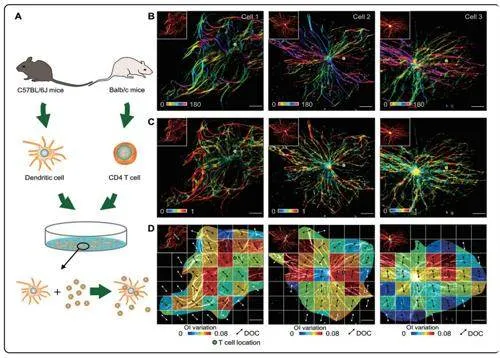
利用ADQ技術,研究人員研究了細胞骨架結構重塑與細胞遷移功能之間的關系,揭示了新現象。課題組發現了在單細胞遷移和多細胞互作誘導遷移這兩種遷移方式中,細胞微管結構重塑的相似性和差異性。
具體而言,在單細胞遷移中,微管在細胞遷移前端和尾端的空間重塑尤為劇烈;而在多細胞互作遷移中,微管在多細胞接觸點附近運動活躍。
有趣的是,在這兩種遷移方式中,微管呈現出一致的取向變化(DOC),并且與細胞遷移方向具有相關性。
這些微管結構重塑特征的發現,有助于研究者們更好地理解微管在細胞遷移過程中所發揮的力學功能,進而開展特異性細胞運動調控。

該研究應用前景廣闊,為生物醫學顯微成像領域提供了一種新的研究范式。從技術創新角度而言,ADQ框架也可用于指導優化結構光照明顯微鏡(SIM)外的其他超分辨成像技術。
從生物應用角度來看,ADQ可用于研究納米尺度下的多種亞細胞結構,如微管、微絲、內質網和線粒體等,有助于科學家更好地理解細胞遷移、代謝、凋亡等功能,進而啟發個性化疾病調控、干預和治療。
“該工作呈現得非常準確和詳盡。該研究和方法同時為亞細胞動態和行為相關的基礎和應用研究打開了新的大門。”
“該工作展示了超分辨顯微成像技術和定量數據分析之間的協同力量和魅力,以及如何啟發重要的細胞生物新發現。該工作對于技術創新和生物應用均具有重要貢獻。
生物醫學顯微成像新范式
該團隊所提出ADQ框架建立在一套多模態SIM儀器之上,該儀器集成了多種二維和三維SIM成像技術。
基于這套多模態儀器,他們提出了細胞結構驅動的ADQ框架。
ADQ框架首先使用寬場成像技術對細胞骨架進行高速拍攝,然后在角譜空間進行實時定量計算,獲取角度分布特征,用于選擇最優的成像模態。當細胞骨架呈扁平/層狀分布時,可選擇二維成像技術,不僅具有低光毒性,也能獲取樣品的較完整信息。
反之,當骨架錯綜復雜地分布在三維空間,此時二維成像技術難以獲取樣品的高保真信息,需要使用三維成像技術。
ADQ框架的另一項優勢在于對獲取的圖像實施高精度定量分析,由此揭示細胞骨架活動的基本規律。
課題組提出了二維/三維有序度指數(OI)算法對超分辨圖像進行全面的時空角譜域定量表征,分析細胞骨架的結構異質分布程度,及其與細胞遷移等功能之間的聯系。
OI算法對于噪聲、樣品密度、彎曲程度、標記方式等都具有較高的魯棒性,其在細胞不同局域上的時間漲落特征反映了細胞在遷移過程中的結構重塑與應激。
總體而言,ADQ通過角度分布預判定,同時選取最優的超分辨成像模態并實施相應的定量表征,從圖像獲取和分析多方面平衡了成像的保真度與光毒性。
與現有的超分辨率成像技術相比,ADQ的改進主要體現在以下兩個方面:
首先,相較于現有超分辨顯微成像技術多基于單一技術分析或多種技術的手動簡單關聯,ADQ提出通過定量計算角度空間分布自動選擇最佳的成像技術。
其次,相比于現有超分辨顯微成像技術多基于定性觀察,ADQ提出有序度指數OI算法進行多維度定量分析圖像,揭示重要的生命活動規律。
這些改進也決定了ADQ的兩大顯著優勢:
第一,ADQ能夠“按需智能成像”,自動平衡數據獲取的保真度和光毒性,以優化條件獲取樣品的全面信息,突破了傳統單一技術的性能局限。
第二,ADQ可以對樣品進行空間域、時間域和角譜域定量表征,多維度挖掘數據中的潛藏信息,推動生物研究的“定量化”。
這些潛在的大量生物應用信息在傳統多基于定性觀察的成像技術中很難被獲取到,且定性分析容易引入人為偏差。而ADQ能夠幫助生物學家更好地研究亞細胞生命過程,揭示新機制。
多學科領域交叉融合的成果
該研究體現了多學科領域之間的交叉合作,可大致分為3個重要階段。
第一階段是初步嘗試合作
劉智毅研究員和丁志華教授課題組長期從事生物醫學圖像的定量表征分析研究,深入探究纖維狀組織空間結構的精準解析,但多是在衍射極限尺度以上。
劉旭教授、匡翠方教授和劉文杰博士團隊致力于從事顯微成像相關研究,并開發了多種新型全內反射熒光顯微鏡(TIRFM)和SIM成像技術,提升了其分辨率和成像速度,但多是在定性成像層面。
因此,兩個團隊的交流產生了激烈的思想碰撞,直接啟發了在更基礎的納米尺度上對亞細胞結構進行定量分析的可能性。在利用已有數據進行初步嘗試后,他們進一步明確了合作的可行性。
第二階段是ADQ框架提出
定量分析一般需要大量的統計數據才能得到較為置信的結果,而單一的超分辨成像技術,受到時空分辨率矛盾限制,想要高效獲取大量有用數據非常費時費力。
為了解決這個問題,他們基于已經開發的空間角度分析方法和多模態SIM成像技術,進一步提出了ADQ框架,構建了一種超分辨成像模態自適應選擇的新方案。
同時,為了對細胞骨架分布的異質程度進行更有效的定量研究,他們開發了有序度指數算法OI。
第三階段是生物應用發現
在ADQ框架指導下,該課題組與姚雨石研究員等生物學家合作,對大量細胞遷移過程中的微管重塑進行了統計分析,發現了不同細胞遷移方式下微管結構重塑的相似性和差異性,揭示了骨架重塑在細胞遷移中的重要特征。
在研究推進的過程中,研究人員意外地發現,微管在細胞遷移過程中的角度變化與遷移方向有著緊密關聯。換言之,角度變化具有預測細胞遷移軌跡的能力。這一發現極大地豐富了ADQ方法的能力與內涵。
據悉,該團隊目前已經在嘗試使用人工智能對圖像進行定量結構分析,人工智能在低信噪比、大批量數據處理等方面具有較大的優勢,有望進一步擴展ADQ的應用前景。
此外,他們在人工智能增強的超分辨顯微圖像重構方面已經開展了系列研究,開發的算法有效提升了傳統光學顯微鏡的分辨率和重構保真度等,其中部分人工智能算法已經實現了商業化應用。
據悉,在后續的研究中,該課題組一方面會進一步發展ADQ框架,通過優化計算過程、圖形處理器(GPU)加速等提高運算速度,人工智能分析提高分析精度和自動化,從而能夠更好地對大批量生物醫學數據進行統計分析。
另一方面,將與生物學家合作,對癌癥等病變的細胞骨架重塑進行研究,以期能更好地理解疾病的形成過程。
