非洲豬瘟病毒p30蛋白與CRM197的融合表達及對小鼠的免疫原性評價

摘 要: 非洲豬瘟是由非洲豬瘟病毒引起的一種急性、高傳染性和致死性的傳染病,對豬養殖業造成了巨大的影響。安全有效的疫苗和有效治療藥物的缺乏給非洲豬瘟防控帶來了巨大的挑戰。作者嘗試設計一種融合蛋白以改善非洲豬瘟病毒p30的免疫原性。白喉毒素的無毒突變體CRM197已被成功地用作多糖-蛋白結合疫苗的載體蛋白,以增強多糖的免疫原性。本研究構建p30與CRM197催化結構域(A片段)的融合表達質粒,純化后的重組蛋白和單獨p30分別使用小鼠評價了其免疫原性。結果顯示:通過原核表達與親和層析純化得到融合蛋白p30-CRM197(A)免疫小鼠后,較單獨表達的p30其可以在更短的時間內激發起高水平針對p30的特異性IgG,并且在初次免疫后56 d后還能維持較高水平的淋巴細胞免疫活力。本研究結果表明,CRM197的A片段作為載體蛋白顯著增強原核表達p30蛋白的免疫原性,其可作為非洲豬瘟亞單位疫苗的候選分子內佐劑。
關鍵詞: 非洲豬瘟;CRM197;p30;免疫原性
中圖分類號: S852.659.1
文獻標志碼:A
文章編號:0366-6964(2024)11-5230-08
收稿日期:2024-01-02
基金項目:“十四五”重點研發子課題(2021YFD1801304)
作者簡介:張 琦(1999-),女,山東濱州人,碩士生,主要從事動物疫病防治研究,E-mail:1658735668@qq.com
*通信作者:孟春春,主要從事動物傳染病和預防獸醫學研究,E-mail:mengcc@shvri.ac.cn;蘇 艷,主要從事動物傳染病診斷技術及免疫防控的研究與教學,E-mail:2006au@163.com
Fusion Expression of African Swine Fever Virus p30 Protein and CRM197 and Evaluation
of Its Immunogenicity in Mice
ZHANG" Qi1,2, DONG" Ningning1, TAN" Xiaomei2, SHI" Zhengwang3, LI" Na2, ZHU" Wenqi1, TANG" Aoxing2, LI" Chuanfeng2, ZHU" Jie2, LIU" Guangqing2, SU" Yan1*, MENG" Chunchun1,2*
(1.Xinjiang Agricultural University, Urumqi 830052," China;
2.Shanghai Veterinary Research
Institute, Chinese Academy of Agricultural Sciences, Shanghai 200241," China;
3.Lanzhou Veterinary Research Institute,
Chinese Academy of Agricultural Sciences, Lanzhou 730050," China)
Abstract:" African swine fever is an acute, highly contagious and deadly infectious disease caused by the African swine fever virus, which has had a huge impact on the pig breeding industry. The lack of vaccines and effective therapeutic drugs has brought great challenges to the prevention and control of African swine fever. We tried to design a fusion protein to improve the immunogenicity of African swine fever virus p30. CRM197, a non-virulent mutant of diphtheria toxin, has been successfully used as a carrier protein in polysaccharide-protein conjugate vaccines to enhance the immunogenicity of polysaccharides. In this study, a fusion expression plasmid of p30 and CRM197 catalytic domain (A fragment) was constructed, and the immunogenicity of the purified recombinant protein and p30 alone were evaluated using mice. After immunizing mice with the fusion protein p30-CRM197(A) purified by prokaryotic expression and affinity chromatography, p30 alone could excite a high level of specific IgG against p30 in a shorter period of time, and maintain a high level of lymphocyte immune activity two months after the initial epidemic. The results of this study showed that the A fragment of CRM197 alone could significantly enhance the immunogenicity of prokaryotic expression p30 protein as a protein carrier, and it could be used as a candidate intramolecular adjuvant for African swine fever subunit vaccine.
Key words: African swine fever; CRM197; p30; immunogenicity
*Corresponding authors:" MENG Chunchun, E-mail: mengcc@shvri.ac.cn; SU Yan, E-mail:2006au@163.com
非洲豬瘟(African swine fever,ASF)是由非洲豬瘟病毒(African swine fever virus,ASFV)引起的一種高度傳染性的出血性疾病,被國際動物衛生組織(WOAH)列為法定報告疫病,也是我國重點防范的一類動物疫病。2018年8月,我國在遼寧省沈陽市發現首例非洲豬瘟病例,并迅速蔓延到全國多地[1]。截至目前,非洲豬瘟已在我國暴發過多起,造成巨大的經濟損失,是危害養豬業的“頭號殺手”。
迄今為止,還沒有安全有效的疫苗預防和控制非洲豬瘟[2],針對ASF疫苗的研究始于20世紀60年代,由于其擁有龐大的基因組結構和復雜的免疫逃逸機制,為疫苗研發工作帶來諸多困難[3]。目前正在研究的ASF疫苗包括滅活疫苗、減毒活疫苗和基因工程疫苗。滅活疫苗不能誘導細胞免疫反應,所以基本上是不可行的一種策略[4]。非洲豬瘟減毒疫苗雖然有一定效果,但是其安全性仍然具有極大不確定性[5-6]。目前最安全有效的策略是開發亞單位疫苗,以特異性抗原為核心的ASFV亞單位疫苗受到了廣泛關注,如p54、p30、p72、CD2v這些參與了病毒附著和內化多個步驟的病毒蛋白[7]。已初步證實,使用桿狀病毒表達的重組p54和p30蛋白免疫后可對強毒攻擊提供不同程度的保護水平,從延遲疾病發作到完全保護[8]。在同一系統中表達的嵌合p54/p30也取得了一些成功,免疫豬產生了中和抗體,并在野毒攻擊后存活[9]。
白喉毒素(diphtheria toxin,DT)及其交叉反應物質197(cross-reacting material 197,CRM197)得到了很好的研究[10]。DT由兩個片段組成:A片段(aa 1-190),包含催化C結構域,B片段包含跨膜(T)和受體結合(R)結構域。CRM197在A片段的第52位氨基酸由甘氨酸變為谷氨酸,從而消除了其細胞毒性[11]。然而其仍然保留了很強的免疫原性,并與DT特異性受體結合,因此已成功地應用于多糖-蛋白結合疫苗。CRM197已被用作幾種獲得許可的多糖-蛋白結合疫苗的載體蛋白,包括PREVNAR7、PREVNAR13和hibitter[12]。例如,用于預防肺炎的Prevnar 13是一種結合疫苗,由13種血清型的肺炎球菌多糖與CRM197共價結合而成[13]。與CRM197偶聯[14]有助于分泌Th1和Th2的T細胞迅速增加,并隨后產生細胞因子,進而誘導B細胞增殖和抗原特異性抗體分泌,從而增強其偶聯的多糖的免疫原性。CRM197作為分子內佐劑的益處已與其他蛋白質一起得到證實:Tobias等[15]最近發現,位于人表皮生長因子受體2上的雜交肽移植到CRM197上后,可誘導有效的免疫應答和抗腫瘤活性。由于CRM197具有較強的免疫原性,無毒性,可作為載體蛋白使用。作者嘗試使用CRM197的A片段作為載體蛋白與ASFV的p30蛋白進行融合表達并進行小鼠免疫評價,來評估CRM197的A片段是否可以有效地增強p30蛋白的免疫原性,為非洲豬瘟亞單位疫苗的研發提供新思路。
1 材料與方法
1.1 實驗動物及主要試劑
BALB/c小鼠購自上海杰思捷實驗動物有限公司。快速DNA連接酶、DNA膠回收試劑盒和高保真DNA聚合酶購自南京諾唯贊生物科技有限公司;限制性內切酶HindⅢ、BamHⅠ購自寶生物工程(大連)有限公司;BeyoGoldTM His-tag Purification Resin (耐還原型)均購自上海碧云天生物技術有限公司;美國通用Rehydragel@LV鋁佐劑購自北京博奧森生物技術有限公司。
1.2 重組質粒pET-32a-p30-CRM197(A)的構建
原核表達質粒 pCold Ⅰ-p30質粒由中國農業科學院上海獸醫研究所魏建超研究員提供。CRM197基因序列由NCBI下載(GenBank登錄號: KU521393.1)由蘇州金唯智生物科技有限公司進行密碼子優化并合成。將p30與CRM197的A片段使用柔性Linker(GGGGSGGGGS)串聯表達,由SnapGene設計兩對擴增引物,如表1所示,由上海生工生物工程股份有限公司合成。按照諾唯贊公司多片段同源重組試劑盒(貨號:c113)說明書進行操作,次日將陽性的單克隆菌落送往上海生工生物工程股份有限公司進行測序,測序結果進行序列比對,將比對正確的單克隆菌落進行質粒的提取,獲得構建成功的重組pET-32a-p30-CRM197(A)質粒。
1.3 p30蛋白和融合蛋白p30-CRM197的原核表達及純化
將pCold Ⅰ-p30和重組的pET-32a-p30-CRM197(A)質粒分別轉化大腸桿菌BL21(DE3)后,將陽性菌落進行少量誘導,pColdⅠ-p30質粒陽性的菌液在37℃搖床培養至OD600 nm為0.8時加入誘導劑IPTG(1 mmol·L-1),轉至16 ℃搖床培養20 h;pET-32a-p30-CRM197(A)質粒陽性菌液的OD600 nm至0.4時加入誘導劑IPTG(1 mmol·L-1),繼續在37 ℃搖床培養8 h。將誘導表達后的菌液在離心收集菌體,后用PBS將菌體重懸進行超聲破碎,將超聲破碎徹底后的菌液進行離心,收集上清和沉淀。將蛋白樣品分別進行12% SDS-PAGE電泳檢測。
根據12% SDS-PAGE的結果分析,確定p30蛋白和p30-CRM197(A)融合蛋白均是在包涵體表達。將包涵體用8 mol·L-1尿素重懸,室溫過夜溶解,離心收集上清,在透析袋中透析復性,將成功復性后蛋白溶液使用碧云天生產的His標簽蛋白純化試劑盒進行純化。
1.4 小鼠免疫及免疫原性評價
1.4.1 小鼠免疫程序制定
在上海杰思捷實驗動物有限公司購買24只4周齡BALB/c雌鼠,將小鼠分為4組,分別為PBS組、p30組、p30+AL佐劑組和p30-CRM197(A)+AL佐劑組,每組6只小鼠。PBS組每只小鼠免疫PBS 200 μL,p30組每只小鼠免疫p30蛋白50 μg,p30+AL佐劑組每只小鼠免疫p30蛋白50 μg與AL佐劑(體積1∶1),p30-CRM197(A)+AL佐劑組每只小鼠免疫p30-CRM197(A)蛋白50 μg和AL佐劑(體積1∶1),共免疫3次,每次免疫間隔14 d。
1.4.2 小鼠血清中特異性抗體IgG的測定
用碳酸鹽緩沖液(0.05 mol·L-1, pH9.6)將純化的p30蛋白稀釋至1 μg·mL-1,加入96孔酶標板,4 ℃包被過夜。洗滌,使用5%的脫脂牛奶進行封閉,4 ℃封閉10 h。洗滌,用PBS稀釋小鼠血清,加入酶標板,37℃孵育30min。洗滌,每孔加入用抗體稀釋液1∶15 000稀釋的山羊抗鼠IgG-HRP(Abcam公司, ab6915),37 ℃孵育30 min。洗滌,每孔加入50 μL TMB,37℃避光條件下顯色12 min,每孔加入50 μL終止液,用酶標儀讀取OD450 nm值。
1.4.3 小鼠脾淋巴細胞增殖水平測定
初次免疫后56 d,每組取3只小鼠,眼眶取血,并處死取脾,使用小鼠脾淋巴細胞分離試劑盒(索萊寶生物有限公司)分離淋巴細胞,將免疫小鼠脾淋巴細胞(2×106個細胞)接種于96孔板,用p30蛋白(20 μg·mL-1),在37 ℃,5% CO2細胞培養箱中刺激72h;無抗原刺激的做空白對照。采用CCK-8方法檢測增殖水平。
1.4.4 流式細胞術檢測T細胞亞群
初次免疫后56 d,每組取3只小鼠,眼眶取血,并處死取脾,使用小鼠脾淋巴細胞分離試劑盒(索萊寶生物有限公司)分離淋巴細胞,制備單細胞懸液。設置不染色對照組,單染管及樣品管。不染色對照組直接取淋巴細胞懸液即可;單染管分別使用PE anti-mouse CD3,FITC anti-mouse CD4和APC anti-mouse CD8a(Biolegend)與淋巴細胞懸液冰上避光孵育30 min;樣品管即同時加入上述3種抗體淋巴細胞懸液冰上避光孵育30 min。單染管和樣品管與熒光抗體結束后,加入Cell Staining Buffer洗兩次(350 ×g離心5 min),上流式細胞儀分析。
2 結 果
2.1 重組表達載體的構建
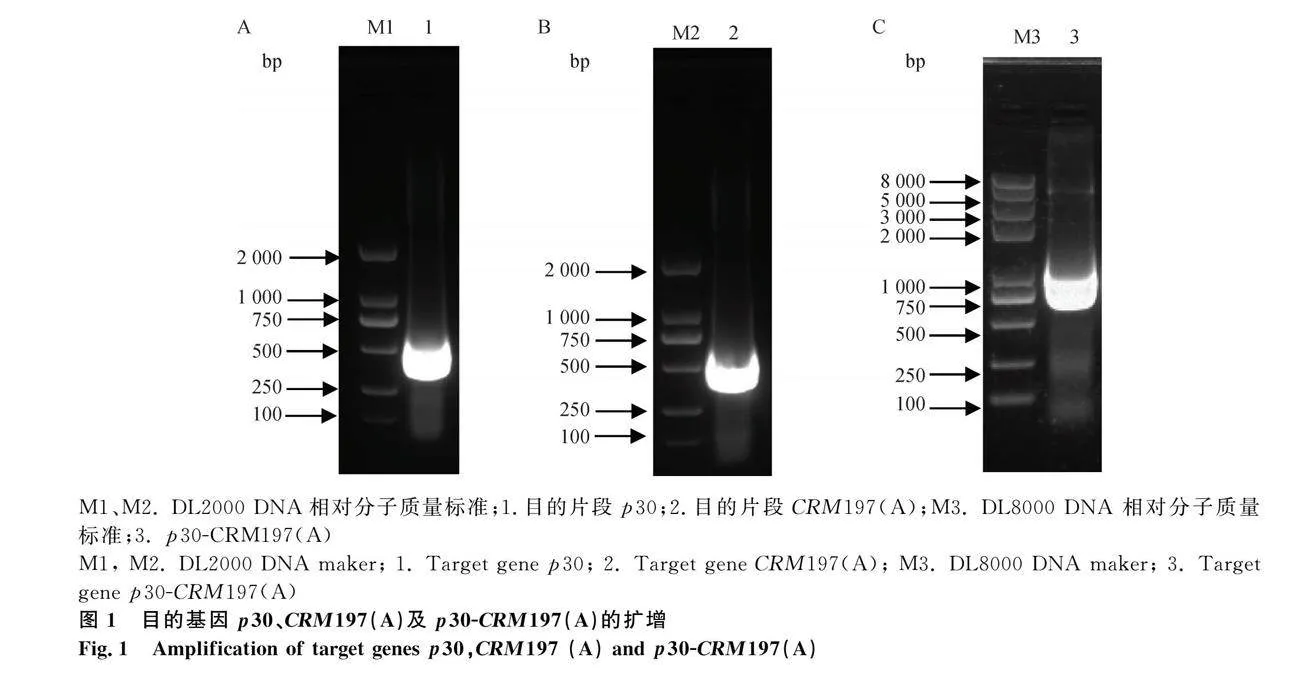
分別擴增p30和CRM197(A)如圖1A和1B所示,陽性條帶膠回收后用于同源重組。挑取重組后的菌落對目的基因p30-CRM197(A)進行菌液PCR鑒定如圖1C所示。隨后將陽性菌送上海生工生物公司進行測序,結果顯示重組質粒pET32a-p30-CRM197(A)構建成功。
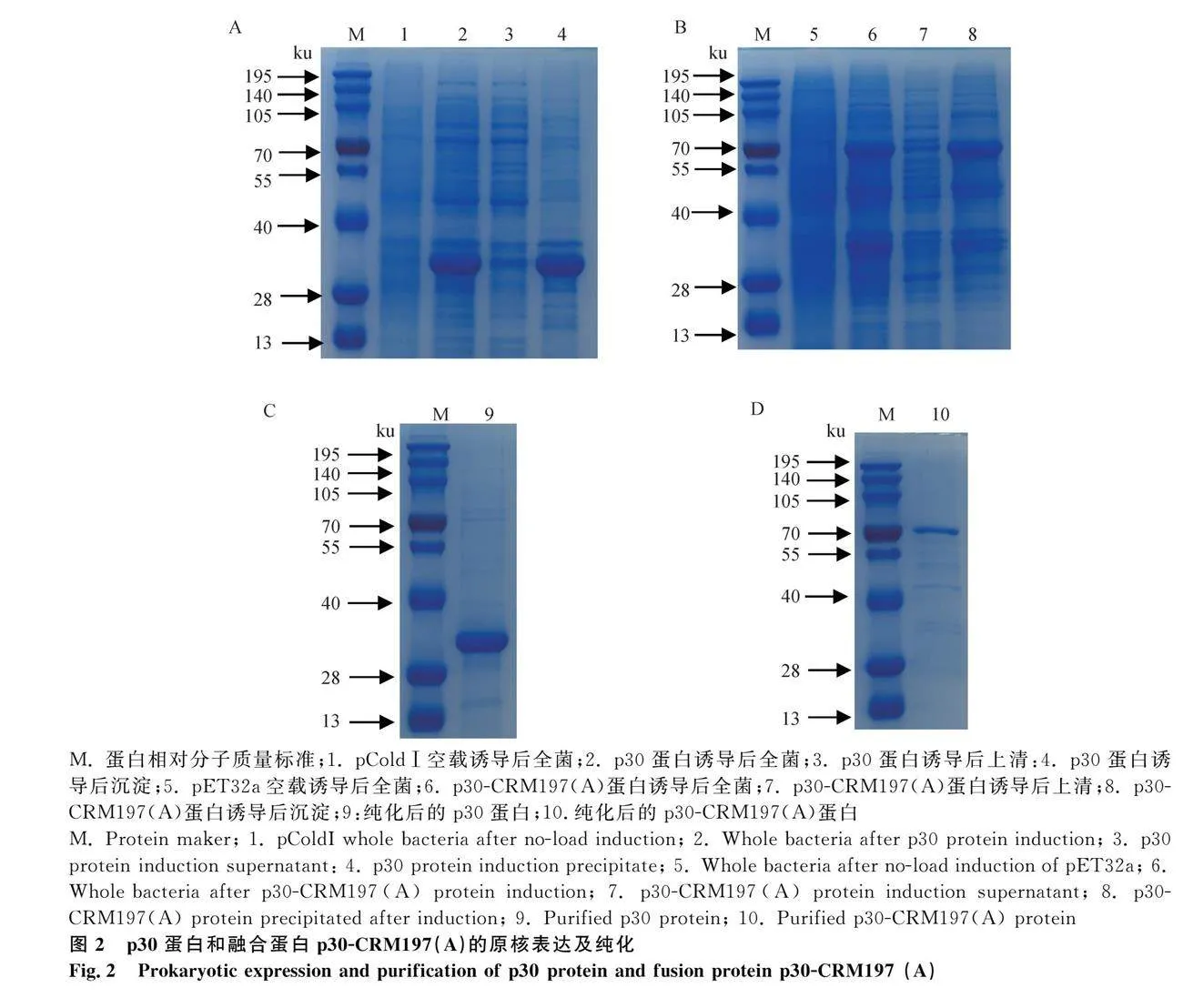
2.2 p30蛋白和融合蛋白p30-CRM197(A)的原核表達及純化
分別將誘導結束后的菌體,進行超聲破碎,收集全菌、上清及沉淀樣品進行12% SDS-PAGE,結果顯示,p30蛋白和p30-CRM197(A)均主要存在包涵體中(圖2A、B)。收集p30蛋白和融合蛋白p30-CRM197(A)洗脫液樣品,分別進行12% SDS-PAGE鑒定(圖2C、D)。
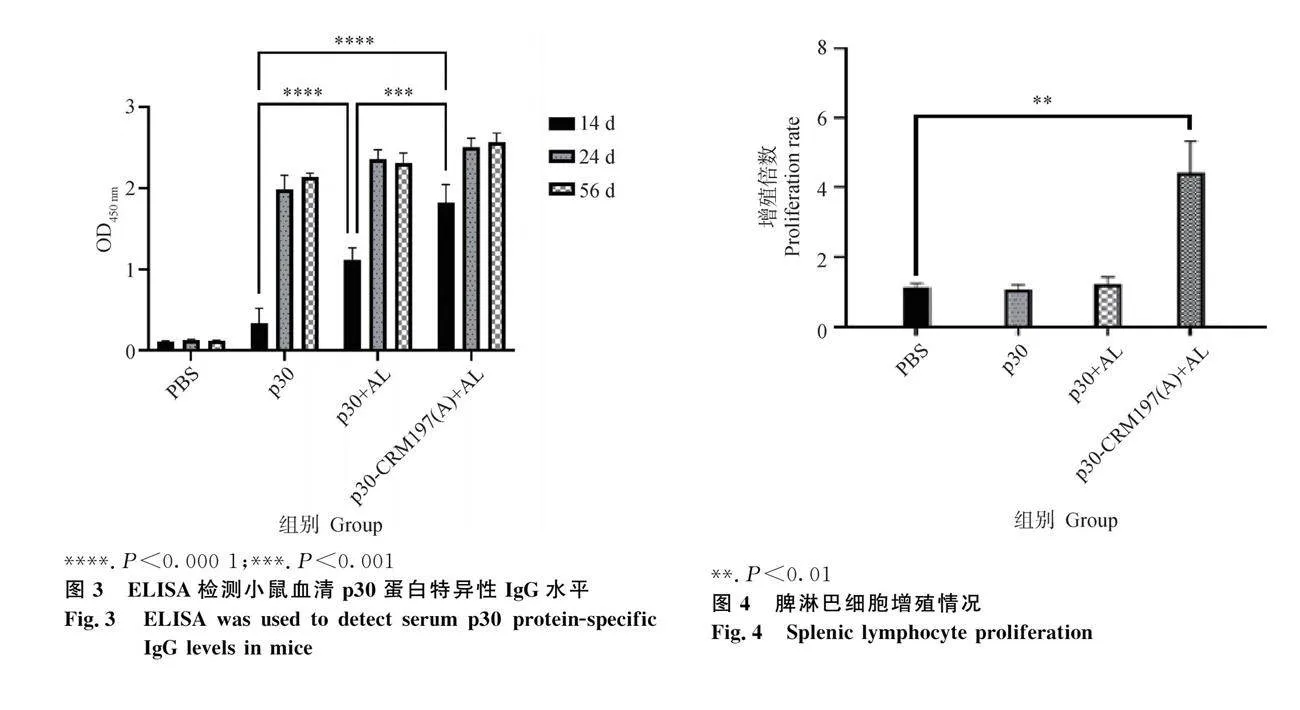
2.3 ELISA測定特異性抗體IgG效價
通過ELISA方法檢測免疫后小鼠血清中p30的特異性抗體IgG的水平,結果(圖3)顯示,在一免之后,p30+AL組和p30-CRM197(A)+AL組均顯著提高了IgG的水平,尤其是p30-CRM197(A)+AL組可以在短時間內激起高水平的IgG。
2.4 脾淋巴細胞增殖
初次免疫后56 d,采集脾,分離脾淋巴細胞,測淋巴細胞的增殖情況,CCK-8結果如圖4所示,p30-CRM197(A)+AL組脾淋巴細胞比較其他組有顯著的特異性增殖,相對于沒有接受抗原刺激的空白對照組比較增殖倍數為4左右。
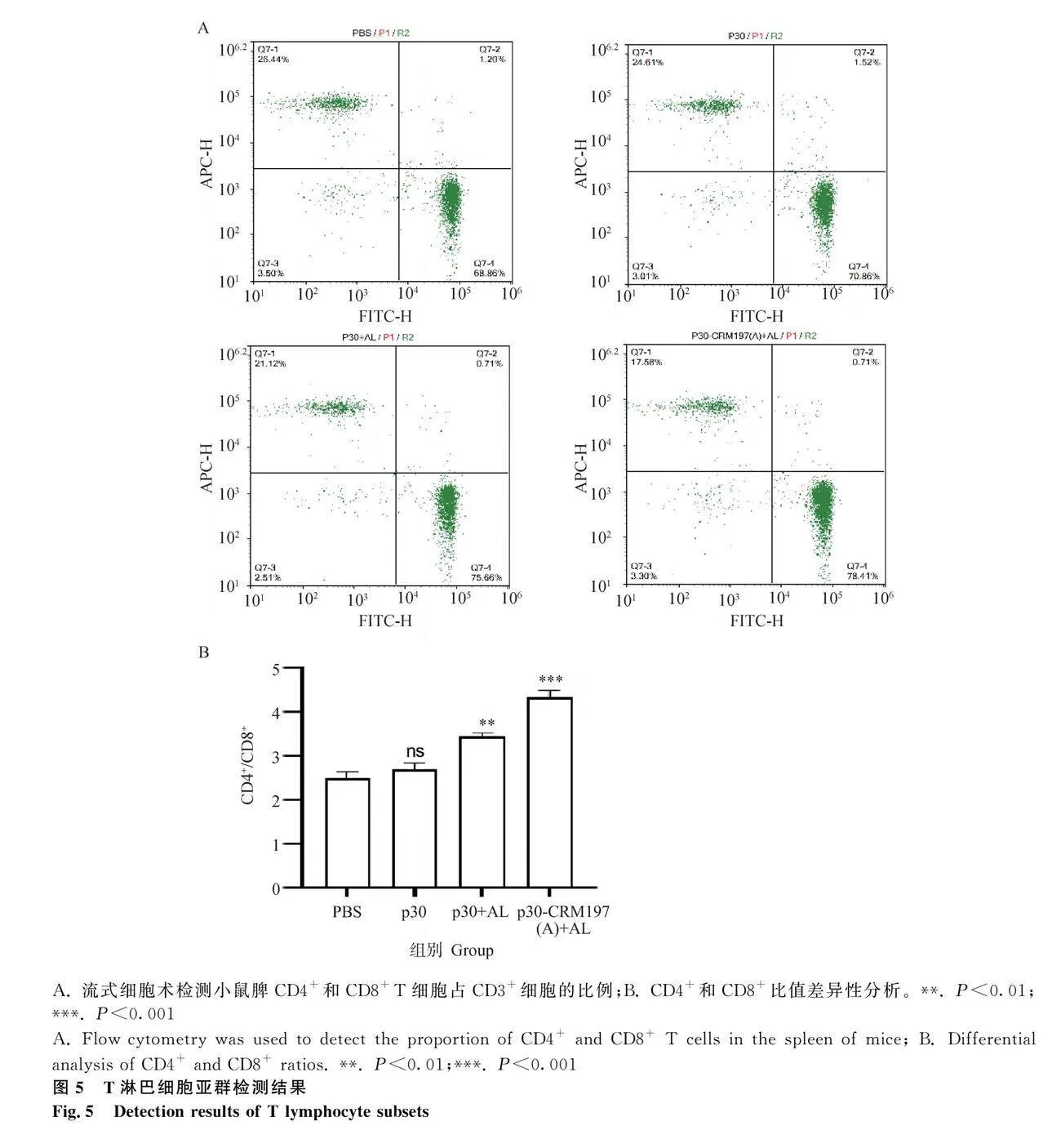
2.5 T細胞亞群分型
初次免疫后56 d,分別取各組小鼠脾淋巴細胞對T淋巴細胞亞群表達情況進行分析,結果如圖5A所示,p30-CRM197(A)+AL組的CD4+T淋巴細胞比例最高,達78.41%,而PBS組CD8+T淋巴細胞比例最高為26.44%。作者還分析了CD4+/CD8+不同組別與PBS組之間的差異性,由圖5B結果所示,p30-CRM197(A)+AL組與PBS組的差異性最為顯著,有顯著的增強。
3 討 論
先前的研究表明,CRM197是一種具有輔助性T細胞表位的載體蛋白,可以激活輔助性T細胞獲取抗原[16]。因此,當CRM197載體蛋白與莢膜多糖結合時,會誘導更強的抗體反應和免疫記憶[17]。然而,通過基因融合將CRM197或其功能域與另一種蛋白質共融合表達的方式來提高免疫原性尚未得到完全評估[18]。A片段作為CRM197的催化結構域,盡管52位的氨基酸突變使其酶活性降低,但仍然保留了與DT特異性受體結合并刺激人體體液和細胞免疫反應的能力[19]。Wang等[18]設計了E2與CRM197催化結構域(A片段)的融合蛋白,并在靈長類動物中評價了其抗原性、免疫原性和疾病預防效果,試驗結果證明CRM197的結構域(A片段)可以單獨作為分子內佐劑。因此,作者評估了CRM197的功能域(即A片段)作為分子內佐劑的潛力。
ASFV的基因組極其復雜,編碼多種與免疫逃逸相關的蛋白質。因此,開發安全有效的非洲豬瘟疫苗仍然是一項具有挑戰性的任務[20-21]。目前,亞單位疫苗具有較高的安全性,但其保護效果不是很理想。因此,有必要開發更多的免疫保護性抗原或組合,或加速抗原的識別和呈遞,迅速產生體液和細胞免疫反應,以產生更強的免疫保護作用[7]。ASFV的p30蛋白可以作為參與病毒內化的必需蛋白,有研究結果顯示,用抗p30抗體預處理可以抑制豬巨噬細胞和Vero細胞95%以上的病毒內化。然而,p30誘導的中和抗體不足以提供有效的免疫保護[22]。
在本研究中,p30-CRM197(A)蛋白在小鼠免疫試驗中相較于單獨的p30蛋白具有更好的免疫原性。ELISA試驗結果表明,p30-CRM197(A)融合蛋白在更短的時間內激起小鼠較高水平的體液免疫反應。評價脾淋巴細胞的增殖能力,能夠有效地評估疫苗的免疫效果[16],本試驗結果顯示,p30-CRM197(A)組與空白對照組有顯著差異性(Plt;0.01),這表明CRM197的A片段作為載體蛋白可以增強小鼠的細胞免疫水平。
T細胞是一個不均一的細胞群體,分類方法有多種,按細胞表面分化抗原(cluster of differentiation,CD)的不同,可分為CD4+和CD8+兩大亞群。CD4+T細胞識別MHC Ⅱ類分子所提呈的外源性抗原肽,活化后主要分化為輔助性T淋巴細胞。CD8+T細胞識別MHC Ⅰ類分子所提呈的內源性抗原肽,活化后主要分化為細胞毒性T淋巴細胞,兩者的比值常用于評價機體免疫系統的狀態[23]。在初次免疫后56 d,作者對小鼠T淋巴細胞亞群進行流式鑒定,發現p30-CRM197(A)組的 CD4 + /CD8 +比值與對照組有顯著的增強。可見CRM197(A)不論是從體液免疫還是細胞免疫水平,均增強了p30的免疫原性,證明CRM197的A片段載體蛋白可以增強亞單位疫苗的免疫效果。
4 結 論
CRM197(A)作為載體蛋白,不論是從體液免疫還是細胞免疫水平,均增強了p30的免疫原性,也進一步證明了CRM197的A片段載體蛋白可以增強亞單位疫苗的免疫效果。然而,需要進一步的研究來評估其在豬上的免疫效力和攻毒保護,還需要篩選更多的ASFV免疫原性蛋白和CRM197的A片段組合,并優化免疫方案。本研究為ASFV亞單位疫苗的佐劑選擇提供了新的參考方向。
參考文獻(References):
[1] ZHOU X T, LI N, LUO Y Z, et al. Emergence of African swine fever in China, 2018[J]. Transbound Emerg Dis, 2018, 65(6):1482-1484.
[2] 石建州, 何 健, 劉陽坤, 等. 非洲豬瘟疫苗研究進展[J]. 中國獸醫學報, 2022, 42(5):1057-1065, 1076.
SHI J Z, HE J, LIU Y K, et al. Progress in development of vaccine against African swine fever[J]. Chinese Journal of Veterinary Medicine, 2022, 42(5):1057-1065, 1076. (in Chinese)
[3] 王西西, 陳 青, 吳映彤, 等. 非洲豬瘟疫苗研究進展[J]. 中國動物傳染病學報, 2018, 26(2):89-94.
WANG X X, CHEN Q, WU Y T, et al. Recent progress on vaccine development against African swine fever[J]. Chinese Journal of Animal Infectious Diseases, 2018, 26(2):89-94. (in Chinese)
[4] SNCHEZ-CORDN P J, MONTOYA M, REIS A L, et al. African swine fever: a re-emerging viral disease threatening the global pig industry[J]. Vet J, 2018, 233:41-48.
[5] ARIAS M, DE LA TORRE A, DIXON L, et al. Approaches and perspectives for development of African swine fever virus vaccines[J]. Vaccines (Basel), 2017, 5(4):35.
[6] RAMIREZ-MEDINA E, VUONO E, O’DONNELL V, et al. Differential effect of the deletion of African swine fever virus virulence-associated genes in the induction of attenuation of the highly virulent Georgia strain[J]. Viruses, 2019, 11(7):599.
[7] TEKLUE T, SUN Y, ABID M, et al. Current status and evolving approaches to African swine fever vaccine development[J]. Transbound Emerg Dis, 2020, 67(2):529-542.
[8] GMEZ-PUERTAS P, RODRGUEZ F, OVIEDO J M, et al. The African swine fever virus proteins p54 and p30 are involved in two distinct steps of virus attachment and both contribute to the antibody-mediated protective immune response[J]. Virology, 1998, 243(2):461-471.
[9] BARDERAS M G, RODRGUEZ F, GMEZ-PUERTAS P, et al. Antigenic and immunogenic properties of a chimera of two immunodominant African swine fever virus proteins[J]. Arch Virol, 2001, 146(9):1681-1691.
[10] BRKER M, COSTANTINO P, DETORA L, et al. Biochemical and biological characteristics of cross-reacting material 197 (CRM197), a non-toxic mutant of diphtheria toxin:use as a conjugation protein in vaccines and other potential clinical applications[J]. Biologicals, 2011, 39(4):195-204.
[11] MALITO E, BURSULAYA B, CHEN C, et al. Structural basis for lack of toxicity of the diphtheria toxin mutant CRM197[J]. Proc Natl Acad Sci U S A, 2012, 109(14):5229-5234.
[12] 陳 柯. 白喉毒素突變體CRM197的研究及應用[J]. 微生物學免疫學進展, 2022, 50(3):70-76.
CHEN K. Research and application of diphtheria toxin mutant CRM197[J]. Progress in Microbiology and Immunology, 2022, 50(3):70-76. (in Chinese)
[13] GRUBER W C, SCOTT D A, EMINI E A. Development and clinical evaluation of Prevnar 13, a 13-valent pneumocococcal CRM197 conjugate vaccine[J]. Ann N Y Acad Sci, 2012, 1263:15-26.
[14] DAGAN R, POOLMAN J, SIEGRIST C A. Glycoconjugate vaccines and immune interference:a review[J]. Vaccine, 2010, 28(34):5513-5523.
[15] TOBIAS J, JASINSKA J, BAIER K, et al. Enhanced and long term immunogenicity of a Her-2/neu multi-epitope vaccine conjugated to the carrier CRM197 in conjunction with the adjuvant Montanide[J]. BMC Cancer, 2017, 17(1):118.
[16] TANG X Z, YU W L, SHEN L J, et al. Conjugation with 8-arm PEG and CRM197 enhances the immunogenicity of SARS-CoV-2 ORF8 protein[J]. Int Immunopharmacol, 2022, 109:108922.
[17] GUTTORMSEN H K, SHARPE A H, CHANDRAKER A K, et al. Cognate stimulatory B-cell-T-cell interactions are critical for T-cell help recruited by glycoconjugate vaccines[J]. Infect Immun, 1999, 67(12):6375-6384.
[18] WANG K H, ZHOU L Z, ZHANG X, et al. Hepatitis E vaccine candidate harboring a non-particulate immunogen of E2 fused with CRM197 fragment A[J]. Antiviral Res, 2019, 164:154-161.
[19] LIU L Q, CHEN T T, ZHOU L Z, et al. A bacterially expressed SARS-CoV-2 receptor binding domain fused with cross-reacting material 197 a-domain elicits high level of neutralizing antibodies in mice[J]. Front Microbiol, 2022, 13:854630.
[20] 趙旭陽, 靳家鑫, 路聞龍, 等. 非洲豬瘟病毒免疫逃逸分子機制研究進展[J]. 畜牧獸醫學報, 2022, 53(7): 2074-2082.
ZHAO X Y, JIN J X, LU W L, et al. Advances in the molecular mechanism of immune escape of African swine fever virus[J]. Acta Veterinaria et Zootechnica Sinica, 2022, 53(7): 2074-2082.(in Chinese)
[21] 黃 劍, 李國新, 童光志. 非洲豬瘟的流行病學及疫苗研究新進展[J]. 中國動物傳染病學報, 2022, 30(4):197-205.
HUANG J, LI G X, TONG G Z. Epidemiology of African swine fever and progress in vaccine research[J]. Chinese Journal of Animal Infectious Diseases, 2022, 30(4):197-205. (in Chinese)
[22] GMEZ-PUERTAS P, RODRGUEZ F, OVIEDO J M, et al. Neutralizing antibodies to different proteins of African swine fever virus inhibit both virus attachment and internalization[J]. J Virol, 1996, 70(8):5689-5694.
[23] 徐婭玲. ASFV亞單位疫苗和多肽疫苗免疫效力的評估[D]. 貴陽:貴州大學, 2022.
XU Y L. Assessment of the immune efficacy of ASFV subunit vaccines and peptide vaccines[D]. Guiyang: Guizhou University, 2022. (in Chinese)
(編輯 白永平)

