穩定導電網絡結構的C-SnO2/MWCNTs復合材料用于鋰漿料電池
關鍵詞:漿料電池;納米尺寸SnO2;碳納米管;碳包覆
1 引言
氧化還原液流電池(RFBs)由于具有高度的可擴展性和高安全性,被認為是最有前景的大規模儲能器件之一1–7。與鋰離子電池(LIBs)相比,它們具有結構設計靈活和輸出功率可調等顯著優勢8–12。然而,傳統的RFBs由于較低的能量密度和使用昂貴的離子交換膜,其商業化受到限制13–15。最近,基于鋰基的漿料電池(LSSFBs)被開發出來以解決上述問題。LSSFBs能夠通過使用非水系漿料電極拓寬電壓窗口并提高活性材料含量,從而顯著提高器件的能量密度16,17。因此,LSSFBs有望成為RFBs的備選18–20。
近年來,鋰基漿料電池(LSSFBs)的發展主要集中在電極活性材料、導電添加劑以及漿料電極流變學特性的優化。其中,電極活性材料的選擇和設計對提高LSSFBs的電化學性能至關重要21,22。漿料電池所使用的負極材料通常與LIBs類似,例如VO2 23、石墨24,25、Li4Ti5O12 26–28和Nb2O5 29。然而,VO2存在毒性和高成本的問題。石墨、Li4Ti5O12和Nb2O5則受限于有限的理論容量、較高鋰插層電位和較低能量密度問題30–33。作為一種金屬氧化物,SnO2由于其高理論容量(1494 mAh?g?1)、相對較低的鋰離子插層/脫出電位(約0.6 V vs. Li+/Li)和儲量豐富,已被用作負極材料并被廣泛研究并34,35。然而,SnO2在合金化反應過程中的高絕緣性和嚴重體積膨脹(約305%)常造成電子傳輸中斷、顆粒粉碎和難以控制的固體電解質界面(SEI)形成,從而導致其倍率性能差和容量衰減嚴重36,37。為了解決這些問題,可以采用減小材料尺寸和碳包覆等策略38–40。與塊狀SnO2相比,SnO2納米顆粒(NPs)具有更高的表面積和更多的反應活性位點,可以提高Li2O與SnO2之間轉化反應的可逆性,縮短離子傳輸距離以加速合金化-去合金化反應41。此外,當Li+插入SnO2 NPs時,由于材料經過預先碳包覆,SnO2 NPs的體積膨脹得到有效限制。然而,與傳統固態電極不同的是,漿料電極中的SnO2和導電添加劑相對獨立,它們之間的弱物理接觸容易在流動過程中受剪切力而斷開42,43。因此,活性材料與導電添加劑有必要有效地結合在一起44。在各種導電添加劑中,多壁碳納米管(MWCNTs)具有較大的長徑比和高導電性45。如果SnO2 NPs能夠生長在MWCNTs表面并進行碳包覆,將形成穩定的導電網絡,從而提高SnO2基漿料負極的電子導電性和結構穩定性。
受此啟發, 碳包覆的SnO2/MWCNTs (CSnO2/MWCNTs)復合材料被制備出來用作LSSFBs的負極材料。在這種復合材料中,高導電性的MWCNTs和碳包覆層構建了一個三維導電網絡,促進電子傳輸。同時碳包覆層還提供保護作用,抑制了SnO2的體積膨脹,顯著增強了材料結構穩定性。與此同時,SnO2 NPs的高比表面積賦予CSnO2/MWCNTs更多的活性位點和更快的Li+擴散動力學。因此,LSSFBs在容量、倍率和循環性能等方面得到了顯著提高。
2 實驗部分
2.1 C-SnO2/MWCNTs復合材料的合成
酸化多壁碳納米管(MWCNTs)的制備參考之前的文獻報道46。將500 mg酸化MWCNTs、x mmolSnCl4 (其中x為0.5、1、2、3)和700 mL去離子水加入高壓釜中,在150 °C的烘箱中恒溫3 h。經過離心并在60 °C干燥后,得到SnO2/MWCNTs前軀體。隨后,將1 g SnO2/MWCNTs前軀體和600 mL葡萄糖溶液(0.2 mol?L?1)加入到高壓釜中,在180 °C的烘箱中恒溫4 h。經過離心并在60 °C干燥后,將產物在Ar 氣氛下500 °C 退火4 h , 得到CSnO2/MWCNTs。SnO2/MWCNTs的制備方法與上述類似,但沒有加入葡萄糖。塊狀SnO2的制備方法與上述類似,但沒有加入酸化MWCNTs和葡萄糖。
2.2 扣式電池組裝
將C-SnO2/MWCNTs和SnO2/MWCNTs漿料分別與聚偏氟乙烯(PVDF)按照9 : 1的質量比例混合,并使用N-甲基-2-吡咯烷酮(NMP)進行溶解。塊狀SnO2漿料是將SnO2、MWCNTs和PVDF按照8 :1 : 1的質量比例混合,并使用NMP溶解。然后將這些漿料涂覆在銅箔上,經過60 °C干燥后,得到CSnO2/MWCNTs、SnO2/MWCNTs和純SnO2電極。采用傳統方法組裝CR2032型扣式電池,使用玻璃纖維和鋰箔分別作為隔膜和負極。扣式電池的電解液為溶于碳酸乙烯酯(EC)和碳酸二甲酯(DMC)(質量比3 : 7)的二(三氟甲基磺酰)亞胺鋰(LiTFSI)(1 mol?L?1)。
2.3 漿料電池組裝
所有漿料電極均在溶于EC/DMC的1 mol?L?1LiTFSI電解液中制備。將C-SnO2/MWCNTs (8%)、Triton X-100 (2%)和電解液(90%)按質量分數混合,通過高速攪拌器(IKA-T18)混合均勻。在組裝過程中,流道中的C-SnO2/MWCNTs漿料電極作為正極,鋰箔作為負極,Celgard作為隔膜。流道放置在空心硅膠墊內( 見圖S1 , SupportingInformation)。兩個銅板作為集流體。最后,兩端固定不銹鋼板。所有組裝過程均在充滿Ar氣體的手套箱中進行。
2.4 電化學測試和表征
使用電化學工作站(CHI 660E,CH Instrument)測試循環伏安法(CV)曲線。使用電池測試系統(LAND CT3001A,LANHE)測試恒流充放電(GCD)曲線和倍率性能,電壓范圍為0.01–2.5 V。使用電化學工作站(IM6ex,Zahner,德國)測試電化學阻抗譜(EIS),測量范圍為100 kHz到100 mHz。使用場發射掃描電子顯微鏡(SEM) (JJSM7500F ,JSM7900F,JEOL,日本)以及配備能量色散譜(EDS)的透射電子顯微鏡(TEM) (Talos F200X G2,FEI,美國)表征材料的形貌和微觀結構。使用Cu Kα射線源的Mini-Flex600 (Riguka,日本)和PHI 1600ESCA (PerkinElmer,美國)采集X射線衍射(XRD)圖譜和X射線光電子能譜(XPS)圖譜。使用STA 449F3 Jupiter分析儀(Netzsch,德國)進行熱重分析(TGA)。使用ASAP 2460 3.01 (Micromeritics,美國)測量比表面積(BET)。使用粘度儀MCR302 (AntonPaar,奧地利)測試漿料電極粘度。
3 結果與討論
3.1 復合材料的合成和表征
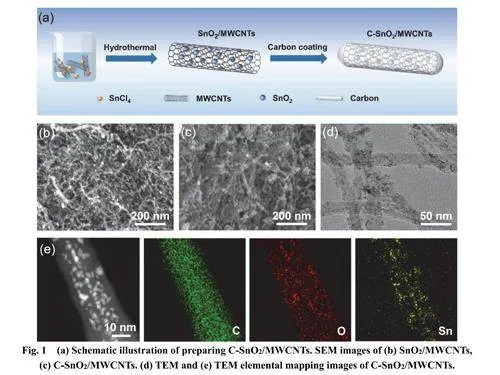
結合水熱和退火方法制備C-SnO2/MWCNTs(圖1a)。在水熱過程中,Sn4+附著在MWCNTs表面,并進一步被氧化成SnO2 納米顆粒, 標記為SnO2/MWCNTs 47。引入葡萄糖作為碳源后,通過水熱和退火方法得到C-SnO2/MWCNTs納米復合材料40。不同SnO2含量的C-SnO2/MWCNTs(標記為C-SnO2/MWCNTs-n;n表示SnO2的質量含量)通過TGA和XRD進行表征(圖S2、S3)。如XRD譜圖所示,復合材料中SnO2納米顆粒的衍射峰與SnO2的四方晶體結構能夠很好匹配48 。其中, CSnO2/MWCNTs-65%種的MWCNTs在碳包覆前后均能良好分散(圖1b,c)。同時,MWCNTs表面被碳層包覆的SnO2顆粒大小為3–5 nm (圖1d),遠小于SnO2塊體的尺寸(圖S4)。納米尺寸賦予SnO2電極高達208.1 m2?g?1的比表面積(圖S5) 49,50。EDS進一步表明,SnO2顆粒在MWCNTs上均勻分布(圖1e)。然而,當SnO2納米顆粒的質量含量超過75%時,部分SnO2顆粒無法附著在MWCNTs表面,甚至會發生團聚(圖S6)。此外,由于SnO2的差的導電性,CSnO2/MWCNTs的電化學性能也受到SnO2納米顆粒含量的影響51。如圖S7a所示,電池的電荷傳輸電阻和Warburg阻抗隨著SnO2含量的增加而增大。同時,電池也表現出較差的倍率性能和循環穩定性。當SnO2納米顆粒含量從55%增加到85%時,電池在2 A?g?1時放電容量從799.1降至449.3 mAh?g?1(圖S7b)。同時,在0.5 A?g?1下經過100次循環后,其容量保持率也從63.96%降至26.77% (圖S7c)。考慮到更優的電化學性能和適當的負載量,選擇CSnO2/MWCNTs-65%用于后續討論。因此,以下討論中的C-SnO2/MWCNTs 均代表C-SnO2/MWCNTs-65%。
3.2 扣式電池的電化學性能
為了進一步了解電池在充放電過程中的電化學反應過程,本工作使用循環伏安法對電極材料進行了測試52。C-SnO2/MWCNTs的循環伏安曲線展示出明顯典型的氧化還原峰(圖2a),這些峰值對應SnO2在嵌鋰/脫鋰過程中的轉化和合金化反應38。同時,恒流充放電曲線也展示出兩個充電/放電平臺, 與CV 結果一致( 圖2b) 。此外, 基于CSnO2/MWCNTs的電池表現出較小的電荷傳輸電阻(圖2c)。這是因為碳包覆層和MWCNTs形成高導電網絡,增加電子傳輸路徑并加速電子傳輸。較小的電荷傳輸電阻有助于提高電池的倍率性能(圖2d)。即使在2 A?g?1的電流密度下,電池仍保持727mAh?g?1的比容量。電池出色的倍率性能是由于CSnO2/MWCNTs具有快速的反應動力學,不同掃描速率下的循環伏安曲線可以表現動力學的快慢(圖2e)。掃描速率(v)與峰電流(i)之間的關系可以通過如下公式得到52:
其中,a和b是可調參數。b值可以反映Li+的存儲機制。當b值接近0.5時,氧化還原過程主要由離子擴散控制。當b值接近1.0時,電容行為將控制電化學過程。需要注意的是,峰1、2、3和4的b值分別為0.685、0.774、0.893和0.780 (圖2f)。此外,CSnO2/MWCNTs還表現出穩定的循環性能(圖2g)。在0.5 A?g?1的電流密度下,C-SnO2/MWCNTs可以在100次循環后保持725 mAh?g?1的放電容量。這歸因于碳包覆層和MWCNTs形成了穩定的電子傳輸網絡,在充放電循環中可以抑制體積膨脹并提高導電性(圖S8)。
3.3 漿料電極的物理性質
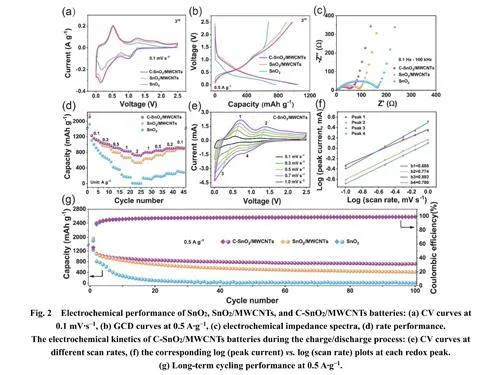
漿料電極的懸浮穩定性、導電性以及流變特性將決定LSSFBs的電化學性能53。通過對不同質量分數的C-SnO2/MWCNTs漿料長期靜置,可以反映出其懸浮穩定性(圖3a,b)。經過15天靜置后,含有7.0%和7.5% C-SnO2/MWCNTs的漿料出現固液分離現象。相比之下,含有8.0%、8.5%和9.0% CSnO2/MWCNTs的漿料保持長期穩定,其中交聯的MWCNTs網絡為漿料提供穩定的機械支撐29。同時,交聯的MWCNTs和碳包覆層在漿料中也形成了導電網絡,隨著C-SnO2/MWCNTs含量的增加,漿料電極的電荷傳輸電阻逐漸降低,其導電性逐漸增加(圖3c)。然而,當添加量超過8.0%時,漿料電極的導電性增加趨勢放緩。這表明漿料在添加量約8.0%處達到了逾滲閾值,漿料電極中形成了良好的支撐網絡和導電網絡。因此,漿料電極的穩定性和導電性同時得到改善54。然而,由于一維MWCNTs的高長徑比,在漿料制備過程中過多的MWCNTs會相互交織,進一步增加活性材料的遷移阻力并導致高粘度( 圖3d,e) 19 。當CSnO2/MWCNTs的含量超過8.0%時,漿料電極的粘度、剪切應力和導電性急劇增加(圖3f和圖S9)。高粘度會阻礙漿料在通道中的流動,并在泵送過程中消耗更多能量55。綜合以上結果,本工作選擇含有8.0% C-SnO2/MWCNTs的漿料作為LSSFBs的漿料電極。
3.4 漿料電池的機理
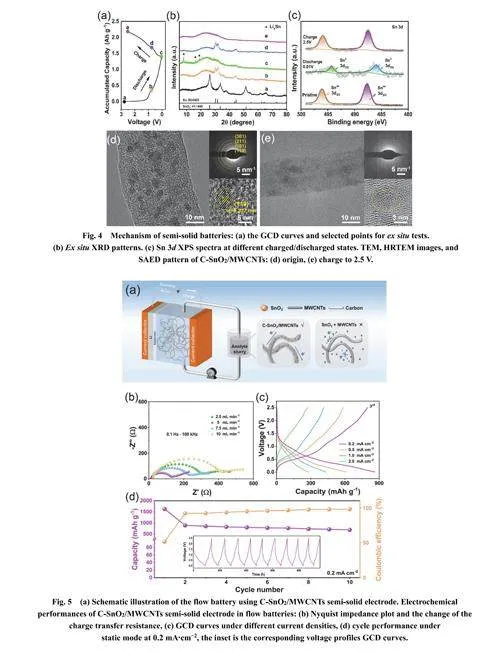
為了深入了解漿料電極的充放電過程,本工作基于8.0% C-SnO2/MWCNTs漿料電極組裝了靜態電池,并通過非原位XRD和XPS對電池首圈不同充放電狀態進行了研究(圖4a–c)。在放電電壓約為0.85 V時,26.45°、33.64°和51.48°三個SnO2的特征XRD峰消失,同時在30.38°、31.96°、43.71°和43.82°發現Sn相峰的生成,表明SnO2被還原為Sn金屬56,57。進一步放電至0.01 V后,所有Sn金屬的峰趨向消失,28.01°、16.12°和19.04°出現LixSn合金相的峰56,57。此外, Sn的價態變化也可通過XPS譜圖體現出來。在Sn 3d XPS圖中,Sn4+ 3d5/2和Sn4+3d3/2的峰位分別位于487.5和496.1 eV (圖4c)。在放電過程中,這些峰向較低結合能方向移動,對應于Sn4+向Sn0的還原。這歸因于放電至0.01 V時,Li+插入SnO2中,隨后從SnO2到Sn金屬再到LixSn的相轉變過程(圖S10) 58,59。進一步充電至2.5 V后,Sn3d峰幾乎恢復到初始狀態,表明Sn已可逆地氧化為SnO2 60,61。這說明Sn4+和Sn0之間的轉化的高度可逆性。此外,充電至2.5 V后,SnO2納米顆粒的尺寸和分布幾乎未改變(圖4d,e)。然而,與初始SnO2不同,充電后的SnO2晶格在高分辨透射電子顯微鏡(HRTEM)圖像中消失(圖4e,子圖),這與充電至2.5 V時SnO2的特征XRD峰消失結果一致(圖4b)。此外,充電后的SnO2的選區電子衍射(SAED)圖案顯示出寬廣的漫反射環(圖4e,子圖),表明充電產物為無定形態56,57。另外,在漿料電極首圈循環中,C-SnO2/MWCNTs的形貌的幾乎未發生變化(圖S11)。表明在Li+嵌入/脫出過程中,SnO2的相轉變不會破壞其結構。
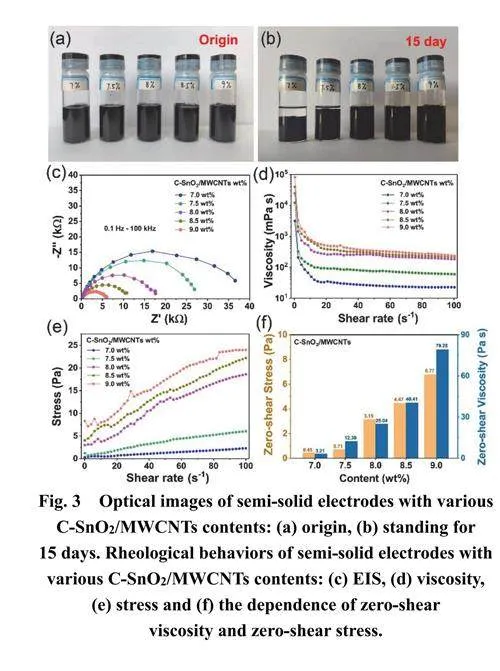
3.5 漿料電池的電化學性能
為了展示C-SnO2/MWCNTs 漿料電極在LSSFBs中的實用性,本工作基于8.0% C-SnO2/MWCNTs漿料電極組裝了流動漿料電池(圖5a)。漿料通過蠕動泵在外部容器和電池內循環,漿料流速可通過蠕動泵控制。隨著流速的增加,漿料電極的電荷傳輸電阻先減少后增加(圖5b)。當漿料的流速低于2.5 mL?min?1時,漿料中的活性材料將因摩擦力附著在通道壁上,這降低了漿料電極中CSnO2/MWCNTs的實際含量,抑制了穩定導電網絡的形成45。當流速超過7.5 mL?min?1時,流速過快將破壞導電網絡的結構完整性,從而導致漿料電極的導電性下降45。當流速為5 mL?min?1時,導電網絡可以達到動態平衡,漿料電極展示出較小的電荷傳輸電阻(圖5b)。因此,后續在5 mL?min?1的流速下對漿料電池的電化學性能進行測試。在0.2mA?cm?2的電流密度下,漿料電池展示出了855.5mAh?g?1的放電容量和256.7 Wh?kg?1的能量密度(圖5c和圖S12)。當電流密度增加至2 mA?cm?2時,電池仍然顯示出275.7 mAh?g?1的放電容量和82.7Wh?kg?1的能量密度,其中容量的下降可歸因于極化電壓的增加(圖S13)。漿料中穩定的導電網絡提高了活性材料的動力學,從而減少了Li+的傳輸路徑并提高了漿料電極的導電性62–64。此外,漿料電池具有良好的循環性能,在0.2 mA?cm?2的條件下循環962 h后仍能保持其初始容量的42.4% (690.8mAh?g?1) (圖5d)。即使電流密度從0.2 mA?cm?2增加到1 mA?cm?2,經過10圈循環后電池放電容量仍保持在250.1 mAh?g?1 (圖S14)。此外,本工作使用C-SnO2/MWCNTs漿料電池點亮了一個1.5 V的LED,證明基于C-SnO2/MWCNTs的LSSFBs實際應用的可行性,如圖S15所示,LED能夠正常工作,表明基于C-SnO2/MWCNTs的LSSFBs具有廣闊的實際應用前景。
4 結論
綜上,本工作開發了C-SnO2/MWCNTs復合材料并將其用作鋰基漿料電池的負極材料。在這種復合材料中,SnO2均勻分布在MWCNTs和碳包覆層的導電網絡中。導電網絡不僅提高了SnO2的電子轉移動力學,還抑制了其體積膨脹,保持了漿料電極的穩定性。因此,C-SnO2/MWCNTs在0.5 A?g?1下經過100次循環后能提供725 mAh?g?1的容量。基于C-SnO2/MWCNTs的LSSFBs在0.2 mA?cm?2的條件下循環962 h后,展示出690.8 mAh?g?1的容量。這項工作提供了一種設計高導電性和長循環穩定性漿料電極的方法。

