稀硝酸與銅反應的改進
楊勇
(南京市寧海中學江蘇南京210024)
稀硝酸與銅反應的改進
楊勇
(南京市寧海中學江蘇南京210024)
摘要:稀硝酸與銅的反應說明了稀硝酸的強氧化性,常規實驗存在觀察不清,尾氣處理不到位的問題,利用U形管可以解決上述問題,同時讓學生體會到工業制硝酸的過程。
關鍵詞:稀硝酸;U形管
稀硝酸與銅反應是說明稀硝酸具有強氧化性的重要實驗。常規實驗是在試管中加入稀硝酸和銅片,微熱后觀察現象,說明硝酸具有強氧化性,并產生了無色的NO。但實際這個實驗不能讓人信服產生的到底是NO還是NO2,同時沒有對尾氣進行處理,會帶來污染和對實驗者的傷害。實際上可以用簡單實驗裝置實現實驗目的,避免污染,培養學生綠色化學的理念以及提高學生思維能力。
一、實驗目的
1.了解稀硝酸的強氧化性;
2.練習U形管,培養創新精神;
3.學習有害尾氣處理方案,培養環保意識,提高學生思維能力。
二、反應原理
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
2NO+O2=2NO2
3NO2+H2O=2HNO3+NO
三、儀器藥品
3.5mol/L HNO3溶液、螺旋形銅絲、橡皮塞、U形管、酒精燈、火柴
四、實驗裝置
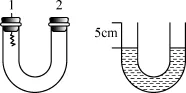
五、實驗步驟
1.配好3.5mol/L HNO3溶液。
2.將螺旋形銅絲如實驗裝置圖所示插入橡皮塞1上,使螺旋形銅絲露出約2cm左右。
3.打開U形管上橡皮塞1和2,注入稀硝酸約使U形管上空部分長度約為5cm(上圖)。
4.塞上橡皮塞1和2,平放U形管將橡皮塞1側內空氣排盡,打開橡皮塞2。
5.試管夾夾住U形管無橡皮塞一側,微熱,引發銅絲和稀硝酸反應后停止加熱,當銅絲和稀硝酸脫離后反應自動停止,觀察橡皮塞1下方產生的氣體顏色。
6.冷卻后,塞上橡皮塞2,將橡皮塞1側的氣體排入橡皮塞2側與空氣混合,觀察氣體顏色的變化,然后小心打開橡皮塞1,觀察無橡皮塞側的液面變化。
六、實驗總結
本實驗所用儀器藥品量少,簡單易準備。并且經過改進后,可以清楚觀察到稀硝酸與銅反應生成無色的NO,同時可以實現在封閉的環境中對NO有毒氣體的尾氣處理,學生在實驗過程中可以看到無色氣體變為紅棕色(2NO+O2=2NO2),然后褪色的過程(4NO2+O2+2H2O= 4HNO3),能培養學生的環保意識和化學經濟意識,這樣做既節省原料,又不會污染環境,該過程正是工業制取硝酸的原理。
文章編號:1008-0546(2010)11-0076-01中圖分類號:G633.8
文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2010.11.042

