槲皮素和8-Br-cAMP對腫瘤增變基因表型改變的影響
李 璇
腫瘤的增變基因表型(mutator phenotype)學(xué)說主要是指由于調(diào)控DNA穩(wěn)定/修復(fù)基因的突變(mutator增變子)而引起監(jiān)督DNA損傷的抑癌基因,如p53、p16等基因的失活/突變而導(dǎo)致腫瘤細胞對多藥耐藥性(MDR)增加和抗凋亡等腫瘤惡性的表型。
在失去生長、增殖調(diào)控的腫瘤細胞內(nèi)PKC信號轉(zhuǎn)導(dǎo)途徑呈激活狀態(tài),而在PKA信號轉(zhuǎn)導(dǎo)途徑中PKAⅡ型受體處于失激活狀態(tài)。槲皮素(類黃酮)具有阻抑PKC/TPK信號轉(zhuǎn)導(dǎo)途徑的作用。8-Br-cAMP是PKARⅡ的激動劑。本文主要探討了槲皮素和8-Br-cAMP單獨作用或聯(lián)合應(yīng)用是否可呈現(xiàn)不同信號轉(zhuǎn)導(dǎo)途徑的互補效應(yīng)和對增變基因表型變動的影響。
1 材料與方法
1.1 材料 Bcl-2單克隆抗體(Santa Cruz)、Bax、XRCC1單克隆抗體(Lab Vision),TUNEL凋亡試劑(Promega),8-BrcAMP(Sigma),槲皮素(上海試劑二廠);POLB單克隆抗體(Lab Vision),MRP單克隆抗體(Zymed)。
1.2 細胞培養(yǎng)及分組 將培養(yǎng)的Eca-109細胞隨機分為4組:①8-Br-cAMP(Br)組,加終濃度為2×10-5mol/L的8-BrcAMP;②槲皮素(Q)組,加槲皮素終濃度為43 μmol/L;③8-Br-cAMP和槲皮素共同作用(Br+Q)組,加終濃度為2×10-5/L的8-Br-cAMP和槲皮素終濃度為43 μmol/L;④對照組(C),僅加DMEM培養(yǎng)液(含10%胎牛血清)。各組細胞均培養(yǎng)48 h后收集細胞,制成1×107/ml細胞懸液滴加至預(yù)先處理過的玻片和硝酸纖維素膜(NCM)上。
1.3 細胞凋亡率檢測 應(yīng)用TUNEL法檢測各組細胞的凋亡率。
1.4 蛋白免疫反應(yīng)性的檢測 應(yīng)用免疫細胞化學(xué)技術(shù)分別對滴片進行MRP、POLB、Bcl-2、Bax和XRCC1免疫反應(yīng)性(IR)的強弱和定位觀察。應(yīng)用免疫斑點印跡技術(shù)檢測NCM膜上的POLB、MRP、Bcl-2、Bax和XRCC1的印跡并應(yīng)用薄層層析掃描儀(Shimadu)以470 nm波長進行掃描。計總積分值。
1.5 統(tǒng)計學(xué)處理 采用SPSS10.0軟件,計量資料用單因素方差分析,結(jié)果判定以α=0.05為水準(zhǔn)。
2 結(jié) 果
2.1 各組細胞凋亡率 C組為4%,Br組為42%,Q組為35%,(Br+Q)組為70%,見圖1~4。(Br+Q)組>Br組或Q組>C組,P<0.01。
2.2 Bcl-IR、Bax-IR和XRCC1-IR Bcl-IR和Bax-IR呈棕黃色顆粒,位于胞質(zhì)內(nèi);XRCC1-IR呈棕黃色顆粒,多位于胞核,也可見到有些細胞的整個細胞呈陽性反應(yīng)。四個實驗組的免疫組化信號強弱積分值見表1。
2.3 各組Eca-109細胞的Bcl-2-IR、Bax-IR和XRCC1-IR的相關(guān)性 Bcl-2-IR與Bax-IR呈顯著負相關(guān),r=-0.984 9,P<0.01;Bcl-2-IR與XRCC1-IR呈顯著正相關(guān),r=0.992 6,P<0.01;Bax-IR與 XRCC1-IR呈顯著負相關(guān),r=-0.996 2,P<0.01。
圖1 Br組Eca-109細胞凋亡增加 TUNEL,×1000

圖2 Q組Eca-109細胞凋亡增加 TUNEL,×1000
圖3 (Br+Q)組Eca-109細胞凋亡顯著增加 TUNEL,×1000
圖4 C組Eca-109細胞凋亡很少見 TUNEL,×1000
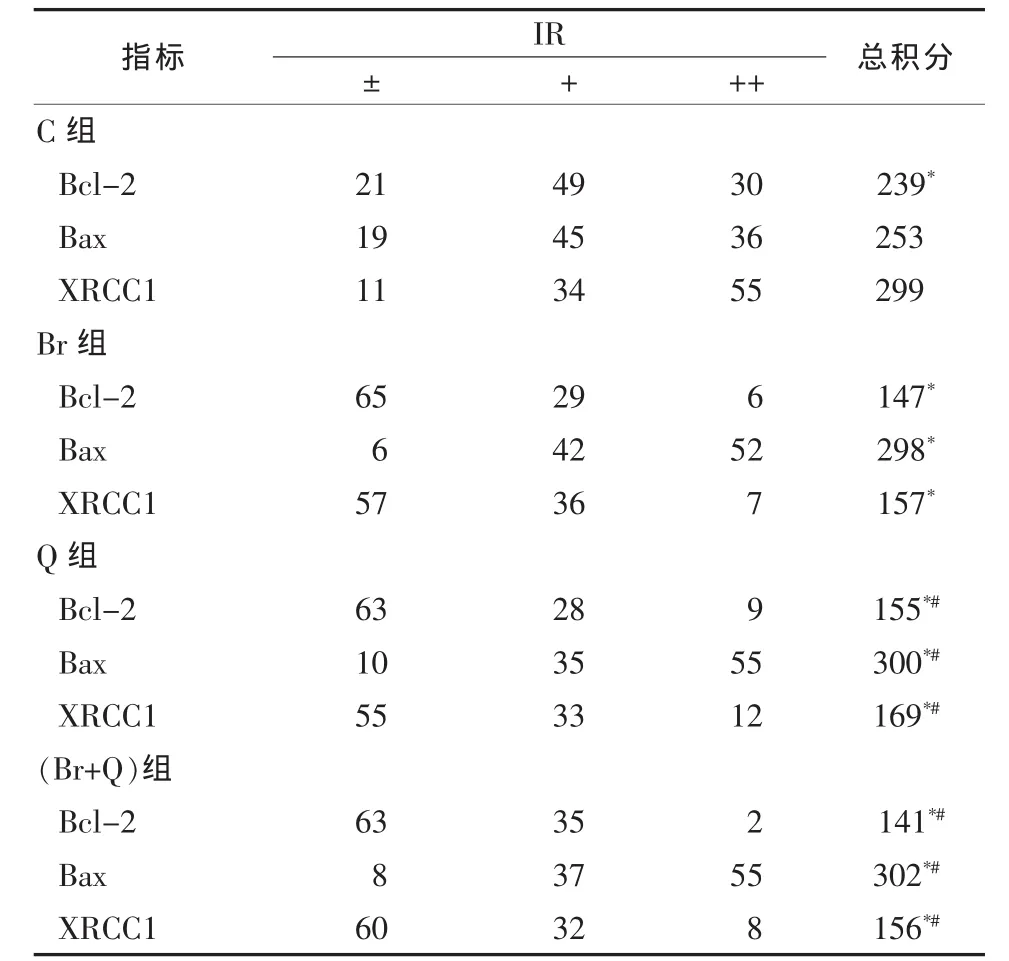
表1 各組細胞Bcl-2、Bax、XRCC1-IR積分
2.4 各組免疫斑點印跡薄層色譜掃描數(shù)值 見表2。
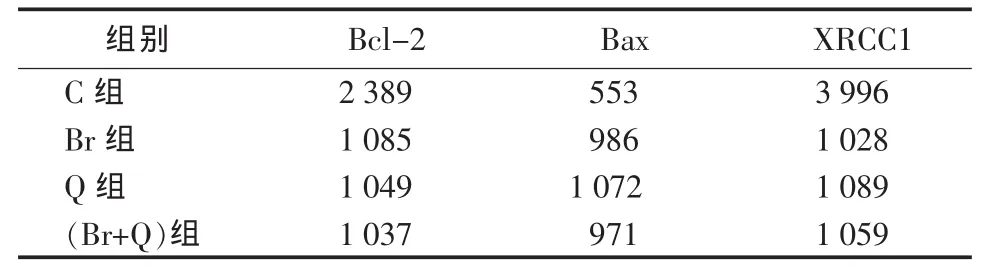
表2 各組免疫斑點印跡掃描數(shù)值
2.5 各組Eca-109細胞的POLB-IR、MRP-IR表達及積分POLB-IR呈棕黃色顆粒,多位于胞核,也可見到有些細胞的整個細胞呈陽性反應(yīng)。MRP-IR呈棕黃色顆粒主要位于細胞質(zhì)。四個實驗組的免疫組化信號強弱的積分值見表3;MRP與POLB呈顯著正相關(guān),r=0.983 8,P<0.01。

表3 各組細胞POLB、MRP-IR積分值
2.6 各組免疫斑點印跡薄層色譜掃描數(shù)值 POLB C組免疫斑點印跡薄層色譜掃描數(shù)值為109,Br組為72,Q組為25,(Br+Q)組為34;MRP C組免疫斑點印跡薄層色譜掃描數(shù)值為111,Br組為37,Q組為30,(Br+Q)組為54。
3 討 論
Bcl-2位于線粒體膜內(nèi)層,可防止線粒體膜的非特異性滲透而提高ADP/ATP的交換[1]。前凋亡(pro-apoptotic)的Bax蛋白是Bcl-2家族成員之一,通過同源或異源二聚體調(diào)控線粒體功能和調(diào)控細胞凋亡。Bax·Bcl-2異二聚體抑制細胞凋亡,而Bax·Bax同源二聚體則促進細胞凋亡[2-5]。有報道Bcl-2/Bax的比例可預(yù)示急性髓性白血病(AML)預(yù)后的結(jié)果[2]。本實驗觀察到Eca-109對照組細胞Bcl-2-IR/Bax-IR的比值高約為4.3,在應(yīng)用Br、Q或(Br+Q)處理后其比值下降分別為1.1、1.0和1.1,表明Bcl-2-IR/Bax-IR比值下降的改變可導(dǎo)致細胞凋亡。XRCC1是DNA修復(fù)蛋白,是DNA polβ聚合酶的異二聚體蛋白,對DNA單鏈斷裂損傷具有修復(fù)作用,修復(fù)蛋白覆蓋于DNA損傷處,可防止核酸酶的消化而具有抗細胞凋亡作用。本實驗中XRCC1-IR與Bcl-2-IR呈顯著正相關(guān),二者與Bax-IR皆呈顯著負相關(guān),這結(jié)果進一步表明XRCC1具有抗細胞凋亡作用,與Guo等[5]檢測正常肝和肝癌細胞的bax、bcl-2、bcl-XL的表達水平和相關(guān)性研究及這些凋亡相關(guān)蛋白對細胞凋亡的調(diào)節(jié)作用相似。本實驗應(yīng)用Br和Q聯(lián)合誘導(dǎo)Eca-109細胞凋亡后bcl-2及XRCC1表達的下調(diào),Bax表達的上調(diào)對該細胞凋亡起著調(diào)節(jié)作用;而且Br及Q的單獨和聯(lián)合用藥對Bcl-2-IR、Bax-IR或XRCC1-IR的影響無統(tǒng)計學(xué)差異,但細胞凋亡率,有統(tǒng)計學(xué)差異。該結(jié)果提示植物類黃酮的中藥與西藥聯(lián)合應(yīng)用可能更具有臨床應(yīng)用意義。
藥物耐藥性在臨床療效上是一個重要因素,已知wtp53與細胞凋亡和耐藥性密切相關(guān),此外,調(diào)控蛋白如:Bcl-2和Bax等可能參與藥物耐藥性機制。有報道乳腺癌細胞系的凋亡與Bcl-2蛋白表達和Caspase-3活性有關(guān),但與Bax和Bcl-Xs無關(guān)[6]。研究結(jié)果表明多藥耐藥性相關(guān)蛋白免疫反應(yīng)性與Bcl-2-IR呈正相關(guān),與Bax-IR呈負相關(guān)。提示:一方面Bcl-2與Bax可能皆參與Eca-109細胞的凋亡,另一方面前凋亡蛋白的Bax可能對8-Br-cAMP及槲皮素誘導(dǎo)凋亡藥物的敏感性較高,細胞的MRP表達減低。相反,Bcl-2可能對促凋亡誘導(dǎo)藥物的敏感性較低,有一定程度的耐藥性而提高MRP的表達。POLB主要是DNA損傷中最常見的DNA單核苷酸的切除修復(fù)酶,當(dāng)高表達時,則對基因毒性藥物,如順鉑,敏感性降低而藥物耐藥性增高。有報道人卵巢癌細胞對順鉑耐藥的細胞比不耐藥的細胞POLB表達水平高3倍[7];結(jié)腸癌細胞對順鉑等藥物耐藥性比對照的POLB表達高2.5倍[8];類似報道也見于乳腺癌細胞[9]。本文結(jié)果表明 8-BrcAMP及槲皮素的聯(lián)合用藥可顯著降低不加藥的Eca-109細胞的POLB表達,同時也下調(diào)MDR表達。兩者之間呈顯著正相關(guān),r=0.983 8,P<0.01。即降低了該細胞的藥物耐藥性,逆轉(zhuǎn)腫瘤惡性。槲皮素和8-Br-cAMP可抑制癌細胞周期進展和增殖,提高藥物敏感性,誘導(dǎo)食管癌細胞分化及凋亡,呈現(xiàn)不同信號轉(zhuǎn)導(dǎo)途徑的互補效應(yīng),提示其下調(diào)Eca-109細胞的增變基因表型。
[1]Belzacg AS,Vieira HL,Verrier F,et al.Bcl22 and Bax modulate adenine nucleotide translocase activity[J].Cancer Res,2003,63(2):541.
[2]Kanauchi H,Wada N,Clark OH,et al.Apoptosis regulatinggenes,bcl22 and bax,and human telomerase reverse transcriptase messenger RNA expression in adrenal tumors:possible and prognostic importance[J].Surgery,2002,132(6):1021.
[3]Thomas D,Yang H,Boffa DJ,et al.Proapoptotic Bax is hyperexpressed in isolated human islets compared with antiapoptotic Bcl22[J].Transplantation,2002,74(11):1489.
[4]Del Poeta G,Vendlttl A,Del Principe MI,et al.The amount of spontaneous apoptosis detected by bax/bcl22 ratio predicts outcome in acute myeloid leukemia(AML)[J].Blood,2003,102(2):2125.
[5]Guo XZ,Shao XD,Liu MP,et al.Effect of bax,bcl22 and bclxl on regulating apoptosis in tissues of normal liver and hepatocellular carcinoma.World J Gastroenterol,2002,8(6):1059.
[6]yang XK,Zheng F Chen JH,et al.Relationship between expression of apoptosis-associated proteins and caspase-3 activity in cisplatin-resistant human ovarian cancer cell line[J].Ai Zheng,2002,21(12):1288.
[7]Valentinis B,Zaffaroni N,Sturani E,et al.Detection of DNA polymerase beta gene expression by competitive polymerasechain reaction in human ovarian carcinoma cells[J].Anticancer Res,1993,13(1):125.
[8]Funato T,Tone T,Miyachi,et al.Detection of drug resistant genes cisplatin-resistant colon carcinoma cells[J].Rinsho Byori,1993,41(1):95.
[9]Raaphorst GP,Cybulski SE,Sobel R,et al.The response of human breast tumor cell line with altered polymerase beta levels to cisplatin and radiation[J].Anticancer Res,2001,21(3B):2079.

