變應性肉芽腫性血管炎一例并文獻復習
符詒慧,董 文,黃奕江
(海南省人民醫院呼吸內科,海南 海口 570311)
變應性肉芽腫性血管炎是少見的一類系統性血管病,該病首發臨床表現可為哮喘,多被誤診為單純性支氣管哮喘。近年來隨著診斷技術水平的提高,該病檢出率增高,亦日益受到重視。現就我院診斷為變應性肉芽腫性血管炎的一例住院病例進行回顧性的分析并文獻復習。
1 病例簡介
患者,男,65歲,因“反復咳嗽、氣促2年,再發加重1周”于2009年1月17日入院。日常一般活動如穿脫衣服等即氣促。既往患過敏性鼻炎、鼻息肉20年,反復行鼻息肉切除術。入院體檢:淺表淋巴結未觸及腫大;雙肺呼吸音減弱,未聞及干濕性啰音,杵狀指,兩次支氣管舒張試驗均呈陽性。初步診斷:“支氣管哮喘急性發作期”,給予霧化吸入糖皮質激素治療癥狀減輕,后加用孟魯司特后咳嗽、氣促加重,稍活動即氣促,并相繼出現眩暈、惡心、嘔吐,四肢遠端麻木,腹痛,腹瀉。輔助檢查:血嗜酸性粒細胞比值為9.11%;胸部CT:彌漫性肺間質改變(見圖1);抗中性粒細胞漿抗體核周型(p-ANCA)陽性,C-反應蛋白(CRP)53.41 mg/L;神經肌電圖:四肢周圍神經遠端受損;鼻竇CT:鼻竇炎。最后診斷:變應性肉芽腫性血管炎。治療:停用孟魯司特,給予甲潑尼龍80 mg qd靜脈滴注,環磷酰胺40 mg靜脈滴注,每周兩次。經過8周的治療,患者咳嗽緩解,氣促明顯好轉,6 min可平地步行約300 m。
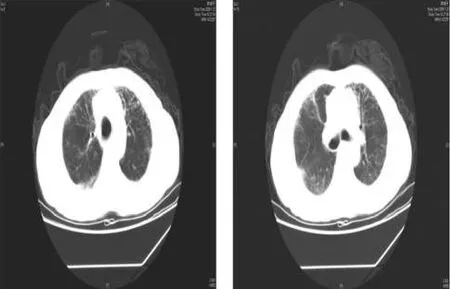
圖1 CT肺內網格狀、斑片狀影
2 討論
變應性肉芽腫性血管炎以過敏性哮喘、嗜酸性粒細胞增多、發熱和全身性肉芽腫血管炎為特征。1951年由Churg和Strauss首先描述,故又稱為Churg Strauss綜合征,簡稱“CSS”。可發生于任何年齡,平均發病年齡為44歲,男女之比為1.3:1。
2.1 臨床表現 CSS可累及多種器官。
2.1.1 肺部表現 肺臟是最常見和最易受累的器官。特異癥狀為呼吸道過敏反應,主要表現為反復發作性咳嗽、呼吸困難。胸部影像學顯示病變呈多發性和易變性。影像學改變包括實變影、斑片影、網格影、網格結節影、肺門增大等。
2.1.2 腎臟病變 約80%患者患局灶性節段性腎小球腎炎,但病變較輕,可有血尿、蛋白尿等腎炎表現,少數發生急性腎衰竭[1]。
2.1.3 神經系統病變 發生率為70%左右,以周圍神經受累發生率最高,又以多發性單神經癥最多見。神經電生理檢查發現感覺及運動纖維均受累,以動作電位波幅下降為主[2]。
2.1.4 心臟病變 發生率高且嚴重,是最常見的死亡原因。心肌肉芽腫形成和冠狀動脈血管炎可導致充血性心力衰竭、心律失常、心內膜炎、心包積液和限制性心肌病。CSS患者主要死于充血性心力衰竭和心肌梗死。據報道,CSS心臟受累患者預后差,但臨床表現缺乏特異性,致使部分患者沒有得到及時明確的診斷。對于臨床上出現的不明原因的心力衰竭、心包積液或者年輕的缺乏常見高危因素的冠狀動脈病變患者,應警惕CSS。
2.1.5 胃腸道病變 約占31%。主要表現為腹痛、腹瀉,少數便血,偶出現肝大、轉氨酶升高、膽囊炎等表現。
2.1.6 皮膚病變 多見,約占70%。呈現多樣性,可表現為紫癜性皮疹、紅斑、皮下結節、蕁麻疹等[3]。
2.2 實驗室檢查 嗜酸性粒細胞增高是CSS的突出表現。CSS活動期血沉、C-反應蛋白增高。故監測血嗜酸性粒細胞、血沉、C-反應蛋白來判斷病情的活動情況,評估療效。抗中性粒細胞胞漿抗體是系統性血管炎的標志性抗體,該抗體結果呈陽性對血管炎有重大診斷價值。
2.3 診斷 1990年美國風濕協會(ACR)制定的診斷標準,符合以下6個條件中的4個者可診斷變應性肉芽腫性血管炎:(1)哮喘;(2)嗜酸性粒細胞比例>10%;(3)單神經炎或多發神經炎;(4)X線表現為非固定的肺部浸潤;(5)鼻竇炎;(6)活檢提示血管外的嗜酸細胞浸潤。符合以上6個條件中的4個者可診斷為CSS,敏感性為85.0%,特異性為99.7%。
2.4 鑒別診斷
2.4.1 特發性嗜酸細胞增多綜合征 Chusid1975年提出的該病診斷標準為:(1)血嗜酸性粒細胞絕對值大于1.5×109,持續半年以上。(2)未找到寄生蟲、變態反應性或其他可引起嗜酸細胞增多癥的原因。(3)有受累器官的體征和癥狀。
2.4.2 慢性嗜酸粒細胞性肺炎、過敏性支氣管肺曲菌病 均有哮喘、外周血嗜酸性粒細胞增多及肺部嗜酸性粒細胞浸潤性肺炎表現,但兩者均無壞死性血管炎及壞死性肉芽腫表現。
2.4.3 韋格納肉芽腫 無哮喘癥狀,肺內病變易形成空洞,腎臟病變較重,大部分為抗中性粒細胞漿抗體胞漿型(c-ANCA)陽性。
2.4.4 結節性多動脈炎 主要累及中等大小的血管,往往無肺部浸潤和血嗜酸性粒細胞增高。
2.4.5 顯微鏡下型多血管炎 是一種壞死性血管炎,大部分為p-ANCA陽性,少部分為c-ANCA陽性,很少或無免疫復合物沉積。主要影響小血管(小動脈、毛細血管和小靜脈),主要表現為壞死性新月體腎小球腎炎、肺毛細血管炎,死亡主要原因為感染、肺出血和腎衰竭。
2.5 治療 (1)糖皮質激素:激素是治療CSS的主要藥物。對重癥患者,甲基強的松龍0.5-1 g/d,連續靜滴3-5 d后改為潑尼松40-60 mg/d口服8周左右,酌情減量,維持治療。(2)免疫抑制劑:免疫抑制劑可以提高緩解率。Ribi等[4]對激素抵抗或復發的CSS患者,使用環磷酰胺或硫唑嘌呤治療半年后均可獲得良好療效。環磷酰胺總量一般達6000-8000 mg。(3)血漿置換:血漿置換可清除免疫復合物,改善內皮細胞的功能,故可用于治療血管炎性疾病。Danieli等[5]對CSS患者采用激素和免疫抑制劑聯合血漿置換和免疫球蛋白靜脈滴注治療,進行為期3年的觀察,結果表明這種方案可很快控制CSS患者的疾病活動,降低復發率,減少血管炎性損害所致的器官功能障礙,并有良好的耐受性。
2.6 預后 變應性肉芽腫性血管炎的首位死亡原因是心衰或心肌梗死,其次是腎衰。
本例的經驗教訓:起初患者按“支氣管哮喘急性發作”給予治療,病情反復并加重,后查胸部CT提示雙肺間質性改變,p-ANCA陽性,才將思路引向血管炎。臨床醫生應警惕難治性支氣管哮喘患者轉變為變應性肉芽腫性血管炎,注意與血管炎甄別。
[1]張智斌.Churg-Strauss綜合征診斷治療新進展[J].邯鄲醫學高等專科學校學報,2004,17(6):590-592.
[2]魏妍平,陳 琳,郭玉璞,等.變應性肉芽腫性血管炎的神經系統表現[J].中華神經科雜志,2005,38(10):651-653.
[3]趙 立.Churg-Strauss綜合征[J].中國實用內科雜志,2008,28(8):628-630.
[4]Ribi C,Cohen P,Pagnoux C,et al.Treatment of Churg-strauss syndrome without poor-prognosis factors:amulticenter,prospective,randomized,open-label study of seventy-two patients[J].Atthritis Rheum,2008,58:586-594.
[5]Danieli MG,Cappelli M,Malcangi G,et al.Long term effectiveness of intravenous immunoglobulin in Churg-Strauss syndrome[J].Ann Rheum Dis,2004,63:1638-1654.

