扁平苔蘚皮損中MIF、MMP-9的表達及意義
王 慧,白 莉
(山西醫科大學第一醫院皮膚科,山西太原 030001)
扁平苔蘚(lichen planus)是一種病因不明的慢性或亞急性炎癥性皮膚病,其組織學特征顯示為上皮基底細胞的液化變性、基底膜帶損傷。目前關于其基底膜帶損傷機制的研究甚少。本文旨在檢測扁平苔蘚中MIF、MMP-9的表達,進一步探討兩者與扁平苔蘚基底膜帶損壞的關系。
1 材料與方法
1.1 材料
病例組30例均系2008~2009年在我院皮膚科就診,經臨床和病理確診的扁平苔蘚患者。其中,男17例,女13例;年齡20~64歲,平均41.9歲。所有患者在半年內均未使用過激素和免疫抑制劑治療。于患者典型皮損處取材。對照組30例為同期在我院整形科、普外科所取的正常皮膚組織,其中,男20例,女10例;年齡 18~60歲,平均37.6歲。兩組患者年齡、性別差異無統計學意義,具有可比性。各標本取材后分兩份,一份經中性福爾馬林液固定,石蠟包埋后用于免疫組化染色;另一份予以液氮迅速冷凍后置于-80℃冰箱保存,用作RT-PCR實驗。
1.2 試劑
兔抗人MIF多克隆抗體為美國Santa Cruz公司產品,兔抗人MMP-9多克隆抗體購自北京博奧森生物技術有限公司。二步法PV-6000免疫組織化學檢測試劑盒由北京中杉金橋生物技術有限公司提供。MIF、MMP-9引物由上海生工生物工程技術有限公司合成。
1.3 方法
1.3.1 免疫組化法 采用PV-6000二步法:備用標本進行4 μm厚連續切片后脫蠟,3%H2O2去離子水阻斷內源性過氧化物酶; 滴加一抗 (MIF濃縮液1∶150稀釋,MMP-9濃縮液1∶100稀釋),37℃孵育 1 h; 滴加二抗 PV-6000,37℃孵育 20 min;二氨基聯苯胺(DAB)顯色,蘇木素復染、脫水、封片。
1.3.2 RT-PCR法 采用Trizol一步法提取各標本總RNA,并用分光光度法檢測其濃度及純度。加入逆轉錄反應體系合成cDNA,將其置于PCR反應體系,按RT-PCR試劑盒說明擴增GAPDH (作為內參照)、MIF、MMP-9。各基因引物如下,GAPDH 上游引物:5′-TGA ACG GGA AGC TCA CTG G-3′,下游引物∶5′-TCC ACC ACC CTG TTG CTG GA-3′,擴增片段 307 bp。MIF 上游引物:5′-AGA ACC GCT CCT ACA GCA AG-3′, 下游引物:5′-ATT TCT CCC CAC CAG AAG GT-3′,擴增片段234 bp。MMP-9上游引物:5′-TTG ACA GCG ACA AGA AGT GG-3′,下游引物:5′-GCC ATT CAC GTC GTC CTTAT-3′,擴增片段179bp。PCR擴增條件:94℃預變性2min,94℃變性 30 s, 58℃(GAPDH)、52℃(MIF)、56℃(MMP-9)退火 20 s,72℃延伸30 s,共32次循環。獲得的PCR產物經1.5%瓊脂凝膠電泳后,用圖像分析儀掃描分析。
1.4 結果判定
免疫組化結果以細胞核或細胞漿著黃色或棕黃色為陽性,每張切片隨機選取5個視野,利用MIAS-2000圖像分析系統分析陽性區域積分光密度(IOD)值,以IOD值大小代表陽性產物的多少;RT-PCR檢測結果以出現擴增條帶為陽性,PCR產物的含量以累積光密度(OD)表示。以同一標本MIF、MMP-9與內參照GAPDH的OD值來判定兩種組織中MIF、MMP-9的表達水平。
1.5 統計學分析
2 結果
2.1 扁平苔蘚組織與正常皮膚組織中MIF、MMP-9的表達水平
免疫組化結果顯示,扁平苔蘚中MIF、MMP-9的陽性表達主要分布在表皮全層角質形成細胞和真皮淺層浸潤的淋巴細胞的胞漿中;而在正常皮膚組織中均呈陰性或弱陽性表達。兩者在扁平苔蘚皮損區的表達明顯高于正常皮膚組織,差異均有統計學意義(P<0.05)。扁平苔蘚皮損中 MIF、MMP-9的表達呈正相關(r=0.636, P<0.01)。扁平苔蘚組與正常皮膚組之間MIF、MMP-9的IOD值比較見表1。
表1 扁平苔蘚與正常皮膚組織中MIF、MMP-9表達水平的比較(±s)Tab.1 The expression of MIF and MMP-9 in lichen planus and normal skin(±s)
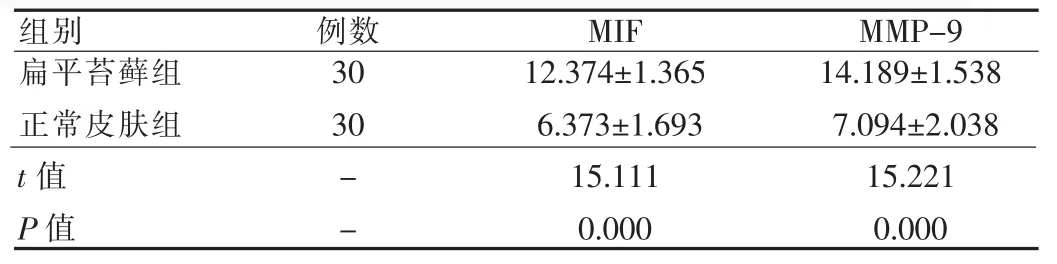
表1 扁平苔蘚與正常皮膚組織中MIF、MMP-9表達水平的比較(±s)Tab.1 The expression of MIF and MMP-9 in lichen planus and normal skin(±s)
組別 例數 MIF 30 30扁平苔蘚組正常皮膚組t值 P值--12.374±1.365 6.373±1.693 15.111 0.000 MMP-9 14.189±1.538 7.094±2.038 15.221 0.000
2.2 扁平苔蘚與正常皮膚組織中MIF、MMP-9 mRNA的表達水平
RT-PCR結果顯示,各組織均穩定表達內參照基因GAPDH。經統計學分析扁平苔蘚皮損中MIF的mRNA、MMP-9的mRNA表達水平顯著高于正常皮膚,差異有統計學意義(P<0.05)。見表2。
表2 扁平苔蘚與正常皮膚組織中MIF、MMP-9 mRNA表達水平的比較(±s)Tab.2 Comparison of the expression of MIF and MMP-9 mRNA in lichen planus and normal skin(±s)
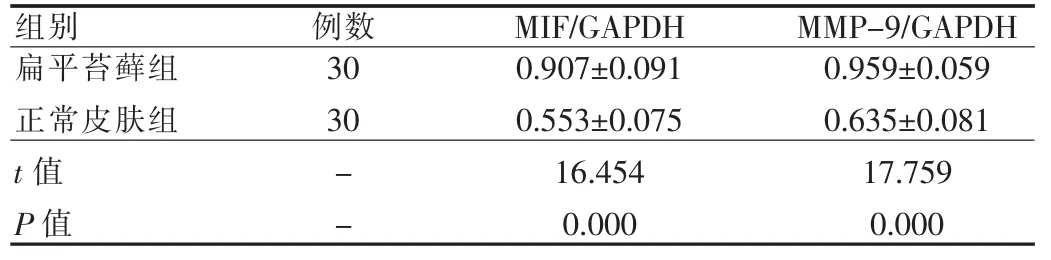
表2 扁平苔蘚與正常皮膚組織中MIF、MMP-9 mRNA表達水平的比較(±s)Tab.2 Comparison of the expression of MIF and MMP-9 mRNA in lichen planus and normal skin(±s)
扁平苔蘚組正常皮膚組t值P值組別 例數 MIF/GAPDH 30 30--0.907±0.091 0.553±0.075 16.454 0.000 MMP-9/GAPDH 0.959±0.059 0.635±0.081 17.759 0.000
3 討論
目前廣泛認為扁平苔蘚是一種細胞介導的自身免疫性疾病。研究證明,CD8+T細胞與LP皮損的基底細胞損傷以及皮損的持續存在有關[1]。巨噬細胞移動抑制因子(MIF)是由活化的T淋巴細胞分泌的一種淋巴細胞因子。它通過抑制巨噬細胞遷移,使巨噬細胞在炎癥局部激活、黏附、浸潤并分泌一些細胞因子,這些因子又可促進MIF的分泌,從而造成一個慢性反復的炎癥過程。MIF可作為免疫調節劑參與機體各種病理生理過程,在自身免疫疾病以及抗原遞呈過程中起重要作用[2]。最近的研究也發現T淋巴細胞內MIF的水平為B淋巴細胞和巨噬細胞中的2倍[3]。本研究顯示,MIF在扁平苔蘚中的表達明顯高于正常皮膚,因此推測MIF的過度表達可能在扁平苔蘚的發病中起重要作用。
MMP-9屬于MMPs中的明膠酶,多來源于T淋巴細胞、巨噬細胞,主要降解基底膜帶中的重要成分Ⅳ型膠原和層黏連蛋白,從而造成基底膜帶的損壞。本實驗結果顯示扁平苔蘚中MMP-9表達增高,表明MMP-9可能與扁平苔蘚基底膜帶破壞有關,這與丁政云等[4]的研究結果一致。
有研究證明MIF能誘導MMP-9的表達上調[5-6],且研究認為MMP-9基因啟動子區有幾個可以與轉錄因子相結合的位點,包括NF-κB和活化蛋白-1(AP-1)等元件的結合位點,這些活化因子的結合是MMP-9表達所必需的[7]。MMP-9的轉錄有賴于一些細胞因子、生長因子等與這些元件的相互作用。本研究表明,扁平苔蘚中MIF、MMP-9的蛋白及mRNA均升高,且二者表達呈正相關,提示MIF可能通過一系列途徑上調MMP-9的轉錄活性而最終調節MMP-9蛋白水平的增高。激活的MMP-9使基底膜帶遭到破壞,除可使OLP表皮細胞失去生存信號而凋亡外,還使更多的淋巴細胞進入上皮加劇其損傷[8]。凋亡的表皮細胞又無法合成基底膜帶的主要成分Ⅳ型膠原和層黏連蛋白,加重了基底膜帶的損傷。這一連鎖反應最終可致基底細胞液化變性,產生扁平苔蘚的臨床和病理變化。
[1]狄正鴻,許靜.扁平苔蘚皮損中浸潤淋巴細胞的研究[J].中國醫科大學學報,2006,35(4)∶427-428.
[2]Nishihira J.Macrophage migration inhibitory factor(MIF)∶its essential role in the immune system and cell growth[J].J Interfeion Cytokine Res,2000,20(9)∶751-762.
[3]Lehmann LE,Weber SU,Fachs D,et al.Intracellular detection of macrophage migration inhibitory factor in peripheral blood leukocytes[J].Free Radic Biol Med,2005,38(9)∶1170-1179.
[4]丁政云,蔡麗,劉麗娟,等.扁平苔蘚皮損MMP-2、MMP-9的表達及外周血 MMP-9 的檢測[J].中國麻風皮膚病雜志,2008,24(2)∶10-11.
[5]Onodera S,Nishihira J,Iwabuchi K,et al.Macrophage migration inhibitory factor up-regulates matrix metalloproteinase-9 and-13 in rat osteoblasts relevance to intracellular signaling pathways[J].J Biol Chem,2002,277(10)∶7865-7874.
[6]李智,林素暇,梁英杰,等.巨噬細胞移動抑制因子對鼻咽癌細胞株MMP-2、MMP-9 和 IL-8 表達的影響[J].癌癥,2004,23(2)∶130-135.
[7]Huhtala P,Chow LT,Tryggvason K.Structure of the human type Ⅳcollagenase gene[J].J Boil Chem,1990,265(19)∶11077-11082.
[8]Zhou XJ,Sugerman PB,Savage NW,et al.Intra-epithelial CD8+T cells and basement membrane disruption in oral lichen planus[J].J Oral Pathol Med,2002,31(1)∶21-23.

