豬胰脂肪酶水解花椒籽油動力學及條件優化
徐懷德,唐 菊,劉立芳
(西北農林科技大學食品科學與工程學院,陜西 楊凌 712100)
豬胰脂肪酶水解花椒籽油動力學及條件優化
徐懷德,唐 菊,劉立芳
(西北農林科技大學食品科學與工程學院,陜西 楊凌 712100)
為開發花椒籽油中的α-亞麻酸,對豬胰脂肪酶水解花椒籽油的酶解特性和水解條件進行研究。結果表明:油水界面面積(αt)與溫度(t)、攪拌速率(ω)、底物濃度(S)的關系為αt=0.04ω0.577t1.242S(1+0.02S)。水解反應速率隨溫度的變化服從Arrhenius方程,反應活化能為21.891kJ/mol。以米氏方程為理論基礎,考慮αt對水解反應速率的影響,建立豬胰脂肪酶對花椒籽油的水解動力學模型。豬胰脂肪酶水解花椒籽油的適宜條件為:溫度50℃、油質量分數30%、酶質量濃度72.9g/L,在此條件下反應4h后水解率達57.13%。
豬胰脂肪酶;花椒籽油;水解;動力學;條件優化
Abstract :In order to exploit α-linolenic acid from prickly ash seed oil, the hydrolysis characteristics of prickly ash seed oil by porcine pancreatic lipase were investigated and some key hydrolysis conditions were explored. The results indicated that an equation expressing oil-water interface (α t) with respect to reaction temperature (t), agitation speed (ω) and substrate concentration (S) was developed as follows: αt= 0.04ω0.577t1.242S (1 + 0.02S). The change in hydrolysis reaction rate with varying reaction temperature obeyed Arrhenius equation. The activation energy was 21.891 kJ/mol. Based on Michaelis-Menten equation and the effect of αt on reaction rate, a kinetic model was established to describe the hydrolysis of prickly ash seed oil by porcine pancreatic lipase. The optimal hydrolysis conditions of prickly ash seed oil by porcine pancreatic lipase were reaction temperature of 50 ℃, oil concentration of 30%, enzyme concentration of 72.9 g/L and reaction time of 4 h. The dgree of hydrolysis reached up to 57.13% under these optimal conditions.
Key words:porcine pancreatic lipase;prickly ash seed oil;hydrolysis;kinetic;condition optimization
花椒(Zanthoxylum bungeanum Maxim)被譽為我國“八大調味品”之一,目前在我國種植面積達80萬hm2。花椒籽是花椒生產中的主要副產物,我國每年約有30~40萬t的花椒籽油亟待開發利用[1-2]。花椒籽油中不飽和脂肪酸含量高達80%,其中亞油酸含量為25%~32%,α-亞麻酸含量為17%~24%[3],是極具開發潛力的油脂資源。α-亞麻酸是重要的醫藥、保健食品原料,具有抗炎癥、抗血栓、抗心率失常、降血脂、改善血管彈性的作用,還具有調節中央神經系統、提高記憶力的功能,具有極高的經濟價值和廣闊的市場需求空間。花椒籽油的深度開發利用對提高花椒的種植效益、改善生態環境等具有重要意義。
近年來,花椒籽油主要用于生產油漆、制造肥皂、制備生物柴油,也有采用尿素包合法和色譜法分離純化花椒籽油中的α-亞麻酸[2-3]。脂肪酸制備方法有酸水解法、皂化-酸水解法和酶催化水解法[4],酸水解法效率較低,皂化-酸水解法得到的產品顏色深,副產物多,為后續分離純化帶來很大困難。脂肪酶水解油脂制備脂肪酸具有條件溫和、產品質量好、能耗低和環境污染小等優勢,目前酶法已成為通過油脂生產脂肪酸的主要方法[5-6]。酶解亞麻油、魚油、棕櫚油、紫蘇子油等制備脂肪酸的研究報道較多,但多數研究只停留在酶解條件的優化[7-10]。國外Okada 等[11]、Sulaiman等[12]對脂肪酶的酶解特性進行了研究,建立了脂肪酶催化油脂水解的動力學模型。而國內相關研究的報道較少,對酶解花椒籽油制備脂肪酸的研究尚未見報道。
本實驗選用豬胰脂肪酶水解花椒籽油,研究其水解動力學特性,并對水解條件進行優化,以為花椒籽油及α-亞麻酸的開發應用提供參考。
1 材料與方法
1.1 材料與試劑
花椒籽油(平均相對分子質量為886) 陜西省韓城市金太陽花椒油脂藥料有限責任公司。
豬胰脂肪酶(比活力8000U/g) 諾維信投資有限公司;KOH 天津市化學試劑廠;Na2HPO4、NaH2PO4天津金匯太亞化學試劑有限公司;酚酞指示劑 武漢市中天化工有限責任公司。
1.2 儀器與設備
DMBA-400數碼顯微鏡 廈門麥克奧迪實業集團公司;MP200B電子天平 上海精密科學儀器有限公司;PHS-3C精密pH計 上海精密科學儀器有限公司雷磁儀器廠;HJ-4A數顯恒溫多頭磁力攪拌器 金壇市杰爾瑞電器有限公司;KDC-40離心機 科大創新股份有限公司偉佳分公司。
1.3 方法
1.3.1 水解動力學實驗
用0.05mol/L的Na2HPO4-NaH2PO4緩沖液(pH7.0)將豬胰脂肪酶配制成20U/mL酶液。將酶液及花椒籽油分別預熱至水解溫度后混合,在磁力攪拌器中恒溫攪拌反應20min,取出后于沸水浴中滅酶15min。將水解產物離心,吸取2mL上層油相,用0.01mol/L KOH滴定,重復兩次取平均值[13]。水解反應速率(υ)按式(1)計算[14]。

式中:V1為反應后樣品消耗的KOH體積/mL;V0為反應前樣品消耗的KOH體積/mL;c為KOH濃度/(mol/L);Vs為樣品的體積/mL;t為反應時間/min。
1.3.2 油水界面面積(αt)的測定[15]
稱取花椒籽油于三角瓶中,按實驗預定的比例加入蒸餾水,在磁力攪拌器中恒溫攪拌30min,吸取1滴樣品于載玻片上,立即用顯微鏡測定分散在水相中的油滴粒徑,每個樣品測定200個油滴。將粒徑按大小分為3組:小于10μm、10~20μm、20~30μm。按公式(2)計算平均粒徑。

式中:D0為油滴平均粒徑/m;i為測定油滴個數;j為粒徑組數;di為第i個油滴的粒徑/μm;θj為第j組油滴的個數在所測油滴總數中占的比例。
方程(3)為Calderbank[16]建立的油水界面面積與溫度(t)、攪拌速率(ω)、底物濃度(S)的關系式:

式中:αt為油水界面面積/m-1;φ為油與反應體系的體積比;S為底物濃度/(mol/L);t為溫度/℃;ω為攪拌速率/(r/min);α、m、k、n為常數。
1.3.3 中心組合試驗[17]
稱取豬胰脂肪酶于磨口三角瓶中,用0.05mol/L的Na2HPO4-NaH2PO4緩沖液(pH7.0)將其溶解,按比例加入花椒籽油,在恒溫磁力攪拌器中恒溫攪拌反應。根據前期預實驗結果,選擇攪拌速率為300r/min,反應時間為4h。以油質量分數、溫度、酶質量濃度為試驗因子,以水解率為響應值,采用中心組合試驗優化豬胰脂肪酶水解花椒籽油的條件。水解率按公式(4)計算。

式中:AV0、AV分別為水解前后花椒籽油的酸價,水解前酸價(以KOH計),1.93mg/g;SV為水解前花椒籽油皂化值(以KOH計),190mg/g。
2 結果與分析
2.1 反應條件對油水界面面積的影響
2.1.1 底物濃度對油水界面面積的影響
磁力攪拌器中恒溫40℃攪拌30min。攪拌速率和底物濃度對油水界面面積的影響如圖1所示。

圖1 底物濃度和攪拌速率對油水界面面積的影響Fig. 1 Effect of substrate concentration and agitation speed onαt
由圖1可知,當底物濃度一定時,隨著攪拌速率的加快,油水界面面積增大;當攪拌速率一定時,隨著底物濃度的升高,油水界面面積增大。在底物濃度低于113mol/L時,油水界面面積的增速較快,底物濃度高于113mol/L時,油水界面面積的增速逐漸變緩。
2.1.2 溫度對油滴平均粒徑的影響
當底物濃度為113mol/L時,磁力攪拌器中攪拌30min,攪拌速率和溫度對油滴平均粒徑的影響如圖2所示。

圖2 溫度和攪拌速率對油滴平均粒徑的影響Fig.2 Effect of reaction temperature and agitation speed on the average diameter of oil droplets
由圖2可見,隨著攪拌速率和溫度的升高,油滴平均粒徑減小。
用方程(3)對圖1和圖2中的數據進行擬合,采用DPS軟件估計模型參數,得到αt與t、ω及S的關系式:

統計檢驗的相關系數r=0.974,說明模型(3)對本實驗數據的擬合是極顯著的。
2.2 反應條件對反應速率的影響
2.2.1 底物濃度對反應速率的影響
酶質量濃度為30000g/L,溫度40℃時,攪拌速率和底物濃度對反應速率的影響見圖3。

圖3 底物濃度和攪拌速率對反應速率的影響Fig.3 Effect of substrate concentration and agitation speed on reaction rate
由圖3可見,隨著底物濃度和攪拌速率的增大,反應速率上升。在同一攪拌速率下,底物濃度增加,油水界面面積增大,引起反應速率增大。當底物濃度高于224mol/L時,反應速率緩慢下降。
2.2.2 酶質量濃度對反應速率的影響
底物濃度為113mol/L,溫度40℃時,攪拌速率和酶質量濃度對反應速率的影響見圖4。
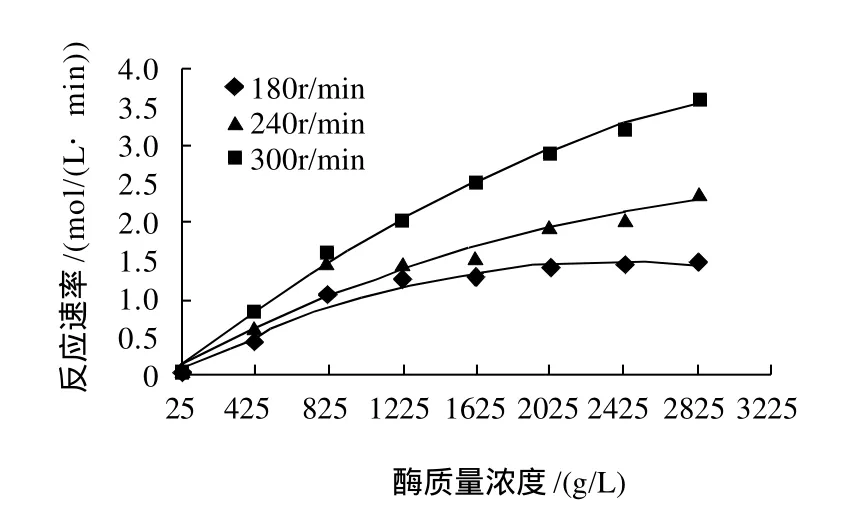
圖4 酶質量濃度和攪拌速率對反應速率的影響Fig.4 Effect of enzyme concentration and agitation speed on reaction rate
由圖4可知,當酶質量濃度低于825g/L時,反應速率與酶質量濃度呈線性關系;酶質量濃度高于825g/L時,隨酶質量濃度的增大,反應速率增速逐漸變緩。另外,攪拌速率加快,油水界面面積增大,酶與底物接觸的機會增多,則酶在油水界面上達到飽和時所需的酶量增多。
2.2.3 溫度對反應速率的影響
底物濃度250mol/L,酶質量濃度250g/L,攪拌速率300r/min條件下,在溫度分別為30、35、40、45、50、60、70℃時進行水解反應,溫度與反應速率的關系見圖5。

圖5 溫度對反應速率的影響Fig.5 Effect of reaction temperature on reaction rate
圖5中的曲線是一條鐘罩形曲線,即溫度從30℃增加到50℃,反應速率增至最大,以后隨著溫度升高,反應速率迅速下降。

圖6 lnν與1/T關系圖Fig.6 Relationship between lnνand l/T
將lnν與1/T作圖,得到如圖6的直線,可見溫度在303~323K范圍內時,lnν與1/T之間呈線性關系,表明水解反應速率隨溫度的變化服從Arrhenius方程[7]:

式中:B為積分常數;R為氣體常數/(J/(mol·K));Ea為活化能/(kJ/mol);T為熱力學溫度/K。
圖6中直線斜率為-Ea/2.303R,由斜率可求出Ea為21.891kJ/mol。
2.3 動力學模型的建立及檢驗
2.3.1 動力學模型的建立[17-18]
在無有機溶劑的體系中,脂肪酶催化油脂水解反應發生在油水界面,脂肪酶催化油脂水解的過程分為3步,首先是脂肪酶通過滲透作用進入油水界面中,形成中間體E*;然后中間體E*與底物形成E*S復合物;最后分解成產物P,反應方程式見式(7)、(8):

由方程(7)和(8)推導出脂肪酶催化油脂水解的反應速率方程(9):

式中:kcat為催化速率常數/min-1;Am為酶在油水界面占的面積;S為底物濃度/(mol/L);ke為平衡常數/(mol/L);kp、kd分別為吸附和解析常數(單位為1);Et為酶質量濃度/(g/L)。
用方程(9)對圖5和圖6中的實驗數據進行擬合,通過DPS軟件分析,相關系數r為0.966,模型的參數見表1。
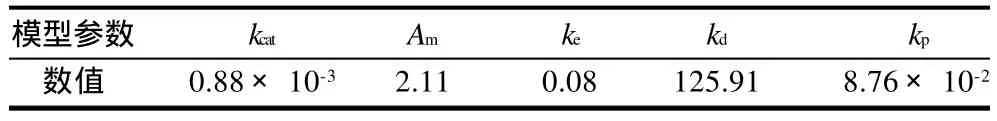
表1 模型參數Table 1 Parameters of the established hydrolysis kinetic model
將表1中參數代入方程(9),得到豬胰脂肪酶水解花椒籽油的動力學模型為:
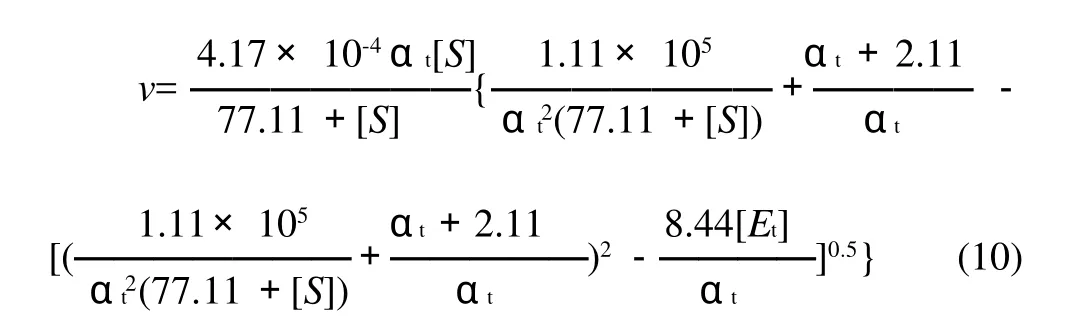
2.3.2 模型檢驗
取酶質量濃度500g/L和2500g/L高低兩個梯度,底物濃度分別為50、100、150、200、250、300、350、400mol/L,按照1.3.1節的方法進行檢驗實驗。圖7為模型預測值與實驗值的比較,模型的預測值與實驗值吻合較好,因此可用該模型來描述豬胰脂肪酶水解花椒籽油的過程。

圖7 模型預測值與實驗值的比較Fig.7 Comparison of predicted and experimental values of hydrolysis reaction rate at different enzyme concentrations
2.4 中心組合試驗優化酶解工藝條件
中心組合設計及試驗結果見表2。以水解率(DH)為固定變量(Y),以溫度(x1)、油質量分數(x2)、酶質量濃度(x3)為因變量,經Design-Expert7.0統計分析得到的數學模型為:

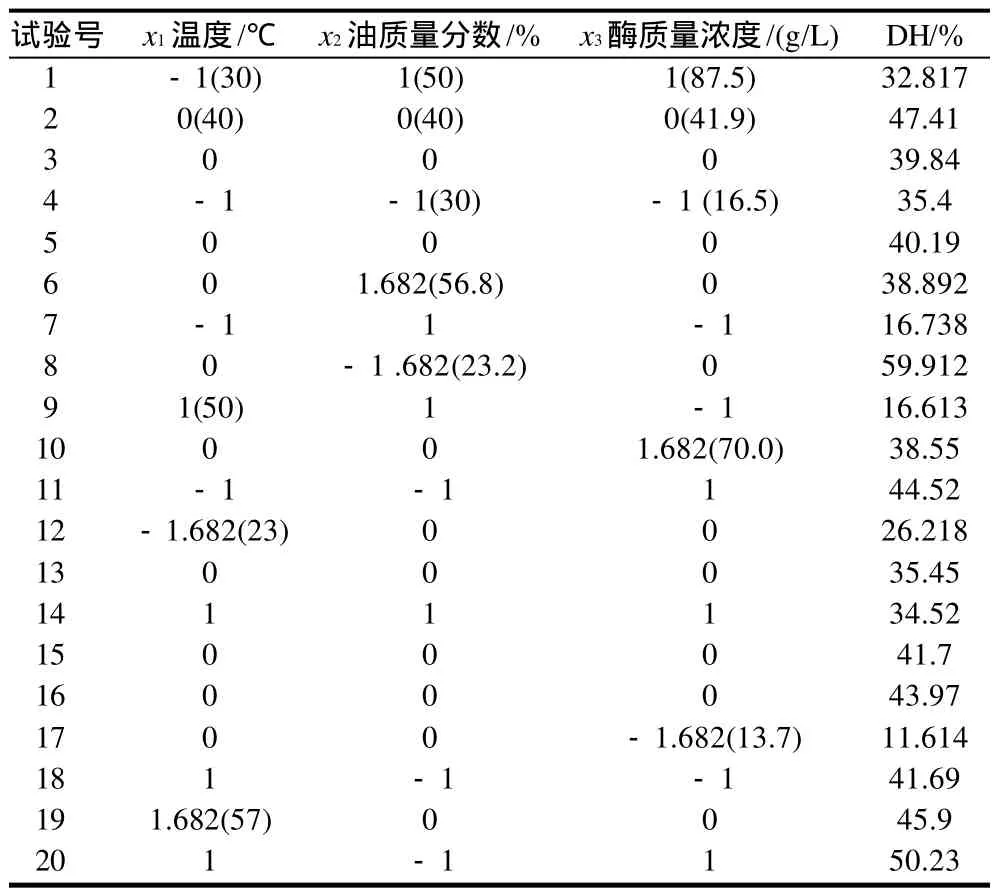
表2 中心組合試驗設計及結果Table 2 Design and results of central composite experiments
2.4.1 回歸模型的檢驗
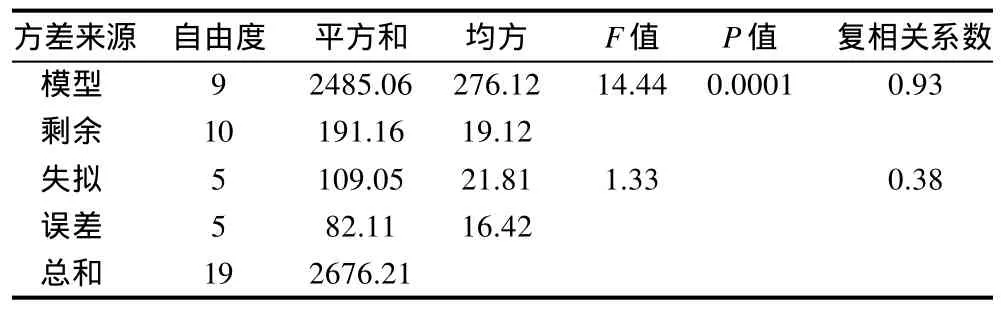
表3 回歸方程顯著性檢驗Table 3 Variance analysis for the developed regression equation
由表3回歸模型的方差分析可知,回歸模型的失擬性檢驗F=1.33<F0.05(5,5)=5.05,不顯著,可以認為所選用的回歸模型是適合的。模型P=0.0001<0.01,表明模型極顯著,復相關系數R=0.93,說明模型的預測值與實際值吻合較好,模型具有實際意義。

表4 數學模型的回歸系數及顯著性檢驗Table 4 Regression coefficients of developed regression equation and corresponding variance analysis
由表4可知,一次項x1(P=0.01)、x2(P<0.0001)、x3(P=0.0001)和二次項x32(P=0.0003)均達到極顯著水平;x12(P<0.05)、x22(P<0.05)達到顯著水平。各因素對水解度的影響次序依次為x2>x3>x1,即油質量分數>酶質量濃度>溫度。
2.4.2 酶解工藝參數的優化
采用Design-Expert7.0統計軟件優化得到豬胰脂肪酶水解花椒籽油的最適反應條件為:溫度50℃、油質量分數30%、酶質量濃度72.9g/L,在此條件下進行驗證實驗,反應4h水解率為57.13%,與預測值54.97%接近,擬和性好,表明了模型的有效性。
3 結 論
3.1 油水界面面積(αt)與溫度(t)、攪拌速率(ω)、底物濃度(S)的關系為:αt=0.04ω0.577t1.242S(1+0.02S)。酶解反應速率隨溫度的變化服從Arrhenius方程,活化能Ea=21.891kJ/mol。
3.2 在米氏方程基礎上,考慮αt的影響,建立的豬胰脂肪酶水解花椒籽油的動力學模型為:

此模型對實驗結果預測性較好,可用于描述豬胰脂肪酶水解花椒籽油的動力學過程。
3.3 豬胰脂肪酶水解花椒籽油的二次回歸數學模型為Y =41.51+3.42x1-7.8x2+7.17x3-2.43x21+2.29x22-6.31x32-1.3x1x2+0.16x1x3+2.04x2x3,適宜的酶解條件為溫度50℃、油質量分數30%、酶質量濃度72.9g/L,在此條件下反應4h后水解率達57.13%,各因素對花椒籽油水解的影響順序為:油質量分數>酶質量濃度>溫度。
[1] 楊飛, 祝詩平, 邱青苗. 基于計算機視覺的花椒外觀品質檢測及其MATLAB實現[J]. 農業工程學報, 2008, 24 (1): 198-202.
[2] 張軍華, 楊芳霞, 蘇印泉, 等. 制備生物柴油用高FFA花椒籽油的酸催化降酸[J]. 中國糧油學報, 2008, 23(1): 84-87.
[3] 張氽, 闞建全, 陳宗道. 尿素包合法分離花椒籽油中的α-亞麻酸的正交試驗研究[J]. 中國食品添加劑, 2004, 15(2): 28-31.
[4] 孫輝, 呂秀陽, 陳良. 不同植物油脂在近臨界水中水解反應動力學的比較[J]. 化工學報, 2007, 58(4): 925-929.
[5] CHEW Y H, CHUA L S, CHENG K K, et al. Kinetic study on the hydrolysis of palm olein using immobilized lipase[J]. Biochemical Engineering Journal, 2008, 39(3): 516-520.
[6] JURADO E, CAMACHO F, LUZON G. Kinetic model for the enzymatic hydrolysis of tributyrin in O/W emulsions[J]. Chemical Engineering Science, 2006, 61(15): 5010-5020.
[7] 甘爭艷, 吾滿·江艾力, 夏木西卡馬爾. 無溶劑體系及微乳體系中脂肪酶催化紅花籽油水解的動力學[J]. 催化學報, 2006, 27(9): 810-814.
[8] 王英雄, 侯相林, 王國富, 等. 不同脂肪酶催化亞麻油水解反應性能的比較[J]. 中國油脂, 2003, 28(8): 54-56.
[9] 魏決, 羅雯, 陳玲. 酶法從紫蘇子油中制取α-亞麻酸工藝研究: 脂肪酶水解工藝的探討[J]. 食品科學, 2005, 26(1): 131-133.
[10] YAO Chuanyi, TANG Shaokun, HE Zhimin, et al. Kinetics of lipasecatalyzed hydrolysis of olive oil in AOT/isooctane[J]. Journal of Molecular Catalysis B: Emzymatic, 2005, 35(4): 108-112.
[11] OKADA T, MORRISSEY M T. Production of n-3 polyunsaturated fatty acid concentrate from sardine oil by lipase-catalyzed hydrolysis[J]. Food Chemistry, 2008, 73(7): 1411-1419.
[12] SULAIMAN A Z, MASITAH H, RAMACHANDRAN K B. Unsteadystate kinetics of lipolytic hydrolysis of palm oil in a stirred bioreactor[J].Biochemical Engineering Journal, 2004, 19(1): 81-86.
[13] 陳良, 呂秀陽. 近臨界水中大豆油無催化水解反應動力學研究[J]. 農業工程學報, 2006, 22(4): 230-233.
[14] RAMACHANDRAN K B, SULAIMAN A Z, FONG C S, et al. Kinetic study on hydrolysis of oils by lipase with ultrasonic emulsification[J].Biochemical Engineering Journal, 2006, 32(1): 19-24.
[15] SULAIMAN A Z, HASAN M, RAMACHANDRAN K B. High enzyme concentration model for the kinetics of hydrolysis of oils by lipase[J].Chemical Engineering Journal, 2004, 103(1): 7-11.
[16] CALDERBANK P H. Physical rate processes in industrial fermentation,Part I: the interfacial area in gas-liquid contacting with mechanical agitation[J]. Tans Inst Chem Eng, 1958, 36(6): 443-447.
[17] 鄭毅, 鄭楠, 吳克剛. 固定化脂肪酶選擇性富集魚油ω-3多不飽和脂肪酸甘油酯[J]. 化工學報, 2006, 57(2): 56-61.
[18] ALBASI C, BERTRAND N, RIBA J P. Enzymatic hydrolysis of sunflower oil in a standardized agitated tank reactor[J]. Bioprocess Engineering,1999, 20(9): 77-81.
Kinetics and Optimization of Porcine Pancreatic Lipase-catalyzed Hydrolysis of Prickly Ash Seed Oil
XU Huai-de,TANG Ju,LIU Li-fang
(College of Food Science and Engineering, Northwest A&F University, Yangling 712100, China)
Q556.1
A
1002-6630(2010)15-0055-05
2009-10-19
陜西省農業科技攻關課題(2007K01-10-2)
徐懷德(1964—),男,副教授,本科,主要從事軟飲料、果品蔬菜貯藏與加工、天然產物提取研究。E-mail:xuhuaide@yahoo.com.cn

