三重態類硅烯HB═SiLiF的結構及其與R—H (R=F,OH,NH2)的插入反應
李文佐 祝洪杰 程建波 李慶忠 宮寶安
(煙臺大學化學生物理工學院,山東煙臺 264005)
三重態類硅烯HB═SiLiF的結構及其與R—H (R=F,OH,NH2)的插入反應
李文佐*祝洪杰 程建波 李慶忠 宮寶安
(煙臺大學化學生物理工學院,山東煙臺 264005)
用密度泛函理論(DFT)和二次組態相互作用(QCISD)方法研究了三重態類硅烯HB═SiLiF的結構及其與RH(R=F,OH,NH2)的插入反應.計算結果表明,類硅烯HB═SiLiF有三種平衡構型,其中四元環構型能量最低,是其存在的主要構型.HB═SiLiF與HF,H2O和NH3發生插入反應的機理相同.QCISD/6-311++G(d,p)// B3LYP/6-311+G(d,p)計算的三個反應的勢壘分別為124.85,140.67和148.16 kJ·mol-1,反應熱分別為-2.22,20.08和23.22 kJ·mol-1.相同條件下發生插入反應時,反應活性都是H—F>H—OH>H—NH2.
插入反應;類硅烯HB═SiLiF;B3LYP;QCISD
類硅烯(silylenoid)是硅烯(silylene)的一種衍生物,通常可以表示為R1R2SiMX(M為堿金屬原子, X為鹵素原子).一般來說類硅烯比其相對應的硅烯穩定,在有機合成中類硅烯是一種重要的有機硅活性中間體.最近二十多年,人們對類硅烯進行了大量研究.1995年,Tamao和Kawachi[1]首次對類硅烯進行了實驗研究,他們證實了類硅烯Ph2SiLi(OBu-t) ([(tert-butoxy)diphenylsilyl]lithium)的存在并研究了其性質.2004年,Lee等[2]在室溫下合成了穩定的類硅烯(Tsi)X2SiLi(Tsi=C(SiMe3)3;X=Br,Cl).2006年,Molev等[3]報道了第一個成功分離出的含F類硅烯(R3Si)2SiFLi·3THF(R3Si=t-Bu2MeSi)的分子結構.其它一些實驗[4-12]也證實類硅烯是重要的活性中間體.對類硅烯的理論研究也很多.自從Clark等[13]首次用從頭算方法研究了最簡單的類硅烯H2SiLiF的結構,至今人們已較系統地研究了多種類硅烯的結構、穩定性、異構化反應、插入反應、加成反應、取代反應和消去反應等[14-37].
與卡賓不同,大部分硅烯的基態是單重態[38-40].因此,以往所研究的類硅烯也均是單重態.然而,人們也發現有些硅烯的基態是三重態[41-47].那么,基態為三重態的類硅烯是否也存在?如果存在,其結構、穩定性與反應性如何?本文中我們通過理論計算,發現了一些基態為三重態的類硅烯,HB═SiLiF是其中之一.插入反應是類硅烯較常見的反應類型[36-37],本文研究了HB═SiLiF的結構及其與RH(R=F, OH,NH2)的插入反應.
1 計算方法
本工作所用研究方法與我們以往對類硅烯的研究所用方法相同[30-31,35,37].利用密度泛函理論(DFT) B3LYP[48-49]方法優化所有駐點的構型,計算時選擇6-311+G(d,p)基組[50].對優化所得的每一個構型在相同計算水平上進行振動頻率分析計算以確定駐點性質.對涉及的過渡態構型,在同一計算水平上進行內稟反應坐標(IRC)[51]計算.為了進一步考慮相關能,在優化構型上對各個物種進行了 QCISD[52-53]/6-311++G(d,p)單點能量計算.如無特殊說明,文中能量均指QCISD/6-311++G(d,p)//B3LYP/6-311+G(d,p)水平上計算所得的能量,并在B3LYP/6-311+G(d,p)水平上進行零點能校正.所有計算均采用Gaussian 03[54]程序.
2 結果和討論
眾所周知,硅烯H2Si:的基態是單重態[55].然而,計算發現硅烯HB═Si:的基態是三重態.硅烯HB═Si:的示意圖見圖1.從表1可以看出,三重態的HB═Si:的能量比單重態的HB═Si:的能量低58.87 kJ·mol-1,因此三重態的HB═Si:比單重態的HB═Si:穩定.三重態類硅烯HB═SiLiF可看作三重態的HB═Si:與LiF結合而成.事實上,我們也計算了單重態的類硅烯HB═SiLiF,結果發現HB═SiLiF的單重態的能量比三重態的高.在QCISD/6-311++G (d,p)//B3LYP/6-311+G(d,p)水平上,單重態比三重態的能量高9.46 kJ·mol-1.因此本文只報道三重態的HB═SiLiF的相關結果,下文出現的HB═SiLiF均指三重態.B3LYP/6-311+G(d,p)優化的HB═SiLiF的可能構型在圖2給出.各構型的總能量、零點振動能和相對能量列于表2.
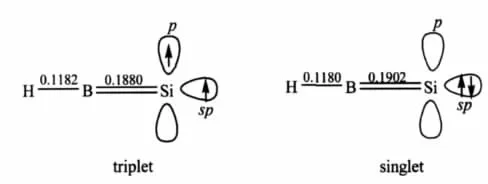
圖1 硅烯HB═Si:的示意圖Fig.1 Schematic diagram of silylene HB═Si: bond length in nm
2.1 HB═SiLiF的平衡構型
B3LYP/6-311+G(d,p)計算表明三重態類硅烯HB═SiLiF有三種平衡構型(圖2中1-3).如圖2所示,構型1是四元環結構.構型1中所有原子在同一平面內,該構型屬于Cs點群.構型1中的Li—F鍵比LiF中的長0.0176 nm,B—Si鍵比HB═Si:中的長0.0077 nm,說明構型1中的Li—F鍵和B—Si鍵比LiF和HB═Si:中的鍵弱.在三個構型中構型1能量最低.構型1的能量比HB═Si:和LiF的能量之和低133.68 kJ·mol-1.構型2是三元環結構,也屬于Cs點群.構型2可看作LiF的Li端和F端分別接近Si的sp和p軌道形成Si—Li和F—Si授受鍵從而形成的配合物.構型2中Li—F鍵比LiF中的長0.0131 nm,B—Si鍵則比HB═Si:中的短0.0016 nm,說明構型2中的Li—F鍵比LiF中的弱,而B—Si鍵比HB═Si:中的強.構型2的能量比HB═Si:和LiF的能量和低65.44 kJ·mol-1.從表2可以看出,構型2的能量比構型1的能量高68.24 kJ·mol-1.從圖2可以看出,構型3幾乎是一個線型結構.構型3中Li—F鍵比LiF中的長0.0014 nm,B—Si鍵則比HB═Si:中的短0.0017 nm,說明構型3中的Li—F鍵比LiF中的弱,而B—Si鍵比HB═Si:中的強.構型3的能量比HB═Si:和LiF的能量和低42.13 kJ·mol-1,比構型1的能量高91.55 kJ·mol-1(見表2).
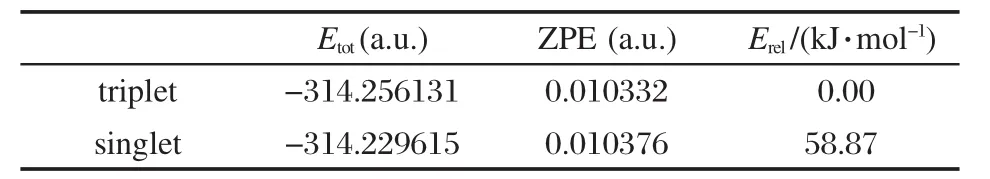
表1 硅烯HB═Si:的三重態和單重態的總能量(Etot)、零點振動能(ZPE)和相對能量(Erel)Table 1 Total energies(Etot),zero-point vibrational energies(ZPE),and relative energies(Erel)of the triplet and singlet silylene HB═Si:

圖2 B3LYP/6-311+G(d,p)水平上優化的HB═SiLiF構型Fig.2 Optimized configurations of HB═SiLiF calculated at the B3LYP/6-311+G(d,p)levelbond length in nm and angle in degree
總之,類硅烯HB═SiLiF有三種平衡構型,從各自的能量比較各構型的穩定性順序應為1>2>3.
2.2 HB═SiLiF與R—H(R=F,OH,NH2)的插入反應
類硅烯HB═SiLiF與R—H(R=F,OH,NH2)的插入反應按下式進行:
HB═SiLiF+R—H→HB═SiRH+LiF
如前所述,三重態類硅烯HB═SiLiF的四元環結構(即構型1)能量最低,應該是其存在的主要構型,因此在研究HB═SiLiF與R—H(R=F,OH,NH2)的插入反應時把構型1作為反應物.下文所提及的HB═SiLiF均指構型1.反應僅考慮三重態勢能面.計算發現,發生插入反應時,先經歷一個前驅體復合物(用Q表示),然后經歷一個過渡態(TS)和一個中間體(IM)到達產物(P).B3LYP/6-311+G(d,p)構型優化所得各個駐點的幾何構型如圖3所示.各個駐點的相對能量列于表3.
2.2.1 前驅體復合物
從圖3可以看出,三個前驅體復合物Q1、Q2和Q3有類似的結構.前驅體復合物中的“HB═SiLiF”部分與構型1非常接近.Si,H2和X(X=F,O,N)原子幾乎在一條線上,即X=F時,θ(SiH2F2)=179.4°;當X=O時,θ(SiH2O)=179.2°;當X=N時,θ(SiH2N)= 179.4°.從表3可以看出,每一個插入反應的前驅體復合物的能量比反應物(HB═SiLiF+R—H)的總能量低,即X=F時,低12.68 kJ·mol-1;X=O時,低6.36 kJ·mol-1;X=N時,低2.22 kJ·mol-1.
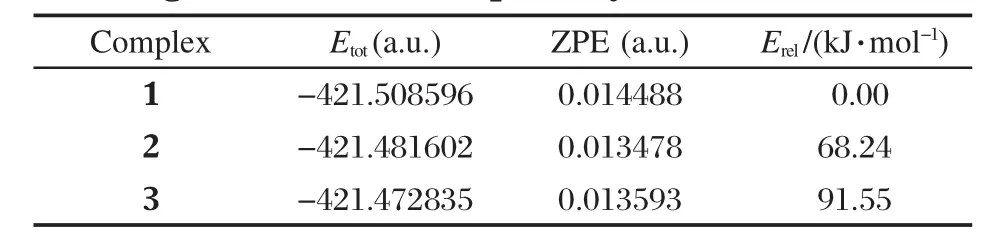
表2 類硅烯HB═SiLiF各構型的總能量(Etot)、零點振動能(ZPE)和相對能量(Erel)Table 2 Total energies(Etot),vibrational zero-point energies(ZPE),and relative energies(Erel)of the configurations of the triplet silylenoid HB═SiLiF
2.2.2 過渡態
從圖3可以看出,三個過渡態TS1、TS2和TS3也有類似的結構.每個過渡態結構中都有一個三元環X—Si—H2(X=F,O,N).各過渡態中的Si—F鍵均比HB═SiLiF中的Si—F鍵略短,即R=F時,短0.0066 nm;R=O時,短0.0034 nm;R=N時,短0.0036 nm.三個過渡態中的R—H2鍵鍵長均比反應物RH中的長,即TS1中,F2—H2鍵(0.1275 nm)比HF中F—H鍵(0.0922 nm)長0.0353 nm;TS2中,O—H2鍵(0.1304 nm)比H2O中的O—H鍵(0.0962 nm)長0.0342 nm;TS3中,N—H2鍵(0.1405 nm)比NH3中N—H鍵(0.1015 nm)長0.0390 nm.R—H鍵鍵長的明顯增大意味著該鍵將要斷裂,同時新的Si—H2鍵和Si—X鍵將要形成.
頻率分析計算表明三個過渡態均存在唯一的虛頻.在B3LYP/6-311+G(d,p)水平上,TS1,TS2和TS3的虛頻分別為1297.5i,1490.5i和1528.8i cm-1.IRC計算表明,過渡態連接前驅體復合物與中間體.過渡態TS1,TS2和TS3相對于各自前驅體復合物(Q)的相對能量分別為124.85,140.67和148.16 kJ·mol-1(見表3).
2.2.3 中間體和產物
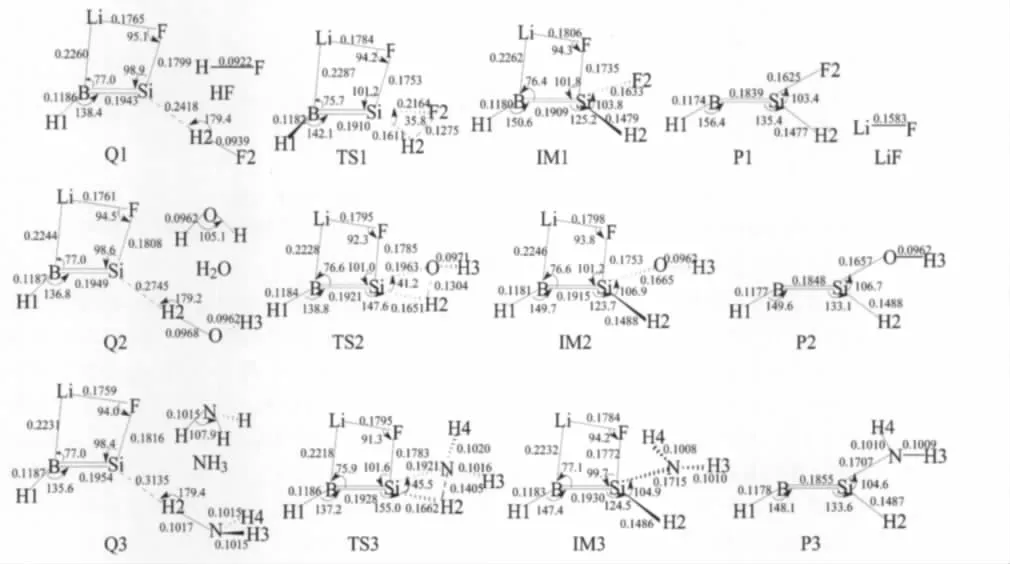
圖3 B3LYP/6-311+G(d,p)水平上優化的反應HB═SiLiF+R—H各駐點的構型Fig.3 Geometries of the stationary points in the reaction HB═SiLiF+R—H calculated at the B3LYP/6-311+G(d,p)levelbond length in nm and angle in degree
IM1,IM2和IM3分別是三個插入反應的中間體(見圖3).很明顯,三個中間體也具有類似的結構.比較中間體與對應過渡態的結構,可以看出,中間體的θ(XSiH2)(X=F,O,N)鍵角明顯大于過渡態的θ(XSiH2)鍵角,即IM1的θ(F2SiH2)(103.8°)比TS1的鍵角θ(F2SiH2)(35.8°)大68.0°;IM2的θ(OSiH2) (106.9°)比TS2的θ(OSiH2)(41.2°)大65.7°;IM3的θ(NSiH2)(104.9°)比TS3的θ(NSiH2)(45.5°)大59.4°.中間體構型中,R—H2鍵已完全斷裂.三個中間體中的Si—H2鍵和Si—X(X=F,O,N)鍵均比各自對應的過渡態中的Si—H2鍵和Si—X鍵短,即IM1中的Si—H2鍵(0.1479 nm)比TS1中Si—H2鍵(0.1611 nm)短0.0132 nm,Si—F2鍵(0.1633 nm)比TS1中Si—F2鍵(0.2164 nm)短0.0531 nm;IM2中的Si—H2鍵(0.1488 nm)比TS2中Si—H2鍵(0.1651 nm)短0.0163 nm,Si—O鍵(0.1665 nm)比TS2中的Si—O鍵(0.1963 nm)短0.0298 nm;IM3中Si—H2鍵(0.1486 nm)比 TS3中 Si—H2鍵(0.1662 nm)短0.0176 nm,Si—N鍵(0.1715 nm)比TS3中Si—N鍵(0.1921 nm)短0.0206 nm.說明新的Si—H2和Si—X鍵已經基本形成.從表3可以看出,反應過程的各個駐點中中間體的能量最低.IM1,IM2和IM3相對于各自前驅體復合物的相對能量分別為-205.56,-177.69和-157.78 kJ·mol-1(見表3).
P1,P2和P3(見圖3)分別是三個中間體IM1, IM2和IM3解離掉LiF后的產物.計算表明,解離過程為能量單調升高的無勢壘過程.P1,P2和P3均屬于Cs點群.從表3可以看出,三個插入反應的產物(HB═SiRH+LiF)的能量均比各自的前驅體復合物的能量高,R=F,OH,NH2時,產物能量分別比復合物能量高10.46、26.44和25.44 kJ·mol-1.
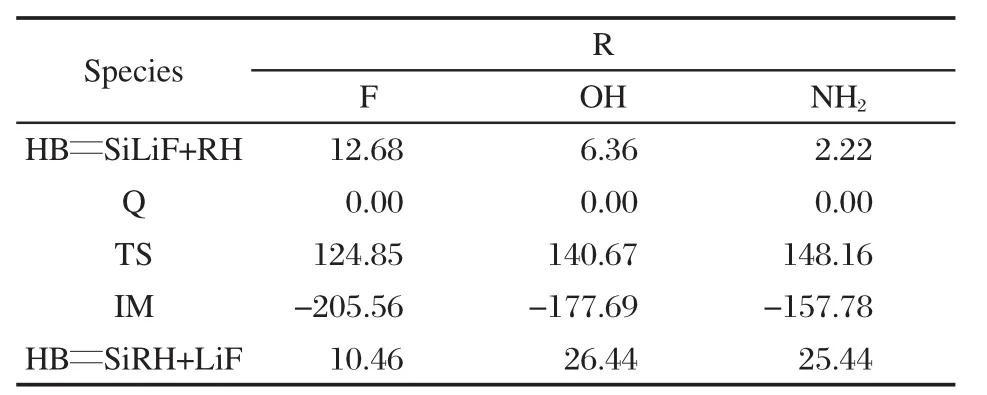
表3 反應HB═SiLiF+R—H的反應物、過渡態、中間體和產物的相對能量(kJ·mol-1)Table 3 Relative energies(in kJ·mol-1)of reactants, transition states,intermediates,and products in the reaction HB═SiLiF+R—H
2.2.4 插入反應的機理分析
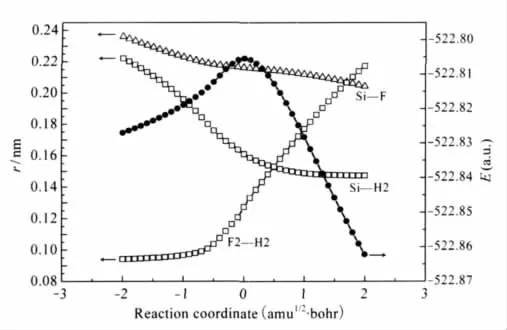
圖4 HB═SiLiF與HF反應的能量和鍵長隨反應坐標的變化曲線Fig.4 Potential energy and bond distance profiles along the reaction coordinates for the reaction of HB═SiLiF and HF
以HB═SiLiF與HF反應為例.以計算的TS1為起始點,在B3LYP/6-311+G(d,p)水平上沿著反應途徑分別向前和向后進行了20個點的IRC計算,所用步長為0.15 a.u..圖4給出了IRC計算所得的能量及鍵長隨反應坐標變化的曲線圖.從圖4可以很直觀地看出,隨著插入反應的進行,F2—H2鍵逐漸拉長乃至斷裂.Si—F2和Si—H2鍵逐漸縮短.
反應過程各個駐點的原子上的電荷變化可以反映反應機理.在B3LYP/6-311+G(d,p)水平上計算了各個前驅體復合物、過渡態、中間體和產物的Mulliken電荷.結果發現,過渡態中的X(X=F,O,N)原子和H2原子上的負電荷都比它們在復合物中的更多,Si原子上的正電荷則比在復合物中的更多.中間體中的X(X=F,O,N)原子和H2原子上的負電荷都比它們在過渡態中的更多.這同樣可以反映出反應過程中X—H鍵的斷裂和Si—H2與Si—X鍵的生成.
2.2.5 三個插入反應的比較
雖然HB═SiLiF與R—H(R=F,OH,NH2)發生插入反應的機理相同,但反應的難易程度不同. QCISD/6-311++G(d,p)//B3LYP/6-311+G(d,p)水平計算的HB═SiLiF與HF,H2O和NH3插入反應的勢壘分別為124.85、140.67和148.16 kJ·mol-1(見表3),反應熱分別為-2.22、20.08和23.22 kJ·mol-1.因此,不管是從熱力學角度還是從動力學角度看,在相同條件下發生插入反應時,反應活性順序都是H—F>H—OH>H—NH2,即相同條件下,HF最容易與HB═SiLiF發生插入反應,H2O次之,NH3則最難.這個順序與RH中H原子上的電荷分布情況相一致:B3LYP/6-311+G(d,p)水平計算的HF,H2O和NH3的 H原子上的Mulliken電荷分別為 0.286e、0.253e和0.227e,當發生類似的親核反應時,反應活性順序應該是H—F>H—OH>H—NH2.HB═SiLiF與R—H(R=F,OH,NH2)的插入反應與其它類硅烯[37]與R—H(R=F,OH,NH2)發生插入反應的情況類似.
3 結 論
應用DFT B3LYP和QCISD方法首次研究了三重態類硅烯HB═SiLiF的結構及其與R—H(R= F,OH,NH2)的插入反應.構型優化計算表明三重態的HB═SiLiF有三種平衡構型,其中四元環結構能量最低,是其存在的主要構型.HB═SiLiF與HF, H2O和NH3發生插入反應的機理相同:反應歷程均經過一個帶有三元環結構部分的過渡態和一個中間體到達產物.相同條件下,HF最容易與HB═SiLiF發生插入反應,H2O次之,NH3則最難.本文結果進一步豐富了類硅烯的研究內容,并為實驗上尋找三重態類硅烯提供了理論參考信息.
1 Tamao,K.;Kawachi,A.Angew.Chem.Int.Edit.,1995,34:818
2 Lee,M.E.;Cho,H.M.;Lim,Y.M.;Choi,J.K.;Park,C.H.;Jeong, S.E.;Lee,U.Chem.Eur.J.,2004,10:377
3 Molev,G.;Bravo-Zhivotovakii,D.;Karni,M.;Tumanskii,B.; Botoshansky,M.;Apeloig,Y.J.Am.Chem.Soc.,2006,128:2784
4 Boudjouk,P.;Samaraweera,U.Angew.Chem.Int.Edit.,1988,27: 1355
5 Tamao,K.;Kawachi,A.Organometallics,1995,14:3108
6 Tamao,K.;Kawachi,A.Pure Appl.Chem.,1999,71:393
7 Sekiguchi,A.;Lee,V.Y.;Nanjo,M.Coord.Chem.Rev.,2000, 210:11
8 Wiberg,N.;Niedermayer,W.J.Organomet.Chem.,2001,628:57
9 Likhar,P.R.;Zirngast,M.;Baumgartner,J.;Marschner,C.Chem. Commun.,2004:1764
10 Kawachi,A.;Oishi,Y.;Kataoka,T.;Tamao,K.Organometallics, 2004,23:2949
11 Lim,Y.M.;Cho,H.M.;Lee,M.E.;Baeck,K.K.Organometallics, 2006,25:4960
12 Harloff,J.;Popowski,E.;Reinke,H.J.Organomet.Chem.,2007, 692:1421
13 Clark,T.;Schleyer,P.R.J.Organomet.Chem.,1980,191:347
14 Feng,S.;Feng,D.;Deng,C.Chem.Phys.Lett.,1993,214:97
15 Tanaka,Y.;Kawachi,A.;Hada,M.;Nakatsuji,H.;Tamao,K. Organometallics,1998,17:4573
16 Feng,S.;Feng,D.;Li,J.Chem.Phys.Lett.,2000,316:146
17 Feng,S.;Feng,D.J.Mol.Struct.-Theochem,2001,514:171
18 Feng,S.;Feng,D.;Li,M.;Bu,Y.Chem.Phys.Lett.,2001,339: 103
19 Feng,S.;Feng,D.;Li,M.;Zhou,Y.Int.J.Quantum Chem.,2002,87:360
20 Feng,S.;Zhou,Y.;Feng,D.J.Phys.Chem.A,2003,107:4116
21 Feng,D.;Xie,J.;Feng,S.Chem.Phys.Lett.,2004,396:245
22 Feng,S.;Lai,G.;Zhou,Y.;Feng,D.Chem.Phys.Lett.,2005,415: 327
23 Flock,M.;Marschner,C.Chem.Eur.J.,2005,11:4635
24 Xie,J.;Feng,D.;Feng,S.;Zhang,J.J.Mol.Struct.-Theochem, 2005,755:55
25 Xie,J.;Feng,D.;He,M.;Feng,S.J.Phys.Chem.A,2005,109: 10563
26 Xie,J.;Feng,D.;Feng,S.J.Organomet.Chem.,2006,691:208
27 Xie,J.;Feng,D.;Feng,S.Struct.Chem.,2006,17:63
28 Xie,J.;Feng,D.;Feng,S.J.Comput.Chem.,2006,27:933
29 Xie,J.;Feng,D.;Feng,S.;Zhang,J.Chem.Phys.,2006,323:185
30 Li,W.Z.;Gong,B.A.;Cheng,J.B.Acta Phys.-Chim.Sin.,2006, 22:653 [李文佐,宮寶安,程建波.物理化學學報,2006,22: 653]
31 Li,W.Z.;Gong,B.A.;Cheng,J.B.;Xiao,C.P.Acta Chim.Sin., 2007,65:1573 [李文佐,宮寶安,程建波,肖翠平.化學學報, 2007,65:1573]
32 Xie,J.;Feng,D.;Feng,S.;Ding,Y.Struct.Chem.,2007,18:65
33 Xie,J.;Feng,D.;Feng,S.J.Phys.Chem.A,2007,111:8475
34 Qi,Y.;Feng,D.;Feng,S.J.Mol.Struct.-Theochem,2008,856: 96
35 Li,W.Z.;Cheng,J.B.;Gong,B.A.;Yu,J.K.;Sun,J.Z.Acta Phys.-Chim.Sin.,2008,24:901 [李文佐,程建波,宮寶安,于健康,孫家鐘.物理化學學報,2008,24:901]
36 Qi,Y.;Feng,D.;Li,R.;Feng,S.J.Organomet.Chem.,2009,694: 771
37 Li,W.Z.;Cheng,J.B.;Gong,B.A.;Yu,J.K.;Sun,J.Z.Acta Chim.Sin.,2009,67:756 [李文佐,程建波,宮寶安,于健康,孫家鐘.化學學報,2009,67:756]
38 Holthausen,M.C.;Koch,W.;Apeloig,Y.J.Am.Chem.Soc., 1999,121:2623
39 Jiang,P.;Gaspar,P.P.J.Am.Chem.Soc.,2001,123:8622
40 Hill,N.J.;West,R.J.Organomet.Chem.,2004,689:4165
41 Cramer,C.J.;Falvey,D.E.Tetrahedron Lett.,1994,35:4943
42 Tachikawa,H.;Yamada,Y.;Lyama,T.Can.J.Chem.,1999,77: 1419
43 Gaspar,P.P.;Xiao,M.;Pae,D.H.;Berge,D.J.;Haile,T.;Chen, T.;Lei,D.;Winchester,W.R.;Jiang,P.J.Organomet.Chem., 2002,646:68
44 Yoshida,M.;Tamaoki,N.Organometallics,2002,21:2587
45 Sekiguchi,A.;Tanaka,T.;Ichinohe,M.;Akiyama,K.; Tero-Kubota S.J.Am.Chem.Soc.,2003,123:4962
46 Xu,Y.;Zhang,Y.;Li,J.J.Phys.Chem.C,2007,111:3729
47 Skryshevski,Y.;Piryatinski,Y.;Vakhnin,A.;Blonsky,I.; Kadashchuk,A.;Ne"pu?rek,S.Optical Materials,2007,30:384
48 Becke,A.D.J.Chem.Phys.,1993,98:5648
49 Lee,C.;Yang,W.;Parr,R.G.Phys.Rev.B,1988,37:785
50 Hehre,W.J.;Radom,L.;Schleyer,P.v.R.;Pople,J.A.Ab initio molecular orbital theory.New York:Wiley,1986
51 Gonzalez,C.;Schlegel,H.B.J.Phys.Chem.,1991,95:5853
52 Gauss,J.;Cremer,C.Chem.Phys.Lett.,1988,150:280
53 Salter,E.A.;Trucks,G.W.;Bartlett,R.J.J.Chem.Phys.,1989, 90:1752
54 Frisch,M.J.;Trucks,G.W.;Schlegel,H.B.;et al.Gaussian 03. Revision B.03.Pittsburgh,PA:Gaussian Inc.,2003
55 Apeloig,Y.;Pauncz,R.;Karni,M.;West,R.;Steiner,W.; Chapman,D.Organometallics,2003,22:3250
Structures of the Triplet Silylenoid HB═SiLiF and Its Insertion Reactions with R—H(R=F,OH,NH2)
LI Wen-Zuo*ZHU Hong-Jie CHENG Jian-Bo LI Qing-Zhong GONG Bao-An
(Chemistry and Biology College,Yantai University,Yantai 264005,Shandong Province,P.R.China)
Density functional theory(DFT)and quadratic configuration interaction with single and double excitations (QCISD)methods were used to investigate the geometries of the triplet silylenoid HB═SiLiF as well as its insertion reactions with RH(R=F,OH,NH2).The calculated results indicated that HB═SiLiF has three equilibrium structures wherein the four-membered ring structure had the lowest energy and it was the most stable structure.The mechanisms of the insertion reactions for HB═SiLiF with HF,H2O,and NH3were identical.The QCISD/6-311++G(d,p)//B3LYP/ 6-311+G(d,p)calculated potential energy barriers of the three reactions were 124.85,140.67,and 148.16 kJ·mol-1,and the reaction heats for the three reactions were-2.22,20.08,and 23.22 kJ·mol-1,respectively.Under the same conditions,the insertion reactions should occur easily according to the following order:H—F>H—OH>H—NH2.
Insertion reaction;Silylenoid HB═SiLiF;B3LYP;QCISD
O641.12
Received:March 17,2010;Revised:April 6,2010;Published on Web:June 29,2010.
*Corresponding author.Email:liwenzuo2004@126.com;Tel:+86-535-6902063.
The project was supported by the Natural Science Foundation of Shandong Province,China(ZR2009BQ006),Open Fund of the State Key Laboratory
of Supramolecular Structure and Materials(Jilin University,China)(SKLSSM200909),and Fund for Doctor of Yantai University,China(HY05B30, HY05B36).
山東省自然科學基金(ZR2009BQ006),超分子結構與材料國家重點實驗室(吉林大學)開放基金(SKLSSM200909)和煙臺大學博士科研基金
(HY05B30,HY05B36)資助項目
?Editorial office of Acta Physico-Chimica Sinica

