增殖誘導配體和受體在大腸癌中的表達及其臨床意義
于 杰,龔治林 (長江大學荊州臨床醫學院 荊州市中心醫院胃腸外科,湖北 荊州 434020)
增殖誘導配體和受體在大腸癌中的表達及其臨床意義
于 杰,龔治林
(長江大學荊州臨床醫學院 荊州市中心醫院胃腸外科,湖北 荊州 434020)
目的:觀察增殖誘導配體(APRIL)及其受體在大腸癌的表達,并探討其臨床意義。方法:應用熒光定量RT-PCR方法檢測大腸癌40份、12份潰瘍性結腸炎、12份腸克羅恩病、12份管狀腺瘤、12份家族腺瘤性息肉、12份正常大腸粘膜中APRIL及其受體的表達,并分析其臨床病理特征的關系。結果:顯示在管狀腺瘤、家族性腺瘤性息肉和大腸癌組織中APRIL及受體HSPG表達水平顯著高于正常對照組、潰瘍性結腸炎和腸克羅恩病(P<0.05),在大腸癌組織中表達水平顯著高于管狀腺瘤和家族性腺瘤性息肉(P<0.05)。結論:APRIL在大腸癌的病變演進過程中呈現累積和漸進趨勢。
大腸癌;增值誘導配體;受體
在世界范圍內,大腸癌年發病近120萬例,發病率在男性惡性腫瘤中排第4位,在女性惡性腫瘤中排第3位[1]。據美國癌癥學會估計,2009年美國有146970例大腸癌新發患者,并有49920例患者死于大腸癌[2]。在我國,2002年大腸癌年齡標化發病率為男性13.6/10萬人,女性9.2/10萬人[3]。研究顯示,早中期大腸癌術后5年生存率高達90%以上,甚至可以長期生存,而晚期大腸癌術后5年生存率僅為50%左右,如術后出現吻合口漏等并發癥,其術后5年生存率僅30%左右[4],因此早期發現大腸癌非常重要。
增殖誘導配體(a proliferation-inducing ligand,APRIL)是腫瘤壞死因子tumor necrosis factor,TNF) 超家族的新成員,可在多種消化道腫瘤中表達,因此有望作為一種腫瘤標志物通過非侵入性來診斷大腸癌。我們熒光RT-PCR法檢測APRIL和它的三個受體TACI、BCMA、HSPG在大腸癌發生各階段組織中的表達情況,探討其在大腸癌發生發展中的作用及其相互關系,旨在為大腸癌的早期診斷和尋找抗癌治療的靶分子提供理論依據。
1 對象與方法
1.1對象100例患者大腸標本中,其中大腸癌40例為我院胃腸外科手術切除標本,其余60份為荊州市中心醫院內鏡中心內鏡下活檢組織,正常大腸粘膜、潰瘍性結腸炎、腸克羅恩病、管狀腺瘤、家族性腺瘤性息肉各12例。所有患者取材前未受過放、化療或生物治療等干預治療。所有標本組織手術切除后于30min內迅速放入液氮,后移至-80℃冰箱凍存,并術后經病理學鑒定證實。
1.2方法
1.2.1 主要試劑 Trizol試劑 (上海生工生物工程公司);cDNA逆轉錄試劑盒 (上海奇康生物科技有限公司);0.5ml dNTP;10×PCR 緩沖液;DiamondTM 250bp DNA Marker;1000U DiamondTM Taq DNA Polymerase ;DEPC;瓊脂糖(均購自上海生工生物工程公司);其他:75%乙醇(RNase free)、氯仿、異丙醇、TAE電泳緩沖液、6×上樣緩沖液等。APRIL、TACI、BCMA、HSPG和β2微球蛋白定量標準品 (上海奇康生物科技有限公司)。
1.2.2實驗設備 DY-501 B型電泳儀(上海琪特分析儀器有限公司),THZ-C恒溫振蕩器(江蘇太倉實驗設備廠),AllegraTM 64R臺式高速離心機(美國Backman-Coulter 公司),U-00800 200V DioE ARRAY BIO PHOTOME核酸紫外檢測儀(日本HITACHI公司),Dolphin-Doc凝膠成像系統(美國WEAITEC公司)LightCycler熒光PCR儀及軟件系統(美國羅氏公司)
1.2.3 引物設計及合成 應用primer premer5.0引物設計軟件,設計APRIL、TACI、BCMA、HSPG、內參照基因β2M的引物,由上海生工生物工程公司合成。引物長度分別為APRIL(150bp)、TACI(113bp)、BCMA(142bp)、HSPG(224bp)、β2M(100bp)。
1.2.4RNA提取及逆轉錄反應 Trizol法提取組織總RNA,核酸蛋白紫外分析儀檢測RNA質量和濃度。將逆轉錄試劑盒從-20℃冰箱取出后室溫融化。取0.2ml的離心管依次加入模板RNA 0.1~5μg,引物Oligo(dT)18(0.5μg/μl) 1μl,DEPC水至12μl,將試管移至PCR儀中用Instant Incubate 程序70℃孵育5min,冰上冷卻至少1min后離心片刻。再按以下順序加入其余試劑5×Reaction buffer 4μl,Ribonuclease inhibitor(20U/μl) 1μl,10mmol/L dNTP mix 2μl,升至70℃,10min以終止反應,隨后冰上冷卻,將反應生成的cDNA分裝,并放入-20℃冰箱保存備用。
1.2.5AP RI L及其受體mRNA含量測定 冰上在0.5ml PCR管內依次加入:10×PCR 緩沖液 2.5μl,25mmol/L MgCl21.5μl,10pmol/μl目的基因上游引物 0.5μl,10pmol/μl目的基因下游引物 0.5μl,10pmol/μl β2上游引物1.0μl,10pmol/μl β2下游引物1.0μl,cDNA模板 1.0μl,1U/μlTaq DNA聚合酶 0.2μl。混勻后加入Roche專用毛細管中各反應 管于Roche熒光定量檢測儀(Lighcycler) 進 行 PCR擴增,94℃,3min,預變性;94℃,30s→54℃,30s→72℃,50s共30個循環。根據各自標準品建立的標準曲線,軟件自動計算 出待測樣本中靶基因或p M mR NA的準確含量。
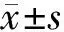
2 結 果
2.1組織總RNA純度與完整性鑒定電泳結果觀察到28、18s兩條清晰的條帶,紫外分光光度計檢測260/280nm的值在1.7~2.2之間才用于進行cDNA合成。
2.2APRIL及其受體的擴增產物特異性鑒定APRIL(150bp)、 BCMA (142bp) 、TACI (113bp)、和 HSPG (224bp)擴增片段經 1.5%瓊脂糖凝膠電泳,擴增片段長度與理論大小一致。
2.3APRIL及受體PCR批內和批間重復性檢測見表1。

表1 APRIL及受體PCR批內和批間重復性檢測結果
2.4APRIL及其受體mRNA的RFQ-PCR檢測結果見表2。結果顯示,在管狀腺瘤、家族性腺瘤性息肉生和大腸癌組織中APRIL及受體HSPG表達水平顯著高于正常對照組、潰瘍性結腸炎和腸克羅恩病(P<0.05),在大腸癌組織中表達水平顯著高于管狀腺瘤和家族性腺瘤性息肉(P<0.05)。APRIL在大腸癌的病變演進過程中呈現累積和漸進趨勢。

表2 大腸癌及對照組織中APRIL及其受體mRNA的水平
注:與正常對照組、潰瘍性結腸炎組和腸克羅恩病組相比,*P<0.05;與管狀腺瘤組相比,#P<0.05;與家族性腺瘤性息肉組相比,△P<0.05。
3 討 論
大腸癌是一種常見的惡性腫瘤,在西方發達國家其發病率居惡性腫瘤譜的第二位。隨著人們生活水平的提高、飲食習慣的改變,我國大腸癌的發病率也日漸增高,已躍居第3~5位。上世紀90年代與70年代相比,我國大腸癌的發病率在城市上升了31.95%,在農村上升了8.51%[5]。
大腸癌不同于其他腫瘤,它一般先由正常粘膜上皮轉變成腺瘤再變成腺癌的過程,很少有一開始就表現惡性的情況。如果能在大腸癌發生前通過對某些分子的檢測達到對其的預警或預測,使其早期能確診,這對降低大腸癌的發病率或提套臨床治愈率有重要意義,但目前仍無單一的分子檢測能進行早期預警。
增值誘導配體(APRIL)亦稱為TAIL-2、TRDL-1和TNASF-13a,1998年首先由 Ha h n e等[6-7]發現并克隆成功。研究發現,APRIL主要通過靶細胞表面的2個受體[穿膜蛋白活化物(transmembrane activator and CAML interaor,TAC)和B細胞成熟抗原(B cell maturation antigen,BCMA) ] 結合, 從而促進腫瘤細胞的增殖,調節體液免疫,并參與B、T淋巴細胞增殖和活化。人BCMA由TNFRS F17編碼,由185個氨基酸組成,胞外區具有50個氨基酸,包括1個富含半胱氨酸結構域(CRD),主要分布在活化的B淋巴細胞中,多發性骨髓瘤細胞系亦高表達,人TACI由TNFRSF13B編碼,定位于17p11.2,由293個氨基酸組成,胞外含有2個CRD,主要分布于B淋巴細胞和活化的T細胞表面。人HSPG基因位于1p36.1,根據不同的核心蛋白和葡胺聚糖鏈HSPG包括大約10余種不同的蛋白聚糖,在哺乳動物主要表達在細胞表面或存在于細胞基底膜和細胞外基質中[8-13]。
我們通過熒光RT-PCR方法測定了APRIL及其受體mRNA在正常大腸粘膜、潰瘍性結腸炎、腸克羅恩病、管狀腺瘤、家族性腺瘤性息肉及大腸癌中的含量,結果發現APRIL在管狀腺瘤、家族腺瘤性息肉及大腸癌中的含量顯著高于正常大腸粘膜、潰瘍性結腸炎及腸克羅恩病(P<0.05),另外APRIL在大腸癌中的含量顯著高于管狀腺瘤及家族腺瘤性息肉(P<0.05),而正常大腸粘膜、潰瘍性結腸炎、腸克羅恩病之間及管狀腺瘤、家族腺瘤性息肉之間APRIL無統計學差異(P>0.05)。以上結果顯示APRIL在結直腸癌的病變、演進過程中呈現累積和漸進趨勢,提示APRIL在大腸癌發生、發展過程中可能起了重要作用,而且有可能成為結直腸癌早期診斷和抗癌治療的靶分子。
總之,通過本研究初步探討了APRIL在大腸癌的不同階段的含量,為以后進一步研究及抗癌藥物的研制提供了一個實驗基礎。
[1]Garcia M,jemal A,Ward EM,etal.Global cancer facts and figures 2007.Atlanta,GA[J].American Cancer Society,2007,78:12.
[2]Jernal A,Siegel R, Ward E,etal.Cancer statistics,2009[J]. CA Cancer J Clin,2009,59:225-249.
[3]Center MM,Jemal A,Ward E,etal.Research articlesinternational trends in colorectal cancer incidence rates cancer epidemioll[J]. Biomarkers Prev,2009,18:1688-1694.
[4]Scholefield JH,Moss S,Sufi F,etal.Effect of faecal occult blood screening on mortality from colorectal cancer:results from a randomized controlled tria1[J]. Gut,2002,50(6):840-844.
[5]LI Lian-di,RAO Ke-qing,ZHANG Si-Wei,etal.statistical analysis of data from 12 cancer registries in China,1993~1997[J]. Bulletin of Chines Cancer,2002,11(9):497-507.
[6]Hahne M,Kataoka T,Schroter M,etal.APRIL, a new ligand of the tumor necrosis factor family,stimulates tumor cell growth[J].Cancer Res,2000,5(12):1021-1027.
[7]Kelly K,Manos E,Jensen G,etal.APRIL/TADL-1.a tumor necrosis factor-like ligand,stimulates cell death[J].Cancer Res,2000,5(12):1021-1027.
[8]Rennert P,Schneider P,Cachero T,etal.A sluble form of B cell maturation antigen,a receptor for the tumor necrosis factor family member APRIL,inhibits tumor cell growth[J]. J Exp Med,2000,192:1677-1684.
[9]Mackay F,Schneider P,Rennert P,etal.BAFF and APRIL:A tutorial on B cell survival[J].Ann Rev Immunol,2003,21(4):231-264.
[10]Roschke V,Sosnovtseva S,Ward C,etal.Blys and APRIL form biologically actibe hetertrimers that are expressed in patients with systemic immune-based rheumatic diseases[J]. J Immunol,2002,168:4314-4321.
[11]Wu Y,Bressette D,Carrell J,etal.Tumor necrosis factor (TNF)receptors superfamily member TACI is a high affibity receptor for TNF family member APRIL and BlyS[J]. J Biol Chem,2000,275:35478-35485.
[12]Yu G,Boone J,Dclaney J,etal.APRIL stimulates B and T cell function by binding BCMA and TACI[J].Nat Immunol ,2000,1(2):252-256.
[13]Stein JV,Lopez-Fraga M,Elustondo FA,etal.APRIL modulates B and T cell immunitu[J]. J Clin Invest,2002,109:1587-1598.
[編輯] 一 凡
10.3969/j.issn.1673-1409(R).2010.03.009
R735.3
A
1673-1409(2010)03-R020-03

