注射用葛根素的細菌內毒素檢查法可行性研究
李 薇,吳 婷
(廣州市藥品檢驗所藥理室,廣東廣州 510160)
葛根素是從豆科植物野葛干燥根中提取的單體,為異黃酮類化合物,臨床及基礎研究證明,該藥具有擴張冠狀動脈和腦血管、降低心肌耗氧量、改善心肌收縮功能、促進血液循環等藥理作用[1-2],臨床上現已用于治療心腦血管及外周血管疾病[3-4]。該品種國家藥品標準WS1-(X-388-1)-2003Z進行熱原檢查[5],未進行細菌內毒素檢查。為考察該品種是否可以用細菌內毒素檢查法來代替熱原檢查法,本文參照《中國藥典》2005年版二部附錄收載的細菌內毒素檢查法對注射用葛根素進行了細菌內毒素檢查研究。
1 儀器與試藥
注射用葛根素(批號:08020301,規格:0.2 g/瓶,華北制藥集團制劑有限公司;批號:20061222,200712131,規格:100 mg/瓶,北京賽生藥業有限公司;批號:20060522,200711303,規格:50 mg/瓶,北京賽生藥業有限公司;批號:07102801,規格:0.4 g/瓶,山東瑞陽制藥有限公司;批號:07121101,規格:0.2 g/瓶,山東瑞陽制藥有限公司;批號:07100401,規格:0.1 g/瓶,山東瑞陽制藥有限公司;批號:07091602,規格:50 mg/瓶,山東瑞陽制藥有限公司);鱟試劑(批號:0807022,規格:0.1 ml/支,標示靈敏度:0.25 EU/ml,湛江安度斯生物有限公司;批號:080506,081012,規格:0.1 ml/支,標示靈敏度:0.25 EU/ml,廈門市鱟試劑實驗廠有限公司鱟試劑);細菌內毒素工作標準品(批號:150601-200860,規格:160 EU/支,中國藥品生物制品檢定所);細菌內毒素檢查用水(批號:0801180,規格:50 ml/支,湛江安度斯生物有限公司);漩渦振蕩器(IKA-MS-1);恒溫水浴箱(德國 Julabo 19A)。
2 方法與結果
2.1 鱟試劑標示靈敏度的復核[6-7]
根據鱟試劑靈敏度的標示值,將細菌內毒素工作標準品用BET水溶解,在漩渦振蕩器上混勻15 min,然后制成2.00λ、1.00λ、0.50λ 和 0.25λ 4個濃度的內毒素標準溶液,按《中國藥典》2005年版二部附錄的細菌內毒素檢查法規定,對湛江安度斯生物有限公司和廈門市鱟試劑實驗廠有限公司兩個廠家的鱟試劑進行靈敏度的復核,鱟試劑靈敏度的測定值(λc)=lg-1(∑X/4),式中 X 為反應終點濃度的對數值(lg),結果見表1。3批鱟試劑靈敏度分別為0.25 EU/ml、0.25 EU/ml和0.42 EU/ml,均在 0.5 λ~2.0 λ 范圍之間,表明 3 批鱟試劑靈敏度均符合規定,可用于細菌內毒素檢查。

表1 鱟試劑靈敏度復核結果Tab.1 The results of tachypleus amebocyte lysate sensitivity test
2.2 注射用葛根素的細菌內毒素限值(L)的確定[6-7]
按《中國藥典》2005年版二部中細菌內毒素檢查法的規定確定細菌內毒素限值。根據公式L=K/M,式中L為供試品的細菌內毒素限值,K為按規定的給藥途徑,人用每公斤體重每小時最大可接受的內毒素劑量,注射劑K=5 EU/(kg·h),M為人用每公斤體重每小時的最大供試品劑量,人均體重按60 kg計算,注射時間若不足1 h,按1 h計算。
從注射用葛根素的產品使用說明書可知本品的最大用藥劑量為600 mg,人均體重以60 kg計,滴注時間按1 h計算,則M=600 mg/60 kg·h=10 mg/(kg·h),L=K/M=[5 EU/(kg·h)]/[10 mg/(kg·h)]=0.5 EU/mg。本品為心血管藥、兒童老人用藥,根據《注射劑安全性檢查法應用指導原則(修訂稿)》的要求安全系數定為3,本品內毒素最終確定限值為L=0.17 EU/mg。
2.3 注射用葛根素的干擾預試驗稀釋倍數的確定[8-9]
目前用于藥品檢驗的市售鱟試劑靈敏度(λ)一般在0.50~0.03 EU/mg范圍內,最小有效稀釋濃度 c=λ/L,L=0.17 EU/mg,故注射用葛根素進行細菌內毒素檢測時,0.50~0.03 EU/mg的鱟試劑相對應的最小有效稀釋濃度為3.00、1.50、0.75、0.38、0.18 mg/ml。
2.4 干擾預試驗試驗[8-9]
取 3 批注射用葛根素(批號:08020301,規格:0.2 g/瓶;批號:200711303,規格:50 mg/瓶;批號:07121101,規格:0.2 g/瓶)各1瓶,分別加BET水適量溶解,制成50 mg/ml的供試品原液,用BET水將供試品原液進行倍比稀釋,制得3.00、1.50、0.75、0.38、0.18 mg/ml共5個濃度梯度的溶液,將此系列濃度溶液標記為供試品管(NPC系列),用上述稀釋液作為溶劑,溶解并稀釋細菌內毒素工作標準品,制得每個稀釋度中細菌內毒素含量均為2 λ(0.5 EU/ml)的注射用葛根素溶液,標記此系列溶液為供試品陽性對照管(PPC系列)。取靈敏度為0.25 EU/ml的湛江安度斯生物有限公司和廈門市鱟試劑實驗廠有限公司兩個不同廠家的鱟試劑進行試驗,每一稀釋度做2管,同時按常規分別設細菌內毒素陽性對照(PC)和檢查用水陰性對照(NC)各2管,結果見表2。

表2 注射用葛根素干擾預試驗結果Tab.2 The results of prerliminary interference test of Puerarin for Injection
由表2結果可知,所用的3批注射用葛根素稀釋到3.0mg/ml濃度的溶液時,有2批樣品對湛江安度斯生物有限公司的鱟試劑與細菌內毒素反應有干擾作用,稀釋到1.5 mg/ml或以下濃度的溶液時,對兩個廠家的鱟試劑與細菌內毒素反應無增強或抑制的干擾作用。
2.5 干擾試驗[6-7]
用兩個廠家的鱟試劑(靈敏度為0.25 EU/ml),按《中國藥典》2005年版二部附錄的細菌內毒素檢查法進行試驗,測定用BET水制成的內毒素標準溶液的反應終點濃度的幾何平均值(Es)和用供試品稀釋液制成的內毒素溶液的反應終點濃度的幾何平均值(Et)。取3批注射用葛根素(批號:08020301,200711303,07121101)各 1 瓶,分別加 BET 水適量溶解,制成50 mg/ml的供試品原液,再用BET水稀釋制成濃度為1.5 mg/ml的供試品稀釋液,用BET水和供試品稀釋液將細菌內毒素工作標準品稀釋成 2.00 λ、1.00 λ、0.50 λ、0.25 λ濃度的BET水系列細菌內毒素溶液和供試品稀釋液系列細菌內毒素溶液,每一稀釋濃度重復4管,同時用上述供試品稀釋液和BET水各做2管陰性對照管,按公式計算BET水和供試品稀釋液反應終點濃度的幾何平均值 (Es和Et),Es=lg-1(∑Xs/4),Et=lg-1(∑Xt/4),結果見表 3。

表3 注射用葛根素的正式干擾試驗結果Tab.3 The results of interference test of Puerarin for Injection
由表 3 結果可知,2 λ 管均為陽性,0.50 λ、0.25 λ 管均為陰性,對于λ=0.25 EU/ml的2組鱟試劑的Es分別為0.25 EU/ml、0.35 EU/ml,Es均在 0.5λ~2.0 λ 范圍內,3 批注射用葛根素測得的 Et均在 0.5 λ~2.0 λ 范圍內,Et和 Es的比值在 0.5~2.0范圍內,說明注射用葛根素在1.5 mg/ml或以下濃度的溶液對兩個不同廠家的鱟試劑與內毒素的反應無增強或抑制的干擾作用,符合《中國藥典》2005年版二部對細菌內毒素檢查有效性的規定,因此可以確定注射用葛根素的最大無干擾濃度為 1.5 mg/ml。
2.6 注射用葛根素的細菌內毒素檢查
取9批注射用葛根素樣品,分別根據“2.5”項下方法制成供試品稀釋液,使用λ=0.25 EU/ml的兩個廠家的鱟試劑進行細菌內毒素檢查,并用此稀釋液將細菌內毒素工作標準品稀釋為2 λ的溶液,作為供試品的陽性對照,另外以細菌內毒素檢查用水建立陽性對照和陰性對照。按 《中國藥典》2005年版二部細菌內毒素檢查法檢查,結果見表4。
由表4結果可知,陰性對照管(NC)均為陰性,供試品陽性對照管(PPC)和陽性對照管(PC)均為陽性,實驗有效;供試品管(NPC)均為陰性,表明樣品中未檢出細菌內毒素,9批注射用葛根素的細菌內毒素檢查均符合規定。
3 結論
3.1 無干擾濃度確定
干擾試驗目的是評價樣品濃度對鱟試劑與內毒素凝集反應的干擾程度及干擾性質,初步篩選出對細菌內毒素檢查無干擾的樣品濃度范圍。本品通過將注射用葛根素稀釋至1.5 mg/ml或以下濃度,消除對鱟試劑凝集反應的干擾。
3.2 鱟試劑的影響
不同廠家的鱟試劑由于生產工藝、質量參數等方面有一定差異,其抗干擾能力存在差異。因此,本實驗采用2個不同廠家的鱟試劑對3個批號的樣品進行實驗。從正式干擾試驗結果可見,樣品稀釋至1.5 mg/ml濃度時,Es或Et均在0.5 λ~2.0 λ范圍之內,可認為注射用葛根素在該濃度下不干擾細胞內毒素檢查。
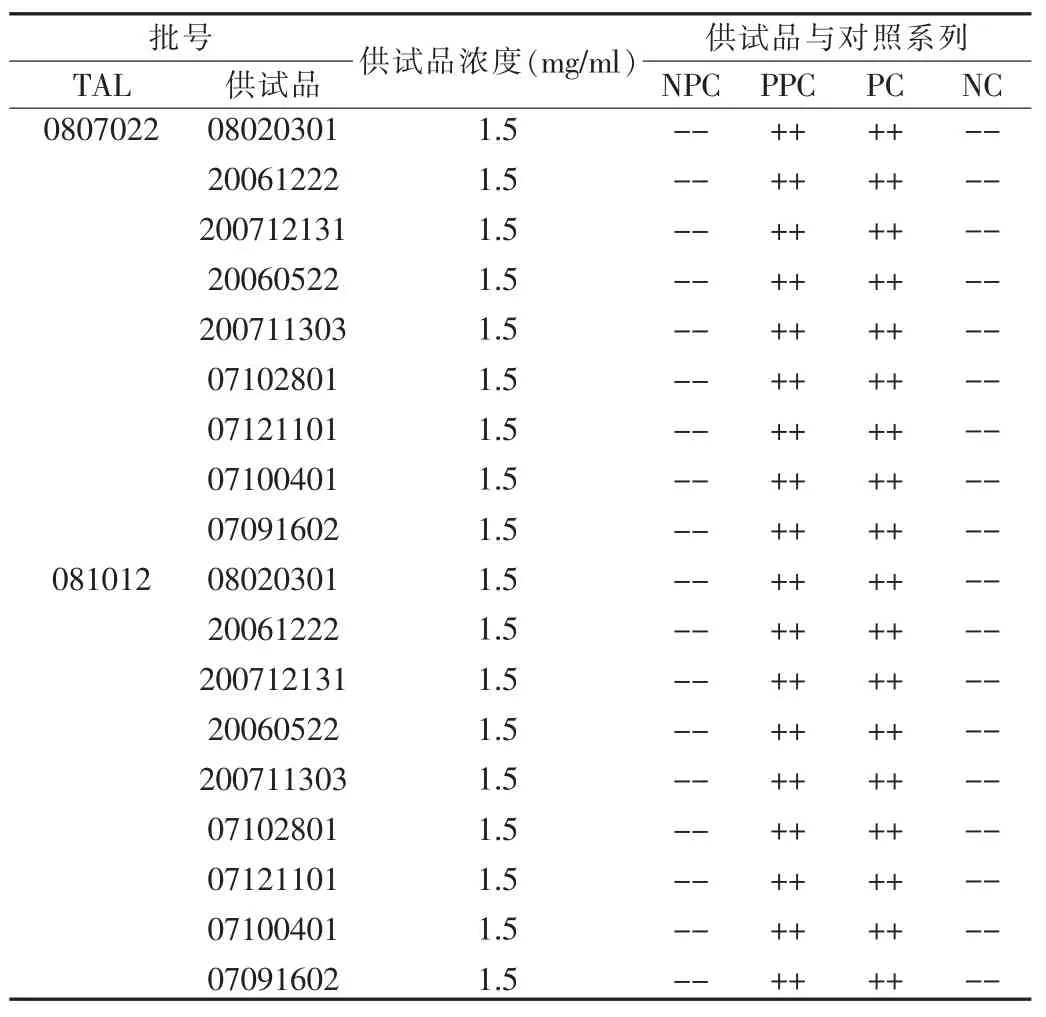
表4 注射用葛根素細菌內毒素檢查結果Tab.4 The results of bacterial endotoxin test of Puerarin for Injection
3.3 檢查結果
用兩個廠家鱟試劑與9批樣品進行細菌內毒素檢查,樣品中細菌內毒素限量均在0.17 EU/mg限值以下。因此,注射用葛根素采用限值0.17 EU/mg進行細菌內毒素檢查法代替熱原檢查法是可行的。
[1]白東義,佟春玲,韓慧,等.葛根素的藥理作用及其臨床應用研究進展[J].江蘇中醫藥,2009,41(3):76-78.
[2]姚丹,丁選勝.葛根素藥理作用機制探討及臨床應用[J].中國臨床藥理學與治療學,2008,13(4):468-474.
[3]劉紹德,莫惠平.葛根素注射液的不良反應及預防[J].中國中西醫結合雜志,2005,25(9):852-855.
[4]張新廣,王冬梅.葛根素提取工藝的研究[J].中藥材,2004,27(9):680.
[5]國家藥典委員會.國家藥品標準新藥轉正標準第46冊[M].北京:化學工業出版社,2004:26-27.
[6]國家藥典委員會.中華人民共和國藥典[M].二部.北京:化學工業出版社,2005:附錄 85-88.
[7]中國藥品生物制品檢定所.中國藥品檢驗標準操作規范[M].北京:中國醫藥科技出版社,2005:287-297.
[8]王慧明,陳邦樹.胞磷膽堿鈉注射液細菌內毒素檢查法[J].中國藥師,2005,8(9):793
[9]潘正興,宋勤.注射用奧美拉唑鈉細菌內毒素檢查法[J].藥物分析雜志,2008,28(2):275-277.

