ZD6474對膀胱癌裸小鼠皮下移植瘤的影響
陳愛武
遼寧省沈陽市于洪區人民醫院,遼寧沈陽 110141
近年來,惡性腫瘤的治療觀念由經驗科學向循證醫學、由細胞攻擊模式向靶向性治療模式轉變,越來越多的學者應用向腫瘤區域定位傳送藥物的“靶向治療”及“靶點治療”。腫瘤靶向治療分為2大類,一為腫瘤細胞靶向治療,腫瘤細胞靶向治療是利用腫瘤細胞表面的特異性抗原或受體作為靶向;二為腫瘤血管靶向治療,利用腫瘤區域新生毛細血管內皮細胞表面的特異性抗原或受體起作用。血管靶向治療與腫瘤細胞靶向治療相比,不僅提高了局部腫瘤組織內的濃度,給藥后可以迅速高濃度地積聚在靶標部位[1]。本文通過建立膀胱癌裸鼠皮下移植瘤,探討ZD6474的抗腫瘤作用,報道如下:
1 材料與方法
1.1 動物與藥品
5~6周齡BALB/c裸鼠購自北京華阜康生物科技股份有限公司;人膀胱移行細胞癌E-J細胞株由中國醫科大學藥理教研室提供,ZD6474標準品購自深圳市明博林生物科技有限公司。
1.2 方法
1.2.1 實驗分組
將接種E-J細胞分為5組,每組6只,并分別于接種后第 7、14、21、28、35 天,測量動物體重及行 MRI檢查,測量腫瘤細胞直徑。
陰性對照組;實驗組 A[0.5 mg/(kg·d)];實驗組 B[3 mg/(kg·d)];實驗組 C[7 mg/(kg·d)];實驗組 D[10 mg/(kg·d)];實驗組將ZD6474添加到飲水中灌胃。
1.2.2 荷人膀胱癌原位移植瘤動物模型的建立
首先使用的胰酶(0.25%)對培養到對數生長期的E-J細胞在37℃的溫度下消化,加入D-Hanks液調整細胞濃度至1.0×107個/ml。裸小鼠麻醉后仰臥位固定、消毒。切開腹壁牽出膀胱,壓迫膀胱排出尿液。用穿刺針穿刺進入膀胱腔內,針尖輕劃黏膜造成損傷,然后向腔內注入E-J細胞懸液200 μl,使用微量止血鉗固定裸小鼠尿道3~5 min,確定無含有腫瘤細胞的尿液外溢后停止,并縫合腹壁切口。
所有裸小鼠置于SPF級動物實驗室飼養,分別于接種后第 7、14、21、28、35 天測量動物體重及行 MRI檢查, 測量腫瘤細胞直徑。
1.3 統計學處理
應用SPSS 15.0統計軟件進行統計學分析,裸鼠體重、腫瘤直徑變化采用重復測量數據方差分析。
2 結果
實驗期間,所有裸鼠健康狀況均可,其體重變化各組比較差異無統計學意義(P>0.05),見表1,表明塞來昔布處理對裸鼠一般狀況及體重無明顯影響。
表1 裸鼠體重變化情況(±s,g)

表1 裸鼠體重變化情況(±s,g)
注:與陰性對照組比較,*P<0.05
組別 0 7 d 12.3±1.7 12.2±1.9 12.4±1.7 11.9±1.9 12.4±1.7陰性對照組實驗組[0.5 mg/(kg·d)]實驗組[3 mg/(kg·d)]實驗組[7 mg/(kg·d)]實驗組[10 mg/(kg·d)]18.3±2.2 18.1±2.0 17.9±1.9 17.8±1.9 18.3±1.9 14 d 24.3±2.6 24.2±2.8 24.5±2.9 23.9±2.7 23.8±2.6 21 d 29.8±1.9 29.7±2.0*29.9±1.9 29.6±2.0 29.8±2.1 28 d 33.9±2.2 33.6±2.0 33.9±2.2 33.6±1.9 33.8±2.2 35 d 37.9±2.2 37.8±2.1 37.6±2.2 37.5±2.1 37.5±2.0
7 mg/(kg·d)組在給予 ZD6474 第 21 天時,腫瘤直徑為(1.20±0.08) mm,與 3 mg/(kg·d)組比較差異有統計學意義;15 mg/(kg·d)組與 7 mg/(kg·d)相比,腫瘤直徑(1.20±0.09) mm,差異無統計學意義,但是有2例死亡,尸體解剖示肝壞死,提示劑量過大肝中毒。見表2。
表2 裸鼠皮下移植瘤直徑變化情況(±s,mm)
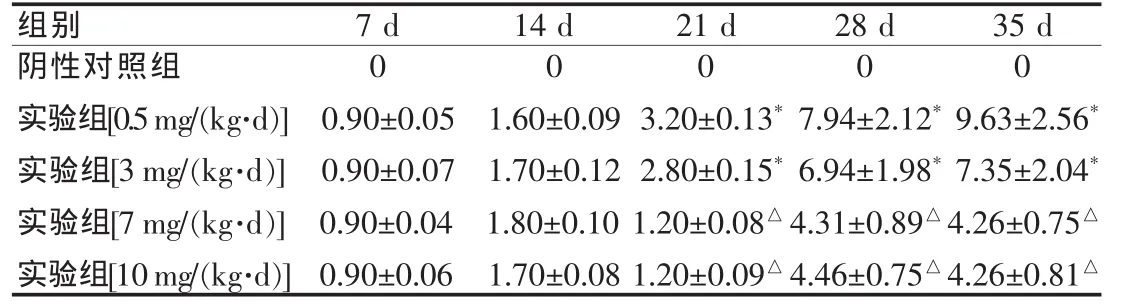
表2 裸鼠皮下移植瘤直徑變化情況(±s,mm)
注:與陰性對照組比較,*P<0.05,△P<0.05
組別 7 d 14 d 0 0.90±0.05 0.90±0.07 0.90±0.04 0.90±0.06陰性對照組實驗組[0.5mg/(kg·d)]實驗組[3 mg/(kg·d)]實驗組[7 mg/(kg·d)]實驗組[10mg/(kg·d)]0 1.60±0.09 1.70±0.12 1.80±0.10 1.70±0.08 21 d 0 3.20±0.13*2.80±0.15*1.20±0.08△1.20±0.09△28 d 0 7.94±2.12*6.94±1.98*4.31±0.89△4.46±0.75△35 d 0 9.63±2.56*7.35±2.04*4.26±0.75△4.26±0.81△
3 討論
血管內皮生長因子(vascularendothelialgrowthfactor,VEGF)是刺激血管形成最重要的生長因子之一,與內皮細胞表面上的特異性受體蛋白結合發揮其活性。絕大多數惡性腫瘤細胞均分泌VEGF,發生游走轉移的腫瘤細胞在局部VEGF刺激生成局部血管是惡性腫瘤發生轉移的重要機制,目前腫瘤血管靶向治療主要針對VEGF。最早,Senger等于1994年從篩選的大鼠腫瘤細胞中發現VEGF-B[2],隨后VEGF-A、PLGE、VEGF-H、VEGF-C、VEGF-D、VEGF-R 等陸續被發現。目前針對VEGF通路的靶向藥物主要有:①VEGF Trap;②抗-VEGF;③抗-VEGFR;④VEGFR酪氨酸激酶抑制劑[3]。目前,貝伐單抗、IMC-1C11等已經在臨床上廣泛應用,在與卡鉑、紫杉醇的聯合應用的臨床實驗中,患者的治療反應率、存活期、無疾病進展生存期均有明顯增加[4-5],但是消化道反應、血栓、高血壓、出血、蛋白尿、心臟毒性等副作用限制了其在臨床的應用[6-7],而VEGFR酪氨酸激酶抑制劑越來越受到人們的重視。
ZD6474是一種合成的小分子酪氨酸激酶抑制劑,可同時作用于表皮生長因子受體(EGFR)、血管內皮生長因子受體(VEGFR)和酪氨酸激酶。不僅可抑制由EGFR誘導的腫瘤細胞增殖,發揮腫瘤細胞靶向治療的作用,還可抑制腫瘤細胞的VEGFR-2阻斷腫瘤血管內皮細胞的信號傳導,從而抑制腫瘤血管生成,因此具有和腫瘤血管靶向治療的雙重作用。
本文采用荷人膀胱癌原位移植瘤動物模型評估ZD6474對膀胱癌裸鼠皮下移植瘤直徑的影響,發現7 mg/(kg·d)組在給予ZD6474 第 21 天時,腫瘤直徑為(1.2±0.08)mm,與 3mg/(kg·d)組比較差異有統計學意義;10 mg/(kg·d)組與 7 mg/(kg·d)組相比,腫瘤直徑為(1.20±0.09)mm,差異無統計學意義,但有2例死亡,尸體解剖示肝壞死,提示劑量過大肝中毒。
ZD6474目前已經用于乳腺癌和肝癌的治療,但是對膀胱癌的作用國內外尚無報道,本實驗通過荷人膀胱癌原位移植瘤動物模型的實驗,提示其對膀胱癌的抗腫瘤作用,開闊了思路,為臨床上膀胱癌生物化療的治療模式提供了一定的理論基礎。
[1]王鷹,李蘇宜.抗腫瘤血管生成分子靶向治療臨床研究進展[J].東南大學學報,2007,26(6):476-480.
[2]Ferrara N.Vascular endothelial growth factor:basic science and clinical progress[J].Endocrine Reviews,2004,25(4):581-611.
[3]Tong RT,Boucher Y,Kozin SV,et al.Vascular normalization by vascular endothelial growth factor receptor-2 blockade induces a pressure gradient across the vasculature and improves drug penetration in tumors[J].Cancer Res,2004,64:3731-3736.
[4]He Y,Rajantie I,Hmonen M,et al.Preexisting lymphatic endothelium but not endothelial progenitor cells are essential for tumor lymphangiogenesis and lymphatic metastasis[J].Cancer Res,2004,64:3737-3740.
[5]Cudmore M,Ahmad S,AI-Ani B,et al.VEGF-E activates endothelial nitric oxide synthase to induce angiogenesis via cGMP and PKG-independent pathways[J].Biochem Biophys Res Commun,2006,345:1275-1282.
[6]Sandler AB,Gray R,Brahmer J.Randomized phase II/III trial of paclitaxel(p)plus carboplatin(c)with or without bevacizumab(NSC704865)in patients with advanced non-squamous non-small cell lung cancer(NSCLC):an Eastern Cooperative Oncology Group(ECOG)trial E4599[J].J Clin Oncol,2005,23:4-10.
[7]Jain R K,Duda D G,Clark J W,et al.Lessons from phase III clinical trials on anti-VEGF therapy for cancer [J].Nat Clin Pract Oncol,2006,3:24-40.

