酶標法檢測CA242不確定度的評估分析
周艷秋,高紅軍,田 穎,王洪武
煤炭總醫院中心實驗室,北京 100028
酶聯免疫吸附試驗(ELISA)可以定性或定量分析樣品中目標蛋白的表達情況,但結果的重復性和可靠性較難控制。測量不確定度(uncertainty in measurement,UM)是醫學實驗室質量管理體系及檢驗標準化工作的重要組成部分[1]。CA242是消化道腫瘤常用的檢測指標,目前臨床檢測CA242以定量酶標法為主,各醫院對該項目的檢測報告未采用UM的形式。為更客觀反映該項目的檢測結果,對我室ELISA法檢測CA242的UM進行了初步研究。
1 材料與方法
1.1 標本來源
三份新鮮血液均為我院住院患者靜脈血,2 000 r/min離心10 min,分離血清,分裝后凍存于-80℃冰箱內。不同樣本中CA242的含量均在試劑檢測的線性范圍內。
1.2 儀器與試劑
瑞典康乃格診斷試劑公司CA242診斷試劑盒(批號:28559∶1);德國Sigma公司大容量冷凍離心機4-16k型;芬蘭BIOHIT 微量加樣器(100~1 000 μl量程及 10~100 μl量程各1支);美國Awareness公司酶標儀STAT FAX2100;中國杭州奧盛儀器有限公司MB100-4P型微孔板恒溫振蕩器。
1.3 檢測方法
1.3.1 檢測步驟 依照商品化試劑盒說明書檢測5個標準品和1個低值質控,各設置5個平行孔;低、中、高值待測樣品各重復5次。酶標儀405 nm波長下檢測吸光度值(OD值)。
1.3.2 建立檢測模型 樣本濃度計算公式:y=f(x)×fV×fA×frep
fV、fA、frep分別表示加樣體積、吸光度值和檢測精密度對檢測結果的影響,f(x)表示樣品吸光度值x與濃度y之間的轉換公式。 fV=fA=frep=1,故 y=f(x)。
1.3.3 UM的分類與來源 根據文獻[1-2]進行A類UM和B類UM進行的評定。
2 結果
2.1 A類UM的評定
2.1.1 重復比色引入的u(A1)三種濃度標本和質控樣品分別固定一孔重復讀數5次后觀察OD值的變化,計算均值、標準差,根據CNAS-GL05:2006測量不確定度要求的實施指南[3],結果見表 1。
2.1.2 重復樣本引入的u(A2)三種濃度標本和質控樣品重復孔檢測引入的UM,結果見表1。
2.1.3 標準 UM 的合成 由于 u(A1)和 u(A2)之間相互獨立,因此標準UMu(frep)等于二者平方和的平方根。

表1 CA 242 A類UM的評定結果
2.2 B類UM的評定
2.2.1 OD值與濃度轉換引入的uf(x)根據試劑使用說明運用上海思橋檢驗軟件中的QUANRATIC-ICON方程擬合標準曲線:y=13.58x2+60.127x-0.252 7(r2>0.999),其中 x 為標準品或樣本OD值,y為標準品或樣本中CA 242的濃度。以x+s為上限,x-s為下限作圖,獲得標準曲線的可接受范圍,參照文獻[4],計算標準 UM,結果見表 2,Ymax、Y、Ymin分別表示樣本的平均吸光度值在曲線上限、標準曲線和曲線下限時的樣本濃度值。
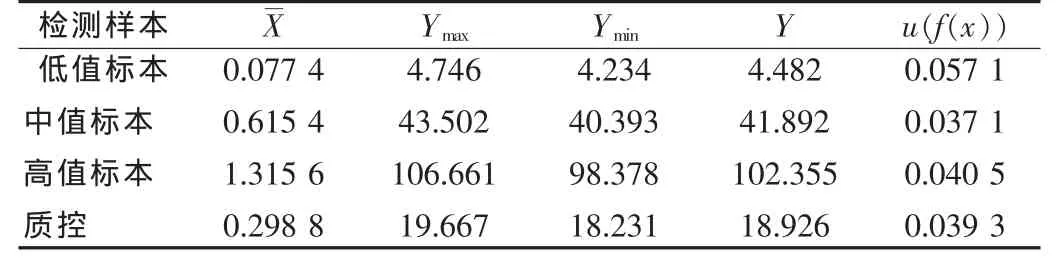
表2 擬合曲線引入的UM計算結果
2.2.2 移液器加樣引入的u(fV) 根據文獻[1-2]移液器加樣引入的 UM,u(fV)=0.080 225 μl。
2.2.3 酶標儀測定引入的UM u(fA)根據文獻[2]酶標儀在不同讀數范圍內的 UM 分別為:u(fA)=0.005 77(0.1~1.5 A);u(fA)=0.011 5(1.5~3.0 A)。
2.3 合成的總 UM uc(y)
根據文獻[2]計算試驗結果總的UM uc(y)見表3。依據CNAS-GL06:2006《化學分析中不確定度的評估指南》[5],以條形圖展示了不同測定樣本中UM分量的大小,見圖1。

表3 樣本檢測UM的結果
2.4 擴展UM
取置信水平P=95%,包含因子K=2.1,不同濃度樣本的擴展 UM 為 U(y)=uc(y)×2.1,見表 3。
2.5 結果報告
待檢測樣品的檢測結果:低值標本=4.482±0.872,中值標本=41.892±8.066,高值標本=102.355±19.732。
3 討論
CA242是一種唾液酸化的黏蛋白型糖類抗原,是與胰腺癌、膽囊癌和結腸癌等相關的腫瘤標記物[6-7]。臨床上常用的檢測方法是用酶標儀進行比色分析,上機檢測前主要依靠手工操作,影響檢測結果可靠性的因素較多,本研究通過UM的評定方法試圖發現酶標法檢測CA242的主要影響因素。
UM是表征被測量值所處量值范圍內的參數,是衡量檢測結果準確性和可靠性的重要參數。只有充分運用UM的評估來識別試驗中各種因素對檢驗結果的影響,才能對檢測設備、標準物質、檢測方法、環境條件、被檢測物質的性能和狀態以及操作者的技能進行比較全面的分析,從而有效控制各個環節,保證檢驗結果的準確可靠。本試驗通過檢測血清CA242的含量,評估酶標法檢測CA242的UM,明確影響該檢測結果的主要因素。
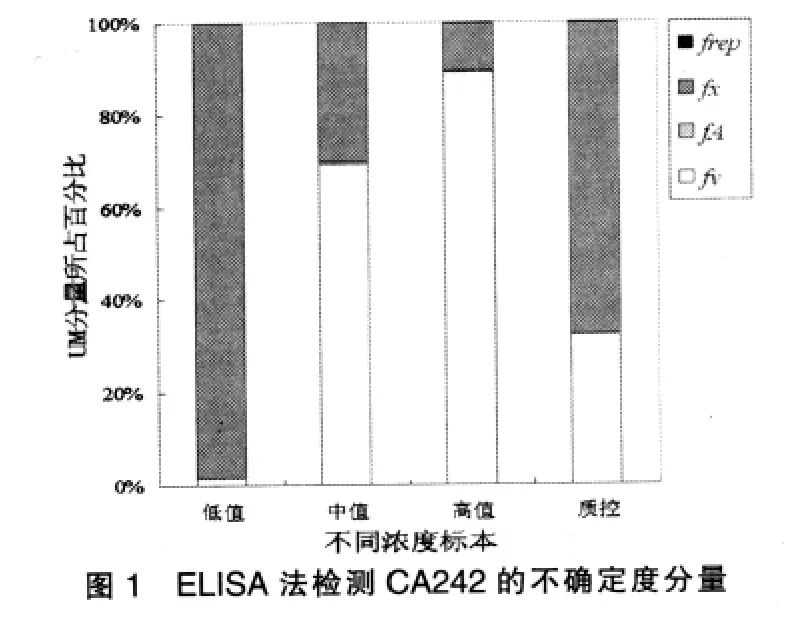
定量ELISA法檢測生物標志物所涉及的影響因素較多,如酶標儀、試劑質量、環境和反應溫度、加樣器加樣、重復檢測、標準曲線擬合等均會產生各自的UM分量。文獻研究結果表明樣品的加樣體積誤差、檢測精密度、標準曲線擬合和酶標儀檢測OD值的準確性對UM的貢獻最大[1,8]。本研究分析了上述不同因素引入的UM,結果表明低、中、高值的檢測范圍與實際檢測結果均較符合。從圖1和表3可以看出,隨著標本濃度的上升,UM不斷增大,移液器加樣引入的UM所占比例隨標本濃度升高逐漸增加,而標準曲線擬合引入的UM隨標本的濃度升高逐漸降低,與本室的TSGF不確定度研究結果一致[2],不同的是精密度和酶標儀測定OD值引入的UM均很小(<0.36%);與秦緒珍等[1]的研究結果略有不同,主要原因是筆者在計算加樣引入的UM時最后一步未開根號,并且包含因子K較小,導致低、中、高值標本的總UM和加樣體積分量UM所占比例較實際偏小。加樣體積引入的UM在中、高值標本中所占比例最高,由此可見加樣體積的準確與否直接關系到檢測結果的可靠性;而標準曲線擬合對低值標本UM影響最大,因此選擇最合理的擬合方程非常關鍵,本研究中二次方程的擬合效果要好于線性方程(r2>0.994)的擬合度。
綜上所述,在日常工作中要嚴格控制實驗室的溫度,加樣器要按照規定到權威部門進行檢驗校準。充分利用UM評定在實驗室管理中的作用,提高檢測能力。
[1]秦緒珍,高學慧,徐二木,等.ELISA方法檢測CA242的不確定度評估[J].中國衛生檢驗雜志,2010,20(4),894-896.
[2]周艷秋,高紅軍,田穎,等.酶標法檢測TSGF不確定度的評估分析[J].中國衛生檢驗雜志,2010,20(2),3355-3357.
[3]測量不確定度要求的實施指南[S].CNAS-GL05:2006.
[4]Cembal S,Ambrosio J,Aranda C,et al.Intra-assay total uncertainty of results in immunoassay techniques [J].J Immunoassay Immunochem,2004,25:1-15.
[5]化學分析中不確定度的評估指南[S].CNAS-GL06:2006.
[6]Rothlin M A,Joller H,Largiader F.CA242 is a new tumor marker for pancreatic cancer[J].Cancer,1993,71:701-707.
[7]Kuusela P,Haglund C,Roberts PJ.Comparison of a new tumour marker CA242 with CA19-9,CA50 and carcinoembryonic antigen(CEA)in digestive tract diseases[J].Br J Cancer,1991,63:636-640.
[8]郭莉莉.酶標法檢測人體血清中HIV-1/HIV-2型抗體結果不確定度評定[J].中國衛生檢驗雜志,2009,19(1),46-47.

