扶正敗毒顆粒對膿毒癥大鼠急性肺損傷保護作用的實驗研究*
張 韌 王丁超 蘇秀平 高 翔 王 靜 吳桂玲 陳曉敏
1河南省濮陽市中醫院(河南濮陽457003)
2河南省中醫院(河南鄭州450008)
急性肺損傷(ALI)是臨床上常見的急性呼吸系統功能失常,其中由感染導致的膿毒血癥是引起ALI的最常見的病因。目前認為膿毒癥是炎癥失控導致的紊亂,是機體對微生物產物發生失控的免疫反應[1],其中腫瘤壞死因子-α(TNF-α)是膿毒癥發生早期的重要炎性細胞因子,大量釋放則對機體造成損傷,白細胞介素-1(IL-1)可與 TNF-α 協同作用加重多器官損傷[2]。 本實驗以膿毒癥大鼠為研究對象,觀察大鼠不同時間點的肺組織含水量、動脈血氣變化、肺組織IL-1、TNF-α表達變化,探討中藥復方扶正敗毒顆粒對膿毒癥大鼠肺損傷的保護作用。
1 材 料
1.1 實驗動物 青年SD大鼠,清潔級,雌雄各半,鼠齡3~4月,體質量(300±50)g,154只。 由河南實驗動物中心提供,合格證號:scxk(豫)2009-0006。
1.2 藥品與儀器 扶正敗毒顆粒(濮陽市中醫院中藥制劑室提供);烏司他丁(廣東天普生化醫藥股份有限公司生產,批號:國藥準字 S19990050);IL-1單克隆抗體及TNF-α單克隆抗體均由武漢博士德生物工程有限公司提供。光學顯微鏡(Olympus optical Co.LTD,JAPAN,型號 PM-10AD)。電子天平(上海精科天平廠,型號 JA1203)。
1.3 分組與造模 將SD大鼠按隨機數字表法分為模型組、扶正敗毒顆粒組、烏司他丁組及扶正敗毒顆粒聯合烏司他丁聯合組(聯合組)各36只,假手術組10只。參考文獻[3-4]加以改良制備膿毒癥動物模型。水合氯醛腹腔注射麻醉大鼠,待完全麻醉后,仰臥位固定大鼠,頸部皮膚常規備皮、消毒,于頸外側下頜至心臟的中點作一約1cm的橫切口,鈍性分離皮下組織,暴露右側頸外靜脈,沿血管向近心端方向插入留置針約1cm,將導管從留置針管與頸外靜脈夾孔中把心導管慢慢置入達右心房,結扎固定,導管末端經皮下隧道從頸后中央引出并固定于皮膚,管內注射125U/mL肝素0.5mL抗凝,插入置管針封閉導管。然后沿腹白線中段作3cm切口,探查取出盲腸,用4號絲線距盲端1cm處結扎,用12號針穿刺3孔,擠出少許糞便于腹腔內,回納盲腸,分層縫合腹腔。手術過程中保持大鼠肛溫(37.0±0.5)℃,保持室溫(26.0±1.0)℃。
1.4 給藥方法 假手術組、模型組、烏司他丁組分別于造模后第1日用生理鹽水灌胃,同時扶正敗毒顆粒組、聯合組用扶正敗毒顆粒(36.8mg/100g)灌胃(灌胃容積為1mL/100g),每日灌胃1次直至取材;烏司他丁組、聯合組大鼠分別于造模后第1日腹腔內注射烏司他丁(1萬U/㎏),假手術組、模型組、扶正敗毒顆粒組同時用同等容積的生理鹽水腹腔注射,每日1次直至取材。
1.5 標本采集與檢測 (1)腹主動脈血氣:測定大鼠口腔溫度,并記錄,取腹主動脈血2mL采用電極法進行血氣測定,PaO2、PaCO2。(2)肺組織含水量:稱取肺組織濕重,然后放入恒溫箱(100±2℃)干燥,24h后取出,稱取干重,計算肺組織含水量。計算公式:肺組織含水量=(肺濕重-肺干重)/肺濕重×100%,以%表示。(3)臟器組織IL-1,TNF-α表達:檢測采用免疫組織化學SP法檢測,在400倍光鏡下觀察,細胞膜、細胞漿呈棕色為免疫組化陽性;用Image-Pro Plus 5.1專業圖像采集與分析系統采集圖像,并進行半定量分析,每張切片隨機選取不重疊的5個視野拍照,測定其平均吸光度及陽性細胞數,取其平均值代表各細胞因子的表達水平。(4)病理觀察:取肺組織4%多聚甲醛固定,經脫水、透明、浸蠟、包埋,切成4~6μm厚的切片,常規脫蠟、脫水,蘇木素-伊紅(HE)染色,脫水、透明、封片。光學顯微鏡觀察肺、腸組織病理形態學改變。
1.6 統計學處理 應用SPSS13.0統計軟件。計量資料采用單因素方差分析方法,數據以s)表示;組內差異比較采用單因素方差分析兩組間比較采用t檢驗。P<0.05為差異有統計學意義。
2 結 果
2.1 各組大鼠動脈血PaO2、PaCO2比較 見表1。與假手術組比較,模型組動脈血 PaO2顯著降低,PaCO2顯著升高(P<0.01);與模型組比較,扶正敗毒顆粒和烏司他丁及聯合組PaO2升高,PaCO2下降,以聯合7d組尤為顯著(P<0.01);與扶正敗毒顆粒通組比較,烏司他丁組無顯著差異(P>0.05),見表1。
表1 各組大鼠動脈血PaO2、PaCO2比較 (mmHg,
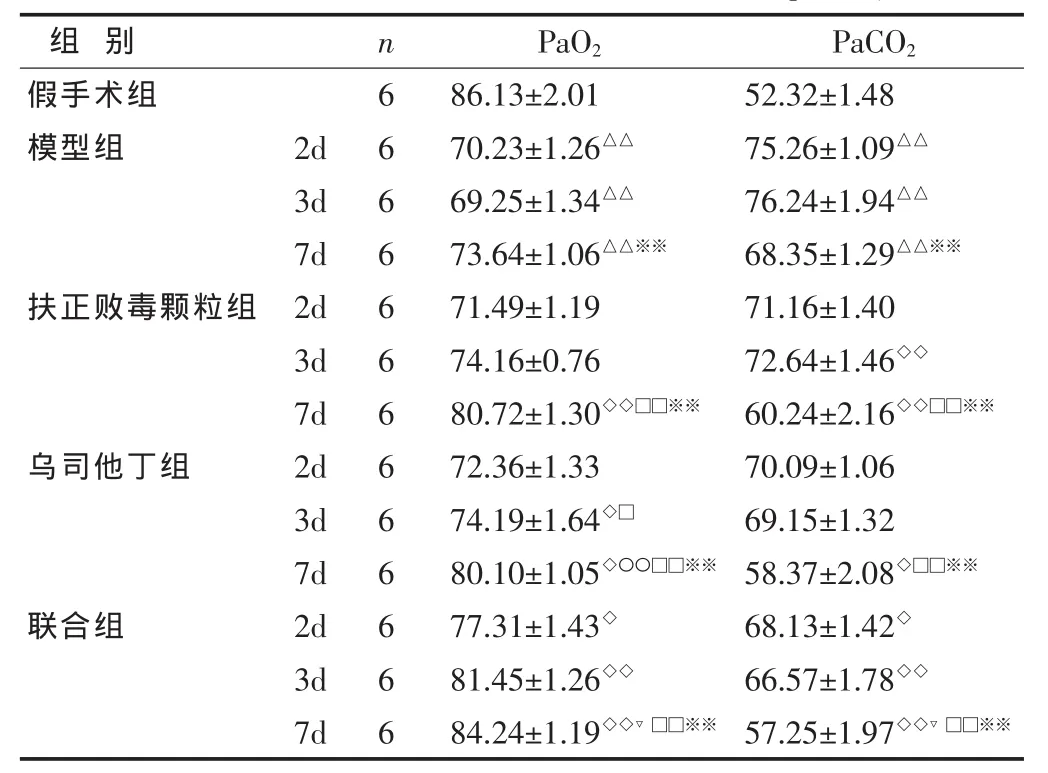
表1 各組大鼠動脈血PaO2、PaCO2比較 (mmHg,
與假手術組比較,△P<0.05,△△P<0.01; 與模型組比較,◇P<0.05,◇◇P<0.01;與扶正敗毒顆粒組比較,▽P<0.05;與聯合組比較,〇P<0.05,〇〇P<0.01;與 2d組比較,□P<0.05,□□P<0.01;與 3d組比較,*P<0.05,*P<0.01。 下同。
?
2.2 肺組織含水量變化結果 見表2。與假手術組比較,模型組大鼠肺組織含水量顯著升高(P<0.01);與模型組比較,扶正敗毒顆粒和烏司他丁及聯合組含水量均顯著降低 (P<0.05或0.01),與2d、3d組相比,扶正敗毒顆粒和烏司他丁7d組的肺組織含水量均顯著降低(P<0.05或0.01),以聯合7d組下降尤為顯著(P<0.01)。
表2 各組大鼠含水量比較(
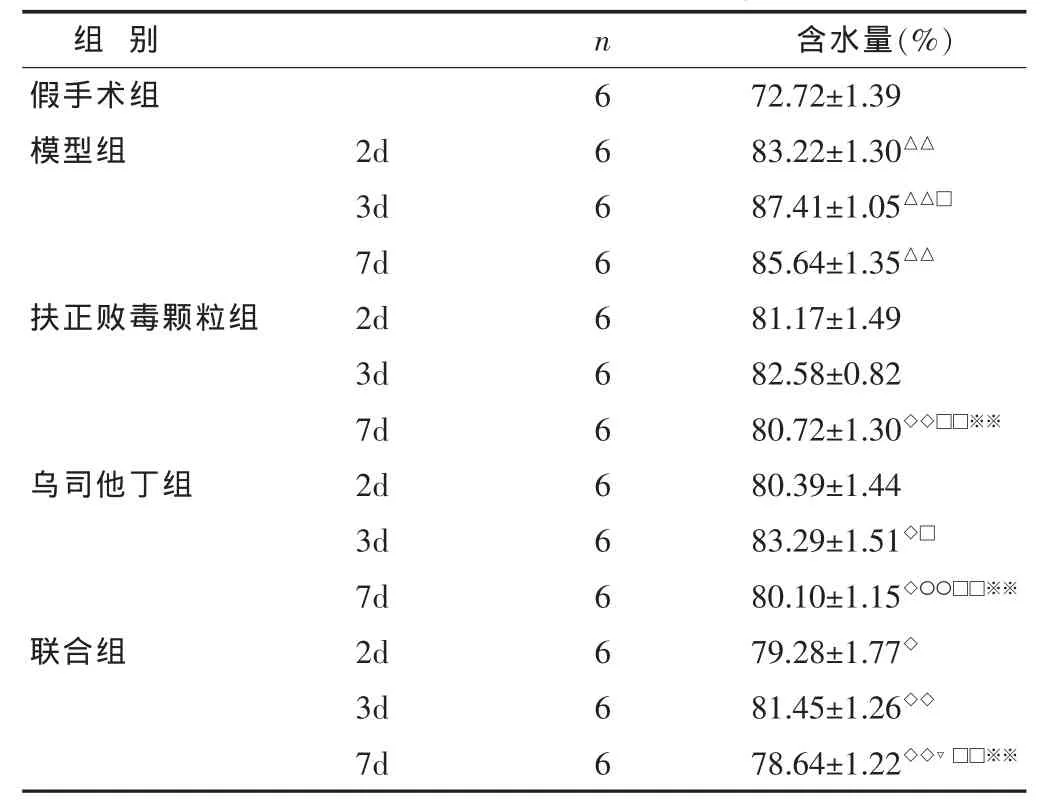
表2 各組大鼠含水量比較(
?
2.3 肺組織TNF-α、IL-1的表達變化 見表3。與假手術組比較,模型組大鼠肺組織TNF-α、IL-1表達均升高 (P<0.05或0.01);與模型組相比,扶正敗毒顆粒和烏司他丁及聯合組各時間點 TNF-α、IL-1的表達水平均顯著下降(P<0.05或 0.01),以聯合7d組的尤為顯著(P<0.01);與聯合組相比,扶正敗毒顆粒組和烏司他丁組TNF-α、IL-1表達水均顯著升高 (P<0.05或0.01),以 2d組尤為顯著(P<0.01)。與 2d 、3d組相比,以聯合 7d組 TNF-α、IL-1 表達水平下降尤為顯著(P<0.01)。
表3 各組大鼠肺組織TNF-α、IL-1陽性細胞表達變化(IOD,
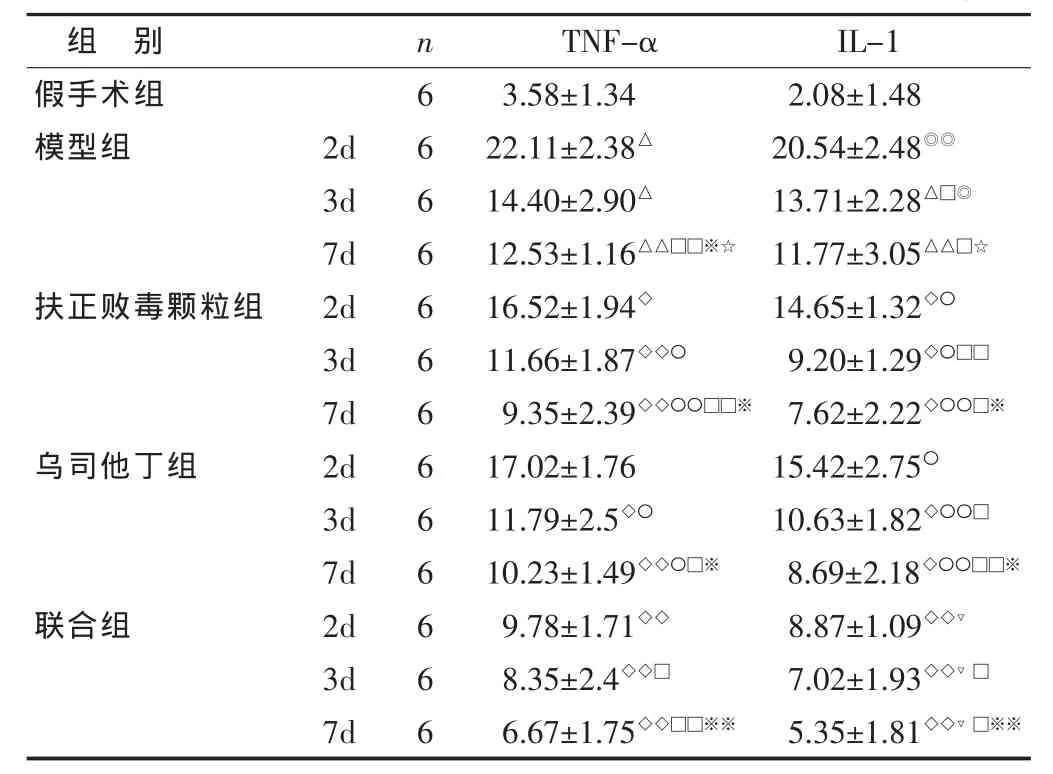
表3 各組大鼠肺組織TNF-α、IL-1陽性細胞表達變化(IOD,
?
2.4 肺組織病理改變 假手術組大鼠肺組織可見肺泡大一致,肺泡壁菲薄,支氣管上皮完整,管腔內無分物,支氣管上皮正常,外周無炎性細胞浸潤。模型2d組可見肺間質有單核細胞、淋巴細胞浸,肺組織出現散在性病灶;3d組可見病灶增大、數量多,肺泡壁廣泛淋巴細胞及單核細胞浸潤,有些區域可見肺泡出血,肺泡壁結構不清。7d組更為明顯,肺泡腔內滿布炎性滲出物、血性滲出物明顯,大量上皮脫落,肺泡壁結構不清,大片的肺實變。扶正敗毒顆粒組在第2、3、7日均較模型組有顯著改善,病變范圍、程度均較模型組明顯減輕。聯合7d組改善尤為顯著,表現為病變范圍較局限,炎細胞密度較低,肺泡腔內滲出物少,肺泡結構較模型組完整。
3 討 論
ALI主要是因機體炎癥反應失控所導致的器官損傷[5]。本組資料顯示模型組大鼠肺組織炎性因子TNF-α,IL-1表達水平明顯高于假手術組,表明促炎細胞因子在膿毒癥大鼠急性肺損傷損傷中發揮了重要作用。TNF-α是由活化的巨噬細胞、單核細胞和T淋巴細胞產生,具有核心作用,是導致炎癥介質級聯反應的始發因子。一旦TNF-α被分泌出來,炎癥連鎖反應即被啟動,促進其他細胞因子的激發釋放,引起組織損害。有報道促炎癥細胞因子TNF-α在感染性休克中發揮關鍵作用,直接導致某些臟器的損傷[6]。IL-1是另一種主要由巨噬細胞產生的促炎性細胞因子,是體內調節免疫和炎癥反應的中心介質,是細胞因子網絡中的關鍵因子,能激活多種免疫和炎癥細胞:刺激單核細胞和巨噬細胞產生IL-6和TNF-α;刺激中性粒細胞釋放炎癥介質;誘導內皮細胞活化,與TNF-α協同作用,促進血管內皮-白細胞黏附分子的表達,趨化中性粒細胞等炎癥細胞進人病變部位,增加血管內皮通透性,加重組織損傷[7-8]。所以,降低促炎細胞因子TNF-α,IL-1水平對防止ALI具有重要意義。本實驗結果顯示,扶正敗毒顆粒能夠降低組織炎性因子TNF-α,IL-1表達水平,提示扶正敗毒顆粒通過降低臟器組織中炎性細胞因子TNF-α,IL-1含量,進而減輕膿毒癥大鼠多器官損傷和降低死亡率。
綜上所述,促炎因子TNF-α,IL-1在ALI中發揮了重要作用,扶正敗毒顆粒能夠降低臟器組織中TNF-α,IL-1表達水平以減輕臟器損傷;降低了肺組織的含水量,提高動脈血氧含量,對膿毒癥大鼠具有確實的防護作用,為扶正敗毒顆粒防治膿毒癥性MODS提供了參考。
[1] SatSharma,MD,FRCPC,etal.Septic shock multiple organ failure and acute respiratory distresss yndrome[J].Medseape,2003,9(12):199-209.
[2] 邱海波,潘家綺,趙永強,等.腫瘤壞死因子-α、白細胞介素-1β和巨噬細胞炎性蛋白-2在感染及器官損傷中的作用及治療探討[J].中國危重病急救醫學,1996,8(3):139-142.
[3] 施新猷.現代醫學實驗動物學[M].北京:人民軍醫出版社,2000:298-335.
[4] Xiang D Z,Vverbeken K,Vanlommela T,etal.Intimal hyperplasia after long-term venous catheterization[J].Eur Surg Res,2000,32(4):236-245.
[5] 陳海龍,關鳳林,吳咸中.多器官功能不全綜合征研究的現狀和展望[J].中國急救醫學,2000,20(7):439.
[6] Andrzejczak D,Gorska D,Czarnecka E.Influence of amlodipine and atenolol on lipopolysaccharide (LPS)-induced serum concentrations of TNF-alpha,IL-1beta,IL-6inspontaneouslyhypertensiverats (SHR) [J].Pharmacol Rep,2006,58(5):711.
[7] 孫衛民,王惠琴.細胞因子研究方法學[M].北京:人民衛生出版社,1999:584.
[8] 羅正曜.休克學[M].天津:天津科學技術出版社,2001:601.

