奧硝唑緩釋膜用于鼠類動物的生物安全性評價
徐全臣,陳秀娟,王志國,劉夢東,耿新杰
(青島大學醫學院附屬醫院,山東青島266003)
羧甲基殼聚糖(CM-C)是殼聚糖的水溶性衍生物,其可溶可吸收的特性作為成膜載體已經越來越受到人們的重視。研究顯示,以CM-C為載體,奧硝唑為主藥制成的緩釋藥膜,質量控制可靠,抑菌性和緩釋性能良好[1,2]。為了保證該藥膜用于人體時安全,2009年12月~2010年10月,我們按照國家規定,對藥膜進行了生物安全性評價。
1 材料與方法
1.1 材料 實驗動物為6周齡左右健康昆明小鼠10只,雌雄各半,體質量17~23 g,由青島市藥品檢驗所提供。白色豚鼠40只,體質量300~350 g,雌雄各半,由青島市藥檢所實驗動物中心提供。SPF級Wistar大鼠10只,雌雄各半,由山東大學醫學院實驗動物中心提供。實驗細胞為V79細胞(中國倉鼠肺成纖維細胞),由中國科學院上海生物科學院細胞資源中心提供。
1.2 方法
1.2.1 藥膜的制備 取 CM-C 1.6 g,溶于40 ml純化水中,配成4%的溶液;取高聚合物聚乙烯醇(PVA)1.6 g,溶于40 ml純化水中,配成4%的PVA溶液。將兩種溶液混合,加入甘油1 ml后攪拌4 h,加入0.48 g奧硝唑,繼續攪拌4 h,然后把共混液倒入一底面光滑的圓形金屬槽中。放入烘箱50℃烘干,12 h后取出即得藥膜。所制藥膜厚0.3 mm,可分切出任意大小形狀。乙醇消毒后裝入密封袋中保存。掃描電鏡觀察見藥膜呈蜂窩狀,孔隙均勻,直徑約 3 μm 。
1.2.2 急性毒性實驗 昆明小鼠10只,隨機分為實驗組和對照組,每組5只;實驗組于尾靜脈恒速注射載體浸提液50 ml/kg、對照組注射同批號滅菌生理鹽水50 ml/kg,于注射后 4、24、48、72 h 觀察動物有無輕、中、重度毒性反應或死亡情況。
1.2.3 細胞毒性實驗 實驗分3組:藥膜浸提液組、陰性對照組(RPMI 1640培養液)、陽性對照組(0.1%苯酚)。將對數生長期的V79細胞用0.25%胰酶消化,制成1×104/ml的細胞懸液,取出96孔細胞培養板,分別加入細胞懸液100 μl,置37℃培養24 h。待細胞貼壁,棄去原培養液,分別加入各組材料(100 μl/孔),同樣條件繼續培養 2、4、7 d 后,每孔加入 MTT 20 μl,再培養4 h,吸棄原培養液,每孔加入緩沖鹽溶液150 μl,清洗2次,棄除余液,立即加入二甲基亞砜150 μl/孔,室溫放置并輕度振蕩15~20 min。使用酶聯免疫檢測儀在490 nm波長處測定各孔的吸光度值(OD),各組細胞按下式計算細胞相對增殖度(RGR)。RGr=實驗組OD/陰性對照組OD×100%。
1.2.4 皮膚過敏實驗[3]40只健康白色豚鼠隨機平均分為4組:奧硝唑藥膜組、基質組、陰性對照組(生理鹽水)、陽性對照組(2,4-二硝基氯苯)。實驗前24 h仔細將豚鼠背部兩側剪毛,面積約3 cm×3cm。分別用0.2 ml 125 g/L奧硝唑藥膜浸提液、等體積基質浸提液、生理鹽水、1%2,4-二硝基氯苯涂于豚鼠左側脫毛區,用1層油紙及2層消毒紗布覆蓋,以膠布固定,持續6 h;7 d和14 d以同樣方法重復1次,共3次。于末次給藥致敏后14 d,將受試物0.2 ml涂于豚鼠右側脫毛區,其中陽性對照用0.1%2,4-二硝基氯苯,6 h后去掉受試物,溫水沖洗干凈,即刻觀察并記錄6、24、48 h皮膚及心率、呼吸等情況。根據出現的紅斑與水腫情況評分計算反應值,最后計算出實驗動物皮膚致敏率結果。
1.2.5 體內降解實驗 10只Wistar大鼠,背部剪毛形成約4 cm×4 cm的術野,沿脊柱作一長約2 cm的切口,取脊柱兩側等距離的兩個肌肉位點,用止血鉗分離脊柱兩側肌肉,形成足夠間隙。奧硝唑藥膜剪成4.0 mm×8.0 mm長方形,烘致恒重,經紫外線消毒,植入大鼠背部肌肉。1、2、4、6周切取標本,洗去黏附物,烘致恒重,按下式計算降解百分率。降解百分率=(W0-W1)/W0×100%;W0為降解前質量(g),W1為降解后質量(g)。
2 結果
2.1 急性毒性實驗 實驗組和對照組小鼠狀況良好,未見明顯毒性癥狀,72 h內活動如常,飲食飲水均正常,無動物死亡現象,動物體質量日益增加。
2.2 細胞毒性實驗 藥膜浸提夜組毒性分級為0~Ⅰ級,說明藥膜對細胞無不良反應,符合國家規定的標準。見表1。
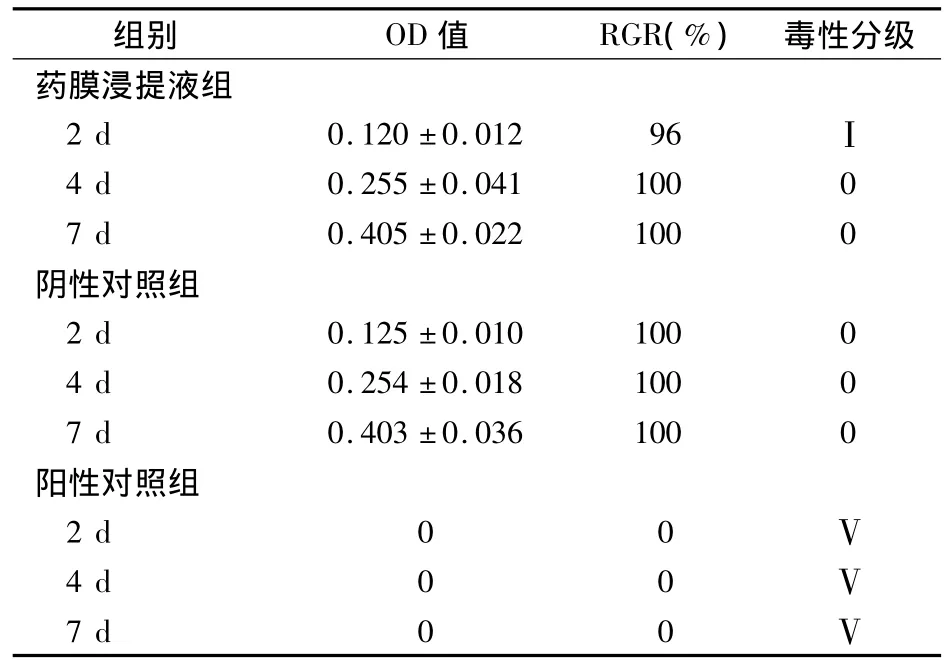
表1 各組在不同培養時間的OD值、RGR及細胞毒性分級
2.3 皮膚過敏實驗 實驗組觀察6、24、48 h,皮膚過敏實驗致敏率均為0,陽性對照組分別為90%、100%、100%。
2.4 體內降解實驗 1周時實驗組內置膜取出后基本完整,表面粗糙,有白色及紅色絮狀附著物。第2周時,內置膜已成凝膠狀,較第1周明顯變薄,與周圍組織易區分。第4~6周呈菲薄致密近透明的銀白色纖維囊,周圍組織顏色正常。1、2、4、6周奧硝唑藥膜降解百分率分別為15%、35%、72%、98%。
3 討論
生物材料在應用于人體之前必須經過嚴格的檢驗,除臨床應用所要求的機械及理化性外,還應具有良好的生物安全性。CM-C是殼聚糖的水溶性衍生物,具有良好的生物相容性以及可降解性[4]。本實驗中,奧硝唑緩釋藥膜無全身急性毒性及皮膚過敏性,埋植于大鼠肌肉后2周時已經融化,6周時幾乎完全降解,齦溝中的液體量多于肌肉組織,推測藥膜在3周左右即可完全降解。
以CM-C為載體的緩釋藥膜質地均勻,在電鏡下觀察,材料表面呈蜂窩狀,縱剖面上有較規則的通道,這些孔和通道相互構成網架,形成三維立體結構,適合細胞的三維生長,能為新生組織提供良好的支架。在細胞毒性實驗中,實驗組細胞在第4天和第7天的細胞相對增殖率大于100%,表現出對細胞生長的促進作用,這種促進作用與文獻報道的CM-C能夠促進成纖維細胞的生長的結論相一致[5]。基于以上兩點我們推測,將緩釋藥膜置于牙周袋內,能夠促進牙周膜成纖維細胞的再生。
綜上所述,以CM-C為載體,奧硝唑為主藥制成的緩釋藥膜具有良好的生物安全性,可望應用于臨床。
[1]徐全臣,鐘德鈺,吉秋霞,等.奧硝唑緩釋膜體內外釋放度的研究[J].中國藥房,2007,18(1):33.
[2]徐全臣,王志國,鄧婧,等.奧硝唑緩釋膜生物學性能的初步研究[J].中國海洋藥物,2009,28(6):36.
[3]孫敬方.動物實驗方法學[M].北京:人民衛生出版社,2001:195-375.
[4]Wang LC,Chen XG,Xu QC,et al.Plasma protein adsorption pattern and tissue-implant reaction of poly(vinyl alcohol)/carboxymethyl-chitosan blend films[J].J Biomater Sci Polym Ed,2008,19(1):113.
[5]王征,劉萬順,韓寶芹,等.不同分子量羧甲基殼聚糖的制備及其對皮膚成纖維細胞和角質形成細胞生長的影響[J].生物醫學工程學雜志,2007,24(2):340.

