螺內酯對高糖培養大鼠腎小球系膜細胞增殖及 TGF-β1、FN 分泌的影響
郭曉理,朱雋雅,施 輝*,王德琴,徐美玉
(1南通大學附屬醫院,江蘇 南通 226001;2海安縣人民醫院)
糖尿病腎病(DN)是糖尿病(DM)常見并發癥,其主要的病理改變是腎小球系膜細胞(GMCs)增殖及異常增多,細胞外基質(ECM)過度沉積。轉化生長因子β1(TGF-β1)是其病理改變的主要介導物,不僅可上調ECM蛋白表達,還可降低ECM蛋白降解酶的活性。ECM的主要成分是FN,FN增多是ECM過度沉積的標志。2009年9月~2010年3月,本研究觀察了高糖刺激對大鼠GMCs增殖的影響,并進一步觀察了螺內酯干預后對大鼠GMCs增殖及TGF-β1、FN分泌的影響。現報告如下。
1 材料與方法
1.1 材料 大鼠GMCs購自上海長征醫院腎內科。低糖、高糖DMEM培養液,青—鏈霉素組合雙抗為Gibco公司產品。胎牛血清為杭州四季青公司產品。0.25%胰蛋白酶,24孔、96孔培養板為碧云天公司產品。螺內酯、二甲基亞砜(DMSO)為Sigma公司產品。噻唑藍(MTT)為Amresco產品,ELISA試劑盒由博士德提供。Thermo MK3酶標儀為美國賽默飛世爾科技公司生產。
1.2 方法
1.2.1 大鼠GMCs培養 大鼠 GMCs常規培養在含10%胎牛血清的低糖DMEM培養液中,置37℃5%CO2孵箱中培養。2~3 d傳代1次。取對數生長期GMCs用于實驗。分組:①低糖(5.5 mmol/L)對照組(LG組);②高糖(25 mmol/L)對照組(HG組);③SPI1 組(HG+0.25 μmol/L 螺內酯);④SPI2組(HG+2.5 μmol/L 螺內酯);⑤SPI3 組(HG+25 μmol/L螺內酯);⑥SPI4 組(HG+50 μmol/L 螺內酯)。每組設6個復孔。
1.2.2 螺內酯對大鼠 GMCs增殖的影響 采用MTT法。調整細胞密度至1×105個/ml,將GMCs接種于96 孔板,每孔 200 μl。分別培養 12、24、48 h,于培養結束前4 h加入20 μl的MTT溶液,37℃繼續孵育4 h棄上清,加入150 μl的DMSO振蕩。用酶標儀(波長490 nm)測定OD值。
1.2.3 TGF-β1、FN 的檢測 采用 ELISA 法。調整細胞密度至2×105個/ml,將 GMCs接種于24孔板,每孔1000 μl。培養24 h后,檢測不同濃度螺內酯作用后 TGF-β1、FN 的含量。并檢測 25 μmol/L螺內酯作用12、24、48 h 時 TGF-β1、FN 的含量。操作過程嚴格按ELISA試劑盒操作說明進行。
1.3 統計學方法 采用Stata7.0統計軟件,數據以表示,組間比較采用t檢驗。P≤0.05為差異有統計學意義。
2 結果
2.1 螺內酯對各組大鼠GMCs增殖的影響 見表1。
表1 各組大鼠GMCs增殖比較(n=6,)
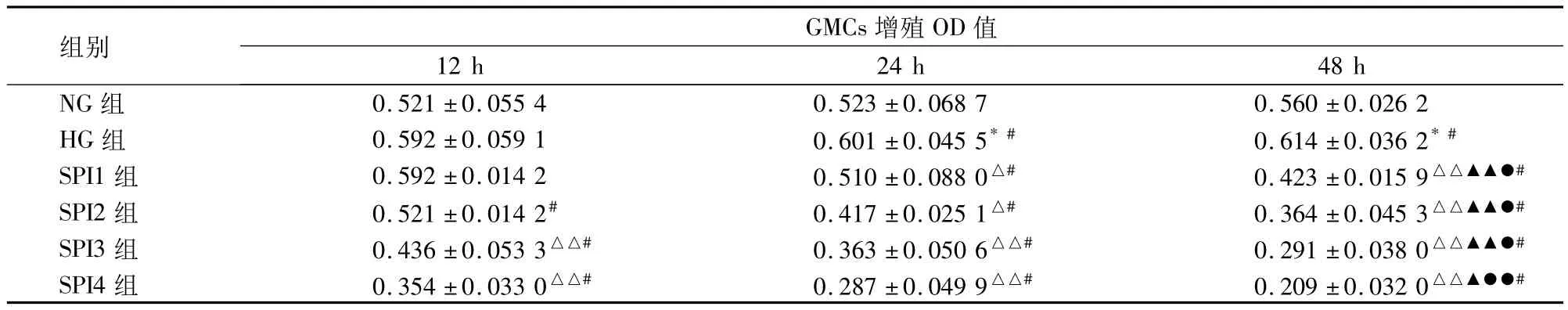
表1 各組大鼠GMCs增殖比較(n=6,)
注:與 NG 組比較,*P <0.05;與 HG 組比較,△P <0.05,△△P<0.01;與同組12 h比較,▲P <0.05,▲▲P <0.01;與同組24 h比較,●P <0.05,●●P <0.01;同一時間各組間比較,#P <0.05
組別GMCs增殖OD值12 h 24 h 48 h NG組0.521 ±0.0554 0.523 ±0.0687 0.560 ±0.0262 HG 組 0.592 ±0.0591 0.601 ±0.0455*# 0.614 ±0.0362*#SPI1 組 0.592 ±0.0142 0.510 ±0.0880△# 0.423 ±0.0159△△▲▲●#SPI2 組 0.521 ±0.0142# 0.417 ±0.0251△# 0.364 ±0.0453△△▲▲●#SPI3 組 0.436 ±0.0533△△# 0.363 ±0.0506△△# 0.291 ±0.0380△△▲▲●#SPI4 組 0.354 ±0.0330△△# 0.287 ±0.0499△△# 0.209 ±0.0320△△▲●●#
2.2 螺內酯對TGF-β1、FN分泌的影響 見表2、3。
表2 各組培養24 h TGF-β1、FN含量比較(n=6,ng/ml,)

表2 各組培養24 h TGF-β1、FN含量比較(n=6,ng/ml,)
注:與 NG 組比較,*P <0.01;與 HG 組比較,△P <0.01;各濃度組后一濃度與前一濃度比較,#P <0.01,##P <0.05
組別 TGF-β1FN NG組0.55 ±0.04 74.5 ±8.9 HG 組 1.03 ±0.03* 118.8 ±6.1*SPI1 組 0.98 ±0.07 103.4 ±7.3△#SPI2 組 0.62 ±0.05△# 81.6 ±6.5△#SPI3 組 0.44 ±0.08△# 68.9 ±5.4△#SPI4 組 0.35 ±0.03△## 51.1 ±6.2△#
表 3 25 μmol/L 螺內酯作用 12、24、48 h TGF-β1、FN含量比較(ng/ml,)

表 3 25 μmol/L 螺內酯作用 12、24、48 h TGF-β1、FN含量比較(ng/ml,)
注:各時間組后一時間組與前一時間組比較,*P<0.01,**P<0.05
檢測項目 25 μmol/L螺內酯作用12 h 24 h 48 h TGF-β1 0.69 ±0.06 0.44 ±0.08* 0.34 ±0.05**FN 80.70 ±9.20 68.90 ±5.40** 60.10 ±7.80**
3 討論
GMCs增殖是DN突出的病理學特征,是引起腎小球ECM增多,并進一步導致腎小球硬化的重要原因。腎素—血管緊張素—醛固酮系統在腎臟纖維化中起著重要作用,但醛固酮的作用一直被忽視。有研究顯示,醛固酮可不依賴于腎素—血管緊張素的效應引起靶器官和血管損傷、纖維化。醛固酮可通過 TGF-β1、鈉氫交換子 1 等誘導 ECM 增生[1,2]。螺內酯是醛固酮受體拮抗劑,其化學結構與醛固酮類似,是醛固酮的競爭性抑制劑,有弱效利尿作用。近年研究證明,醛固酮也是腎纖維化過程中一個重要因素。因而,螺內酯具有預防和減輕腎臟纖維化的作用[3,4],能下調 TGF-β1,減少Ⅰ型膠原的沉積和FN的分泌,減輕了小管間質纖維化[5]。
正常生理情況下,ECM處于不斷產生和降解的動態平衡中。GMCs增殖后,可導致 ECM大量分泌,而ECM對GMCs有正反饋作用,以致這類物質在基質中聚集增多[6]。當各種損傷因子和有害成分如高糖、細胞因子等出現或發生改變時,以上的平衡被打亂,GMCs的形態和功能發生改變,細胞因子和ECM分泌增多[7]。本研究結果表明,高糖環境下GMCs增殖明顯,ECM分泌增多。使用螺內酯干預后增殖受到抑制,基質分泌減少,且呈劑量依賴性。其原因可能與螺內酯能下調TGF-β1等細胞因子水平有關。以往研究發現,體外高糖環境對GMCs的生長具有雙重作用,早期可以刺激細胞增殖,48 h后則抑制細胞增殖[8]。本研究將25 mmol/L葡萄糖作用于GMCs發現,48 h內可促進GMCs的增殖,未出現對細胞的抑制作用,與報道相符,并隨作用時間的延長,細胞增殖越明顯,具有時間依賴性。
綜上所述,螺內酯可以抑制高糖誘導的GMCs增殖及ECM的分泌,為螺內酯防治DN提供了一定的實驗依據。但螺內酯長期使用會引起水、電解質平衡紊亂,雖然本實驗無明顯的細胞損傷,若長期使用,有待進一步研究。
[1]賴凌云,顧勇,郁勝強,等.醛固酮通過Smad2依賴的轉化生長因子-β1途徑刺激大鼠系膜細胞纖連蛋白合成[J].中華腎臟病雜志,2005,21(3):153-156.
[2]張敏敏,顧勇,賴凌云,等.醛固酮可通過鈉氫交換子1誘導腎小球系膜細胞外基質增生[J].中華腎臟病雜志,2006,22(8):477-482.
[3]Epstein M.Aldosterone as a mediator of progressive renal dysfunction:evolving perspectives[J].Intern Med,2001,40(7):573-583.
[4]Mehdi UF,Adams-Huet B,Raskin P,et al.Addition of angiotensin receptor blockade or mineralocorticoid antagonism to maximal angiotensin-converting enzyme inhibition in diabetic nephropathy[J].J Am Soc Nephrol,2009,20(12):2641-2650.
[5]Feria I,Pichardo I,Juarez P,et al.Therapeutic benefit of spironolactone in experimental chronic cyclosporine a nephrotoxicity[J].Kidney Int,2003,63(1):43-52.
[6]Floege J,Johnson RJ,Gordon K,et al.Increased synthesis of extracellular matrix in mesangial proliferative nephritis[J].Kidney Int,1991,40(3):477-488.
[7]房輝,徐剛,于德民,等.TGF-β1和ECM與糖尿病腎病關系的實驗研究[J].中國糖尿病雜志,2000,8(4):227-230.
[8]Wolf G,Sharma K,Chen Y,et al.High glucose induced proliferation in mesangial cells is reversed by autocrine TGF-beta[J].Kindney Int,1992,42(3):647-656.

