Fe2 O3/TiO2復合光催化劑的制備及其表征
劉 紅,陳仕祥,彭秀達,王 翠
(武漢科技大學資源與環境工程學院,湖北武漢,430081)
以TiO2為代表的半導體光催化劑用于污水處理越來越受到普遍關注。TiO2在紫外光作用下能產生氧化能力很強的羥基自由基,可使有機污染物氧化后生成CO2、H2O及其它簡單無機離子[1]。但由于TiO2光催化劑禁帶較寬,只對紫外光響應,光激發產生的電子-空穴對容易復合,其催化效率較低。改進研究發現,用能隙較窄的半導體與TiO2復合制成的光催化劑,可使光催化活性得以提高[2-5]。有關復合半導體光催化劑的研究報道很多[6-15],這些復合半導體光催化劑幾乎都表現出高于單一半導體光催化活性的性質。上述復合光催化劑的制備大多采用浸漬法、水熱法和混合溶膠法。微乳液法是近年來興起的一種合成納米材料的理想方法,具有反應條件溫和、實驗裝置簡單、操作方便、應用領域廣等優點[16]。
本文以九水硝酸鐵為鐵源、硫酸鈦為鈦源,采用微乳液法制備Fe2O3/TiO2復合光催化劑,并用SEM、FTIR、XRD、BET和甲基橙降解率對復合光催化劑性能進行表征,考察不同制備條件下復合光催化劑的活性。
1 實驗
1.1 試劑
試劑為十二烷基硫酸鈉(SDS)、正庚烷、正丁醇、硫酸鈦、九水硝酸鐵、氨水和甲基橙,均為分析純。
1.2 Fe2 O3/TiO2復合光催化劑制備
將4 g十二烷基硫酸鈉、5 m L正丁醇與30 m L正庚烷混合并攪拌均勻,按照一定Fe與Ti的摩爾比,在快速攪拌下緩慢滴加一定體積的九水硝酸鐵和硫酸鈦水溶液,得到澄清的微乳液,用氨水調節微乳液p H值至6,超聲波分散30 min,放入內襯為聚四氟乙烯的不銹鋼密閉反應釜中,在160℃下水熱合成2 h,冷卻至室溫,取出產物進行抽濾,所得固體用蒸餾水和無水乙醇洗滌,干燥后充分研磨,再于一定溫度下煅燒1.5 h,自然冷卻后得到Fe2O3/TiO2復合光催化劑。
1.3 光催化活性評定
光催化活性測定在圓形玻璃缸中進行,以300 W高壓汞燈為紫外光源,反應液液面與紫外燈距離為10 cm。室溫下,將0.05 g光催化劑加入到100 m L濃度為25 mg/L的甲基橙溶液中,關閉紫外光源,在光催化反應器暗環境內攪拌0.5 h,進行吸附,打開紫外光源,15 min后移取約10 m L混合液,離心分離,取上層清液,用日本島津公司UV2550型分光光度計測定吸光度,用甲基橙的降解率來評定光催化劑的活性。降解率計算公式為
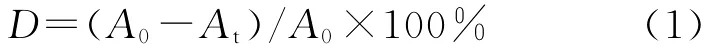
式中:A0、At分別為反應前后甲基橙溶液的吸光度。
1.4 結構與性能表征
用日本理學公司D/MAX-ⅢA型全自動X射線衍射儀進行晶相分析(Cu Kα輻射,40 k V/50 m A,掃描范圍5°~70°),用德國VERTEX 70型傅立葉紅外光譜儀進行結構分析,用德國Nava 400 Nano掃描電鏡觀察微觀形貌,用美國貝克曼庫爾特公司SA3100比表面積和孔徑分析儀對樣品的比表面積、孔徑和孔容進行表征,采用多點BET法和BJH法,利用相對壓力為0.05~0.2所對應的N2吸附數據計算總孔體積和比表面積。
2 結果與討論
2.1 Fe2 O3/TiO2晶相轉變
Fe/Ti摩爾比為1∶3時,不同煅燒溫度下所制Fe2O3/TiO2樣品XRD圖譜如圖1所示。從圖1中可看出,經300℃煅燒后的Fe2O3/TiO2樣品,其銳鈦礦相TiO2的特征峰位于25.3°處;當煅燒溫度為500℃時,代表銳鈦礦相的幾個最強特征衍射峰已非常明顯,同時還有少量的金紅石相出現;隨著煅燒溫度進一步升高,金紅石相逐漸增多,銳鈦礦相所占比例相對減少。此外,500℃煅燒過的Fe2O3/TiO2在25.3°處的銳鈦礦相TiO2特征衍射峰最為尖銳,表明此時晶型結構最好;600℃時,金紅石相特征峰不僅增多,衍射峰強度也在進一步增大,明顯呈現出TiO2由銳鈦相向金紅石相轉變的趨勢。
隨煅燒溫度不斷升高,Fe2O3/TiO2由淺黃色變為深紅色,表明有鐵的氧化物生成。從圖1中可看出,樣品在500℃時出現了α-Fe2O3的特征衍射峰,并且在600℃下其進一步增多。

2.2 Fe2 O3/TiO2紅外光譜分析
經500℃×1.5 h煅燒,TiO2和不同Fe/Ti摩爾比時所制Fe2O3/TiO2樣品紅外光譜如圖2所示。從圖2可看出,3 742 cm-1和1 650 cm-1處的吸收峰屬于O—H的彎曲振動吸收峰,3 422 cm-1處的寬峰是是由O—H的伸縮振動引起的[17]。此外,2 923 cm-1處的峰為C—H鍵的伸縮振動引起[18],表明有少量的有機物殘留在樣品中。在1 129 cm-1處,有3種不同Fe/Ti摩爾比的Fe2O3/TiO2樣品均出現α-FeOOH的特征吸收峰;在656 cm-1處,只有n(Fe)∶n(Ti)=1∶3的Fe2O3/TiO2出現了與TiO2對應的Ti—O—Ti鍵特征峰,其他兩種Fe2O3/TiO2則在976 cm-1處出現了代表α-Fe2O3結構的Fe—O鍵特征吸收峰,這是由于α-FeOOH因脫水而發生部分結構演變所致[15]。
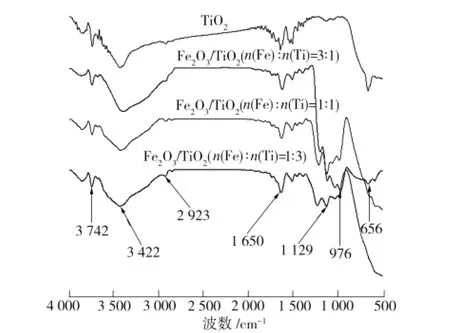
圖2 TiO2和不同Fe/Ti摩爾比所制Fe2 O3/TiO2紅外光譜Fig.2 FTIR spectra of the TiO2 and Fe2 O3/TiO2 nanoparticles
2.3 Fe2 O3/TiO2顆粒形貌
不同Fe/Ti摩爾比時所制Fe2O3/TiO2樣品SEM照片如圖3所示。從圖3中可看出,Fe/Ti摩爾比為1∶3時所制Fe2O3/TiO2樣品疏松多孔、顆粒細小且分散性較好(圖3(a));Fe/Ti摩爾比為1∶1時所制Fe2O3/TiO2樣品粒徑分布雖較均勻,但粒徑較大,且存在少量團聚現象,顆粒之間存在明顯的界限(圖3(b));Fe/Ti摩爾比為3∶1時所制Fe2O3/TiO2樣品為無數分布極不均勻的顆粒聚集而成的團聚體(圖3(c))。
2.4 Fe2 O3/TiO2比表面積及孔徑分布
經500℃×1.5 h煅燒,Fe/Ti摩爾比為1∶3時所制Fe2O3/TiO2樣品孔徑分布及N2吸附等溫曲線如圖4所示。由圖4孔徑分布曲線可以看出,Fe/Ti摩爾比為1∶3時所制Fe2O3/TiO2孔徑分布主要聚集于5.45~6.14 nm,平均孔徑為5.79 nm。不同Fe/Ti摩爾比所制Fe2O3/TiO2及TiO2和P-25總孔體積和比表面積如表1所示。從表1中可見,n(Fe)∶n(Ti)=1∶3時所制Fe2O3/TiO2樣品比表面積為60.282 m2/g,Fe/Ti摩爾比為1∶3時所制Fe2O3/TiO2復合光催化劑比TiO2、P-25光催化劑具有更大的比表面積,是一種孔徑細小的多孔材料,這種多孔結構有利于光催化反應物的吸附和產物的快速擴散,提高了光催化反應效率。

圖3 不同Fe/Ti摩爾比所制Fe2 O3/TiO2 SEM照片Fig.3 SEM images of Fe2 O3/TiO2
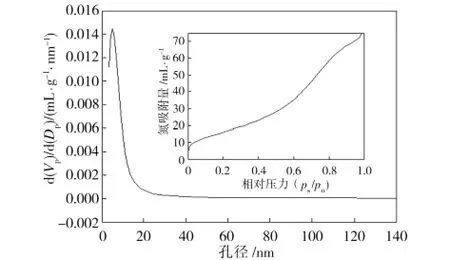
圖4 Fe2 O3/TiO2孔徑分布及N2吸附曲線Fig.4 Pore size distribution curve and N2 adsorption isotherms curve of Fe2 O3/TiO2

表1 不同光催化劑總孔體積和比表面積Table 1 Total pore volume and specific surface area of different photocatalysts
2.5 Fe2 O3/TiO2對甲基橙降解率
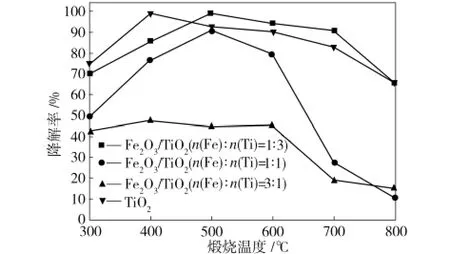
圖5 不同煅燒溫度下Fe2 O3/TiO2和TiO2對甲基橙的降解率Fig.5 Comparison of photocatalytic degradation of methyl orange over Fe2 O3/TiO2 and TiO2
不同煅燒溫度下所制Fe2O3/TiO2和TiO2對甲基橙的降解率如圖5所示。由圖5中可看出,煅燒溫度低于500℃時,除n(Fe)∶n(Ti)=3∶1時所制Fe2O3/TiO2外,其他Fe2O3/TiO2對甲基橙的降解率均隨煅燒溫度升高而增高,500℃時n(Fe)∶n(Ti)=1∶3所制Fe2O3/TiO2對甲基橙的降解率高達99.7%,優于相同條件下的TiO2光催化劑。
3 結論
鐵與鈦的摩爾比為1∶3、煅燒溫度為500℃和煅燒時間為1.5 h條件下所制Fe2O3/TiO2復合光催化劑樣品疏松多孔、顆粒細小且熱穩定性高,經紫外光照15 min后對甲基橙的降解率為99.7%,與相同條件下制備的TiO2相比具有更好的光催化活性和更大的比表面積。
[1] Masakazu A,Masato T.The design and development of highly reactive titanium oxide photocatalysts operating under visible light irradiation[J].J Catal,2003,216:05-16.
[2] 陳曉青,楊娟玉,蔣新宇,等.摻鐵TiO2納米微粒的制備及光催化性能[J].應用化學,2003,20(1):73-76.
[3] 付川,祁俊生,潘杰,等.Fe2O3-TiO2光催化降解水中酸性橙Ⅱ研究[J].環境科學與技術,2009,32(9):49-52.
[4] 張廷相,楊芬.TiO2-Fe2O3復合材料降解甲基橙溶液的研究[J].化學工程與裝備,2009,11(11):32-36.
[5] 謝立進,馬峻峰,趙忠強,等.半導體光催化劑的研究現狀及展望[J].硅酸鹽通報,2005,24(6):80-84.
[6] Wang C Y,Shang H M,Ying T,et al.Properties and morphology of CdS compounded TiO2visiblelight photocatalytic nanofilms coated on glass surface[J].Separation and Purification Technology,2003,32(1-3):357-362.
[7] Takayuki H,Keiko S,Isao K.Preparation and photocatalytic properties of composite CdS nanoparticles-titanium dioxide particles[J].Colloid Interface Science,2001,244(2):262-265.
[8] Fang J H,Lu X M,Zhang X F,et al.CdSe/TiO2nanocrystalline solar cells[J].Supramolocular Science,2001,5(5-6):709-711.
[9] 李志杰,侯博,徐耀,等.水熱法制備氧化硅改性的納米二氧化鈦光催化劑[J].石油化工,2004,33:789-791.
[10]蒲玉英,方建章,彭峰,等.微乳法制備納米TiO2/SiO2的結構及光催化研究[J].無機化學學報,2007,23(6):1 045-1 049.
[11]Wang M,Liu S W,Xiu Z L.Preparation and photocatalytic properties of silica gel-supported TiO2[J].Materials Letters,2006,60(7):974-978.
[12]K Tennakone,J Bandara.Enhanced rates of photocatalytic degradation of an azo dye using coupled SnO2/TiO2semiconductor thin films[J].Environ Sci Technol,2005(29):841-845.
[13]孫旋,劉紅,倪昕.Fe2O3-TiO2光催化劑的制備及其對堿性嫩黃的降解[J].水處理技術,2008,34(4):61-64.
[14]Hong L,H K Shou,Xuan S,et al.Preparation and characterization of visible light responsive Fe2O3-TiO2composites[J].Applied Surface Science,2011(257):5 813-5 819.
[15]龔瀟,陳天虎,慶承松,等.TiO2/α-Fe2O3復合光催化劑的制備及表征[J].硅酸鹽學報,2008,36(6):838-843.
[16]牛新書,許亞杰,張學治,等.微乳液法制備納米二氧化鈦及其光催化活性[J].功能材料,2003,5(34):548-550.
[17]Yu J G,Zhao X J,Yu J C,et al.The grain size and surface hydroxyl content of super-hydrophilic TiO2/SiO2composite nanometer thin films[J].Journal of Materials Science Letters,2001,20(18):1 745-1 748.
[18]李躍軍,曹鐵平.靜電紡絲法制備Fe2O3/TiO2復合納米纖維及光催化性能研究[J].河北師范大學學報,2010,34(6):702-706.

