吡咯烷二硫代氨基甲酸對脂多糖致急性肺損傷大鼠NF-κB P65蛋白表達的影響
王紅嫚 薛關生 萬義增 王 健 臧東鈺 (遼寧醫學院附屬第三醫院呼吸科,遼寧 錦州 200)
急性肺損傷(ALI)/急性呼吸窘迫綜合征(ARDS)可引起頑固性低氧血癥,病死率極高,發病機制復雜,缺乏有效治療措施〔1〕。核轉錄因子-κB(NF-κB)是啟動眾多炎癥介質基因轉錄的關鍵性因子,能夠與DNA結合,幾乎存在于體內所有細胞。在脂多糖(LPS)、腫瘤壞死因子-α(TNF-α)等激活劑的刺激下,NF-κB進入細胞核與DNA特定的κB序列結合,使炎性介質和細胞因子基因轉錄增強,在炎癥反應過程中發揮重要作用〔2〕。目前發現,ALI存在NF-κB激活,在ALI/ARDS中起著重要作用,控制NF-κB的活化可能成為治療ALI/ARDS的關鍵環節。為此,本文通過觀察LPS致大鼠ALI時肺組織胞質、胞核中P65蛋白變化及NF-κB抑制劑吡咯烷二硫代氫基甲酸(PDTC)對P65蛋白分布的影響,進一步探討PDTC對ALI的保護作用。
1 材料與方法
1.1 動物分組及模型制備 54只300~350 g健康雄性Wistar大鼠,隨機分為三組。對照組6只,ALI組(L組)24只;PDTC干預組(P+L組)24只;ALT組和PDTC干預組分別于腹腔注射LPS后1、2、4、8 h作為觀測時間點。在各不同觀測時間點取10%鹽酸氯胺酮溶液(50 mg/kg)腹腔注射麻醉。
1.2 方法
1.2.1 細胞質和細胞核核蛋白的提取 制模后,取右肺中、下葉肺組織約100 mg,用0.01 mol/L磷酸鹽緩沖液(PBS)充分洗滌,加入核蛋白提取裂解緩沖液 A 1.5 ml,冰上放置15~30 min,用電動勻漿器制成勻漿后加入500μl 10%NP-40,渦旋10 s,4℃、12 000 r/min離心30 s,上清即為細胞質蛋白。將沉淀物用冷PBS洗滌一次,4℃、12 000 r/min離心30 s,棄上清。加入1.5 ml核蛋白提取裂解液B,冰上放置30 min,然后4℃、12 000 r/min離心2 min,吸出上清(核蛋白),Bradford比色法測定核蛋白濃度,并調至0.5~1.0μg/μl,置于-70℃保存。
1.2.2 Western印跡半定量檢測NF-κB p65 20μg蛋白,10%聚丙烯酰胺凝膠電泳、轉膜、封閉,一抗4℃過夜,二抗室溫1 h,增強化學發光法(ECL)顯色。將免疫印跡所得結果經圖像掃描分析,以積分灰度值(IDV)表示P65相對含量。
1.3 統計學方法 應用SPSS13.0統計軟件進行分析,數據用±s表示,組間比較采用t檢驗。
2 結果
將對照組胞質P65蛋白的IDV設為1,用其他各組P65蛋白的IDV與其的比值作為相對表達強度。結果顯示:ALI組各時相肺組織胞質中NF-κB P65蛋白的表達強度較對照組顯著降低(P<0.01)而胞核中P65蛋白表達強度較對照組顯著升高(P<0.01);但PDTC干預組與ALI組比較,肺組織胞質中P65蛋白的表達強度較對照組升高(P<0.05),而胞核中P65蛋白表達強度較ALI組降低(P<0.05)。見表1,圖1。
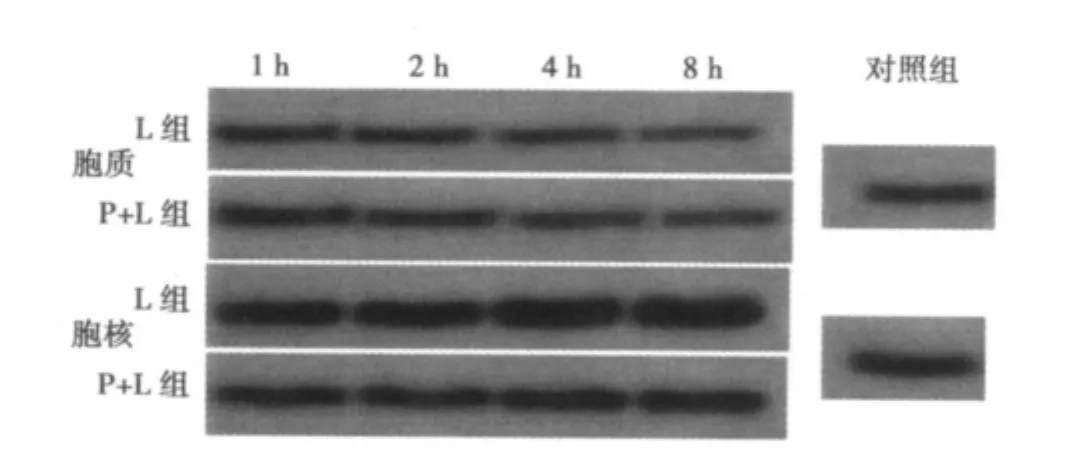
圖1 不同時相肺組織胞質、胞核NF-κB P65蛋白表達變化
3 討論
研究表明,ALI存在著 NF-κB 激活,NF-κB 可使 TNF-α 等炎性介質的轉錄最大化;活化后參與許多基因的轉錄調控,在感染、炎癥反應、氧化應激、細胞凋亡等病理過程中發揮重要作用。它是由P50、P52、P65、c-Rel、RelB 五種亞單位組成的同源或異源二聚體,發揮主要生理功能的是P50/P65異源二聚體,其中NF-κB P65為其主要亞單位。通常狀態下,蛋白以二聚體形式與IκB抑制蛋白(NF-IκB)直接結合形成三聚體復合物 ,以非活性形式存在于細胞質中。在LPS等激活劑的刺激下,IκB抑制蛋白降解,使NF-κB進入細胞核與DNA特定的κB序列結合,其中P50與DNA結合有關,P65則因含有轉錄活化區域負責轉錄激活。本研究發現ALI組各時相肺組織胞質中P65蛋白的表達強度較對照組顯著降低,而胞核中P65蛋白表達強度較對照組顯著升高。說明P65蛋白在ALI/ARDS的發生和發展中起著重要作用,控制NF-κB的活化可能成為治療ALI/ARDS的關鍵環節。
PDTC是NF-κB的特異性抑制劑,可調節NF-κB活化,控制致炎細胞因子的表達,具有抗氧化、抗細菌、真菌及抗腫瘤等特性〔3,4〕。研究發現,PDTC 通過抗氧化作用阻礙抑制蛋白 IκB從NF-κB復合體上解離,從而抑制NF-κB活化,阻礙NF-κB的P65、P50亞基向細胞核轉移,使細胞核中的表達明顯減少,在轉錄水平上抑制TNF-α、白介素-1等炎性細胞因子的產生〔5〕;還可直接降低NF-κB與DNA結合能力,干擾NF-κB激活的信號通路〔6〕。本研究發現,PDTC干預組與ALI組比較,肺組織胞質中P65蛋白的表達強度較ALI組升高,而胞核中P65蛋白表達強度較ALI組降低。因此,通過抑制NF-κB的活化來控制炎性介質的過度釋放,可拓展臨床治療ALI/ARDS的新路徑。
1 中華醫學會重癥醫學分會.急性肺損傷/急性呼吸窘迫綜合征診斷與治療指南2006〔J〕.中華內科雜志,2007;46(5):430-5.
2 徐 嫻,孫士其.重癥急性胰腺炎核因子-κB及炎癥介質與肺損傷的實驗研究〔J〕.醫學臨床研究,2003;20(2):84-7.
3 鄧朝勝,王 辰,龐寶森,等.中性粒細胞在肺血栓栓塞癥犬肺缺血-再灌注損傷中的作用〔J〕.中華結核和呼吸雜志,2006;29(9):603-60.
4 Hart SP,Dransfield I,Rossi AG.Phagocytosis of apoptotic cells〔J〕.Methods,2008;44(3):280-5.
5 Bellas RE,FitzGerald MJ,Fausto N,et al.Inhibition of NF-κB activity induces apoptosis in murine hepatocytes〔J〕.Am J Pathol,1997;151(4):891-6.
6 Li YQ,Zhang ZX,Xu YJ,et al.N-Acetyl-L-cysteine and pyrrolidine dithiocar-bamate inhibited nuclear factor-kappaB activation in alveolar macrophages by different mechanisms〔J〕.Acta Pharmacol Sin,2006;27(3):339-46.

