卡培他濱聯(lián)合放療的抗瘤效應研究
弋振營 邢月明 晉剛
(1.開封市第一人民醫(yī)院腫瘤科 河南開封 475000; 2.山西醫(yī)科大學第二醫(yī)院腫瘤1科 太原 030001)
放療是非小細胞肺癌的主要治療手段之一,但放射治療5年生存率低。本實驗探討卡培他濱聯(lián)合放療對小鼠Lewis肺癌的抑瘤效應。
1 材料與方法
1.1 主要實驗材料
動物及模型:C57BL/6J近交系雄性小鼠48只,引自中國醫(yī)學科學院實驗動物中心,許可證號:SCXK(京)2004-0001。鼠齡6周,體重18~22g。
卡培他濱片:規(guī)格500mg/片,批號:SH0075。上海羅氏制藥有限公司提供。
照射方法:采用北京大恒公司KB1800型醫(yī)用電子直線加速器,6MV-X線進行照射,SSD為100cm,劑量率為3Gy/min。
1.2 分組及處理
移植瘤直徑達1cm左右時,隨機分為:4組,每組12只。(1)對照組,不做任何處理;(2)放療組,X射線照射腫瘤局部5Gy/次×4次,隔日進行1次;(3)卡培他濱組,按60mg/(kg·d),每只小鼠每天灌胃200μL卡培他濱混懸液,連用10d;(4)卡培他濱+放療組,放療和卡培他濱用法用量同前。
1.3 療效觀察
每天觀察荷瘤鼠活動、毛色、進食等情況。每2天用游標卡尺測量并計算腫瘤體積:V=1/6AB2π(A>B)[1]一次。(A:腫瘤的最大長徑;B:與A垂直的最大寬經),觀察腫瘤的生長情況并繪制腫瘤生長曲線。
1.4 病理形態(tài)觀察
放療結束后5d,引頸脫臼處死小鼠,取腫瘤組織切片、HE染色,普通光鏡下(100倍)觀察腫瘤組織。
1.5 測定瘤組織微血管密度(MVD)、血管內皮生長因子(VEGF)表達陽性率:
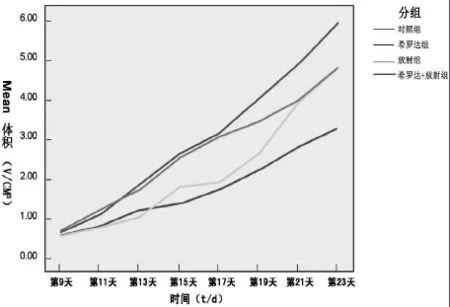
圖1 移植瘤體積生長曲線

圖2 移植腫瘤組織內MVD(免疫組化x200)

圖3 腫瘤組織內VEGF表達陽性率(免疫組化x400)
CD34或VEGF抗體為Ⅰ抗,SABC法免疫組化染色,具體方法根據試劑盒說明書。MVD計數按Weidner[2]的評判標準進行。低倍鏡(x40)下選擇5個血管最多的“熱點”區(qū)域,在200倍視野下計數,每例標本計數5個視野,最后取平均值。VEGF表達陽性率:隨機選取5個腫瘤外周區(qū)域,計數高倍鏡(×400)下染色陽性的腫瘤細胞,陽性細胞數除以同一視野下腫瘤細胞總數,求得腫瘤細胞VEGF表達陽性率(%)[3]。
1.6 統(tǒng)計分析
利用SPSS13.0軟件進行統(tǒng)計分析。計量資料以均數土標準差表示,治療前腫瘤體積指標采用單因素方差分析,多個樣本間均數比較采用析因設計方差分析。P<0.05認為差異有顯著性。
2 結果
(1)治療前各組腫瘤體積無差別(P>0.05)。隨著時間的延長,各組腫瘤的體積均逐漸變大。對照組小鼠的腫瘤生長曲線最陡,各治療組小鼠的腫瘤生長曲線變平緩,放療+卡培他濱組曲線最平緩,說明對腫瘤抑制作用最強(圖1)。
(2)實驗結束后,進行移植瘤組織病理學檢查,移植瘤組織內有壞死,鏡下均可見癌組織,癌細胞圓形或橢圓形,核大,核仁明顯,濃然,細胞大小不等,癌細胞被纖維組織分隔成大小不等的癌巢。①組癌細胞生長旺盛,壞死很少。②組內可見大片狀壞死。
(3)腫瘤組織切片中,微血管多集中于腫瘤細胞浸潤的邊緣部位。CD34陽性染色主要位于細胞的胞漿、核膜上,為棕黃色或褐色顆粒(圖2)。
VEGF主要表達于腫瘤細胞的細胞質,陽性染色的腫瘤細胞多位于浸潤邊緣,表現為胞漿內均勻棕黃色細顆粒狀。血管內皮細胞可呈弱陽性染色(圖3)。
析因設計方差分析結果:MVD的放療因素與卡培他濱因素主效應均有統(tǒng)計學意義(P<0.001);VEGF放療因素與卡培他濱因素主效應均有統(tǒng)計學意義(P<0.001);卡培他濱和放療聯(lián)合應用組的MVD、VEGF均數最小,即放療與卡培他濱2種方法同時應用,腫瘤組織的MVD值、VEGF表達陽性率最低。放療因素與卡培他濱組因素之間存在交互作用(P<0.001;P<0.05)。
3 討論
肺癌是臨床常見、病死率最高的惡性腫瘤之一,其中以非小細胞肺癌最常見。約80%肺癌病例需接受放療或放化療綜合治療。提高放射治療增益比是腫瘤放射治療的根本目標[4]。腫瘤劑量越大,腫瘤控制率就越高,但同時,對正常的組織和細胞損傷也越大。因此放療劑量不能無限提高。
5-Fu可抑制DNA放射損傷的修復及使周期敏感細胞成分增加,從而產生良好的放療增敏作用。但由于5-Fu的嚴重粘膜反應和用藥的復雜性,限制了其臨床應用[5]。卡培他濱是5-FU的前體藥物,通過TP酶轉化為5-Fu而激活。TP酶在腫瘤組織中的濃度增高,如其在肺癌中的陽性率達63.8%[6],正常肺組織無表達。這種現象有利于發(fā)揮卡培他濱的放療增敏作用;同時有研究表明放療可增強人類腫瘤移植物中TP酶的表達,從而間接增加腫瘤內氟尿嘧啶的濃度,但對周圍正常組織無影響,即放療提高了卡培他濱本身對腫瘤組織的殺傷力。
Folkman[7]首先發(fā)現了新生血管對腫瘤生長的重要作用。此后,多數人充分肯定了MVD與多種惡性腫瘤的發(fā)生、發(fā)展的密切關系。作為反映腫瘤血管生成的最有效的客觀指標,目前多用二維平面上即顯微鏡焦平面上微血管的數量定量微血管密度。VEGF是一種具有高度生物活性的功能性糖蛋白,最早在牛垂體的腺泡細胞中發(fā)現并提取[8],是最強的一種促血管生成物質,對血管內皮細胞的增殖、基膜降解、內皮細胞遷移和血管構建的調控作用較強,且特異性高[9]。目前,抗血管生成已迅速發(fā)展為重要的抗癌策略,并成為腫瘤治療領域的研究熱點。研究顯示放療有明顯的抗腫瘤血管生成作用[10]。
本課題通過動物實驗對卡培他濱與放療協(xié)同作用進行了初步探索。從實驗資料中可看出,卡培他濱加放療抑瘤作用最明顯,移植瘤組織內新生血管的數量減少最明顯,而且血管內皮生長因子表達率在所有處理組中均最低。二者協(xié)同抗瘤的具體機制還有待進一步研究。但由于樣本量較小,有待進一步研究。
4 結語
卡培他濱聯(lián)合放療對C57BL/6J小鼠Lewis肺癌有協(xié)同抗瘤作用。
[1]姜揚文,錢莉,蔣桂花,等.ber-abl基因疫苗對小鼠SP2/0/BCR-ABL移植瘤的影響[J].中國實驗血液學雜志,2006,14(4):800~803.
[2]Weidner N,Folkman J,Pozza F,et al.Tumor angiogenesis:a new significant and independent prognositic indicator in early strage breast carcinoma[J].Natl Cancer Inst,1992,84(24):1875~1887.
[3]Vermeulen PB,Gasparini G,Fox SB,et al.Quantification of angiogenesis in solid human tumors:An international consensus on the methodology and criteria of evaluation[J].Eur J Cancer,1996,32A:2474~2484.
[4]殷蔚伯,余子豪,徐國鎮(zhèn),等.腫瘤放射治療學[M].北京:中國協(xié)和醫(yī)科大學出版社,2008:141.
[5]駱華春.鼻咽癌放射增敏藥物的臨床研究進展[J].實用癌癥雜志,2010,25(4):430.
[6]姜麗娜,于世英,熊慧華,等.胸苷磷酸化酶在癌組織中表達的研究[J].中華腫瘤雜志,2004,26(5):297~299.
[7]Folkman J.What is the evidence that tumors are angigenesis depent[J].Journal of the National CancerInstitute,1990,82:4~6.
[8]Carmeliet P,Collen D.Molecular basis of angiogenesis.Role of VEGF and VE-cadherin[J].Ann NY Acad Sci,2000,902:249~264.
[9]趙利枝,楊日芳,汪海.內皮細胞與血管形成[J].中國藥理學通報,2002,18(4):361~364.
[10]陳洪雷,張苗,王雅杰.放療對荷瘤鼠腫瘤血管生成的抑制作用[J].現代腫瘤醫(yī)學2006,14(12):1494.

