培養濾液MPT64抗原檢測結核分枝桿菌復合群生長的效能分析
許婉華 黃業倫 劉燕文 胡麗環 羅少珍 孟繁榮 劉志輝
結核分枝桿菌復合群(Mycobacterium tuberculosiscomplex,MTBC)特異性分泌蛋白 MPT64的發現、免疫膠體金法檢測方法的創立及相關檢測試劑的成功研發,為分枝桿菌培養物的MTBC與非結核分枝桿菌(non-tuberculous mycobacteria,NTM)的鑒定帶來了極大的便利[1-2]。筆者在應用 MPT64分泌蛋白檢測鑒定MTBC的研究中還發現:不管是采用液體培養基還是固體培養基,只要有MTBC生長,在絕大多數情況下均可檢測到MPT64分泌蛋白[3]。這就提示人們MPT64蛋白的分泌可以作為MTBC的生長指示而成為MTBC培養的檢測標志物,而且目前的研究表明MPT64為MTBC早期分泌蛋白,應用其作為MTBC生長檢測標志物可能具有快速的特點,筆者的初步研究結果證實了這一特點[4]。為進一步確證這一實驗方法的檢測效能,筆者進行了大樣本量的對照研究,現報道如下。
材料和方法
一、臨床樣本來源
2010年8月至2010年12月我院結核病防治所門診2064例患者送檢的分枝桿菌分離培養標本,其中2012例痰標本、12例胸腔積液標本、40例支氣管灌洗液標本。
二、儀器和試劑
儀器分析法采用BACTEC MGIT 960分枝桿菌快速培養系統;培養基應用儀器系統專用培養基(美國BD公司生產),主要成分為 Middlebrook 7H9;MPT64抗原免疫膠體金法檢測試劑盒購自杭州創新生物檢控技術有限公司。
三、研究方案設計
以目前人們公認檢測性能優良的BACTEC MGIT 960分枝桿菌快速培養儀器法(簡稱“儀器法”)為參照,分析培養濾液MPT64抗原檢測法(簡稱“MPT64檢測法”)指示MTBC生長的準確性和快速性。考慮到MPT64檢測法不能實現連續監測,則根據成本-效益原則將整個研究分為3個階段:(1)參照國家關于新型實驗方法臨床驗證強制性樣本量要求,采用雙盲方法對一定數量儀器法已經報告結果(包括陽性、陰性和污染)的分枝桿菌培養瓶培養濾液進行一次MPT64抗原檢測,初步評估MPT64檢測法的準確性。(2)在培養的第7、14、21、28、35、42天(即第1~6周末)與儀器法同步進行培養濾液MPT64抗原檢測,以“周”為時間單位比較兩種方法各周的累積陽性檢出率(%),分析其快速性能。(3)綜合前2個階段的實驗結果,以儀器法為參照標準,分析對于全部標本和儀器法陽性標本MPT64檢測法的符合率(%),分析MPT64檢測法的準確性。
四、實驗方法
1.儀器法:主要實驗步驟包括標本收集與前處理、標本接種、上機與儀器監測、儀器報告陽性標本的涂片確認及MTBC與NTM分群等。標本收集與前處理嚴格按BACTEC MGIT 960分枝桿菌快速培養儀推薦方法進行;儀器培養檢測步驟按儀器說明書進行;儀器報告陽性者經涂片抗酸染色法確認,抗酸染色陽性者報告“有抗酸桿菌生長”,陰性者報告“污染”;MTBC與NTM分群應用對硝基苯甲酸(paranitrobenzoic acid,PNB)培養生長試驗,1個月未見菌落生長者為MTBC。
2.MPT64檢測法:按研究設計方案適時對培養濾液進行MPT64抗原檢測,具體檢測方法和結果判讀按試劑盒說明書嚴格進行:在生物安全柜中,以無菌方法取培養液約0.1ml加入試劑檢測孔中,15min后觀察結果,1h內觀察完畢;檢測線和質量控制(簡稱“質控”)線均出現紫紅色條帶為陽性,質控線出現檢測線未出現紫紅色條帶者為陰性,質控線未出現者表示試劑存在問題而必須重新檢測。并且在第2研究階段強調:在儀器系統監測時點間隔間(筆者的儀器設置整點為檢測時點)取出適量標本,所取標本必須在監測時點間隔內完成檢測操作并放回儀器系統,以免影響儀器對分枝桿菌生長的檢測。在本實驗研究中,納入第1、2階段研究的樣本量分別為799例和1265例樣本。
五、統計學處理
和儀器法比較:應用χ2檢驗對所有2064例樣本檢測結果進行統計學分析,并計算于全部標本和儀器法陽性標本MPT64檢測法的符合率(%),評估MPT64檢測法的準確度;以“周”為時間單位比較兩種方法各周的累積陽性檢出率(%),并應用t檢驗比較分析MPT64檢測法的快速性。兩種統計學方法均以P<0.05為有統計學意義。
結 果
一、兩種方法檢測結果比較
對于2064例分枝桿菌培養的臨床標本,儀器法報告298例MTBC、108例NTM、1521例培養陰性及137例污染(后三者即無MTBC生長),其中分別有279、6、0、2例 MPT64檢測陽性,即 MPT64檢測法可報告有MTBC生長,兩者間差異無統計學意義(χ2=0.12,P=0.742)。與儀器法的總體一致性為98.69%(2037/2064),對儀器法報告為 MTBC者MPT64檢測法的陽性率為93.62%(279/298),具有較高的陽性符合水平(表1)。
二、兩種方法1~6周陽性檢測結果比較
每周進行MPT64監測的1265例培養液樣本中,兩種方法均檢測到MTBC者168例,其中:儀器法在培養1~6周儀器報告陽性率分別為25.60%(43/168)、66.67%(112/168)、92.26%(155/168)、98.21%(165/168)、98.81%(166/168)和100.00%(168/168),MPT64檢測法的陽性檢出率則分別為17.26% (29/168)、61.90% (104/168)、89.88%(151/168)、95.24%(160/168)、98.81%(166/168)和100.00%(168/168)。兩者陽性報告時間差異無統計學意義(t=1.68,P=0.366)(表2)。
討 論
創建準確、快速、簡便、經濟的結核病病原學實驗診斷方法一直是人們追求的目標,但無論是以菌落生長為觀察終點的傳統固體培養方法、還是以監測分枝桿菌呼吸活動的各種儀器系統快速培養法、亦或是以特定基因序列為檢測靶標的各類分子技術以及其他的實驗技術(如噬菌體生物擴增法、變色培養基法等),迄今為止仍無一種實驗方法盡如人意。本研究評估的MPT64檢測法是否可以解決部分問題?目前鮮見同類文獻報道。
從本研究檢測結果看,無論是對于整體樣本還是MTBC陽性樣本,MPT64檢測法和目前檢測效能優良但實驗費用不菲且需專門儀器的BACTEC MGIT 960分枝桿菌快速培養儀器法間具有高度的一致性,說明其準確性可以與儀器法相媲美。從陽性樣本報告時間看,兩者陽性報告時間非常接近,但儀器報告陽性時間并不能直接代表實驗報告時間,實驗報告時間還需加上抗酸桿菌確認、MTBC與NTM分群等實驗時間,如本研究分群采用的PNB培養生長試驗則需4周之久。因此,可以毫無疑問地認為MPT64檢測法比儀器法更為快速。實驗操作程序簡單,MPT64檢測法可直接報告“有MTBC生長”,不需要儀器法的后續步驟,且其實驗操作本身也極其簡單(只須以無菌方法取培養液0.1ml加入試劑檢測孔中一個簡單操作,15min后即可觀察結果)。而且,MPT64檢測法國內有上市的試劑盒,也不需要任何儀器設備,亦不需要儀器法的后續實驗費用,與需要進口專門儀器與專用試劑的儀器法相比,檢測費用相對較低,符合實驗方法的經濟性原則。另外,本研究儀器法報告為“NTM”或“污染”的245例樣本中MPT64檢測法有8例呈現陽性,也許可以認為其對與其他細菌混合生長的MTBC具有較強的甄別能力。綜上所述,MPT64檢測法具有準確、快速、簡便、經濟的特點,值得在臨床中推廣應用,尤其適合在基層醫療單位開展。
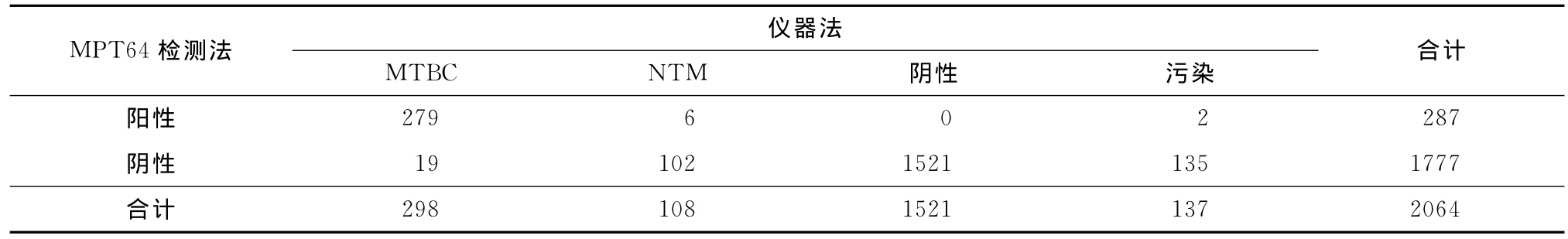
表1 2064例分枝桿菌培養濾液MPT64檢測結果與儀器法檢測比較(例)
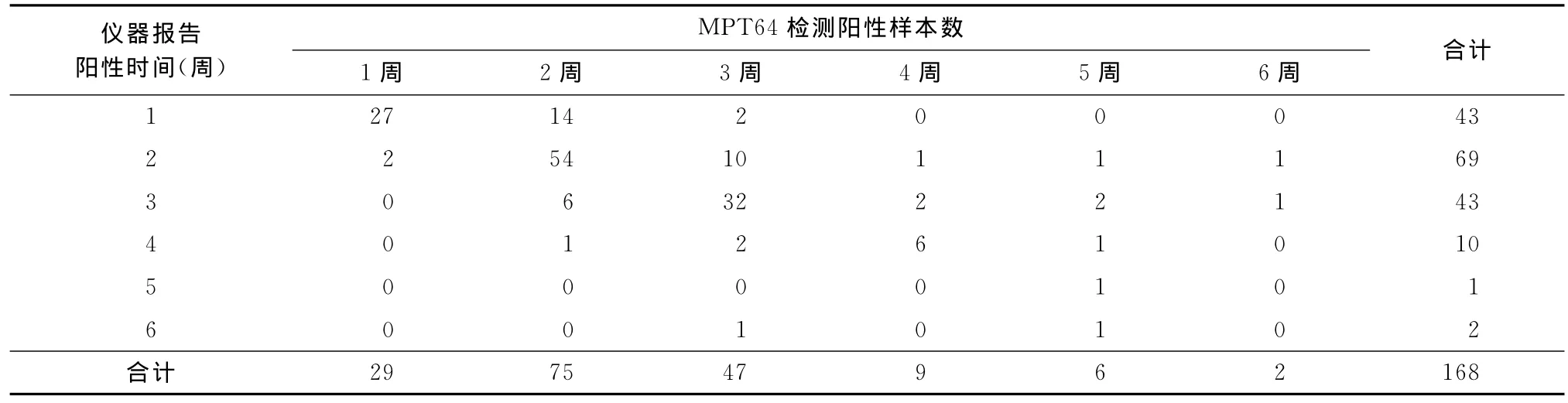
表2 1265例分枝桿菌培養中168株MTBC在兩種方法中的陽性檢出時間(例)
當然,MPT64檢測法也存在一定的缺陷,筆者認為至少有三:一是不能實現連續監測,在培養時間終點檢測會大大影響其快速性,實施多時點檢測則會較大增加實驗成本;二是目前的研究表明一些MTBC菌株可能不分泌 MPT64蛋白[3,5],這會相對降低本實驗方法對MTBC的檢測能力;三是不能檢測樣本中的NTM,丟失了分枝桿菌培養實驗本來固有的部分臨床意義。這些問題均值得進行深入研究,更加希望研究成果能夠快速面世,以滿足結核病臨床診療的迫切需要。
[1]Abe C,Hirano K,Tomiyama T.Simple and rapid identifica-tion of theMycobacterium tuberculosiscomplex by immunochromatographic assay using anti-MPB64monoclonal antibodies.J Clin Microbio,1999,37(11):3693-3697.
[2]Fabre M,Vong R,Gaillard T,et al.Evaluation of the SD BIOLINE TB Ag MPT64Rapid?for the diagnosis of tuberculosis.Pathol Biol(Paris),2011,59(1):26-28.
[3]劉志輝,蔡杏珊,劉玉美,等.MPB64分泌蛋白檢測鑒定結核分枝桿菌復合群的應用研究.國際呼吸雜志,2010,30(18):1100-1103.
[4]何霞,譚守勇,羅春明,等.應用MPT64為靶標快速檢測結核分枝桿菌生長的研究.廣東醫學,2010,31(2):222-224.
[5]吳雪瓊.結核分枝桿菌保護性抗原的研究進展.中華結核和呼吸雜志,2006,29(4):340-342.

