麻黃堿聯合6%HES共同負荷對硬膜外麻醉剖宮產胎兒臍動脈血血氣的影響
黃 格,譚冠先,陳 峻,黃小云,黃金會,廖 莎
(廣西民族醫院,廣西 南寧 530001)
剖宮產術腰麻或硬膜外麻醉后產婦低血壓是常見并發癥。麻醉前單純輸液晶體或膠體預負荷已被證明不能有效預防椎管內麻醉后誘導的低血壓發生,在輸液負荷同時給予適當的血管收縮藥是更有效的措施[1-2]。以往防治椎管麻醉后低血壓一般首選麻黃堿,但有研究認為麻黃堿可使產婦和胎兒心率增快,導致新生兒酸血癥[3-4]。但也有一些研究觀察到麻黃堿和去氧腎上腺素對新生兒臍帶血血氣分析結果統計學意義無[5-6]。本研究是探討硬膜外麻醉剖宮產手術麻黃堿持續靜脈輸注聯合6%羥乙基淀粉氯化鈉溶液(6%HES130/0.4)共同負荷對胎兒出生時臍動脈血血氣的影響。
1 資料與方法
1.1 一般資料 2010年6月至2011年10月在我院住院需行擇期剖宮產術足月妊娠單胎初產婦60例,孕38~40周,年齡23~30歲,體重56~70 kg,身高154~168 cm,ASAⅠ或Ⅱ級,無高血壓、糖尿病、妊高征和心肺疾病等,肝腎功能正常。隨機分為兩組:麻黃堿聯合6%HES130/0.4共同負荷組(A組)和6%HES 130/0.4組(B組)。本研究經本院醫學倫理委員會審查批準,所有患者術前簽署知情同意書。
1.2 麻醉方法 術前30 min給予苯巴比妥鈉0.1 g肌肉注射。入室后以18 G留置針開放上肢靜脈,常規監測產婦血壓(BP)、心率(HR)、心電圖(ECG)和血氧飽和度(SpO2),面罩或鼻導管吸氧。在左側臥位下行硬膜外穿刺,穿刺點為L1~2,向頭端置管3~4 cm,妥善固定硬膜外導管后置產婦于仰臥位,右側抬高約15o并將子宮推移向左側,然后硬膜外注入試驗劑量2.0%鹽酸利多卡因3 ml,證實無脊麻后,以0.5%鹽酸布比卡因10 ml分兩次硬膜外注入,每次5 ml,間隔3 min。以針刺皮膚測定感覺阻滯平面,調節感覺阻滯平面上界達T6。如感覺阻滯平面未達T6則追加0.5%布比卡因3~5 ml。兩組產婦均于硬膜外麻醉藥前以復方林格溶液6~8 ml/kg快速輸入(20 min輸完),適當補充術前禁飲食缺失量。A組在硬膜外腔注入試驗量局麻藥后以麻黃堿10 mg加入6%HES 130/0.4 500 ml加入麻黃堿10 mg快速靜脈輸注(約25~30 min輸完),如產婦收縮壓(SBP)>140 mmHg(1 mmHg=0.133 kPa),調慢輸注速度;如SBP<100mmHg則調快輸注速度。術中維持液按4-2-1法即補充基礎生理需要量+禁飲食缺失量+第三間隙損失量,并根據產婦術中出血量以兩倍復方林格溶液補充。如出現低血壓(SBP下降>基礎值30%或SBP<90 mmHg),給予麻黃堿3 mg靜脈注射,必要時重復使用;如出現心動過緩(HR<50次/min),給予阿托品0.25 mg靜脈注射,必要時重復使用。B組于硬膜外注入試驗劑量后以6%HES 130/0.4 500 ml快速輸入(25~30 min輸完),術中維持輸液與A組相同。如出現低血壓給予去氧腎上腺素30μg靜脈注射,必要時重復使用;如出現心動過緩,給予給予阿托品0.25 mg靜脈注射,必要時重復使用。
1.3 觀察指標 記錄兩組產婦麻醉前(T0)及硬膜外腔注入實驗量后5 min(T1)、10 min(T2)、15 min(T3)、20 min(T4)、25 min(T5)和 30 min(T6)的 SBP 及HR;記錄兩組產婦最低SBP、最高SBP、最低HR、最高HR和心動過緩、心動過速(HR>120次/min)及惡心嘔吐的發生情況;記錄胎兒出生時1 min和5 min的Apgar評分;在胎兒娩出后尚未出現第一呼吸之前用兩把血管鉗鉗夾一段臍帶,以肝素化注射器抽取臍動脈血和臍靜脈血1 ml,用Abbtt i-STAT便捷式血氣分析儀行血氣分析。記錄臍帶血pH、二氧化碳分壓(PCO2)、氧分壓(PO2)及堿剩余BE值。
1.4 統計分析 用SP-SS10.0統計學軟件分析,計量資料以均數±標準差(x ±s)表示,組間比較采用t檢驗,不同時點比較采用單因素方差分析,計數資料采用χ2檢驗。
2 結果
2.1 一般資料比較 兩組產婦年齡、身高、體重、ASA分級及手術時間差異無統計學意義(P>0.05)。A組產婦阻滯平面上界T6(T5~6),B 組為 T6(T5~7)(中位數)差異無統計學意義(P>0.05)。兩組在胎兒娩出之前均輸入6%HES 130/0.4 500 ml,A組預防性加入麻黃堿10 mg,A、B兩組總輸液量分別為(1 364.8±24.6)ml VS(1 442.6±28.4)ml,差異無統計學意義(P>0.05)。
2.2 麻醉后情況比較 A組產婦硬膜外麻醉后血壓平穩,無低血壓、心動過緩、心動過速和惡心嘔吐發生;B組產婦在麻醉后T3、T4時點SBP顯著降低(P<0.01)并顯著低于A組(P<0.01)(見表1);出現低血壓8例(26.6%),惡心嘔吐7例(23.3%),顯著高于A組(P<0.01)(見表2)。B組產婦給予去氧腎上腺素糾正低血壓8例,共11次。兩組胎兒出生后1 min和5 min Apger評分均>9分;兩組胎兒出生時臍動脈和臍靜脈血pH、PCO2、PO2和BE值差異無統計學意義(P>0.05)(見表3)。
表1 兩組產婦硬膜外麻醉前后SBP和HR變化(±s)
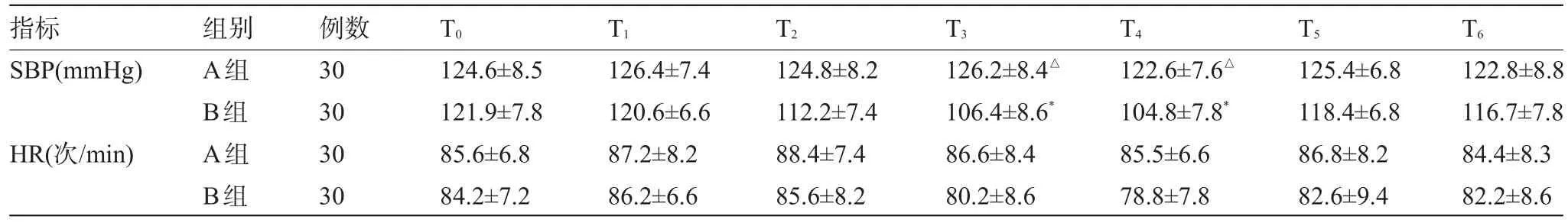
表1 兩組產婦硬膜外麻醉前后SBP和HR變化(±s)
注:與麻醉前比較,*P<0.01;與B組比較,△P<0.01。
指標SBP(mmHg)T0T1T2T3T4T5T6 HR(次/min)組別A組B組A組B組例數30 30 30 30 124.6±8.5 121.9±7.8 85.6±6.8 84.2±7.2 126.4±7.4 120.6±6.6 87.2±8.2 86.2±6.6 124.8±8.2 112.2±7.4 88.4±7.4 85.6±8.2 126.2±8.4△106.4±8.6*86.6±8.4 80.2±8.6 122.6±7.6△104.8±7.8*85.5±6.6 78.8±7.8 125.4±6.8 118.4±6.8 86.8±8.2 82.6±9.4 122.8±8.8 116.7±7.8 84.4±8.3 82.2±8.6
表2 兩組產婦最低SBP、最高SBP、最低HR、最高HR和低血壓及惡心嘔吐發生率(±s)

表2 兩組產婦最低SBP、最高SBP、最低HR、最高HR和低血壓及惡心嘔吐發生率(±s)
注:與B組比較,*P<0.01。
組別A組B組例數30 30最低SBP(mmHg)118.8±6.6*98.8±12.6最高SBP(mmHg)129.4±7.8 124.6±8.2最低HR(次/min)76.8±8.4 72.4±9.3最高HR(次/min)88.4±10.4 84.2±8.6低血壓[例(%)]惡心嘔吐[例(%)]0*0*8(26.6)7(23.3)
表3 兩組新生兒臍帶血血氣分析(±s)
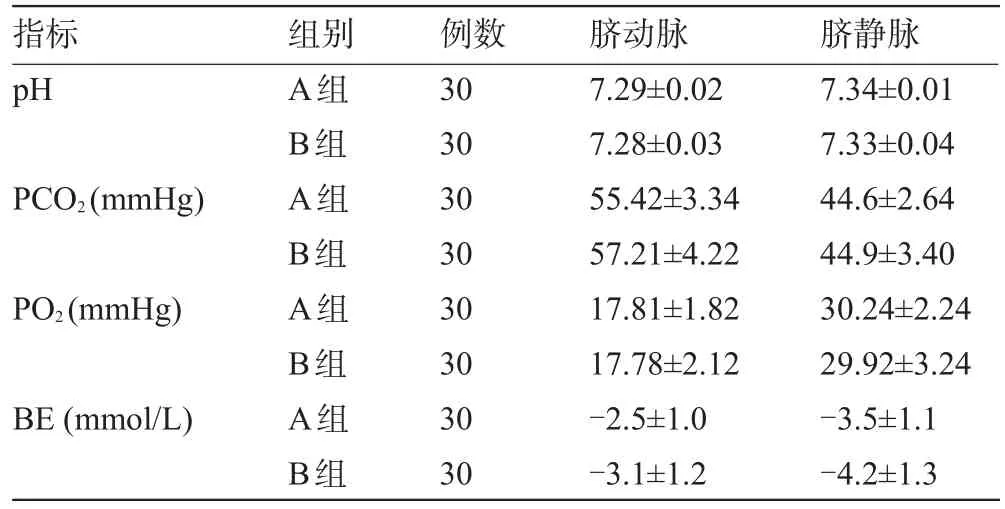
表3 兩組新生兒臍帶血血氣分析(±s)
指標pH PCO2(mmHg)PO2(mmHg)BE(mmol/L)組別A組B組A組B組A組B組A組B組例數30 30 30 30 30 30 30 30臍動脈7.29±0.02 7.28±0.03 55.42±3.34 57.21±4.22 17.81±1.82 17.78±2.12-2.5±1.0-3.1±1.2臍靜脈7.34±0.01 7.33±0.04 44.6±2.64 44.9±3.40 30.24±2.24 29.92±3.24-3.5±1.1-4.2±1.3
3 討 論
剖宮產術腰麻或硬膜外麻醉后產婦低血壓是常見并發癥,嚴重心低血壓不僅可導致使產婦心腦等重要器官缺血、缺氧,出現惡心嘔吐不良反應,也可導致胎兒缺氧、酸中毒。因此,預防剖宮產術麻醉后產婦低血壓十分重要。近年的研究推薦在麻醉前預負荷或麻醉給藥后(共同負荷)快速輸入晶體或膠體負荷同時給予適量血管收縮藥可更有效地預防椎管內麻醉剖宮產手術產婦低血壓[1-2]。本研究觀察到A組產婦硬膜外麻醉后血壓平穩,無低血壓發生,而B組產婦的最低SBP顯著低于A組,并有8例(26.6%)出現低血壓。表明以麻黃堿10 mg持續靜脈滴注聯合6%HES 130/0.4快速靜脈輸入共同負荷,能保持產婦血壓平穩,有效預防硬膜外麻醉后低血壓發生。此外,本研究的結果顯示A組胎兒娩出后臍動脈血pH、PCO2、PO2和BE均在正常范圍,與未使用麻黃堿的對照組比較差異無統計學意義(P>0.05),而且A組胎兒臍動脈血pH、PCO2、PO2和BE還稍高于B組。表明適量麻黃堿對胎兒酸堿無明顯影響,與國外研究報道[5,7]和國內畢嚴斌等[8]報道一致。
麻黃堿是交感類血管活性藥物,激動α和β受體,使外周血管收縮,靜脈回流量增加,血壓上升,預防性靜脈注射或持續輸注可使產婦椎管麻醉后血壓更為平穩。麻黃堿的作用較去氧腎上腺素相對緩和,容易調控,不易出現血壓過高情況。由于麻黃堿同時具有激動α和β受體作用,可導致心率增快,但本研究中A組產婦在輸注麻黃堿過程中心率增加不顯著,這可能與本組麻黃堿用量較小、稀釋度較大、單位時間血藥濃度較低有關。此外,快速輸注膠體擴容,保證了心輸出量也可能是其中一個重要因素。聯合輸液擴容可能會減少該藥對胎兒心率的影響。胎兒臍動脈血pH、PCO2、PO2和BE值受多種因素影響,除血管收縮藥外,還包括產婦的子宮和胎盤血流、新生兒體重、產婦血紅蛋白及血容量、麻醉對產婦呼吸及循環影響等。保持產婦血壓平穩,充分供氧十分重要。
綜上所述,小劑量麻黃堿聯合6%HES 130/0.4共同負荷不會導致硬膜外麻醉剖宮產術中胎兒酸血癥的發生。
[1]Davies P,French GWG.A randomized trial comaring 5 ml/kg and 10 ml/kg of pentastarch as a volume preload before spinal aneasthesia for elective ceasarean section[J].International journal of obstetricAne-sthesia,2006,15:279-283.
[2]Tamilselvan P,Femando R,Johanna B,et al.The effects of crystalloid and colloid preload on cardiac output in parturient undergoing planned cesarean delvery underspinal aresthesia:A raundomized trial[J].InternationalAnesthesia Research Society,2009,109:1916-1921.
[3]Ngan Kee WD,Khaw KS.Vasopressors in obstetrics:what should we be using?[J].Curr OpinAnaesthesiol,2006,19:238-243.
[4]Cooper DW,Gibb SC,Meek T,et al.Effect of intravenous vasopressors on spread of spinal anesthesia and fetal acid-base eguilibrium[J].Br JAnaesth,2007,98:649-656.
[5]Ngan Kee WD,Khaw KS,Lau TK,et al.Randomised doubl-blinded comparison of phenylelephrine vs ephedrine for maintaining blood pressure during spinal anaesthesi for non-elective Caesarean Seetion[J].Anaesthesia,2008,63:1319-1326.
[6]Ngan Kee WD,Khaw KS,Tan PE,et al.Placental transfer and fetal metabolic effects of phenylephrine and ephedrine during spinal anesthesia for cesarean delivery[J].Anertheiology,2009,111:506-512.
[7]Cooper DW,Sharma S,Orakkan P,et al.Retrospective study of association between choice of vasopressor given dring spinal anaesthesia for high-risk ceasarean delivery an fetal pH[J].International Journal of ObstetricAnesthesia,2010,19:44-49.
[8]畢嚴斌,王月蘭.麻黃堿治療腰麻剖宮產術低血壓對臍動脈血氣及胎兒的影響[J].臨床麻醉學雜志,2008,24(7):580-582.

