鏈霉菌YIM 245次生代謝產物的研究
靳榮線,曹艷茹,2,苗翠蘋,李文均,姜 怡* ,吳少華*
1云南大學云南省微生物研究所西南微生物多樣性教育部重點實驗室,昆明 650091;2西北農林科技大學資源環境學院,楊凌 712100
從經典的抗生素篩選到當今借助微生物基因組學、宏基因組學等手段輔助藥物篩選,放線菌在天然產物的產生與篩選中都占有重要位置。所以,探尋新型放線菌資源、改善分離方法和提高未知放線菌的出菌率一直是放線菌研究的重要內容。放線菌具有豐富的生物多樣性,其天然產物有著廣泛的生物學活性,是發現具有生物活性新型次生代謝產物的重要資源[1]。
隨著藥物研發水平的進步,對先導化合物的發現也不再局限于陸生植物。相對于植物內生放線菌,對動物腸道放線菌的研究發展較快,特別是對昆蟲共生放線菌的研究[2-4]。本實驗室從2007年開始對西南特有幾種動物的糞便放線菌進行研究,并對從中得到的一些有生物活性的菌株進行代謝產物的初步研究[5]。
菌株YIM 245為從長頸鹿糞便中分離得到的一株放線菌,通過對其培養特征和16S rRNA基因序列分析,屬于鏈霉屬(Streptomyces sp.)。抗菌活性檢測顯示該菌株的發酵產物具有較強的抗菌活性。因此,我們進一步對其發酵產物的化學成分進行了研究,從發酵提取物中分離得到7個化合物。依據理化性質及波譜數據分析,分別鑒定為2'-脫氧胞嘧啶核苷(1)、2'-脫氧胸苷(2)、2'-脫氧尿苷(3)、2’-脫氧腺苷(4)、菜油甾醇(5)、大豆素(6)和鄰氨基苯甲酸(7),7個化合物均顯示較弱的抗菌活性。
1 材料和方法
1.1 發酵菌株
菌株YIM 245從長頸鹿糞便中分離得到,經純培養后,以38#瓊脂斜面保存在4°C。
1.2 指示菌株
枯草芽孢桿菌(Bacillus subtilis),金黃色葡萄球菌(Staphylococcus aureus),白色念珠菌(Candida albicans),大腸桿菌(Escherichia coli),黑曲霉菌(Aspergillus niger)。
1.3 培養基
38#:葡萄糖4 g,酵母膏4 g,麥芽膏5 g,復合維生素微量(3.7 mg),微量鹽1 mL,瓊脂13 g,蒸餾水1000 mL,pH7.2
302#:甘露醇20 g,大豆 20 g,蒸餾水1000 mL,pH7.8
LB:胰蛋白胨10 g,氯化鈉5 g,酵母膏5 g,蒸餾水 1000 mL,pH7.2
PDA:土豆200 g,葡萄糖10 g,蒸餾水1000 mL,pH自然
1.4 儀器與試劑
儀器:超凈工作臺(AirTech);隔水式電熱恒溫培養箱(上海市躍進醫療器械廠);高速臺式離心機(上海醫用分析儀器廠);SHI-22型水浴恒溫振蕩器(江蘇太倉醫療器械廠);電子天平(中山市新和科技開發有限公司);紫外燈(Shimadzu);Bruker DRX-500型超導核磁共振儀;Agilent G3250AA LC/MSD TOF型質譜儀;EYELA旋轉蒸發儀。
試劑:反相硅膠RP-18(Merck),Sephadex LH-20(Pharmacia),薄層層析用硅膠G板和柱層析硅膠200~300目(青島海洋化工廠);其他試劑均為分析純。
1.5 發酵液的制備
種子液制備:從新鮮斜面培養基中將菌株轉接到裝有100 mL 38#培養基的500 mL錐形瓶中,于28℃、200 rpm搖床培養2 d。
將種子液轉接到裝有100 mL 302#培養基的500 mL錐形瓶中相同條件下搖床培養7 d,共獲得發酵產物40 L。
1.6 提取分離
發酵產物經4500 rpmn離心10 min得到發酵液和菌絲體,發酵液經大孔樹脂HP-20吸附和乙酸乙酯萃取后減壓濃縮,菌絲體經95%乙醇浸泡后減壓濃縮,根據TLC檢測,合并發酵液和菌絲體粗體物共140 g。發酵粗提物經硅膠柱層析,用氯仿-甲醇梯度洗脫,得到6個組分。組分1經硅膠柱層析,用石油醚-乙酸乙酯(95∶5)洗脫得化合物6(5 mg)。組分2經硅膠柱層析,用石油醚-乙酸乙酯(4∶1)洗脫得化合物2(8 mg)。組分3(5 g)經硅膠柱層析,用石油醚-丙酮(7∶3)洗脫,再經凝膠Sephadex LH-20柱層析,用甲醇洗脫得化合物3(3 mg)。組分3經硅膠柱層析,用氯仿-甲醇(9∶1)洗脫得化合物4(3 mg)。組分4經硅膠柱層析,用石油醚-乙酸乙酯(95∶5)洗脫得化合物5(4 mg)。組分6經硅膠柱層析,用氯仿-丙酮(9∶1),再經 RP-18 反相柱層析,用甲醇-水(5∶95)洗脫得化合物7(5 mg)。組分7經硅膠柱層析,用氯仿-甲醇(3∶1)洗脫得化合物1(2 mg)。
1.7 化合物的抑菌活性檢測
在長有指示菌的固體斜面培養基中加入1 mL無菌水,震蕩片刻制成指示菌懸液。將化合物1~7分別溶解于50%DMSO的水溶液中,配制成濃度為800(g∕mL的母液,用LB和PDA液體培養基將樣品分別倍比稀釋為八個濃度:800、400、200、100、50、25、12.5、6.25(g ∕ mL.按每孔 50 μL 將它們分別加入到96孔板中,再向每孔中加入50 μL活性指示菌菌懸液。以100(g∕ mL制霉菌素和青霉素為陽性對照,加入等體積PDA液體培養基的孔為陰性對照,不加菌液的孔為空白對照。上述每組樣品設置3個平行處理。將96孔板置于28℃培養箱中培養24 h后,肉眼觀測活性指示菌的生長狀況,以沒有指示菌生長的目標產物的最低濃度為最小抑菌濃(MIC)。
2 結果與分析
2.1 化合物的結構鑒定
化合物1 白色固體;1H NMR(CD3OD,500 MHz)δ:8.06(1H,d,J=7.4 Hz,H-6),6.29(1H,t,J=6.1 Hz,H-1’),5.94(1H,d,J=7.2 Hz,H-5),4.38(1H,m,H-4’),3.96(1H,m,H-3’),3.82(1H,dd,J=11.8,3.0 Hz,H-5’a),3.75(1H,dd,J=11.8,3.6 Hz,H-5’b),2.38(1H,m,H-2’a),2.16(1H,m,H-2’b);13C NMR(CD3OD,125 MHz)δ:168.6(C-4),158.5(C-2),144.7(C-6),98.6(C-5),89.3(C-4’),88.0(C-1’),73.4(C-3’),63.4(C-5’),42.4(C-2’)。以上數據與文獻對照一致[6],故鑒定為2'-脫氧胞嘧啶核苷。
化合物2 白色晶體;1H NMR(Pyridine-d5,500 MHz)δ:8.13(1H,s,H-6),7.01(1H,t,J=5.5 Hz,H-1’),5.01(1H,m,H-4’),4.45(1H,m,H-3’),4.22(1H,d,J=11.7 Hz,H-5’a),4.13(1H,d,J=11.7 Hz,H-5’b),2.65(2H,m,H-2’),1.98(3H,s,CH3);13C NMR(Pyridine-d5,125 MHz)δ:165.8(C-4),152.7(C-2),137.5(C-6),111.3(C-5),89.6(C-4’),86.2(C-1’),72.3(C-3’),63.1(C-5’),42.2(C-2’),13.5(5-CH3)。以上數據與文獻對照一致[7],故鑒定為2'-脫氧胸苷。
化合物3 白色晶體;1H NMR(Pyridine-d5,500 MHz)δ:8.34(1H,d,J=8.0 Hz,H-6),6.96(1H,t,J=6.5 Hz,H-1’),5.80(1H,d,J=8.0 Hz,H-5),4.99(1H,m,H-4’),4.46(1H,m,H-3’),4.19(1H,d,J=11.7 Hz,H-5’a),4.11(1H,d,J=11.7 Hz,H-5’b),2.69(1H,m,H-2’a),2.58(1H,m,H-2’b);13C NMR(Pyridine-d5,125 MHz)δ:166.0(C-4),153.4(C-2),142.4(C-6),104.0(C-5),90.5(C-1’),87.1(C-4’),72.9(C-3’),63.8(C-5’),43.1(C-2’)。以上數據與文獻對照一致[7],故鑒定為2'-脫氧尿苷。
化合物4 淡黃色粉末;1H NMR(CD3OD,500 MHz)δ:8.40(1H,s,H-8),8.18(1H,s,H-2),6.45(1H,m,H-1’),4.61(1H,m,H-3’),4.10(1H,m,H-4’),3.80(1H,m,H-5’a),3.78(1H,m,H-5’b),2.85(1H,m,H-2’a),2.81(1H,m,H-2’b);13C NMR(CD3OD,125 MHz)δ:157.9(C-6),153.9(C-2),150.3(C-4),141.9(C-8),121.2(C-5),90.3(C-1’),87.5(C-4’),73.4(C-3’),64.0(C-5’),41.9(C-2’)。以上數據與文獻對照一致[7],故鑒定為2'-脫氧腺苷。
化合物 5 白色粉末;1H NMR(CDCl3,500 MHz)δ:5.38(1H,brs,H-6),3.57(1H,m,H-3),1.04(3H,s,H-19),0.94(3H,d,J=6.7 Hz,H-28),0.90(3H,d,J=6.7 Hz,H-21),0.84(3H,d,J=6.5 Hz,H-26),0.79(3H,d,J=6.7 Hz,H-27),0.70(3H,s,H-18);13C NMR(CDCl3,125 MHz)δ:141.2(C-5),122.0(C-6),72.2(C-3),56.6(C-8),56.5(C-9),42.7(C – 14),40.2(C-17),37.6(C-4),36.9(C-6),32.5(C-1),32.3(C-20),32.1(C-2),30.0(C-11),29.7(C-24),29.4(C-25),28.6(C-12),26.6(C-15),24.7(C-16),23.5(C-22),21.6(C-12),21.5(C-23),20.1(C-19),19.7(C-21),19.4(C-24),19.3(C-28),19.1(C-27)。以上數據與文獻對照一致[8],故鑒定為菜油甾醇。
化合物6 淡黃色晶體;1H NMR(DMSO-d6,500 MHz)δ:10.79(1H,s,H-7),9.55(1H,s,H-4’),8.26(1H,s,H-2),7.98(1H,d,J=8.6 Hz,H-5),7.39(2H,d,J=7.9 Hz,H-2’,6’),6.94(1H,d,J=8.2 Hz,H-6),6.86(1H,s,H-8),6.83(2H,d,J=7.9 Hz,H-3’,5’);13C NMR(DMSO-d6,125 MHz)δ:175.0(C-4),162.8(C-7),157.8(C-9),153.1(C-2),130.8(C-2’),130.4(C-6’),127.6(C-5),123.8(C-1’),122.9(C-3),117.0(C-10),115.8(C-6),115.4(C-3’),115.3(C-5’),102.4(C-8)。以上數據與文獻對照一致[9],故鑒定為大豆素。
化合物7 淡黃色晶體;1H NMR(CD3OD,500 MHz)δ:7.83(1H,d,J=8.0 Hz,H-5),7.25(1H,td,J=8.0,1.4 Hz,H-3),6.75(1H,d,J=8.3 Hz,H-2),6.58(1H,t,J=8.0 Hz,H-4);13C NMR(CD3OD,125 MHz)δ:172.0(C-7),153.2(C-1),135.4(C-3),133.0(C-5),118.1(C-4),117.0(C-2),112.2(C-6)。以上數據與文獻對照一致[10],故鑒定為鄰氨基苯甲酸。

圖1 化合物1~7的化學結構Fig.1 The structures of compounds 1-7
2.2 化合物的抑菌活性結果
采用96孔板法測定了化合物1~7對5種病原指示菌的抑菌活性,結果均顯示較弱的抑菌活性(見表1)。
3 討論
本研究從非洲特有動物長頸鹿的糞便環境中分離得到一株放線菌YIM 245,經16S rRNA基因序列初步分析,其屬于鏈霉菌屬。從該菌株的發酵產物中分離獲得了7個化合物,均為首次從該動物糞便極端生境中分離獲得到,本研究為微生物資源的挖掘及代謝產物的分離提供一條新途徑。抗菌實驗結果表明,7個化合物均顯示較弱的抑菌活性。在研究過程中由于某些代謝產物的含量較低、成分復雜,不能進行有效的分離和結構鑒定,今后還需對其中的微量成分進一步深入研究,提高動物糞便環境中放線菌資源及其活性代謝產物的開發與應用。
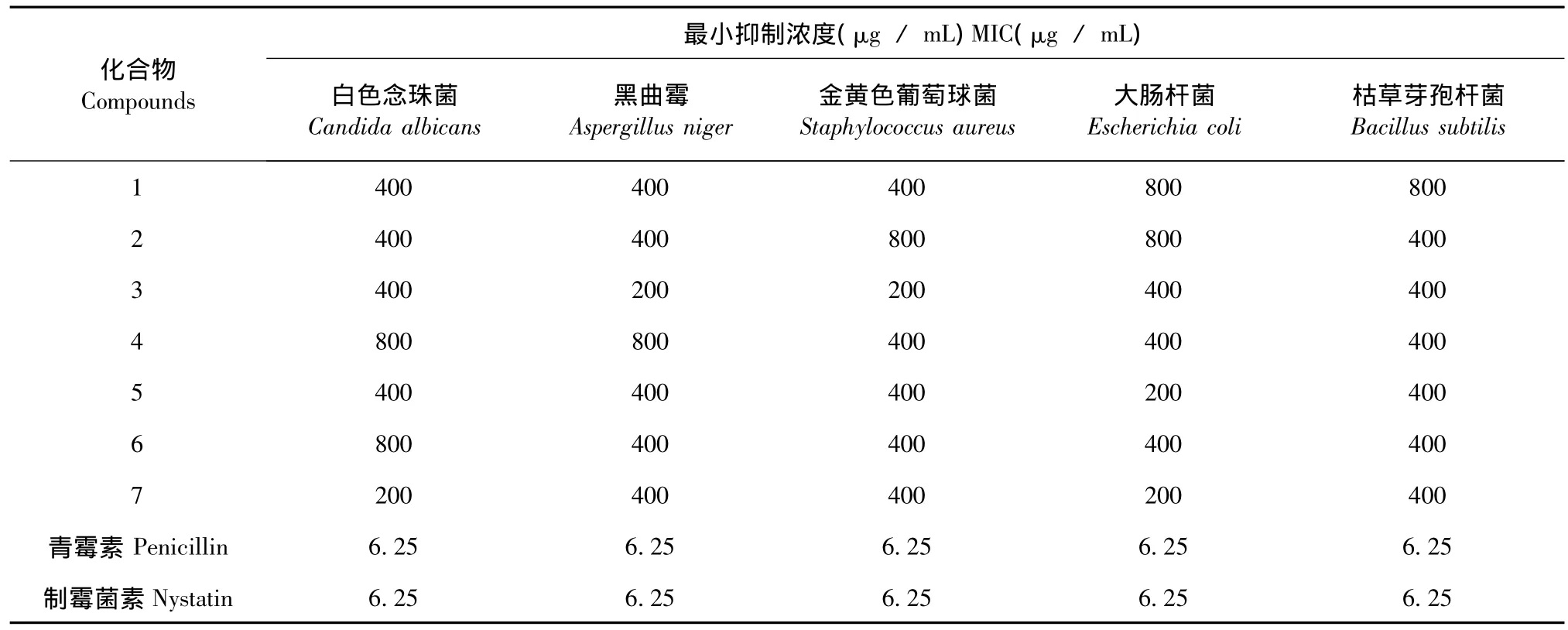
表1 化合物1~7的抑菌活性Table 1 The antimicrobial activities of compounds 1-7
1 Cao LX(曹理想).The perspectives of animal symbiotic actinobacteria.Microbiology(微生物學通報),2010,37:1811-1815.
2 Haygood MG,Schmidt EW,Davidson SK,et al.Microbial symbionts of marine invertebrates:opportunities for microbial biotechnology.J Mol Microbiol Biotenol,1999,1:33-43.
3 Kim TK,Garson MJ,Fuerst JA.Marine actinomycetes related to the‘Salinospora’group from the Great Barrier Reef sponge Pseudoceratina clavata.Envir Microbiol,2005,7:509-518.
4 Ward AC,Bora N.Diversity and biogeography of marine actinobacteria.Curr Opin Microbiol,2006,9:279-286.
5 Jiang Y(姜怡),et al.Diversity and bioactivities of cultured actinomycete isolated from animal feces and Xylocopa dissimilis.Acta Microbiol Sin(微生物學報),2009,49:1152-1157.
6 Chandrasegaran S,et al.Isolation and purification of deoxyribonucleosides from 90%13C-enriched DNA of algal cells and their characterization by1H and13C NMR.Nucleic Acids Research,1985,6:2097-2110.
7 Li YQ(李云秋),Wang B(王賓),Yang B(楊斌).Study on the compounds of marine sponge Haliclona sp.J Trop Ocea(熱帶海洋學報),2011,30:124-126.
8 Wang JR(王賤榮),Zhang J(張健).Chemical constituents from the seeds of Ziziphus jujuba var.spinosa.Chin J Nat Med(中國天然藥物),2008,6:268-270.
9 Lu HY(盧海英),Liang JY(梁敬鈺).Isoflavones and their derivatives from the rootofDerriselliptica (Roxb.)Benth.Chin J Nat Med(中國天然藥物),2008,6:265-267.
10 Zheng D(鄭丹),Jiang Y(姜怡).Chemical constituents from the mycelium of a new Streptomycete.Chin J Med Chem(中國藥物化學),2010,20:201-205.

