楊梅中硒含量測定的消化方法
蔣步云,柴振林,呂愛華,尚素微,朱杰麗
(浙江省林產品質量檢測站,浙江 杭州 310023)
楊 梅 (Myrica rubra Sieb) 是 楊 梅 科(Myricaceae)楊梅屬 (Myrica L.)中的一個種,是我國南方特產果樹之一[1],深受廣大消費者的喜愛。楊梅營養價值豐富,且有藥用價值,含有碳水化合物、有機酸、蛋白質及多種維生素等成分,具有生津止渴、和胃消食、益腎利尿和解暑止瀉之功效,同時也具有抗氧化和抗衰老的作用[2-3]。硒是人體必不可少的微量元素之一,具有抗氧化、保護心血管、解毒、防癌和提高免疫力等作用[4-5]。隨著科技的進步,人們生活水平的提高,富硒楊梅開始日益走俏。但何謂富硒,楊梅中硒含量究竟有多少等等都是重點關注的問題,因此,準確、快速地測定楊梅中硒的含量顯得尤為重要。
目前,測定硒的方法主要有原子光譜法、吸光光度法、熒光光度法、電化學法及色譜法等,各種聯用技術也已經用于硒的測定及形態分析[6]。本實驗使用的是氫化物原子熒光光譜法。原子熒光法測定的范圍寬,具有方法簡單、靈敏度高、準確性好的特點[7]。應用氫化物原子熒光光譜法測定必須對樣品進行消解,為提高測定結果的正確性和效率,進行了微波消解法和濕法消解 (電熱板加熱消解)法對測定結果影響的實驗。現將有關結果報道如下。
1 材料與方法
1.1 材料
1.1.1 儀器
AFS-930 型雙道原子熒光光度計 (北京吉天儀器有限公司),Multiwave3000 微波消解儀 (奧地利安東帕公司),可控式電爐,硒空心陰極燈等。
1.1.2 試劑
硝酸,高氯酸,鹽酸 (優級純),過氧化氫(分析純),硼氫化鉀溶液10 g·L-1,硒標準儲備液100 mg·L-1,硒標準使用液0.1 mg·L-1,載流5%鹽酸溶液,10 g·L-1鐵氰化鉀溶液 (掩蔽劑:可明顯消除Pb、Cu 的干擾[8]),標準茶葉對照樣 (國家標準物質,樣品編號GSB-7)。
1.2 方法
1.2.1 原理
樣品經酸加熱消化后,在6 mol·L-1鹽酸介質中,將試樣中的六價硒還原成四價硒,用硼氫化鉀作還原劑,將四價硒在鹽酸介質中還原成硒化氫,由載氣(氬氣)帶入原子化器中進行原子化,在硒空心陰極燈照射下,基態硒原子被激發至高能態,在去活化回到基態時,發射出特征波長的熒光,其熒光強度與硒含量成正比。與標準系列比較定值[9]。
1.2.2 樣品制備
取楊梅可食用部分打成勻漿后備用,余樣放冷柜冰凍儲藏。
1.2.3 樣品前處理
濕法消解 (電熱板加熱消解)。參考 GB 5009.93—2010 食品中硒的測定中第1 法 (氫化物原子熒光光譜法),準確稱取處理好的待測試樣1~2.000 g 于消化瓶中,加入混合酸 (硝酸∶高氯酸4∶2)10 mL,蓋上表面皿冷消化過夜,于次日電爐上加熱。當溶液變為澄清透明并伴有白煙時,再繼續加熱至剩余體積2 mL 左右,不可蒸干。冷卻,再加5 mL 6 mol·L-1鹽酸,繼續加熱至溶液變為澄清透明并伴有白煙出現,將六價硒還原成四價硒。冷卻,用去離子水定容到25 mL 容量瓶中,待測,同時做試劑空白。
微波消解法。準確稱取處理好的待測試樣0.5~2.000 g 于微波消解罐內,加混合酸為4 mL硝酸+3 mL 過氧化氫,放置過夜,次日置于微波消解儀器內按設定程序進行消解。當室內溫度低于10℃時,應先放于趕酸架上40℃預熱10 min 左右,以便微波消解儀能正常啟動。程序運行結束后取出反應罐冷卻一段時間,放置于趕酸架上120℃趕酸至剩余2 mL 左右時取下,冷卻后加入5 mL 6 mol·L-1鹽酸溶液,繼續放回趕酸架上消化至剩余溶液澄清透明,將六價硒還原成四價硒。取下冷卻至室溫,0.5%硝酸溶液定容到25 mL 容量瓶中,待測,同時做試劑空白。32 位微波消解儀設置條件經多次試驗摸索得到最佳化條件。
1.2.4 測定方法
原子熒光光度計儀器工作條件設置。光電倍增管負高壓270 V,屏蔽氣流量800 mL·min-1,原子化器溫度200℃,讀數時間7 s,原子化器高度8 mm,延遲時間1.5 s,燈電流80 mA,測量方式Std.Curve,載氣流量400 mL·min-1,讀數方式Peak.Area。
標準曲線繪制。取硒標準使用液0.1 mg·L-12.5 mL 到25 mL 容量瓶中,用5%鹽酸溶液稀釋,加入1 mL 鐵氰化鉀溶液為掩蔽劑,定容到刻度線,搖勻作為硒的標準工作溶液。儀器設置為自動進樣,標準系列分別為1.000,2.000,4.000,6.000 和10.000 μg ·L-1。得出標準系列濃度(x)與熒光強度 (y)的關系式:y=15.225 1x-0.871 1,R2=0.999 8。
樣品測定。向2種消化方法 (微波消解法和濕法消解法)消化好后定容到25 mL 容量瓶中的樣品溶液內加入1 mL 10 g·L-1鐵氰化鉀溶液作為掩蔽劑,搖勻,同標準曲線一樣上機測定含量。載流為5%鹽酸溶液,還原劑為10 g·L-1硼氫化鉀溶液。
2 結果與分析
2.1 測定值
標準茶葉對照樣GSB-7 經過原子熒光光譜法測定后,2種消化方法對結果的影響見表1。
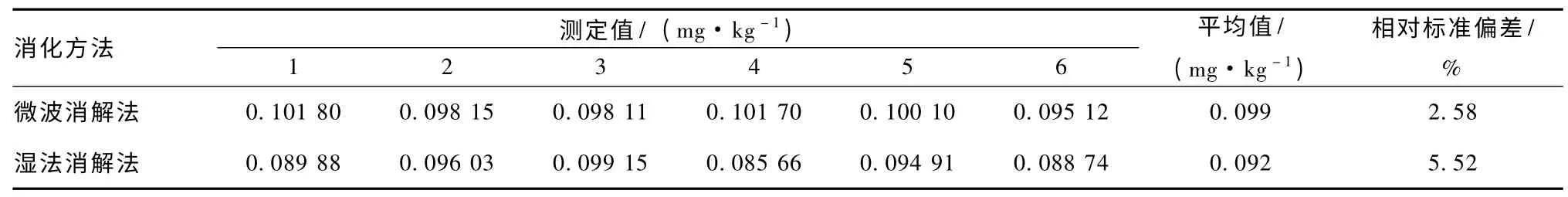
表1 微波消解法和濕法消解法測定標準茶葉對照樣的結果
從表1 可知,微波消解法的測定平均值高于濕法消解法 (電熱板加熱法)的測定平均值,兩者都在標準值范圍內。微波消解法的相對標準偏差較低,說明微波消解標樣更完全更徹底,硒含量損失較少且平行性良好。
從2種消化方法處理后得到的待測楊梅樣品測定結果 (表2)來看,同樣可得出微波消解法優于濕法消解法。
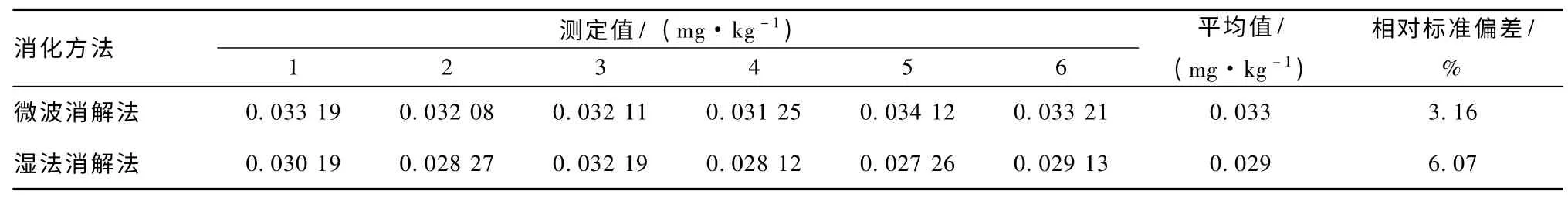
表2 微波消解法和濕法消解法測定楊梅樣品的結果
2.2 加標回收率
對微波消解法作為消化方法的標準茶葉對照樣進行加標回收試驗,3個加標濃度得到的回收率為90%~110% (表3),符合加標回收的要求,說明微波消解法消解楊梅樣品是可行有效的。

表3 微波消解法的加標回收率
通過加標回收試驗評估樣品預處理產生的不確定度。18個加標樣品的平均回收率99.33%,標準偏差S 為2.91%,標準不確定度設為U (R),有U (R)=0.008 774,則其相對標準不確定度為U (R)/R=0.008 833。
2.3 精密度
對微波消解法消化標準茶葉對照樣進行11 次精密度試驗,相對標準偏差為5.11%,說明其符合要求。
3 小結
在楊梅中硒含量測定的過程中,通過2種消化方法的比較,可以看出微波消解相對于濕法消解,具有消耗樣品和試劑少、消解徹底、快速簡便、準確度高、精密度好等優點,是一種較理想的前處理方法,且污染少更利于操作者的安全[10-11]。因此,楊梅中硒含量測定的消化方法可采用微波消解法。
[1]謝小波,求盈盈,邱立軍,等.堿性土壤對楊梅生長結果的影響[J].浙江農業學報,2008,20 (4):261-265.
[2]馬瑞,徐麗珊,程躍微,等.不同品種楊梅用途研究[J].山西農業科學,2011,39 (12):1287-1290.
[3]張澤煌,盧新坤,林旗華,等.10個楊梅品種果實糖和氨基酸含量分析[J].浙江農業學報,2011,23 (7):18-20.
[4]李麗輝,林親錄.食品中硒的生理功能及其檢測方法[J].食品工程,2007 (1):28-29.
[5]余光輝,溫琰茂,何樹悠,等.廣州市26種水果中硒含量特征分析[J].食品科學,2007,28 (8):344-347.
[6]劉興艷,馬建華,朱靜平,等.食品中硒的分析進展[J].微量元素與健康研究,2005,22 (1):26-28.
[7]袁菊,洪濤,陳鳳凰,等.微波消解一氫化物發生原子熒光法測定土壤中硒[J].貴州工業職業技術學院學報,2011,6 (1):54-56.
[8]彭新元,朱攀.原子熒光光譜測定土壤中硒的方法研究[J].實用預防醫學,2008,15 (5):1599.
[9]GB 5009.93—2010,食品中硒的測定[S].
[10]侯曉芳,遲忠云,王悅霞.氫化物發生原子吸收法測定保健食品中硒含量[J].海峽預防醫學雜志,2009,15(1):55-56.
[11]馮信平.熱帶水果中硒形態分析的不確定度研究[J].熱帶農業科學,2010,30 (4):8-11.

