煉焦煤尾煤熱解特性及富氫氣體析出研究
劉海兵,惠賀龍,付興民,柳樹成,賈晉煒,舒新前* ,顧軍
1.中國礦業大學(北京)化學與環境工程學院,北京 100083
2.北京建筑材料科學研究總院有限公司,固廢資源化利用與節能建材國家重點實驗室,北京 100041
煤炭約占我國一次能源消費的70%,隨著煤炭工業和選煤工業的迅速發展,煤炭洗選廢棄物處理已成為制約選煤工業可持續性發展的重大難題。目前平均原煤入洗率已達50.9%,據測尾煤產生量約占入洗量的2.5%~3%。按2010年煤炭開采量32.4億t計,年產生尾煤量約4000萬~4800萬t,以49%灰分計算,折合標煤為近1800萬t[1-4]。
氫氣不僅是化學工業的基礎原料也是一種清潔的燃料。常規制氫技術的成本較高,通過廢棄物熱解技術制備氫氣[5-7]可以降低成本。尾煤的轉化和潔凈利用是推動選煤工業發展的重要動力,探索尾煤的高效利用技術研究對煤礦廢棄物處置和環境保護具有特別重要的意義。尾煤的常規處理方法是將其摻到煤中燃燒,該方法不但產生二次污染,且對尾煤的形態、輸送、燃燒裝置等技術要求也較高[8-10]。Finney等[10]對尾煤進行熱處理比較研究,熱解得到一定的低熱值產品,氣化試驗結果不理想。Krevelen等[11]研究認為,煤熱解中氫氣在低加熱速率下生成溫度范圍較寬,主要是因為大量重疊的一階反應結合導致;熱解初期產品中氫氣是由脂環族脫氫形成,在高溫階段,熱解產品中的氫來源于縮聚反應和其他反應中的脫氫環化。Samaras等[12-13]已證實,在煤熱解轉化過程中,煤中的無機礦物和有機物轉化存在一定聯系。Slaghuis等[14]對高灰煤進行的熱解認為,無機礦物對煤熱解有一定催化作用。我國一些學者[15-16]研究認為,煤中礦物質對熱解過程有抑制作用,該種作用隨礦物質增加而增加。
尾煤熱解不僅關系到燃燒設備的設計和可靠運行,也是煤系廢棄物資源化利用的重要補充。筆者結合熱重分析和固定床管式爐熱解裝置,對尾煤熱解特性和產物析出進行了研究,重點探討了富氫氣體的析出特性、產量及分布特性。
1 試驗
1.1 原料
以山西某煤礦煉焦煤的尾煤為試驗原料,其工業分析與元素分析如表1所示,尾煤灰成分分析如表2所示。
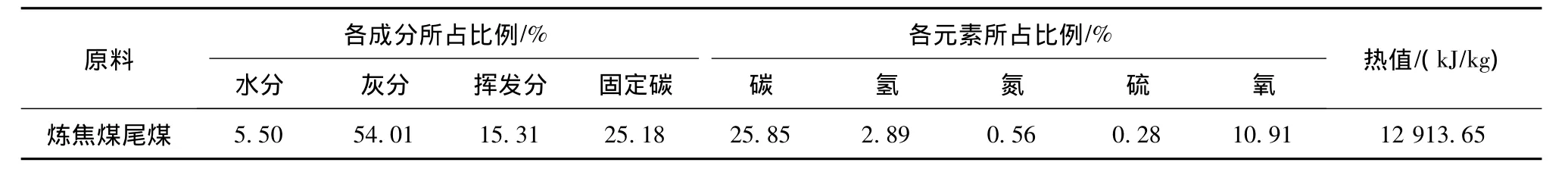
表1 尾煤的成分與元素分析Table 1 Proximate and ultimate analysis of tailings

表2 尾煤灰成分分析Table 2 Ash composition of tailings
由表1和表2可見,尾煤具有高灰、低硫、低H/C和低熱值特點,灰成分中 SiO2、Al2O3的比例較高。
1.2 儀器
熱重分析采用北京恒久HCT-2型熱重分析儀測定。熱解采用電加熱固定床管式爐裝置(天津中環實驗電爐有限公司)測定,該裝置由一根直徑為30 mm,長1200 mm的石英管及帶程序溫控儀的電加熱裝置和D07-11C累積積分質量流量計(北京七星華創電子股分有限公司)組成。熱解氣采用GC-2014C型氣相色譜儀(日本島津公司)測定。原料的工業分析采用XL-1型箱式電阻爐(天津中環實驗電爐有限公司)和DHG-9707A型電熱恒溫鼓風干燥箱(天津中環實驗電爐有限公司)測定。
1.3 方法
熱重分析在熱天平上進行,將(30.0±0.1)mg尾煤或焦煤粉試樣放入差熱天平坩堝內,并通入流量為60 mL/min的氮氣,分別以10,20和40℃/min的升溫速率對尾煤加熱到950℃,焦煤以10℃/min的升溫速率加熱到950℃。熱解試驗在固定床管式爐上進行,試驗裝置如圖1所示。
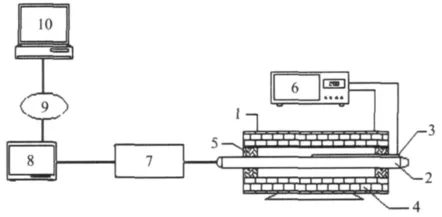
圖1 尾煤熱解固定床裝置Fig.1 The pyrolysis process of tailings in the fix-bed equipment
將30 g原料放在熱解爐恒溫段熱解,終溫控制為800,850,900和950℃,記錄質量流量計的瞬時產率和累計流量。當溫度升至所設溫度后,流量計的流量顯示數值接近0即可認為熱解結束。熱解氣體經一級水冷凝收集熱解油,氣體產物經過盛有CaCl2的干燥裝置,用集氣袋收集后進行氣相色譜分析。試驗中測得的固態、液態產物的質量與原料質量比即為其產率,混合氣的產率=(原料質量-固態物質量-液態物質量)/原料質量。
2 結果與討論
2.1 升溫速率對尾煤熱解過程的影響
在升溫速率分別為10,20和40℃/min的條件下,對尾煤的失重量(TG)和失重速率(DTG)進行熱重分析,結果如圖2所示。
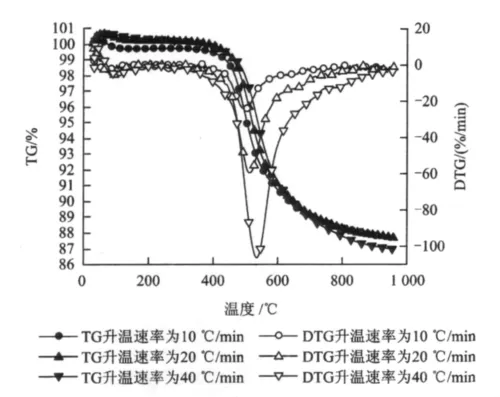
圖2 不同升溫速率下尾煤TG/DTG分析Fig.2 TG/DTG analysis of tailings at different heating rates
由圖2可以看出,尾煤的線性升溫熱解可以分為四個階段。
第一階段為室溫~200℃。該階段主要進行尾煤的脫水、脫除吸附氣體以及脫羧基反應等,其失重量大致占總失重的5%左右。由于尾煤中含水量較少,所以脫水過程不是很明顯。
第二階段為200~400℃。該階段主要是一次揮發分析出。從TG曲線看,升溫速率對揮發分析出影響很小,可能與尾煤中高灰分有關,由于礦物質熱容大,影響了熱傳遞;DTG曲線在該階段比較平緩,曲線均接近水平直線,失重速率無明顯變化。
第三階段為400~650℃。該階段是活潑熱解階段。TG曲線明顯下降,DTG曲線迅速下降后又迅速上升出現峰值,其最大失重速率所對應的溫度約為500℃,失重量占總失重的80%,該階段為尾煤的熱解階段,尾煤在熱解聚成膠體之后,迅速分解析出高分子有機物,即焦油。結果與西部煤熱解該階段的DTG曲線最大失重速率對應溫度基本吻合[17],但失重速率有所增加。造成尾煤該階段峰溫延遲的原因可能是尾煤中高濃度的礦物質阻礙了熱傳導過程,并阻礙了揮發分的析出過程[18-19]。
第四階段為650~900℃。該階段屬于熱解后期階段。TG曲線緩慢下降,DTG曲線緩慢上升,失重速率在15%/min左右,該過程主要是半焦的縮聚反應,半焦縮聚成焦炭,并放出以H2和CH4為主的低分子量氣體。
從圖2可知,升溫速率對尾煤最終失重速率的影響較小。但是,隨著升溫速率增大,樣品的最大失重速率逐漸增大,并且樣品的初始熱解溫度、熱解終溫、最大失重速率所對應的溫度均向高溫區推移。當升溫速率由10℃/min升高到40℃/min,尾煤的最大失重速率所對應的溫度增加38.4℃(表3),隨著升溫速率逐漸增大,樣品最大失重速率所對應的溫度間隔逐漸增大。其原因是尾煤的熱解是吸熱反應,特別是尾煤中含有很高的礦物質成分,導熱性能和傳熱的差異,使樣品內部和外表的溫度差較大,導致尾煤中有機分子的分解過程延緩、揮發物的析出阻力增大。隨著升溫速率增大,原料在低溫區的停留時間縮短,整個熱解體系會被迅速加熱到高溫區域,導致尾煤中的有機組成在高溫區域迅速分解、聚合并析出。同時,揮發分的快速析出會導致物料攪動,提高了熱解體系的熱傳導和對流效果,促進尾煤進一步熱解,導致熱失重速率增大。但是由于升溫速率增大導致停留時間縮短,整個熱解過程隨著熱解時間延續而向高溫區推移。

表3 尾煤熱解特性參數Table 3 Parameters of pyrolysis of tailings
2.2 尾煤熱解動力學分析
為了更好地描述尾煤的熱解失重特性,構建尾煤熱解的表觀動力學模型,采用Coats-Redfern積分法進行擬合運算[20-21],求解了尾煤熱解的動力學參數。通過離變量,積分整理并取近似值可以得到:


式中,R為影響因子;T為熱解溫度,℃;當2RT/E?1,則接近常數,設Y=,則可以得直線方程Y=a+bX,求解a和b值,就可得到尾煤熱解反應的活化能(E)和頻率因子(A)。經過模擬演算,得出尾煤的熱解反應為二級反應,其動力學參數如表4所示。
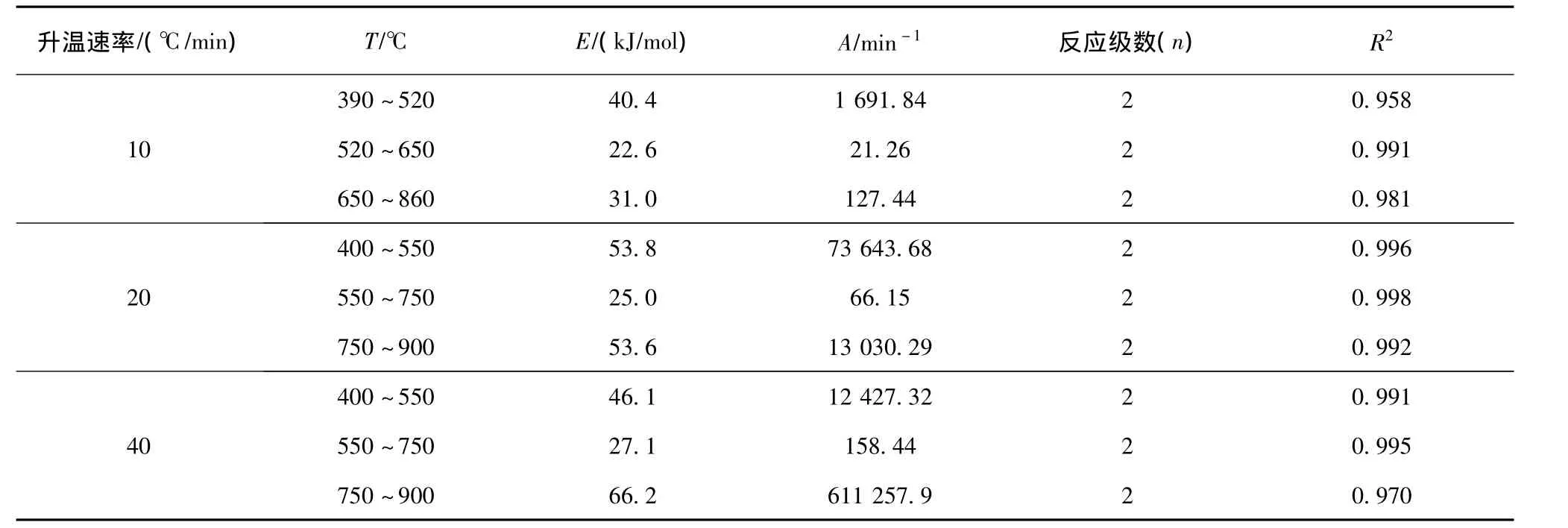
表4 尾煤熱解動力學參數Table 4 Kinetics parameters of tailings pyrolysis
由表4可知,尾煤熱解反應的活化能為22.6~66.2 kJ/mol,熱解反應用三個二級反應過程描述。隨著升溫速率增大,熱解活化能呈現出先降低后增加的現象。原因是尾煤熱解第一階段大致相當于半焦形成前膠體的塑性階段[22],主要發生大分子鍵斷裂,需要提供較高的能量,使得其表觀活化能較高。隨著溫度的升高,膠體迅速分解,大量揮發分析出。當溫度高于最大熱失重速率所對應的溫度時,由于揮發分快速析出導致熱解體系不穩定,活化能降低。第三階段是在第二階段劇烈反應的基礎上發生縮聚和半焦的固化反應,所需的能量相應高于第二階段。
2.3 固定床熱解試驗分析
2.3.1 終溫對尾煤熱解過程影響
分別選擇800,850,900和950℃作為熱解終溫,進行尾煤熱解過程探討,結果如圖3,表5和圖4所示。
由圖3可以看出,隨著熱解溫度升高,熱解焦(固相)的產率逐漸降低;氣相析出呈遞增態勢,產率逐漸升高;液相在850℃前產率呈遞增趨勢,850℃時達到最大值(6%),隨著溫度升高焦油二次分解,液相產率逐漸減少。熱值也逐漸增大。
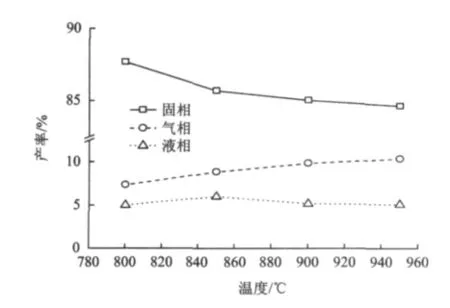
圖3 尾煤熱解產物分布特性Fig.3 Distributions of pyrolysis products of tailings
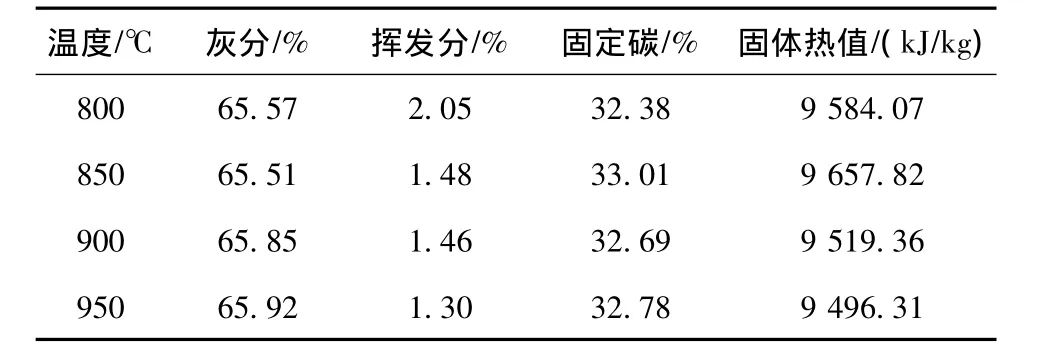
表5 尾煤熱解焦工業分析Table 5 Proximate analysis of pyrolysis coke of tailings

圖4 尾煤熱解不同溫度的氣體產量Fig.4 Gas production of different temperatures of tailings pyrolysis
結合尾煤熱解焦的工業分析結果(表5)表明,隨著溫度升高,熱解焦的揮發分逐漸降低,終溫是影響尾煤熱解的重要參數,高溫為尾煤中化學鍵斷裂提供了更高能量,有利于促進尾煤中高分子有機組分裂解和揮發分析出,最終決定了尾煤熱解反應的進程。
由圖4可以看出,整個氣體析出曲線由200℃左右和900℃左右兩個析出峰組成。隨著溫度升高,氣體產量不是線性增加。200℃左右出現一個析出峰,是物理吸附狀態存在的水和氣體的析出引起的,收集到的氣體基本是水蒸汽。隨著溫度升高瞬時產量下降,到400℃左右收集到的氣體產量達到最小。這與TG分析基本吻合。之后隨著溫度升高,氣體產量增加。在800℃左右瞬時氣體產量達到最大,之后瞬時氣體產量下降,在900℃左右氣體析出基本停止。
2.3.2 氣體分布及產氫特性
尾煤熱解過程中的氣相組成以H2,CH4和CO為主,同時含有少量的CO2。氣體產量及熱值如表6所示,氣體析出曲線如圖5所示。
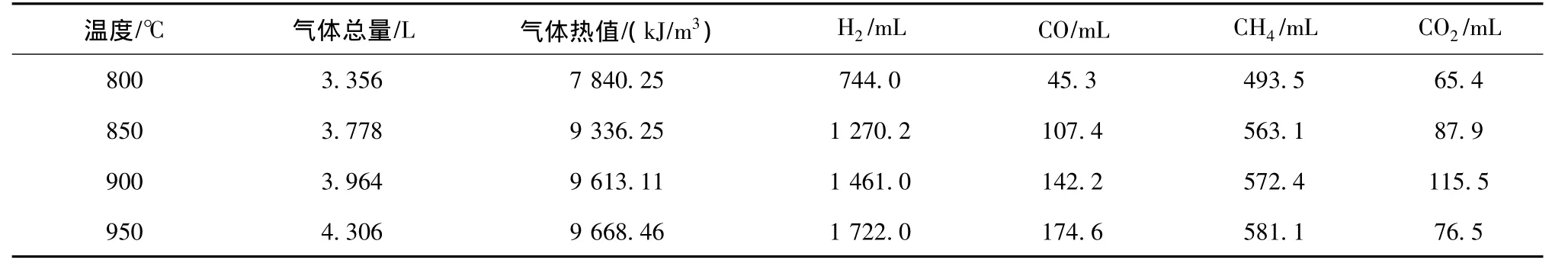
表6 不同溫度下的氣體產量及熱值Table 6 Gaseous yield distribution and caloric value at different temperatures
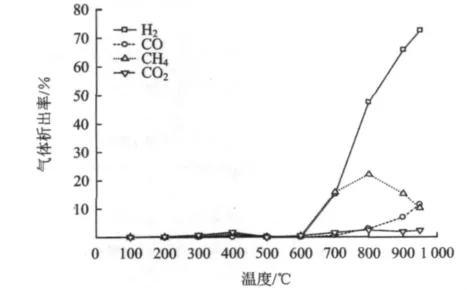
圖5 尾煤熱解氣體組分析出特性Fig.5 Evolution characteristics of gas components during pyrolysis
從圖5可以看出,當溫度低于600℃時,氣相產物很少,當溫度超過600℃后,各氣體組分析出明顯。氫氣和一氧化碳隨著溫度升高保持增加趨勢,伴隨整個反應過程。甲烷和二氧化碳先增加后減少。氫氣在600℃前析出很少,400℃前后有少許變化但不明顯,在600~700℃時析出突然增加,達到15%,比典型煤熱解在500℃后大量析出推遲近100℃;此時H2的來源多由煤熱解的一次產物受到二次熱解作用和煤結構單元中芳香部分的進一步縮聚反應生成[23],隨著溫度升高,H2濃度迅速升高,析出峰出現在900℃左右,高于正常煤熱解氫氣析出峰溫度,氫氣濃度最高可達72.61%。認為是由于熱解后期縮聚反應造成的[21],由環數較小的芳環變成環數更大的芳環,同時伴隨著氫氣的釋放。由表6也可看出,隨著溫度升高氫氣濃度遞增,熱值也遞增。
煤熱解過程中CO的主要來源有醚鍵、羥基和含氧雜環的斷裂、分解,所以煤中的氧濃度高,CO的釋放量大。CO在600℃前基本收集不到,隨著溫度升高其濃度緩慢升高,在900℃左右達到高析出峰,最高可達11.51%。低溫時CH4主要由煤熱解過程中脂肪側鏈斷裂而生成,CH4的產率與煤中脂肪的甲基官能團的數量有關,隨著脂肪甲基濃度的增加CH4的產率也增加。試驗中CH4在200℃前有微量生成,600℃前隨溫度升高生成緩慢。600℃后濃度增加迅速,800℃出現最大析出峰,最高值為22.09%;此后隨溫度升高呈下降趨勢。CO2在整個熱解過程中濃度一直較低,在600~800℃的變化趨勢與CH4相同。造成該現象的原因是在600℃之前,尾煤中的礦物處于欠活化狀態,阻礙了熱傳導過程,抑制了氣相成分析出;當溫度高于600℃,礦物質開始活化,促進了尾煤中有機成分裂解、聚合以及揮發分的析出過程。
3 結論
(1)尾煤的熱解分為四個階段,活潑熱解主要發生在650~850℃。通過Coats-Red fern公式擬合計算,尾煤熱解的活化能為22.6~66.2 kJ/mol,熱解過程用三個二級反應過程進行描述。升溫速率主要通過影響尾煤熱解反應的活化能和頻率因子起作用。
(2)尾煤熱解過程中H2最大析出峰出現在900℃左右。甲烷生成量隨溫度升高先增后減,在750~800℃達最大;CO析出隨溫度升高而升高;CO2隨溫度升高先增后減,最大析出峰集中在800℃左右。950℃時熱解產富氫氣體為4.306 L,氫氣產量為1.722 L,具有較高產率和利用價值。
[1]YANG Y,SUN W,LI S F.Tailings dam stability analysis of the process of recovery[J].Procedia Engineering,2011,26:1782-1787.
[2]FOURIE A.Preventing catastrophic failures and mitigating environmental impacts of tailings storage facilities[J].Procedia Earth and Planetary Science,2009,1(1):1067-1071.
[3]ZHENG X,XU X H,XU K.Study on the risk assessment of the tailings dam break [J].Procedia Engineering,2011,26:2261-2269.
[4]DUONG C,CHONG J,XU Z J,et al.A novel process for recovering clean coal and water from coal tailings[J].Minerals Engineering,2000,13(2):173-181.
[5]張磊.煤泥水熱解制氫及相關催化劑的研究[D].北京:中國礦業大學,2009:9-12.
[6]KIDENA K,MURATA S,NOMURA M.Studies on the chemical structural change during carbonization process[J].Energy and Fuels,1996,10(3):672-678.
[7]UCAR S,KARAGOZ S,YANIK J,etal.Copyrolysis of scrap tires with waste lubricant oil[J].Fuel Processing Technology,2005,87(1):53-58.
[8]FINNEY K N,SHARIFY V N,SWITHENBANK J.Combustion of spent mushroom compost and coal tailing pellets in a fluidisedbed[J].Renewable Energy,2009,34(3):860-868.
[9]ANTHONY E J.Fluidized bed combustion of alternative solid fuels,status,successes and problems of the technology[J].Progress in Energy and Combustion Science,1995,21(3):239-268.
[10]FINNEY K N,CHANGKOOK R,SHARIFI V N,et al.The reuse of spent mushroom compost and coal tailings for energy recovery:comparison of thermal treatment technologies[J].Bioresource Technology,2009,100(1):310-315.
[11]van KREVELEN D W.Coal[M].3rd ed.Amsterdam:Elsevier,1993:979.
[12]SAMARAS P,DIAMADOPOULOS E,SAKEKKAROPOULOS G P.The effect of mineral matter and pyrolysis conditions on the gasification of greek lignite by carbon dioxide[J].Fuel,1996,75(9):1108-1114.
[13]FRANKLIN H D,PETER W A,HOWARD J B.Mineral matter effects on the rapid pyrolysis and hydropyrolysis of a bituminous coal:2.effects of yields of C3-C8hydrocarbons[J].Fuel,1982,61(12):1213-1217.
[14]SLAGHUIS J H,FERREIRA L C,JUDD M R.Volatile materialin coal:effect of inherent mineral matter[J].Fuel,1991,70(3):471-473.
[15]李凡,張永發,謝克昌.礦物質對煤顯微組分熱解的影響[J].燃料化學學報,1992,20(3):300-306.
[16]朱金波.煤中礦物質對熱解過程的影響研究[J].選煤技術,2005(6):10-13.
[17]王俊宏,常麗萍,謝克昌,等.西部煤的熱解特性及動力學研究[J].煤炭轉化,2009,32(3):1-5.
[18]OZTAS N A,YURUM Y.Pyrolysis of Turkish Zonguldak bituminous coal:part1.effect of mineral matter[J].Fuel,2000,79(10):1221-1227.
[19]LIU Q R,HU H Q,ZHOU Q,et al.Effect of inorganic matter on reactivity and kinetics of coal pyrolysis[J].Fuel,2004,83(6):713-718.
[20]LáZARO M J,MOLINER R,SUELVES I.Non-isothermal versus isothermal technique to evaluate kinetic parameters of coal pyrolysis[J].J Analytical and Applied Pyrolysis,1998,47(2):111-125.
[21]趙云鵬.西部弱還原性煤熱解特性研究[D].大連:大連理工大學,2010:4-6.
[22]CHRISTIANSEN J V,FELDTHUS A,CARLSEN L.Flash pyrolysis of coals:temperature-dependent product distribution[J].Anal Appl Pyroly,1995,32(3):51-63.
[23]郭崇濤.煤化學[M].北京:化學工業出版社,1996:90-92.○

