蠶豆-土壤系統對14CO2的吸收和積累
史建君 (浙江理工大學理學院,浙江 杭州 310018)
蠶豆-土壤系統對14CO2的吸收和積累
史建君*(浙江理工大學理學院,浙江 杭州 310018)
為了探明14CO2在環境中的行為,采用核素示蹤技術研究了蠶豆-土壤系統對14CO2的吸收和積累動態.結果表明,通過蠶豆葉片光合作用從空氣中吸收的14CO2會向蠶豆其他部位組織輸送并形成積累趨勢,被檢測到的14C比活度數值比較大,表明空氣中的14CO2易于通過葉片吸收而進入蠶豆各組織器官中;蠶豆各部位組織中14C比活度隨時間呈線性增長,增長速率介于20.3~45.1Bq/(g?d),大小次序為:葉>莖>根>豆殼>豆粒.蠶豆對14CO2(14C)具有較強的富集作用,各部位的富集系數隨時間呈快速增加, 其中葉片中的富集系數最高(56d時高達31.61),豆殼次之(56d時達25.57).利用蠶豆的這一富集特性可監測大氣14CO2污染的情況.
蠶豆-土壤系統;14CO2;吸收;積累
核電在正常運行條件下是一種比較安全、清潔和經濟的能源,但因其“三廢”中含有放射性核素,人們對核電站的安全及對環境的影響問題一直非常關注.特別是切爾諾貝利核電站事故,造成大量放射性核素進入環境,許多人和動、植物因此受到輻射損傷[1-2].核電站正常運行時主要通過氣態與液態排放物對環境構成影響,氣態排放物主要有131I、134Cs、137Cs、58Co、60Co、90Sr、14C、144Ce等,液態排放物主要有3H、131I、134Cs、137Cs、58Co、60Co與90Sr等.14C作為主要放射性氣態流出物,是最受關注的核素之一,它半衰期為 5730a,以14CO2形態存在的14C,將參與植物的光合作用而進入食物鏈,危害環境和人類健康.有關核電站排放的放射性核素137Cs、90Sr、60Co、95Zr、3H等在生態系統中的行為和特性研究報道較多[3-9].但對14C的研究相對較少,作者研究了樟樹對14CO2的吸收和積累,孫桂蓮等[11]研究了14C在水-金魚藻系統中的消長動態,林明明等[12]研究了小麥對14CO2的吸收和積累動態,Linda等[13]研究了14C在海洋中的遷移模型.有關蠶豆-土壤系統對14C的吸收和積累研究尚未見報道.
為了探明生態環境中14CO2的行為特性,本試驗應用同位素示蹤技術研究了蠶豆-土壤系統對14CO2的吸收和積累動態,為科學評定蠶豆-土壤系統對14CO2的吸收、積累狀況提供基礎數據,為制定適合我國國情的標準、法規提供依據.
1 材料與方法
1.1 供試核素
NaH14CO3由中國原子能研究院同位素研究所提供,為透明液體,放化純度>95%,比活度3.7×106Bq/mL,使用前按質量比 1:1.05×105配制成0.84mol/L濃度的NaH14CO3+NaHCO3混合液,混合液的14C比活度為1.85×107Bq/L.
1.2 供試土壤
供試砂壤土,取自浙江大學華家池實驗農場,其理化性質參見文獻[10] .
1.3 試驗方法
在3只1000mm×1000mm×300mm的水泥池中各盛入砂壤土300kg(土壤含水量約18%,每池土均勻拌人90g(NH4)2SO4和120g KH2PO4作基肥),土層厚度約24cm.于當年11月20日播種蠶豆,每池播16穴,每穴3粒種子,出苗后每穴保留2株健壯蠶豆苗.在蠶豆的生長過程中適時施肥,試驗水池建于露天網室中.于次年3月20日將3只與水泥池相配套的800mm×850mm×700mm污染試驗箱罩(透明有機玻璃制成,內置CO2發生器和微型風扇,頂部設有4個(100×100)mm2的采樣口)罩在對應的水泥池上,箱體與水泥池的接口部位用碎土填充密封,取 2.00mL NaHCO3+ NaH14CO3)混合液與5mLHClO4溶液(0.37mol/L,適度過量)在污染試驗箱體內置CO2發生器中作用產生14CO2+CO2混合氣體,同時開啟微型風扇使其均勻擴散,初次引入后污染試驗箱體內大氣CO2濃度約為0.04%,14C比活度為77.7Bq/L,每隔7d引入一次,共引入8次.
1.4 采樣和制樣
于首次14CO2+CO2引入后第0,7,14,21,28,42, 56d采樣(采樣在當天引入14CO2+CO2前進行),每池隨機取蠶豆2株,3池共6株,根部用清水沖洗后用吸水紙吸去表面水,稱重后將蠶豆分為根、莖、葉、豆殼和豆粒(如果有的話)5部分;用半筒式不銹鋼取土器每池取土柱 1個,3池共 3個,隨即將土柱按約每40mm橫向均等分割成6段,所有樣品(植物和土壤)分別稱重后置于干燥箱中于60℃下烘干,每種樣品3個重復.
將烘干后的樣品磨碎混合均勻后,植物樣品稱取60mg,土壤樣品稱取100mg(每種樣品3個重復)置于 OX-600型生物氧化燃燒儀上于850oC下燃燒3min,用含乙醇胺的閃爍液收集燃燒產生的14CO2,氧氣通量和清洗氮氣的通量約為 350mL/min,以提取植物和土壤中的14C.燃燒前接收管中先裝8mL閃爍液,燃燒后將其倒入測樣瓶中,并用 2mL閃爍液沖洗一次,沖洗液一并加入測樣瓶中.閃爍液配方為: 0.5g POPOP+5gPPO+600mL二甲苯+150mL乙醇胺+150mL乙二醇乙醚+100mL甲醇.
1.4 14C活度測定與數據處理
所用樣品均在Wallac 1400 DSA液閃儀上測定,測量誤差控制在5%以內.測量結果經相應的燃燒回收效率校正和扣除本底后,換算成樣品的比活度. 整株蠶豆中的濃度按其各部位中的濃度加權平均計算獲得.土壤的14C比活度指全土平均.富集系數 CF[14]=生物中的14C比活度(Bq/g)/空氣中14CO2比活度(Bq/L).
2 結果與討論
2.1 蠶豆-土壤系統對14CO2吸收和積累動態
由表1可見,在蠶豆的根、莖、葉、豆殼和豆粒(如果有的話)中均檢測到了14C的存在,表明通過光合作用從空氣中吸收的14CO2會在蠶豆各組織中積累,被檢測到的14C比活度數值比較大,表明空氣中的14CO2易于通過葉片吸收而進入蠶豆各組織器官中.
蠶豆各部位組織的14C比活度均隨時間呈逐漸上升的趨勢,具有明顯的積累特征.葉片是進行光合作用的器官,光合作用產生的同化產物首先在葉片中積累,致使葉片中的14C比活度高于其他部位;莖桿具有輸送同化產物的作用,其14C比活度次之;根中的14C比活度相對較低,可能與根系生長相對上部組織比較緩慢,需要的同化產物較少有關.生長后期結出豆粒后,豆殼和豆粒中的14C比活度略低于葉片,但高于莖和根部的14C比活度,豆粒是新生組織,光合作用產生的同化產物向新生組織輸送的量較多,致使豆粒中的14C比活度水平較高.
蠶豆各部位中的14C比活度均隨時間而增長,對表 1數據進行線性回歸分析表明: 蠶豆組織中14C比活度C的變化與時間t間呈線性正相關,擬合方程如下:
根: C=29.9t-83.6 r2=0.944;比活度隨時間的增長速率為29.9Bq/(g·d)
莖: C=34.6t-77.1 r2=0.978;比活度隨時間的增長速率為34.6 Bq/(g·d)
葉: C=45.1t+81.7 r2=0.979;比活度隨時間的增長速率為45.1 Bq/(g·d)
豆殼: C=24.2t+783.1 r2=0.760;比活度隨時間的增長速率為24.2 Bq/(g·d)
豆粒: C=20.3t+879.9 r2=0.692;比活度隨時間的增長速率為20.3 Bq/(g·d)
整株: C=40.0t-48.5 r2=0.935;比活度隨時間的增長速率為40.0 Bq/(g·d)
根、莖、葉和整株中14C比活度與時間的線性相關性相當好,豆殼和豆粒略差一些,其原因是豆粒在生長初期大量吸收同化產物,致使14C比活度迅速上升,在經過灌漿期后,生長逐漸趨緩,呈現出先快速上升,后逐漸走平的特性.
蠶豆各部位14C比活度隨時間的增長速率介于 20.3~45.1Bq/(g·d)范圍內, 大小次序為:葉>莖>根>豆殼>豆粒.其中葉片中14C比活度的增長速率最大,達45.1Bq/(g·d),是豆粒的增長速率的2.22倍.
與放射性金屬離子(89Sr、95Zr和137Cs)相比較,14CO2在作物中的分布特性與137Cs相近[15-16],與89Sr、95Zr不同,89Sr主要積累在根和莖葉組織中,果實中的含量較低[17],95Zr主要蓄積在地下部和浸于水中的莖桿下部,上部組織幾乎為0[18].
土壤中的14C比活度總體上處于較低水平,隨時間呈現逐漸上升的趨勢,14C進入土壤的途徑主要是來源于空氣中的14CO2及通過植物根系與土壤溶液發生交換而進入土壤.
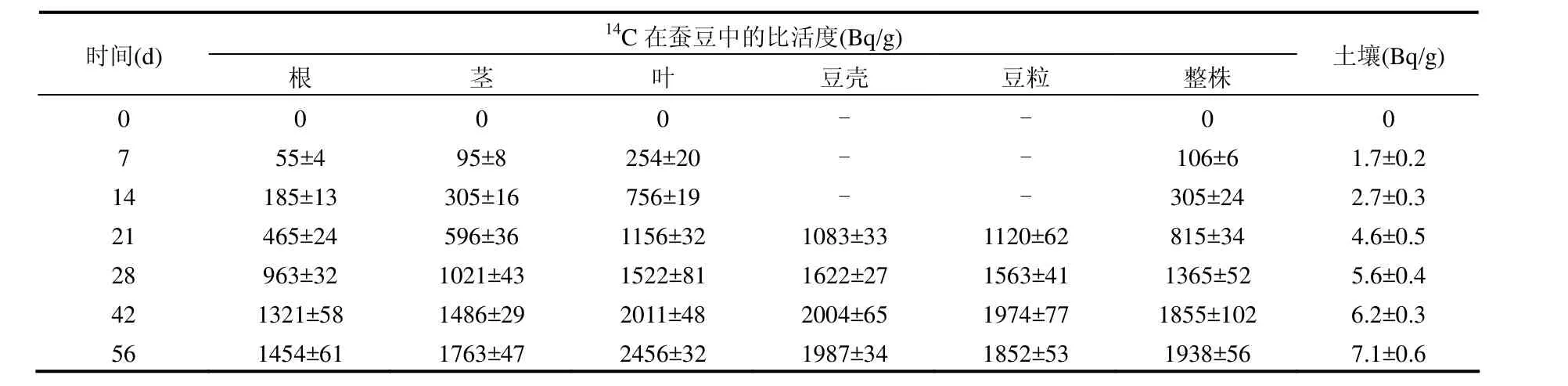
表1 14C在蠶豆-土壤系統各組分中比活度的動態變化(干重)Table 1 Dynamic change in 14C specific activity in a broadbean-soil system (dry weight)
2.2 蠶豆對14CO2的富集特性
14C的生物學性質類似于普通碳,被生物體吸收后會參于生物的各種新陳代謝過程, 蠶豆各組織對來源于空氣中14CO2的14C的富集系數除 7d時的根外均大于 1(表 2),表明蠶豆對14CO2(14C)具有較強的富集作用;蠶豆各部位組織對14C的富集系數隨時間呈增加趨勢,具有明顯的積累效應,且各部位組織的富集系數有所不同,其中葉片中的富集系數最高(56d時高達31.61),豆殼次之(56d時達 25.57),富集特性與小麥相似[12].利用蠶豆的這一富集特性可監測大氣14CO2污染的情況.
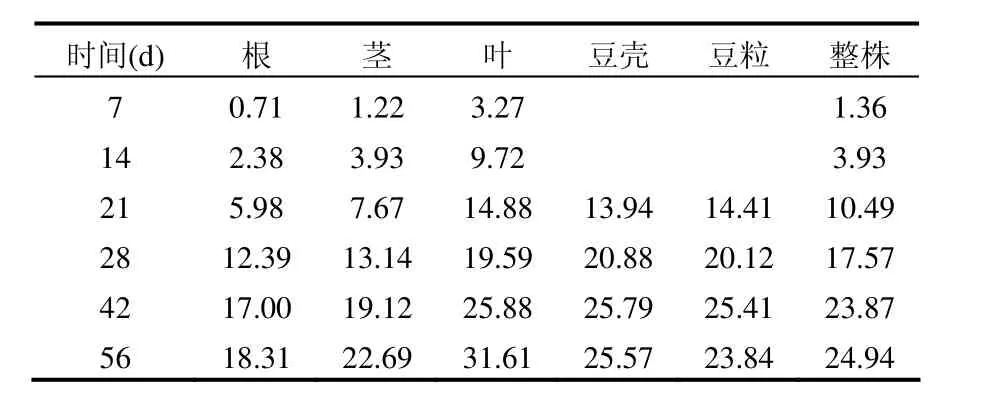
表2 蠶豆對14CO2的富集系數Table 2 Concentration factor values of 14C in broadbean
2.3 14C在土壤中的垂直分布
14C在土壤中的比活度隨土壤深度及時間的變化如表3所示,總體上看處于較低水平.表層土略高一些,分析其原因,表層土中的14C主要來源于空氣中的14CO2,空氣中的14CO2與表土中的水分接觸溶解成碳酸而進入表土,致使表土14C比活度高于中下層土壤,且隨時間的增加溶解量增加,致使表土中的14C比活度呈逐漸增加的趨勢.中層土壤(4~16cm)也有少量分布,其來源主要為植物根系與土壤溶液發生離子交換而致使14C進入土壤(植物根系主要分布在中層土壤).下層土壤很少,接近于本底.
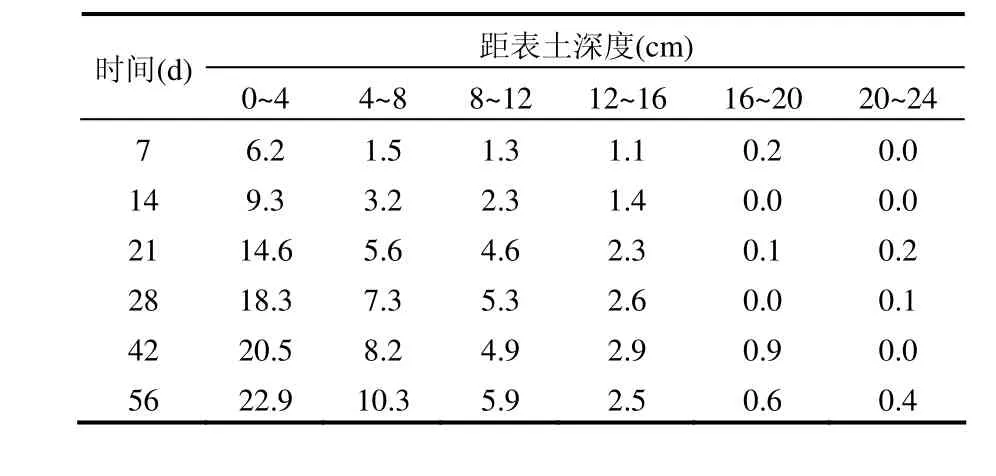
表3 14C在土壤中的垂直分布(Bq/g)Table 3 Vertical distribution of 14C specific activity in the soil (Bq/g)
2.4 14CO2引入量與14C積累量的關系
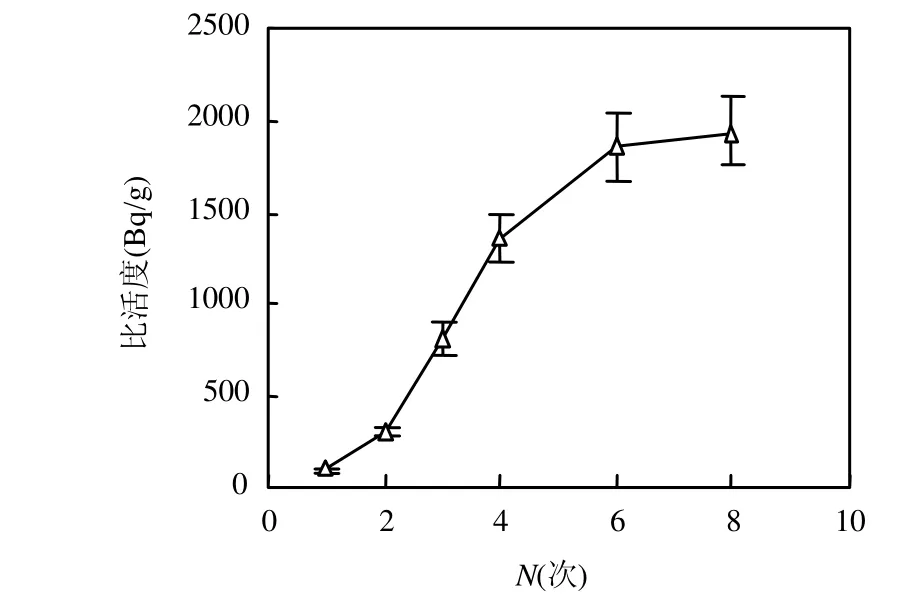
圖1 蠶豆植株中14C的積累動態Fig.1 Accumulation of 14C specific activity in broadbean
由圖1可見,蠶豆植株中的14C比活度隨引入次數的增加而增大,至后期增長速率有所減緩,其原因是生長后期蠶豆植株已進入老熟期,光合作用和對同化產物的需求均減弱,因此表現出對14C積累效應減弱的現象.
蠶豆植株中14C比活度與14CO2引入次數的線性關系為:C=285.85N-79.41,r2=0.9151;隨引入次數的增長速率為 285.85Bq/(g·次),線性關系略差一點,這主要與豆的生長周期有關.
3 結論
3.1 通過蠶豆葉片光合作用從空氣中吸收的14CO2會在蠶豆各組織中積累,被檢測到的14C比活度數值較大,表明空氣中的14CO2易于通過葉片吸收而進入蠶豆各組織器官中.
3.2 蠶豆各部位組織的14C比活度隨時間呈逐漸上升的趨勢,增長速率介于 20.3~45.1Bq/(g·d)范圍內,大小次序為:葉>莖>根>豆殼>豆粒.其中葉片中14C比活度的增長速率最大.蠶豆對14CO2(14C)具有較強的富集作用,富集系數也隨時間呈增加趨勢,其中葉片中的富集系數最高(56d時高達31.61),豆殼次之(56d時達25.57).
3.3 來源于空氣中的14CO2也會輕微污染土壤,其主要途徑有二:其一為空氣中的14CO2與表土中的水分接觸溶解成碳酸而進入表土,其二為通過植物根系與土壤溶液發生離子交換而致使14C進入土壤.
[1] Moore D H, Tucker J D, Jones I M, et al. A study of the effects of exposure on cleanup workers at the chernobyl nuclear reactor accident using multiple and points [J]. Radiation Research, 1997,148(5):463-475.
[2] Hutchins D A, Stupakoff I, Hook S, et al. Effects of Arctic temperatures on distribution and retention of the nuclear waste radionuclides241Am,57Co and137Cs in the bioindicator bivalve macoma balthica [J]. Marine Environmental Research, 1998, 45(1):17-28.
[3] Liu L L, Shi J J, Zhao X Y, et al. Dynamics of transfer and distribution of95Zr in the broadbean-soil ecosystem [J]. Journal of Environmental Radioactivity, 2005,80:217-233.
[4] Golikov V, Logacheva I, Bruk G, et al. Modelling of long-term behaviour of cesium and strontium radionuclides in the Arctic environment and human exposure [J]. Journal of Environmental Radioactivity, 2004, 74 (1-3):159-169.
[5] Chao J H, Chiu C Y, Lee H P. Distribution and uptake of137Cs in relation to alkali metals in a perhumid montane forest ecosystem [J]. Applied Radiation and Isotopes, 2008,66(10):1287-1294.
[6] Choi Y H, Lim K M, Lee W Y, et al. Tissue free water and organically bound tritium in the rice plant acutely exposed to atmospheric HTO vapor under semi-outdoor conditions [J]. Journal of Environmental Radioactivity, 2002,58(1):67-85.
[7] Wei G X, Wang Y B, Wang Y L. Using137Cs to quantify the redistribution of soil organic carbon and total N affected by intensive soil erosion in the headwaters of the Yangtze River, China [J]. Applied Radiation and Isotopes, 2008,66(12):2007-2012.
[8] Shi J J, Guo J F. Uptake from soil and distribution of95Zr in Chinese cabbage [J]. Journal of Agricultural Science, 2002,139: 431-435.
[9] Zhao X Y, Cai Z Q, Gong F H, et a1.Transference kinetics of60Co in an aquatic-terrestrial ecosystem [J]. Nuclear Science and Techniques, 2008,19(4):213-217.
[10] 史建君.樟樹對14CO2的吸收和積累 [J]. 中國環境科學, 2010, 30(12):733-737.
[11] 孫桂蓮,史建君.14C在水-金魚藻系統中的消長動態 [J]. 中國環境科學, 2006,26(2):219-223.
[12] 林明明,史建君,陳 暉.小麥對14CO2的吸收和積累動態 [J].中國環境科學, 2007,27(6):841-844.
[13] Linda K, Michael G, Ulrik K, et al. An ecosystem model of the environmental transport and fate of carbon-14 in a bay of the Baltic Sea, Sweden [J]. Ecological Modelling, 2003,166(3): 193-210.
[14] 陳傳群,王壽祥,徐寅良,等.放射生態學論文集 [C]. 北京:原子能出版社, 1995.201-219.
[15] 徐寅良,陳傳群, 陳 斌,等.水稻對134Cs的吸收和134Cs在水稻-土壤中的分配 [J]. 核農學報, 1991,5(1):19-24.
[16] 商照榮,于鳳義,路子顯.秦山、大亞灣核電站周圍地區土壤盆栽水稻對137Cs的吸收規律 [J]. 輻射防護, 1995,19(3):183-188.
[17] 史建君,王壽祥.水稻對放射性鍶的吸收及撒灑硅藻土對其行為的影響 [J]. 核農學報, 2003,17(3):203-206.
[18] Shi J J, Guo J F, Chen H. Dynamics of95Zr in the Rice/Water/Soil System [J]. Applied Radiation and Isotopes, 2002,56:735-740.
Uptake14CO2from air and accumulation of14C in broadbean-soil system.
SHI Jian-jun*(Institute of Science, Zhejiang Sci-Tech University, Hangzhou 310018, China). China Environmental Science, 2012,32(1):120~124
Uptake14CO2from air and accumulation of14C in broadbean-soil system were studied by using the isotope-tracer techniques, which was used to get a better understanding of the environmental behavior of14CO2. The14CO2, which was absorbed from the air by the leaf photosynthesis of broadbean, would be sent to the other parts of the broadbean and form a accumulating trend.14C specific activity was detected high, which demonstrated14CO2in the air easily got into every tissue of broadbean through photosynthesis. The specific activity of14C in every tissue increased linearly with time. And the increasing rate was within the range from 20.3 to 45.1 Bq/(g·d). The order of the rate in tissues was as below: leaf blade >stalk> root >husk>seed. The broadbean had an intensive concentration of14CO2. The concentration factor values increased rapidly with time, and those in the leaf blade reach the highest level(31.61 in 56 days) and followed by the husk (25.54 in 56days). Owing to its high accumulation of14CO2, the broadbean could be used as the indicator plant in the supervisor of14CO2air pollution.
broadbean-soil system;14CO2;uptake;accumulation
2011-03-30
國家自然科學基金資助項目(20477040);浙江省自然科學基金資助項目(Y505076)
* 責任作者, 教授, jjshi61@sohu.com
X591
A
1000-6923(2012)01-0120-05
史建君(1961-)男,浙江杭州人,教授,主要從事環境科學和放射生態學研究.發表論文80余篇.

