檢驗氫氧化鈉溶液明顯變質的最佳方法——一道化學試題引起的教學反思
章永軍
(蘇州工業園區星海實驗中學 江蘇 蘇州 215021)
一、問題的提出
在一節復習課上和學生討論了這樣一道題目:現有一瓶因長期露置在空氣中而變質的氫氧化鈉溶液。
(1)如何用實驗方法證明該氫氧化鈉已經變質? 簡要敘述實驗方法和現象,寫出有關化學方程式。
(2)如何除去該氫氧化鈉溶液中的雜質? 簡要說明實驗方法和現象,并寫出有關化學方程式。
在回答第一小問題時, 主要總結了以下三種方法。方法一:取樣品,加入稀鹽酸或稀硫酸,如果看到有氣泡,則氫氧化鈉已變質;方法二:取樣品,滴加氫氧化鈣溶液,如果產生沉淀,則已變質;方法三:取樣品,滴加氯化鋇溶液或氯化鈣溶液,如果產生沉淀,則已變質。
二、對以上結論進行反思,事實果真如此?
筆者進行了如下實驗:首先取剛開封的氫氧化鈉固體,用蒸餾水配成8%的氫氧化鈉溶液。
實驗1.取樣品滴加氯化鋇溶液,無沉淀生成,說明該氫氧化鈉基本不變質。 另取樣品,滴加氯化鈣溶液,有大量的白色沉淀生成(原因:2NaOH+CaCl2=Ca(OH)2↓+2NaCl),這說明用氯化鈣溶液無法檢驗出氫氧化鈉溶液中的碳酸鈉。
實驗2.取上述8%的氫氧化鈉溶液,滴加飽和石灰水,也產生白色沉淀。 氫氧化鈣溶液和氫氧化鈉溶液不發生化學反應,那么白色沉淀是什么呢? 通過查閱相關資料得到,根據同離子效應,氫氧化鈣在氫氧化鈉溶液里溶解度很小,也會析出得到氫氧化鈣沉淀。 此實驗說明用飽和石灰水也無法證明氫氧化鈉溶液里的碳酸鈉。
實驗3.仍取上述配好的氫氧化鈉溶液,加入碳酸鈉溶液,再滴加5%的氯化鋇溶液,有大量的白色沉淀生成。說明:用5%氯化鋇溶液可以檢驗氫氧化鈉中的碳酸鈉。
實驗4.再取上述8%的氫氧化鈉溶液,滴入1-2 滴酚酞試劑,滴加稀鹽酸至紅色消失,基本無氣泡產生。 再從剛開封的試劑瓶中取出氫氧化鈉固體,直接滴加稀鹽酸,產生大量的氣泡。 這說明,該氣泡應該不是二氧化碳氣體,那怎么會有氣泡產生呢? 原因分析:氫氧化鈉固體和稀鹽酸反應放出大量的熱,使少量的稀鹽酸溫度迅速升高,短時間內達到沸騰,所以產生了“氣泡”的假象。 所以:用稀鹽酸直接滴加到氫氧化鈉固體中,也不能證明氫氧化鈉固體中是否含有碳酸鈉。
實驗5.同樣取上述8%的氫氧化鈉溶液加入一定量的碳酸鈉溶液,逐滴加入稀鹽酸至過量,開始氣泡不明顯,后來有大量的氣泡產生。 可見用稀鹽酸來檢驗氫氧化鈉溶液里的碳酸鈉時, 應該先將氫氧化鈉配成溶液,再滴加過量稀鹽酸或稀硫酸。
三、檢驗氫氧化鈉溶液已明顯變質的各試劑的濃度范圍
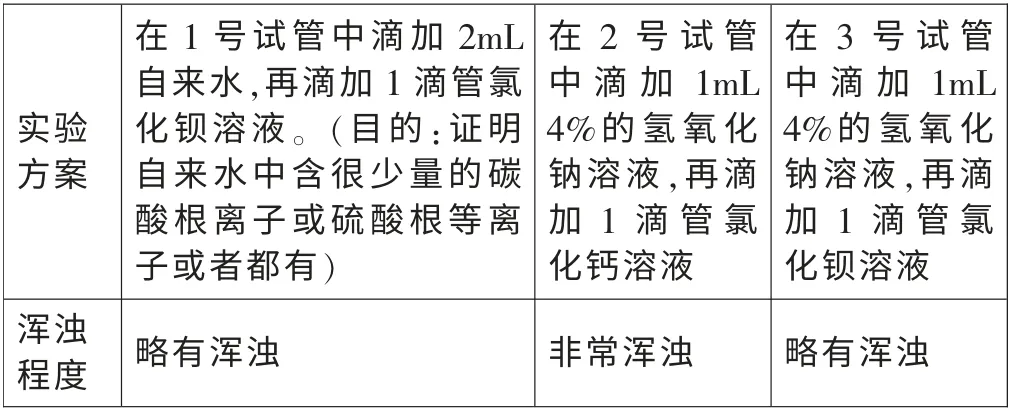
實驗1: 在室溫下配制溶質質量分數均為10%的氯化鋇溶液和氯化鈣溶液。 分別滴加到質量分數約為4%的氫氧化鈉溶液和自來水中。 實驗記錄如下表:
?
通過實驗1 分析, 氯化鋇溶液滴入到新配制的4%的氫氧化鈉溶液,略有渾濁,說明該氫氧化鈉溶液中含極少量的碳酸根離子(其渾濁程度和自來水相當)。 氯化鈣溶液滴入到新配制的4%的氫氧化鈉溶液,非常渾濁。室溫下,Ksp(CaCO3)=8.7×10-9,Ksp(BaCO3)=8.1×10-9[1]兩者相差不大,但是沉淀卻相差很多,這說明2 號試管中的沉淀主要不是碳酸鈣,而是氫氧化鈣。 該實驗進一步說明, 氯化鈣溶液和4%的氫氧化鈉溶液反應有氫氧化鈣沉淀生成。 也就是說用氯化鈣去檢驗氫氧化鈉溶液是否變質是不可靠的。
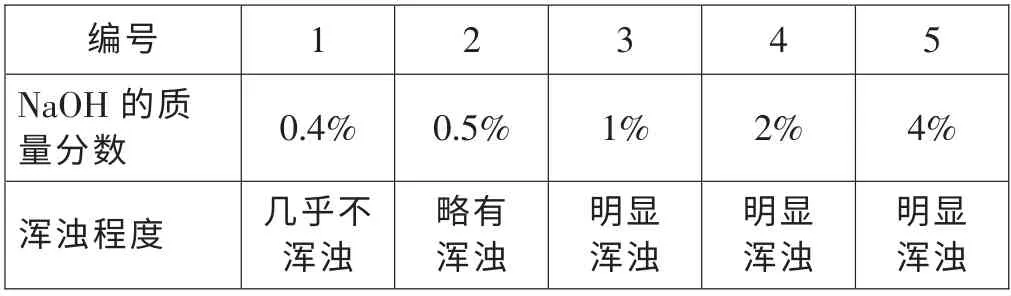
實驗2: 將10%的氯化鈣溶液分別滴加到不同濃度的氫氧化鈉溶液中,實驗記錄如下:
?
通過實驗2 分析,用10%氯化鈣溶液來區別氫氧化鈉溶液是否變質時,只有當氫氧化鈉質量分數小于0.5%才適合。
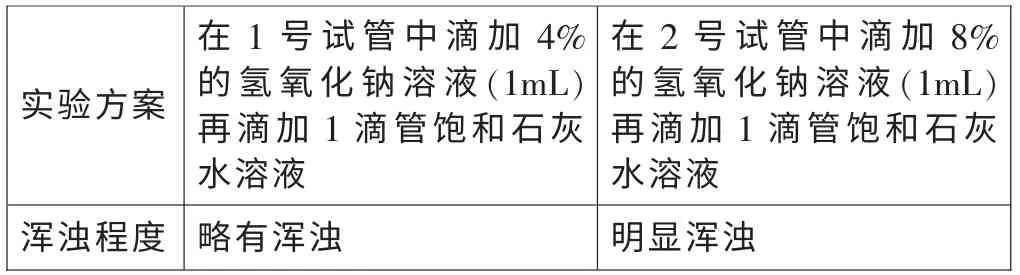
實驗3:將飽和的石灰水分別滴加到,溶質質量分數約為4%和8%的氫氧化鈉溶液中,實驗記錄如下:
?
通過實驗3 分析,用飽和的石灰水檢驗氫氧化鈉是否變質時,只有在氫氧化鈉質量分數小于4%時,才比較適合。
四、實驗結論
結論1:用稀鹽酸來檢驗氫氧化鈉是否明顯變質時,最好是將氫氧化鈉配成溶液,然后加稀鹽酸,如觀察到有明顯的氣泡,可說明氫氧化鈉已經明顯變質。
結論2: 用質量分數為10%左右的氯化鈣溶液來檢驗氫氧化鈉是否明顯變質時,只有將溶液配成極稀的溶液(如果原溶液是4%的氫氧化鈉溶液和水的體積比在1∶10 左右),然后滴加氯化鈣溶液,如果有明顯的沉淀生成,說明氫氧化鈉已經變質。
結論3: 用質量分數為10%左右的氯化鋇溶液來檢驗氫氧化鈉是否明顯變質時,只有當原氫氧化鈉溶液溶質質量分數小于4%,然后滴加氯化鋇溶液,如有明顯的沉淀生成,說明氫氧化鈉已經變質。
結論4: 用飽和石灰水來檢驗氫氧化鈉是否明顯變質時,只有當原氫氧化鈉溶液溶質質量分數小于4%,然后滴加飽和石灰水,如有明顯的沉淀生成,說明氫氧化鈉已經變質。 同樣用飽和石灰水來除去氫氧化鈉溶液中的雜質,也要在很稀的溶液中進行。
五、教學應用
如果在教學中,該探究實驗和學生一起探討明顯難度太大,不利于初中生的學習和理解。 所以在教學中要讓學生知道,剛生產的氫氧化鈉本身都含有少量的碳酸鹽和其他雜質,在長期存放的過程中也難免有變質的情況。 所以在檢驗氫氧化鈉是否明顯變質時,先把氫氧化鈉配成溶液用稀鹽酸來檢驗,觀察是否有明顯氣泡是最可靠的方法。
[1] 北京師范大學無機化學教研室等編.無機化學(上冊)[M].北京:高等教育出版社,1997
[2] 中學化學國家課程標準研制組.義務教育課程標準實驗教科書[M].上海:上海教育出版社,2010:204
[3] 萬信華.關于NaOH 變質情況的探究[J].教育學論,2010,(21):196

