超聲內鏡對良惡性胃潰瘍的鑒別診斷及術前分期中的應用價值
沈健 阮洪軍 費寶瑩 魏夫榮
超聲內鏡對良惡性胃潰瘍的鑒別診斷及術前分期中的應用價值
沈健 阮洪軍 費寶瑩 魏夫榮
胃癌是消化道最常見的惡性腫瘤之一,病死率高,選擇合理的治療方案或手術方式非常關鍵,因此術前準確分期顯得尤其重要。良、惡性胃潰瘍的鑒別一直受到臨床醫師的高度重視,但有時內鏡檢查及活檢很難及時給以準確判斷。近年來超聲內鏡(endoscopic ultrasonography,EUS)檢查在消化道疾病的診治中應用越來越廣泛[1-2]。EUS檢查能清晰顯示消化道管壁5層結構及其周圍情況,判斷胃癌浸潤深度及有無局部鄰近臟器浸潤和淋巴結轉移。本研究通過對65例常規內鏡檢查懷疑為惡性胃潰瘍的患者進行EUS檢查,分析其在良、惡性胃潰瘍鑒別診斷中的意義,同時對惡性胃潰瘍進行TN分期,評估其在手術前的分期價值。
1 資料和方法
1.1 一般資料 收集2007-05—2012-12浙江省人民醫院內鏡中心經常規內鏡檢查懷疑為惡性胃潰瘍的65例患者進行EUS檢查,其中男43例,女22例,年齡22~76歲,平均50.21歲。胃鏡下潰瘍直徑大小約為1.5~3.0cm,潰瘍表面覆污白苔,周圍黏膜堤狀隆起,形狀不規則,疑似BorrmannⅡ型41例,BorrmannⅢ型24例。
1.2 儀器與方法 選用Olympus公司生產的GFUM2000型和UM-2R型,術前肌肉注射安定10mg、山莨菪堿針20mg。EUS檢查時采用水囊法或水囊法加浸泡法探查,觀察潰瘍大小、浸潤深度、底部以下及潰瘍周圍胃壁各層超聲結構,測量潰瘍處及周圍胃壁厚度等,并結合有無胃周淋巴結腫大、轉移對惡性胃潰瘍進行TN分期,胃壁浸潤深度及其周圍淋巴結轉移情況參照2010年美國癌癥聯合會(American Joint Committee on Cancer,ACJJ)公布的第7版TNM分期方法[3]。檢查結束后,良性胃潰瘍患者行正規抗潰瘍治療8周后復查胃鏡并活檢,而惡性胃潰瘍患者均行外科手術治療,將EUS檢查的診斷結果與術后病檢結果進行對照。
1.3 良、惡性胃潰瘍的診斷 惡性胃潰瘍表現為低回聲病灶邊緣不規則,邊界呈浸潤狀,層次結構消失,外周可見圓形或類圓形、回聲低、直徑>10mm的淋巴結。部分患者胃壁增厚明顯。良性胃潰瘍表現為低回聲病灶,邊緣規則,邊界呈非浸潤狀,周圍隆起的胃壁呈“水腫性”圖像即回聲偏低,但層次結構正常,外周未見腫大的淋巴結或淋巴結直徑<10mm。
2 結果
2.1 EUS檢查診斷良、惡性胃潰瘍的準確率 經EUS檢查,65例患者中23例考慮為良性胃潰瘍,其中疑似BorrmannⅡ型16例,疑似BorrmannⅢ7例,經正規抗潰瘍治療8周后復查胃鏡,發現潰瘍均愈合,再次活檢證實為良性潰瘍,準確率為100%;考慮惡性胃潰瘍的42例患者,術前胃鏡活檢找到癌細胞31例,未找到癌細胞11例;術后2例患者病理證實為良性胃潰瘍,胃鏡下表現為疑似BorrmannⅡ型,余40例術后診斷胃癌,準確率為95.24%(40/42)。其中早期胃癌3例,進展期胃癌37例;表現BorrmannⅡ型23例,表現BorrmannⅢ15例,另有2例術后診斷為BorrmannⅣ型。
2.2 惡性胃潰瘍術前、術后病理T分期的比較 見表1。
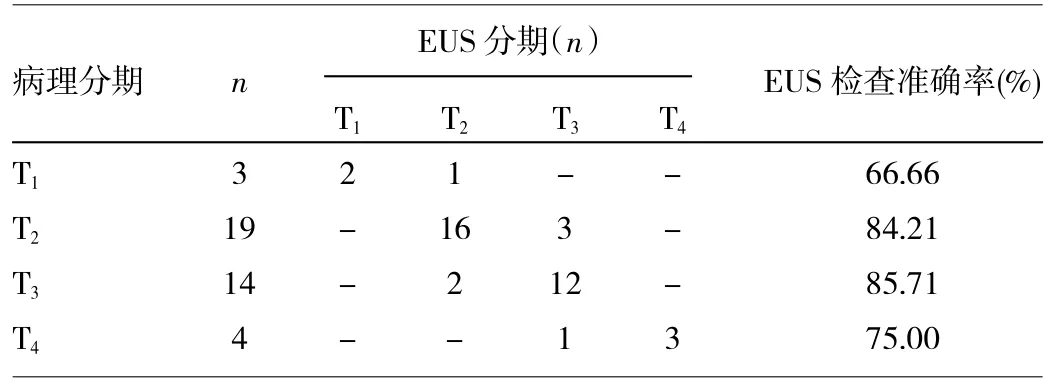
表1 惡性胃潰瘍術前、術后病理T分期的比較
由表1可見,EUS檢查對腫瘤T分期的準確率為82.50%(33/40),7例患者EUS檢查與術后病理T分期結果不符,其中分期過度4例,即T1分為T21例,T2分為T33例;分期不足3例,即T3分為T22例,T4分為T31例。
2.3 惡性胃潰瘍術前、術后病理N分期的比較 見表2。
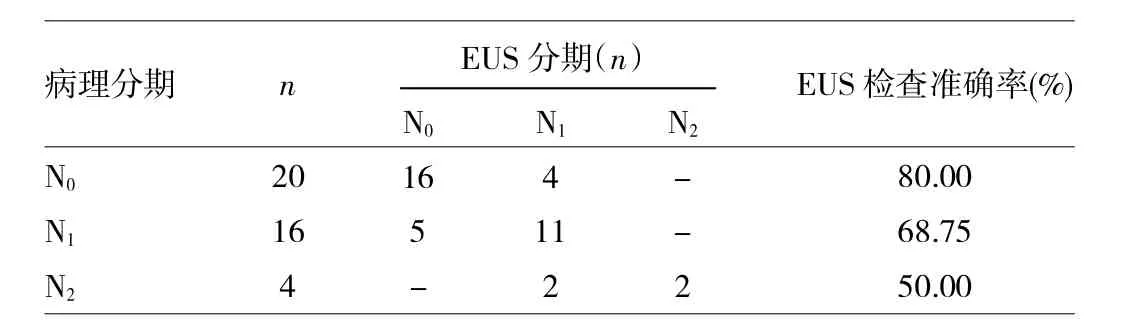
表2 惡性胃潰瘍術前、術后病理N分期的比較
由表2可見,EUS檢查對腫瘤N分期的準確率為72.50%(29/40),11例與術后病理分期不符,其中將轉移性淋巴結誤認為炎癥性淋巴結5例,將炎癥性淋巴結誤認為轉移性淋巴結4例,未發現有淋巴結遠處轉移2例。
3 討論
良、惡性胃潰瘍在EUS掃描圖像上的共同特點是局部胃壁結構的缺損、破壞,表現為胃壁不同深度的回聲層缺失,可見潰瘍的低回聲區和周圍胃壁隆起的偏低回聲。筆者發現潰瘍的回聲強度、均勻性對其良、惡性的鑒別意義不大,而有無浸潤性生長是鑒別診斷的重要依據。惡性胃潰瘍多向周圍胃壁或胃外組織侵犯,良性潰瘍雖周圍胃壁隆起,但超聲圖像呈“水腫樣”表現,同時胃周有無淋巴結腫大、腹水也是鑒別的依據。本組有2例巨大良性潰瘍被誤認為惡性胃潰瘍,EUS圖像顯示其低回聲區已侵犯漿膜,但未見周圍胃壁浸潤性生長和明顯淋巴結腫大,誤判可能由于經驗不足所致。
胃鏡檢查高度懷疑惡性胃潰瘍,但病理學組織檢查未發現癌細胞,經常給臨床診治帶來困難,特別是惡性胃潰瘍向深部浸潤生長而潰瘍周圍增生不明顯時,病理檢查往往為壞死組織。因此,EUS檢查對這類潰瘍性質的鑒別意義更大。本組有9例胃鏡活檢陰性但EUS檢查高度懷疑為惡性胃潰瘍,經手術證實為惡性。其中有2例為腫瘤深部浸潤生長,術后病理證實為BorrmannⅣ,這類胃癌即使反復活檢,其陽性率也很低,EUS檢查可及時準確發現深部病灶,為進一步診斷和手術治療提供幫助。另外,EUS引導下細針吸取細胞學檢查也是提高診斷準確率的一個有效方法[4]。
EUS檢查作為胃癌術前分期的重要檢查方法,國內外已有較多報道[5-7]。Kwee等[8]對22例研究進行系統分析發現,胃癌患者EUS檢查術前T分期總準確率為65.0%~92.0%,與多層螺旋CT和MRI檢查相比,EUS檢查仍是胃癌術前T分期的第一選擇方式。但有些學者持不同的意見,Arocena等[9]比較MRI和EUS檢查在胃癌術前分級的準確性發現,在評估腫瘤在胃壁的浸潤程度方面MRI檢查優于EUS檢查。本研究中EUS檢查對40例潰瘍型胃癌T分期的準確率為82.50%,與大部分文獻報道相近[5-8],說明EUS對潰瘍型胃癌術前T分期有重要的價值。本組患者中分期過度4例,可能由于潰瘍表面壞死組織及瘢痕纖維化使病變回聲衰減,周圍的炎癥被誤認為腫瘤浸潤;分期不足3例,可能與組織的微小浸潤灶或局部破壞不易為低頻超聲談及有關。此外,胃壁增厚明顯或病變隆起過大,超聲波穿透深度有限等也常為分期不足的原因。
有文獻報道,EUS檢查對早期胃癌T分期有較高的準確性,是選擇合理治療方案的重要依據[6,10-11]。本研究中早期胃癌3例,1例過度分期為T2,準確率為66.6%,明顯低于文獻報道中的隆起型和平坦型早期胃癌[12]。Akashi等[13]發現潰瘍改變影響EUS對早期胃癌的胃壁浸潤程度的判斷準確率,EUS檢查對潰瘍型早期胃癌T分期不充分。因此,對潰瘍型早期胃癌采取內鏡下黏膜切除術要慎重。
本研究中EUS檢查對腫瘤N分期的準確率為72.50%,誤判11例,其中轉移性淋巴結和炎癥性淋巴結混淆9例。一般來說,EUS檢查可根據淋巴結的大小、形態、內部回聲、邊緣等作出準確判斷,但有時轉移性淋巴結和炎癥性淋巴結鑒別很困難,其原因可能與良、惡性淋巴結鑒別缺乏金標準或微轉移及炎癥反應等有關,借助內鏡超聲引導下細針穿刺可進一步提高其診斷的準確率。因EUS檢查對遠處轉移病灶的發現率低,對應M分期需結合CT、腹部B超等其他相關檢查。
綜上所述,EUS檢查在良、惡性胃潰瘍的鑒別中有重要的價值,對惡性胃潰瘍的TN分期有較高的準確性,對外科手術方式的選擇有很大幫助。
[1]El Saadany M,Jalil S,Irisawa A,et al.EUS for portal hypertension:a comprehensive and critical appraisal of clinical and experimental indications[J].Endoscopy,2008,40(8):690-696.
[2]Jani N,Dewitt J,Eloubeidi M,et al.Endoscopic ultrasound-guided fine-needle aspiration for diagnosis of solid pseudopapillary tumors of the pancreas:a multicenter experience[J].Endoscopy, 2008,40(3):200-203.
[3]American Joint Committee on Cancer.Cancer Staging Manual [M].7th.New York:Springer-Verlag,2010:153-155.
[4]Vander Noot M R,Eloubeidi M A,Chen V K,et al.Diagnosis of gastrointestinal tract lesions by endoscopic ultrasound-guided fine-needle aspiration biopsy[J].Cancer,2004,102(3):157-163.
[5]Ganpathi I S,So J B,Ho K Y.Endoscopic ultrasonography for gastric cancer:does it influence treatment[J]?Surg Endosc, 2006,20(4):559-562.
[6]Tsendsuren T,Jun S M,Mian X H.Usefulness of endoscopic ultrasonography in preoperative TNM staging of gastric cancer[J]. World J Gastroenterol,2006,12(1):43-47.
[7]Potrc S,Skalicky M,Ivanecz A.Does endoscopic ultrasound staging already allow individual treatment regimens in gastric cancer[J].Wien Klin Wochenschr,2006,118(Suppl 2):48-51.
[8]Kwee R M,Kwee T C.Imaging in local staging of gastric cancer: a systematic review[J].J Clin Oncol,2007,25(15):2107-2116.
[9]Arocena M G,Barturen A,Bujanda L,et al.MRI and endoscopic ultrasonography in the staging of gastric cancer[J].Rev Esp Enferm Dig,2006,98(8):582-590.
[10]Ichikawa T,Kudo M,Matsui S,et al.Endoscopic ultrasonography with three miniature probes of different frequency is an accurate diagnostic tool for endoscopic submucosaldissection[J]. Hepatogastroenterology,2007,54(73):325-328.
[11]Miquel J M,Abad R,Souto J,et al.EUS-guided mucosectomy for gastrointestinal cancer[J].Rev Esp Enferm Dig,2006,98 (8):591-596.
[12]董光宏,鄒曉平,李兆申.內鏡超聲檢查對胃及食管早期癌的診斷價值[J].中華消化內鏡雜志,2005,22(3):185-187.
[13]Akashi K,Yanai H,Nishikawa J,et al.Ulcerous change decreases the accuracy of endoscopic ultrasonography diagnosis for the invasive depth of early gastric cancer[J].Int J Gastrointest Cancer,2006,37(4):133-138.
2013-03-08)
(本文編輯:嚴瑋雯)
310014 杭州,浙江省人民醫院消化內科(沈健、阮洪軍、費寶瑩,沈健系海寧市第三人民醫院進修醫師);海寧市第三人民醫院(魏夫榮)
阮洪軍,E-mail:ruanhongjun@aliyun.com

