2型糖尿病合并微量蛋白尿患者頸動脈CDFI超聲表現與實驗室檢查的相關性
張宗華
(天津市中醫藥研究院附屬醫院功能檢查科,天津 300121)
合并微量蛋白尿(microalbuminuria,MA)的2型糖尿病(type2 diabetes mellitus,T2DM)患者是早期糖尿病腎病的表現[1],不僅局限于腎臟的微血管改變,同時對全身血管造成損害,尤以動脈粥樣硬化明顯[2]。糖尿病人群中動脈粥樣硬化的患病率較高,病情進展快[3],了解其易患因素尤為重要。筆者重點研究T2DM合并MA患者頸動脈粥樣硬化的彩色多譜勒(CDFI)超聲表現與實驗室檢查的關系。
1 對象與方法
1.1 研究對象
選擇2011年6月至2012年10月在天津市中醫藥研究院附屬醫院糖尿病科住院的T2DM患者178例,均符合1999年WHO糖尿病診斷標準。排除1型糖尿病、高血壓、心臟瓣膜病、冠心病、心功能不全、腎功能不全者。將178例患者按尿白蛋白排泄率(UAER)分為2組,UAER≥30~300 mg·24 h-1者為合并MA組(T2DM1組,104例),男49例,女55例,年齡43~82(59.16±11.87)歲,病程0.4~28.6(8.64±3.65)年;UAER<30 mg·24 h-1者為不合并MA組(T2DM2組,74例),男38例,女36例,年齡31~79(57.65±9.93)歲,病程0.2~26.4(7.42±3.57)年。2組性別、年齡及病程等方面比較差異均無統計學意義(均P>0.05)。
1.2 主要儀器及檢測方法
應用PHILIPS IE33彩色多普勒超聲診斷儀,線陣寬頻探頭頻率為3~12 MHz,選擇儀器預設的頸動脈為檢查條件。患者取仰臥位,靜息狀態下,橫縱結合掃查頸動脈,二維觀察測量管腔內徑、內-中膜厚度(IMT)、管壁斑塊情況(有無、位置、大小、回聲等)。
頸動脈IMT測量方法:在頸總動脈(距分叉前1 cm處)、分叉部、頸內動脈(竇部末端1 cm處)分別測量后壁IMT值,為內膜交界面與外膜交界面間垂直的距離,均測量3次,取其平均值,測量時避開斑塊。頸總動脈IMT>1.0 mm、分叉處>1.2 mm為增厚。斑塊標準:局部IMT增厚>1.5 mm,突入管腔,范圍清晰。據斑塊聲學特性將其分為低/等回聲(低于/等于周圍的胸鎖乳突肌)、強回聲(斑塊鈣化產生的強反射,可伴后方聲影)及混合回聲斑塊(回聲高低不等,雜亂不均勻)。
CDFI檢測:觀察血流充盈情況、方向及色彩,測量血流速度。
實驗室檢查:包括餐后2 h血糖(2 hPG)、空腹血糖(FPG)、UAER、尿酸(URIC)、血肌酐(CREA)、糖化血紅蛋白(HbA1c)、血清總膽固醇(TC)、三酰甘油(TG)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)等指標。
1.3 統計學方法
2 結果
2.1 2組IMT測量結果的比較
2組患者頸動脈斑塊檢出數目及斑塊回聲比較差異均無統計學意義(χ2=0.645,P>0.05)。斑塊檢出率排序為低/等回聲>混合回聲>強回聲(P<0.05)。T2DM1組IMT厚度高于T2DM2組(P<0.05)。見表1。
2.2 2組實驗室各項指標的比較
T2DM1組BMI、UAER、2 hPG、CREA、HbA1c、TC均高于T2DM2組(均P<0.05)。2組FPG、URIC、TG、LDL、HDL比較差異均無統計學意義(均P>0.05)。見表2。
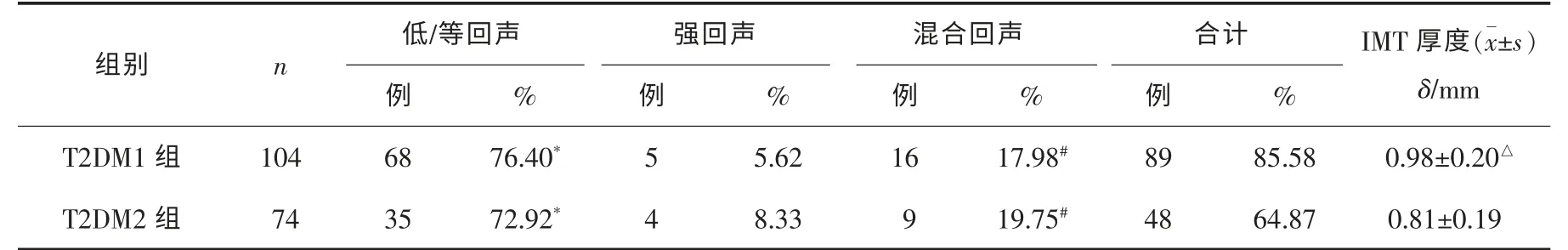
表1 2組患者斑塊情況的比較
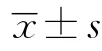
表2 2組實驗室指標的比較
2.3 Pearson相關分析
Pearson相關分析結果:IMT與UAER、CREA、HbAlc及病程呈正相關(r=0.315、0.320、0.463及0.354,均P<0.05)。多元線性回歸分析結果:病程、UAER、HbAlc是IMT增厚的獨立預測因子(r=0.362,0.240、0.395,均P<0.05)。
3 討論
T2DM出現微量蛋白尿,即UAER為30~300 mg·24 h-1,是糖尿病腎病早期改變,難用常規方法檢測出來。腎臟血流動力學異常是T2DM合并MA早期的重要特點,表現為高灌注狀態,腎血管內皮損傷及腎小球損傷。在腎臟微血管損害的同時,也預示著全身性血管的破壞,增加了動脈管壁對脂質微粒的通透性,使血管IMT增厚、粥樣斑塊形成。T2DM合并動脈硬化時,主要侵犯主動脈、冠狀動脈、腦動脈、腎動脈及肢體動脈等[4]。在全身動脈系統中,頸動脈粥樣硬化斑塊最容易觀察,CDFI超聲是評價頸動脈斑塊最方便且無創的方法。頸動脈分叉處至頸內外起始部是斑塊好發部位。低回聲斑塊含有大量脂類物質的纖維脂肪,含細胞較少,使高低密度脂蛋白血癥、斑塊潰瘍和腦缺血風險加大;等回聲斑塊是以膠原蛋白為主的纖維斑塊,頸總動脈的斑塊多為等回聲纖維斑塊;強回聲斑塊是斑塊鈣化所致;混合回聲斑塊回聲雜亂,纖維帽存在蛻變可能,易引起血小板凝聚、血栓形成,有造成栓塞的潛在風險,發生暫時性腦缺血或腦卒中的概率較均值回聲斑塊高[5]。本研究結果顯示,T2DM合并MA患者頸動脈斑塊檢出以低/等回聲斑塊為主,有學者認為,低/等回聲斑塊和混合回聲斑塊是不穩定斑塊,是引起腦出血及腦梗死等腦血管病變的主要危險因素[6]。
本研究結果表明,合并MA的T2DM患者頸動脈IMT增厚更明顯,具有更高的IMT值及動脈粥樣硬化斑塊數。T2DM本身是動脈硬化的危險因素,當合并MA時更使動脈硬化的危險性加大[7]。實驗室檢查中,T2DM1組2 hPG、UAER、CREA、HbAlc及TC指標均高于T2DM2組(均P<0.05),表明合并MA的T2DM患者血糖及血脂控制不理想,血管內皮損傷更明顯,血管通透性增加,更容易出現動脈粥樣硬化及斑塊形成。HbAlc反映的是體內糖基化的終末產物,可以反映中長期血糖水平,是微血管硬化病變的重要病理因素[8]。當HbAlc及TC增高時,機體可發生多種代謝異常,導致蛋白質非酶糖化終產物不可逆性地增高,隨著病程延長,蛋白質非酶糖化終產物在組織中聚集,使糖尿病患者發生大血管病變。本研究中的Pearson相關分析結果顯示:UAER、CREA及病程與IMT呈正相關,表明當病程越長,UAER、CREA指標越高時,IMT增厚越明顯,發生頸動脈粥樣硬化及斑塊形成的可能性越大。
綜上所述,CDFI超聲能準確地檢出T2DM患者頸動脈IMT及粥樣斑塊,當合并MA時,提示糖尿病腎病的早期病變;在腎臟微血管損害的同時,也預示著全身性血管的破壞;頸動脈IMT增厚與UAER、CREA、HbAlc及病程呈正相關。可指導臨床對糖尿病腎病患者及頸動脈粥樣硬化做到早診斷、早治療。
[1]趙建國.腦梗死[M].北京:人民衛生出版社,2006:53-65.
[2]陸再英,鐘南山.內科學[M].北京:人民衛生出版社,2008:770-793.
[3]唐杰,溫朝陽.腹部和外周血管彩色多普勒診斷學[M].北京:人民衛生出版社,2007:143-168.
[4]孫峰雷.糖尿病與心血管疾病[M].2版.濟南:山東科學技術出版社,2007:262.
[5]Dinneen S F,Gerstein H C.The association of microalbuminuria and mortality in non-insulin-dependent diabetes mellitus.A systematic overview of the literature[J].Arch Intern Med,1997,157(13):1413-1418.
[6]楊毅軍.頸動脈粥樣硬化斑塊與相關因素的探討[J].臨床超聲醫學雜志,2009,11(1):34-36.
[7]韓玲玲,張翠玲.2型糖尿病患者頸動脈內膜增厚及其危險因素[J].中國實驗診斷學,2004,2(1):61-62.
[8]歐陽娟,姜儻.腎臟的損傷性診斷[J].中華檢驗醫學雜志,2005,28(8):877-880.

