原發性局灶節段性腎小球硬化癥152例臨床病理特征分析
潘 玲,黃 尤,廖蘊華
(1廣西醫科大學第一附屬醫院,南寧530021;2廣西醫科大學研究生院)
原發性局灶節段性腎小球硬化癥(FSGS)是臨床常見的一種難治性腎小球疾病,也是導致終末期腎病的常見病因,近年來其發病率有明顯的上升趨勢。雖然目前對原發性FSGS已有相對統一的病理診斷標準,但對不同病理類型原發性FSGS患者臨床特點的認識仍不一致[1,2]。2002 年 11 月 ~2010年11月,我們分析了152例原發性FSGS患者的臨床病理特征。現報告如下。
1 資料與方法
1.1 臨床資料 選擇同期在廣西醫科大學第一附屬醫院住院的原發性FSGS患者152例,均經腎活檢病理診斷確診,并排除先天性和繼發性腎病(如狼瘡性腎炎、紫癜性腎炎、血管炎、IgA腎病及高血壓等)所致的FSGS患者。其中男97例、女55例,男女比為1.76∶1,發病年齡 14 ~76(35.1 ±15.0)歲。
1.2 方法
1.2.1 臨床資料收集 患者入院后記錄發病年齡、病程(起病到腎活檢時間)、浮腫、肉眼血尿、血壓等臨床特點,留取晨尿及24 h尿液行尿常規及24 h尿蛋白定量檢查,抽空腹血檢測血常規、腎功能、肝功能、血脂、C反應蛋白、血清免疫球蛋白、血糖、自身抗體、乙肝病毒學指標、腫瘤標記物、血免疫固定電泳等。診斷標準:①血尿:正常新鮮尿液離心后沉渣鏡檢,紅細胞>3個/HP;②蛋白尿:每24 h尿蛋白量超過150 mg,或尿蛋白定性陽性,或尿蛋白/尿肌酐>200 mg/g;腎病范圍蛋白尿≥3.5 g/24 h;③高血壓:收縮壓≥140 mmHg和(或)舒張壓≥90 mm-Hg,或既往確診高血壓目前服藥治療者;④腎性糖尿:同步檢查空腹血糖及尿糖,血糖水平正常、尿糖陽性;⑤腎功能不全:血肌酐>133μmol/L或腎功能下降[腎小球濾過率估計值(eGFR)<60 mL/(min·1.73 m2)[3]];⑥腎病綜合征:血白蛋白 <30 g/L,24 h尿蛋白定量≥3.5 g/d或尿蛋白≥+++,伴或不伴高脂血癥及水腫。
1.2.2 腎臟病理學檢查 腎活檢標本制片后,常規行光鏡(HE、PAS、PASM和Masson染色)及免疫病理(免疫酶標或免疫熒光)檢查,部分行電鏡檢查。被檢查的腎小球不少于8個。FSGS病理診斷參照2004年國際腎臟病理協會制定的標準[4],病理分型為非特殊型、門部型、細胞型、頂端型和塌陷型。腎小球硬化程度分4級:0級:無腎小球硬化;1級:腎小球硬化比例<25%;2級:腎小球硬化比例25% ~50%;3級:腎小球硬化比例>50%。腎小管間質病變(TIL)程度評分:包括腎小管變性、壞死,腎小管萎縮,間質炎癥細胞浸潤,間質纖維化4個參數,各參數評分根據病變累及的范圍按無、<25%、25% ~50%、>50%分別計為0~3分。按TIL總評分將腎小管間質病變分為4級:0級為0分,Ⅰ級為1~4分,Ⅱ級為 5~8分,Ⅲ級為 9~12分[5]。參照文獻[6]方法對FSGS的病理活動性和慢性化病變進行評分。
1.2.3 統計學方法 采用SPSS13.0統計軟件,計量資料以±s或中位數(四分位數間距)表示,組間比較采用t檢驗或秩和檢驗,多組間比較采用單向方差分析;計數資料比較采用χ2檢驗或Fisher's精確檢驗;相關分析采用Spearman法,危險因素分析采用Logistc多因素回歸分析。P≤0.05為差異有統計學意義。
2 結果
2.1 不同病理類型FSGS患者臨床的特點 152例患者中,20~59歲的中青年患者118例(77.6%)。臨床表現為水腫120例,高血壓65例,蛋白尿145例,腎病范圍蛋白尿101例,血尿77例(其中鏡下血尿74例、肉眼血尿3例),腎功能不全46例,尿糖陽性33例,低IgG 108例,高尿酸血癥55例,貧血25例;腎病綜合征107例,慢性腎炎40例,隱匿性腎炎5例。病理類型:非特殊型78例、頂端型42例、門部型26例、細胞型6例,無塌陷型。不同病理類型患者的臨床特點見表1、2。
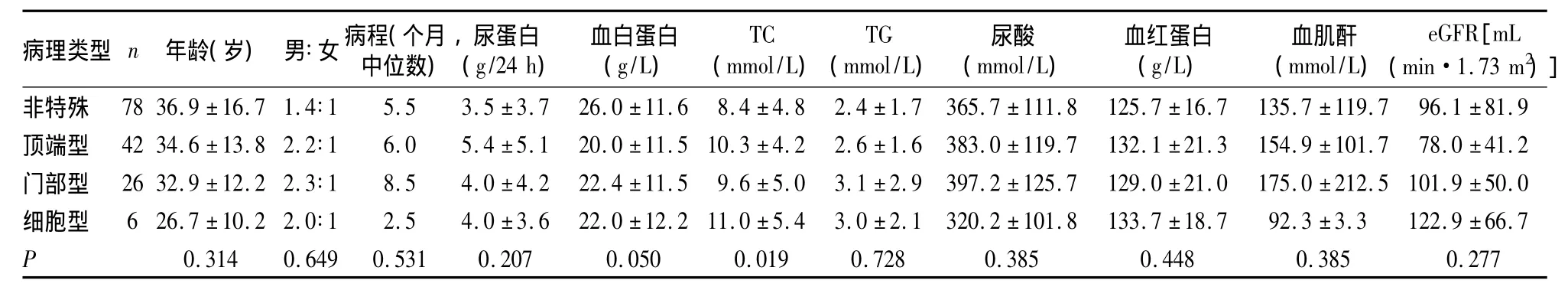
表1 不同病理類型FSGS患者性別、年齡、病程及實驗室檢查結果比較
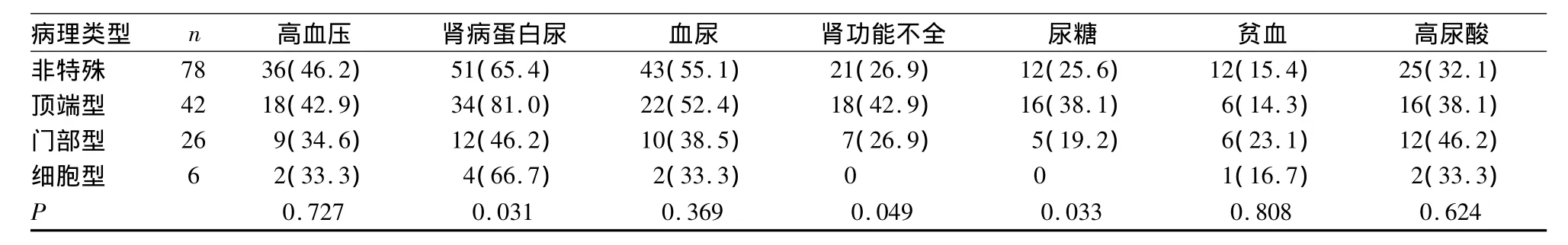
表2 不同病理類型FSGS患者的相關病史[例(%)]
2.2 病理特征 免疫熒光或免疫組化顯示,主要以IgM呈顆粒狀在毛細血管攀硬化區和團塊狀在系膜區沉積,其中單純IgM沉積98例、IgM伴C3或伴其他指標沉積41例、IgG+C3復合沉積3例、全部陰性10例。鏡檢顯示系膜細胞及基質增生142例,腎小管萎縮124例,腎小管急性病變68例,間質纖維化增生119例,腎小球球性硬化100例,其中2~3級23例、1級77例,無球性硬化52例。間質細胞浸潤121例,蛋白管型104例,血管病變23例,球囊粘連28例,新月體11例。有4例第1次腎穿病理為輕微病變型,再次腎穿病理為FSGS。腎小管間質病變TIL分級:0級1例、Ⅰ級134例、Ⅱ~Ⅲ級17例。不同病理類型FSGS患者的腎臟病理積分比較見表3。
表3 不同病理類型FSGS患者的腎臟病理積分比較(分±s)
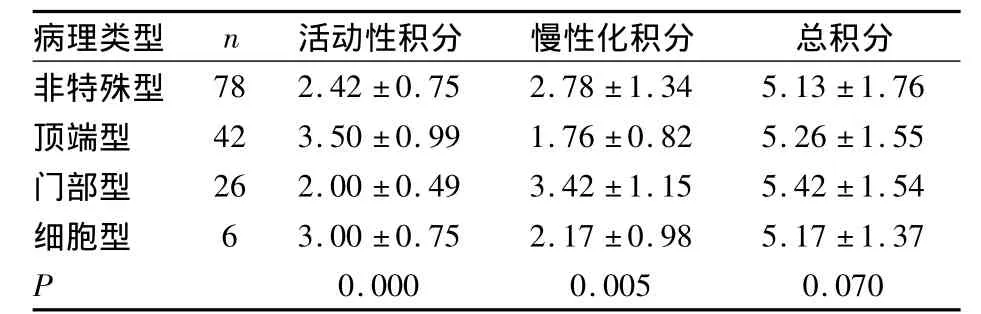
表3 不同病理類型FSGS患者的腎臟病理積分比較(分±s)
病理類型 n 活動性積分 慢性化積分 總積分非特殊型78 2.42 ±0.75 2.78 ±1.34 5.13 ±1.76頂端型 42 3.50 ±0.99 1.76 ±0.82 5.26 ±1.55門部型 26 2.00 ±0.49 3.42 ±1.15 5.42 ±1.54細胞型 6 3.00 ±0.75 2.17 ±0.98 5.17 ±1.37 P 0.000 0.005 0.070
2.3 影響FSGS患者預后因素分析 Spearman相關分析顯示,腎小球球性硬化與年齡、腎功能下降及小管間質病變呈正相關(r分別為 0.395、0.192、0233,P均<0.05)。小管間質病變與血肌酐水平、高尿酸、低IgG及腎功能下降呈正相關(r分別為0.238、0.192、0.189,P 均 <0.05)。Logistc 多因素回歸分析顯示,年齡、腎小管間質病變是腎小球硬化的危險因素(OR 分別為 3.30、6.62,P 均 <0.05),高尿酸、腎小球硬化比例是腎小管間質病變的危險影響因素(OR 分別為0.984、5.225,P 均 <0.05)。
3 討論
原發性FSGS臨床表現多為蛋白尿(特別是腎病綜合征),常伴鏡下血尿,少數出現肉眼血尿,伴高血壓、腎小管受損和腎功能損害[7,8]。本研究發現,原發性FSGS患者以中青年為主,男性發病率高于女性,其臨床表現為不同程度的蛋白尿、鏡下血尿等,且伴有高血壓、腎功能不全、腎性糖尿等,與文獻報道相似。此外,還伴有低IgG、貧血、高尿酸血癥等。因此,臨床上對于中青年男性,表現為蛋白尿(尤其是腎病綜合征)、血尿、高血壓及早期腎功能不全、伴低IgG、尿糖及高尿酸血癥者,應考慮原發性FSGS,及時行腎活檢證實。
FSGS的病理特點為局灶分布的節段性硬化的腎小球,多數見球性硬化。可不同程度地伴有足細胞增生、節段性內皮細胞及系膜細胞增生,腎小管上皮細胞損傷及灶性萎縮,腎間質灶性淋巴、單核細胞浸潤及纖維化等[1]。免疫熒光檢查可見腎小球內以IgM沉積為主,伴或不伴C3沉積,可有相對較弱的C4、IgG、IgA、C1q沉積,也可全部陰性。長期以來國際上對FSGS形態學分型標準不統一,其中FSGS哥倫比亞五型分類法[4]影響最大,本研究按此標準進行分型,非特殊型最多,其次為頂端型、門部型、細胞型,無塌陷型,與師素芳等[9]的報道不盡一致,可能與樣本數量大小、腎活檢指征、診斷水平、病理標準掌握差異、不同種族或不同地域人群有關。
不同病理類型原發性FSGS的臨床表現,國內外報道不盡相同。Deegens等[7]報道,頂端型FSGS患者的24 h尿蛋白水平、腎病綜合征百分率較非特殊型和門部型明顯增高,頂端型血清白蛋白較非特殊型和門部型低;多數文獻報道,頂端型血肌酐水平比各型低,門部型的平均病程比各型長;也有文獻認為,各亞型的臨床區別不明顯。本研究中,頂端型血清白蛋白水平明顯低于非特殊型,頂端型TC、蛋白尿水平和病理活動性積分明顯高于非特殊型。本組頂端型血肌酐水平較高,eGFR比各型低,腎功能不全發生率最高,與文獻報道不一致;但此組尿糖發生率較高,病理活動積分偏高,故頂端型伴腎功能異常可能與病變處于活動期及出現小管間質損害有關;且病變還在活動中,如積極治療可能對腎功能恢復有益。而門部型慢性積分偏高,提示預后可能不佳。
尿蛋白是影響FSGS的重要因素之一。有研究認為,腎病綜合征患者比非腎病綜合征預后差;但也有研究者認為,蛋白尿程度與預后無相關性。本研究提示,蛋白尿是腎功能不全和腎小管病變的危險因素,高尿酸是腎功能不全及腎小管間質病變的危險因素,但蛋白尿與重度球性硬化無明顯相關性。提示FSGS患者治療上如積極控制蛋白尿及降低高尿酸,也許能一定程度上改善預后。
目前,關于FSGS腎小球硬化程度與各臨床指標關系的大宗病例研究較少。本研究結果顯示,腎小球硬化比例與年齡及腎功能下降呈正相關。Hong等研究發現,腎功能不全患者重度腎小球硬化的比例顯著高于腎功能正常患者,但未能得出其是影響預后的獨立危險因素。另外,過去對原發性FSGS認識多關注腎小球病變,而忽略腎小管間質病變。近年研究發現,腎小球硬化程度越重,伴小管間質損害程度也越重。本研究中,FSGS小管間質病變發生率高達99%,腎功能不全患者的Ⅱ~Ⅲ級腎小管間質病變比例明顯高于腎功能正常患者,腎小管間質病變與血肌酐、腎功能下降正相關,提示腎小球硬化和腎小管間質病變與腎功能不全的發生密切相關。另外,腎小球球性硬化比例與腎小管間質病變呈正相關,說明腎小管間質病變與腎小球硬化是相互影響因素。本研究中,IgG降低者占87.1%,血IgG降低組腎病綜合征及小管間質Ⅱ~Ⅲ級病變發生率較非腎病綜合征高。張文等[10]報道,腎病綜合征患者血清IgG水平的降低與尿蛋白丟失有關,但Deegens等[6]認為,lgG的排泄分數不一定與預后相關。故關于lgG的排泄分數與FSGS預后的關系尚存在爭議。
總之,FSGS臨床及病理表現多且不均一,不同病理類型之間的臨床及病理表現既有相似之處又存在差異,其預后與腎小球硬化、小管間質病變、蛋白尿及高尿酸血癥有關。
[1]潘碧霞,姜宗陪,常潔,等.263例成人原發性局灶節段性腎小球硬化性腎小球腎炎臨床病理分析[J].中華腎臟病雜志,2007,23(1):13-17.
[2]Thomas DB,Franeesehini N,Hogan SL,el al.Clinical and pathological characteristics of focal segmental glomerulosclerosis pathologic variants[J].Kidney Int,2006,69(5):920-926.
[3]全國eGFR課題協作組.MDRD方程在我國慢性腎臟病患者中的改良和評估[J].中華腎臟病雜志,2006,22(10):589-595.
[4]D'Agati VD,Fogo AB,Bruijin JA,et al.Pathologic classification of focal segmental glomerulosclerosis:a working proposal[J].Am J Kidney Dis,2004,43(2):368-382.
[5]Stokes MB,Markowitz GS,Lin J,et al.Glomerular tip lesion:a distinct entity within the minimal change disease/focal segmental glomerulosclerosis spectrum[J].Kidney Int,2004,65(5):1690-1702.
[6]Deegens JK,Wetzels JF.Fractional excretion of high-and low-molecular weight proteins and outcome in primary focal segmental glomerulosclerosis[J].Clin Nephrol,2007,68(4):201-208.
[7]Deegens JK,Steenbergen EJ,Borm GF,et al.Pathological variants of focal segmental glomerulosclerosis in an adult Dutch population-epidemiology and outcome[J].Nephrol Dial Transplant,2008,23(1):186-192.
[8]曾彩虹,劉志紅,蘇健,等.局灶節段性腎小球硬化腎組織形態學特點與臨床表現的聯系[J].腎臟病與透析腎移植雜志,2006,15(1):18-24.
[9]師素芳,王素霞,章友康,等.不同病理類型局灶節段性腎小球硬化癥的臨床病理分析[J].中華病理學雜志,2007,36(1):11-14.
[10]張文,劉志紅,曾彩虹,等.塌陷型和細胞型局灶節段性腎小球硬化患者臨床病理特征的比較[J].腎臟病與透析腎移植雜志,2009,18(2):125-132.

