對(duì)海鹽制備試劑級(jí)氯化鈉實(shí)驗(yàn)的改進(jìn)
桑雅麗
(赤峰學(xué)院化學(xué)化工學(xué)院,內(nèi)蒙古赤峰024000)
對(duì)海鹽制備試劑級(jí)氯化鈉實(shí)驗(yàn)的改進(jìn)
桑雅麗
(赤峰學(xué)院化學(xué)化工學(xué)院,內(nèi)蒙古赤峰024000)
本文在給定的實(shí)驗(yàn)條件下,結(jié)合實(shí)驗(yàn)實(shí)際情況,對(duì)實(shí)驗(yàn)裝置及實(shí)驗(yàn)內(nèi)容進(jìn)行了改進(jìn),同時(shí)通過(guò)多組實(shí)驗(yàn)探索不同的試劑用量對(duì)氯化鈉的產(chǎn)率和純度的影響,從中找出BaCl2溶液,Na2CO3溶液和鹽酸的最佳用量.節(jié)省了實(shí)驗(yàn)時(shí)間,提高了產(chǎn)品等級(jí)和試劑純度,達(dá)到了較好的實(shí)驗(yàn)效果.
氯化鈉;提純;試劑用量;實(shí)驗(yàn)裝置
海鹽的主要成分是氯化鈉.除了氯化鈉外,還含有泥砂、草屑等不溶性雜質(zhì)以及鉀、鈣、鎂、硫酸鹽等可溶性無(wú)機(jī)鹽.若要提取試劑級(jí)氯化鈉必須除去各種雜質(zhì).在實(shí)驗(yàn)開(kāi)展過(guò)程中,能夠讓學(xué)生練習(xí)溶解、過(guò)濾、蒸發(fā)、結(jié)晶、氣體的發(fā)生和凈化等基本操作,因此一直作為無(wú)機(jī)化學(xué)實(shí)驗(yàn)課程的保留實(shí)驗(yàn).但是,在實(shí)驗(yàn)過(guò)程中,實(shí)驗(yàn)裝置和試劑的用量及濃度對(duì)實(shí)驗(yàn)進(jìn)度和結(jié)果有一定的影響.在給定的實(shí)驗(yàn)條件和試劑的用量范圍下,本文通過(guò)實(shí)驗(yàn)對(duì)海鹽制備試劑級(jí)氯化鈉的反應(yīng)裝置進(jìn)行了改進(jìn),對(duì)部分實(shí)驗(yàn)內(nèi)容和試劑用量進(jìn)行了探索.
1 實(shí)驗(yàn)原理
海鹽中的不溶性雜質(zhì)可用溶解過(guò)濾的方法除去.可溶性無(wú)機(jī)鹽可以用化學(xué)方法除去[1]:在海鹽溶液中加入稍過(guò)量的BaCl2溶液時(shí),可將SO42-轉(zhuǎn)化為難溶解的BaSO4沉淀而除去.過(guò)濾溶液,除去BaSO4沉淀.再加入NaOH和Na2CO3溶液,由于發(fā)生了下列反應(yīng):
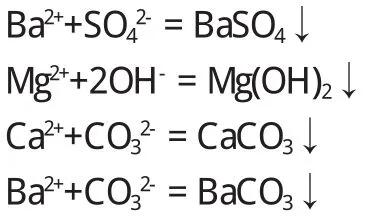
食鹽中的雜質(zhì)Mg2+,Ca2+及沉淀SO42-時(shí)加入的過(guò)量Ba2+便相應(yīng)地轉(zhuǎn)化為難溶的Mg(OH)2,CaCO3,BaCO3沉淀而過(guò)濾除去.過(guò)量的NaOH和Na2CO3可用鹽酸中和.少量可溶性雜質(zhì)(如KCl),通過(guò)向飽和NaCl溶液中通入HCl氣體,由于同離子效應(yīng),NaCl晶體析出,而KCl的溶解度比NaCl大,無(wú)需對(duì)產(chǎn)品重結(jié)晶,K+殘留在母液中被除去.吸附在NaCl晶體上的HCl可用酒精洗滌除去,再進(jìn)一步水浴加熱,除掉少量水、酒精和HCl,即得到純度很高的NaCl[2].
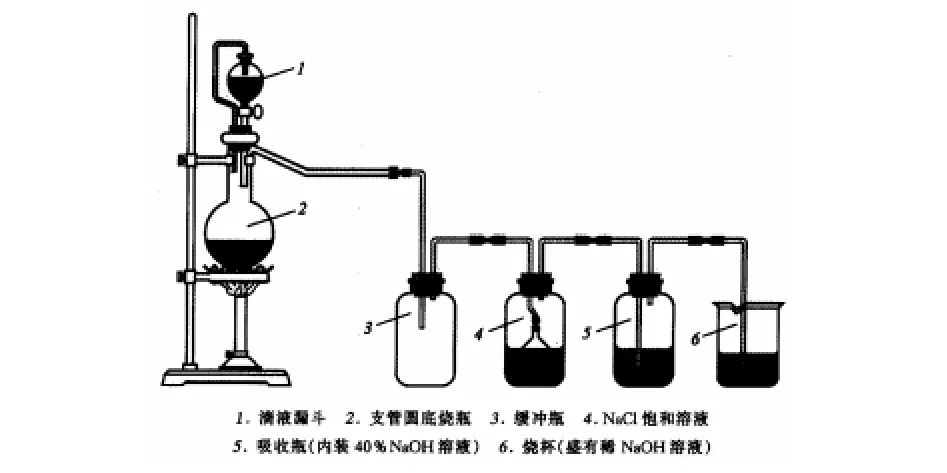
圖1 原精制氯化鈉裝置圖
2 原實(shí)驗(yàn)內(nèi)容
2.1 海鹽提純
用臺(tái)秤稱(chēng)取10.0g海鹽,放入小燒杯中.加入35mL蒸餾水,用酒精燈加熱,并攪拌促其溶解.至沸,在攪拌下,滴加1-2mL1mol·L-1BaCl2溶液至沉淀完全(BaCl2溶液滴入時(shí)不再產(chǎn)生新的渾濁),繼續(xù)加熱煮沸10分鐘,使BaSO4顆粒長(zhǎng)大而易于沉淀和過(guò)濾.為了試驗(yàn)沉淀是否完全,取下燒杯,待沉淀沉降后于上層清液中加入1-3滴BaCl2,至無(wú)渾濁產(chǎn)生為止.在上述液體中趁熱加入1mL2mol?L-1NaOH溶液和4-5mL1mol·L-1Na2CO3溶液,待沉淀沉降后,過(guò)濾,棄去沉淀.將濾液轉(zhuǎn)移至廣口瓶,攪拌下逐滴加入2mol·L-1HCl,調(diào)至溶液的pH=1.組裝HCl氣體發(fā)生裝置,并將HCl氣體的導(dǎo)出管與緩沖瓶、裝有NaCl母液的廣口瓶、裝有NaOH溶液的吸收瓶,依次相連,最后將尾氣吸收管導(dǎo)入盛有NaOH稀溶液的燒杯中,二次吸收過(guò)剩的HCl.稱(chēng)取20.0g化學(xué)純NaCl于蒸餾燒瓶?jī)?nèi),用滴液漏斗將20mL濃硫酸緩慢滴加至燒瓶?jī)?nèi),用酒精噴燈控制氣體發(fā)生速率,使HCl氣體平穩(wěn)放出,經(jīng)緩沖瓶至裝有NaCl母液的廣口瓶,此時(shí)有NaCl晶體析出.反應(yīng)至無(wú)NaCl晶體析出時(shí),停止反應(yīng).冷卻,減壓過(guò)濾,95%乙醇淋洗2-3次后,水浴烘干,稱(chēng)量,計(jì)算產(chǎn)率.并對(duì)產(chǎn)品的純度進(jìn)行檢驗(yàn).
2.2 純度檢驗(yàn)
Fe3+的限量分析
在酸性介質(zhì)中,F(xiàn)e3+與SCN-生成血紅色配離子[Fe(SCN) n](3-n)+(n=1~6),其顏色,隨配位體數(shù)目n的增大而變深.
試樣溶液配制:分析天平稱(chēng)量3.00g NaCl于25mL比色管中,10mL蒸餾水溶解,加入2.00mL25%KSCN溶液和2mL3mol·L-1HCl溶液,用蒸餾水稀釋至刻度,搖勻.將試樣溶液與標(biāo)準(zhǔn)溶液進(jìn)行目視比色,確定產(chǎn)品的純度等級(jí).
SO42-的限量分析
SO42-與BaCl2溶液反應(yīng),生成難溶的BaSO4白色沉淀而使溶液產(chǎn)生混濁.溶液的混濁度,在BaCl2的含量一定時(shí),與SO42-濃度成正比.
試樣溶液配制:分析天平稱(chēng)量1.00g NaCl于25mL比色管中,10mL蒸餾水溶解,加入3.00mL25%BaCl2溶液、1mL3mol·L-1HCl溶液和5mL95%乙醇,用蒸餾水稀釋至刻度,搖勻.將試樣溶液與標(biāo)準(zhǔn)溶液進(jìn)行目視比色,確定產(chǎn)品的純度等級(jí).
3 改進(jìn)實(shí)驗(yàn)內(nèi)容
常規(guī)的海鹽制備試劑級(jí)氯化鈉實(shí)驗(yàn)存在著下列問(wèn)題:(1)實(shí)驗(yàn)過(guò)程中使用酒精噴燈作為加熱裝置(見(jiàn)圖1),導(dǎo)致反應(yīng)溫度過(guò)高,反應(yīng)速率過(guò)快,大量氣體溢出,難以控制氯化氫氣體發(fā)生速率.(2)實(shí)驗(yàn)所用儀器為普通支管燒瓶和廣口瓶,市售恒壓滴液漏斗多為磨口玻璃制品,故不適用于本實(shí)驗(yàn)反應(yīng)過(guò)程.(3)為了試驗(yàn)SO42-沉淀是否完全,直接在溶液中滴加BaCl2溶液時(shí),由于溶液中的沉淀不能在短時(shí)間內(nèi)沉降完全,此時(shí)溶液渾濁.因此很難判斷出SO42-是否已經(jīng)完全沉淀.導(dǎo)致成品中含有雜質(zhì)離子,除雜不徹底,產(chǎn)品純度低,從而影響實(shí)驗(yàn)結(jié)果.(4)實(shí)驗(yàn)除雜過(guò)程中給出Na2CO3溶液的用量范圍,但沒(méi)有明確的體積用量,無(wú)法判斷其用量對(duì)產(chǎn)品的產(chǎn)率和純度的影響.一般說(shuō)來(lái),引入過(guò)多的Na2CO3,后續(xù)反應(yīng)需要過(guò)多的鹽酸中和,因此除雜過(guò)程引入了過(guò)多的NaCl,導(dǎo)致NaCl的產(chǎn)率比實(shí)際產(chǎn)率偏高,為實(shí)驗(yàn)帶來(lái)誤差.(5)中和濾液用的鹽酸濃度過(guò)低,引入大量水溶液,致使溶液中NaCl的濃度過(guò)低,后續(xù)反應(yīng)中通入氯化氫氣體后產(chǎn)品析出量過(guò)少或很難達(dá)到飽和析出,從而降低了NaCl的實(shí)際產(chǎn)率.(6)過(guò)濾溶液中的沉淀時(shí)采用普通過(guò)濾方法,沉淀顆粒附著在濾紙上,過(guò)濾速度很慢,導(dǎo)致此過(guò)程耗時(shí)過(guò)長(zhǎng).
3.1 實(shí)驗(yàn)裝置的改進(jìn)
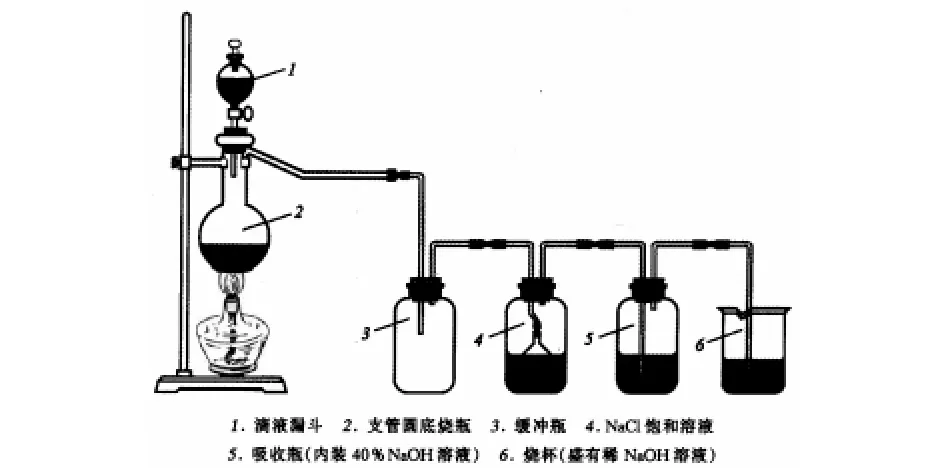
圖2 改進(jìn)后的精制氯化鈉裝置圖
在氯化氫氣體發(fā)生裝置中(見(jiàn)圖2),用酒精燈代替了酒精噴燈,避免了溫度過(guò)高,HCl氣體產(chǎn)生過(guò)快,不易控制氣體發(fā)生速度的情況.使用酒精燈后,產(chǎn)生HCl氣體速度平穩(wěn),易于控制.可防止氣體溢出或液體倒吸.同時(shí)將實(shí)驗(yàn)用的恒壓滴液漏斗簡(jiǎn)化為普通滴液漏斗,HCl氣體產(chǎn)生過(guò)程中,燒瓶?jī)?nèi)氣體增多產(chǎn)生壓強(qiáng),導(dǎo)致滴液漏斗滴加過(guò)慢或者氣體由滴液漏斗溢出.故用滴液漏斗將濃硫酸全部滴加至燒瓶?jī)?nèi),然后關(guān)閉旋塞,用酒精燈控制氣體發(fā)生速率,使HCl氣體平穩(wěn)放出.在一定程度上加快了反應(yīng)進(jìn)程,有效防止了氣體的溢出,避免環(huán)境受到污染.
3.2 實(shí)驗(yàn)內(nèi)容的改進(jìn)
在SO42-除雜過(guò)程中,增加離心檢驗(yàn)步驟,具體操作:為了試驗(yàn)SO42沉淀是否完全,取1mL溶液于離心管中,離心機(jī)內(nèi)離心分離1-2min,然后于離心管的上層清液中加入2滴BaCl2,檢驗(yàn)有無(wú)渾濁產(chǎn)生,至無(wú)渾濁產(chǎn)生為止.將化學(xué)除雜后得到的溶液使用普通過(guò)濾方法改為減壓過(guò)濾,加快了過(guò)濾速度,縮短了實(shí)驗(yàn)時(shí)間,提高了實(shí)驗(yàn)效率.將調(diào)節(jié)溶液pH=1的2mol·L-1鹽酸溶液用6mol·L-1鹽酸溶液代替.除雜后的濾液中含有大量的OH-和CO32-,因此用來(lái)中和濾液的鹽酸用量很大,使用低濃度的鹽酸溶液會(huì)在反應(yīng)中引入大量的水,導(dǎo)致濾液中的NaCl濃度偏低.使用6mol·L-1鹽酸溶液代替后,在一定程度上保持了原濾液中NaCl的濃度,通入氯化氫氣體后很快析出NaCl晶體,減少了實(shí)驗(yàn)失敗的風(fēng)險(xiǎn).
3.3 試劑用量的改進(jìn)
通過(guò)多組實(shí)驗(yàn)(見(jiàn)表1),對(duì)比探索BaCl2溶液的用量范圍(1.0-2.2 mL)、Na2CO3溶液的用量范圍(4.0-5.2 mL)和鹽酸溶液的用量范圍(1.7-2.2 mL)發(fā)現(xiàn):當(dāng)加入1.1mLBaCl2溶液、4.1mLNa2CO3溶液和1.7mL鹽酸溶液時(shí),得到NaCl產(chǎn)品為8.2g,產(chǎn)率為82%,F(xiàn)e3+純度等級(jí)為二級(jí),SO42-純度等級(jí)為一級(jí),此時(shí)產(chǎn)品的純度和試劑等級(jí)最好.當(dāng)逐漸增加BaCl2溶液用量時(shí),引入溶液中的Cl-不斷增多;當(dāng)逐漸增加Na2CO3溶液用量時(shí),引入溶液中的Na+也不斷增多,隨著溶液中Cl-和Na+的不斷增多,向飽和NaCl溶液中通入HCl氣體時(shí),析出的NaCl晶體也會(huì)增多,從而提高了產(chǎn)品的實(shí)際產(chǎn)量和產(chǎn)率,但是卻降低了產(chǎn)品的純度和試劑等級(jí).給實(shí)驗(yàn)帶來(lái)不必要的誤差.

表1 實(shí)驗(yàn)制備試劑級(jí)氯化鈉的試劑用量、產(chǎn)量產(chǎn)率及純度檢驗(yàn)數(shù)據(jù)
4 結(jié)論
本文依據(jù)實(shí)驗(yàn)教材,結(jié)合實(shí)驗(yàn)開(kāi)展的條件和實(shí)驗(yàn)過(guò)程中出現(xiàn)的問(wèn)題,通過(guò)實(shí)驗(yàn)對(duì)部分實(shí)驗(yàn)裝置和實(shí)驗(yàn)內(nèi)容進(jìn)行了改進(jìn),同時(shí)探索了所用BaCl2溶液和Na2CO3溶液的最佳用量及其與產(chǎn)品的產(chǎn)率和純度之間的關(guān)系.在此實(shí)驗(yàn)改進(jìn)的基礎(chǔ)上開(kāi)展學(xué)生實(shí)驗(yàn),不但節(jié)省了實(shí)驗(yàn)時(shí)間和試劑用量,而且提高了實(shí)驗(yàn)效率.
〔1〕北京師范大學(xué)無(wú)機(jī)化學(xué)教研室,等.無(wú)機(jī)化學(xué)實(shí)驗(yàn)(第三版)[M].北京:高等教育出版社,2001.
〔2〕袁紅梅,趙雪英.由海鹽制備試劑級(jí)氯化鈉[J].棗莊學(xué)院學(xué)報(bào),2006(5).
O614.112
A
1673-260X(2013)09-0007-02

